В статье предложен метод гистохимического выявления в панкреатических B-клетках одновременно инсулина и ионов Zn2+, участвующих в его депонировании. Отмечено, что метод основан на окраске в замороженных срезах поджелудочной железы комплекса <йп2+-инсулин» дитизоном, окрашивающим комплекс в ярко-красный цвет. Определено, что интенсивность окраски может быть оценена количественно с помощью фотометрии. Доказано, что метод позволяет выявлять гистохимически как инсулин, так и содержание ионов Zn2+ в B-клетках. Авторами метод рекомендован для использования в виде прижизненной гистохимической реакции.
Известно, что цинку принадлежит важная роль в процессах депонирования инсулина в В-клетках кроликов, кошек, мышей, белых крыс, лошадей, собак, человека [1-4]. Синтезированный в В-клетках инсулин соединяется с имеющимся в В-гранулах цитоплазмы В-клеток цинком, образуя депо-форму. Цинк, выявленный методом электронной гистохимии [5], содержится только в В-гранулах, а в других органеллах В-клеток и в ее цитоплазме не обнаружен.
Разрушение В-клеток сопровождается параллельным снижением в их цитоплазме как инсулина, так и цинка. Резкое снижение содержания цинка в В-клетках происходит при тяжелых формах сахарного диабета. В подавляющем большинстве случаев наблюдается строгий параллелизм между содержанием в В-клетках ионов Zn2+ и инсулина.
Однако в отдельных, редких, искусственно созданных экспериментальных условиях, не связанных с наличием сахарного диабета, такой параллелизм может отсутствовать. В отсутствие диабета снижение содержания цинка в В-клетках может свидетельствовать о нарушении обмена цинка или о его временной мобилизации из В-клеток, например, при введении высоких доз сульфаниламидных сахароснижающих препаратов животным, что, в свою очередь, создает условия для нарушения процессов депонирования инсулина в клетках. То есть гистохимическими методами ионы в клетках при этом не выявляются ввиду их отсутствия, однако способность В-клеток синтезировать инсулин при этом не нарушается, нарушаются лишь процессы его депонирования, которые быстро восстанавливаются при прекращении действия причин, приводящих к мобилизации ионов Zn2+ из В -клеток.
Известен абсолютно специфичный флюоресцентный метод определения ионов Zn2+, однако химически он выявляет только ионы данного металла и не может служить критерием оценки содержания инсулина в цитоплазме клеток [6-8].
Существующие методы гистохимического выявления инсулина в В-клетках — иммуно-гистохимический, иммунофлюоресцентный, альдегидфуксиновый, псевдоизоцианиновый, Виктория-4 [9-16], являясь специфичными или абсолютно специфичными в отношении инсулина, имеют 3 существенных недостатка, ограничивающих их применение. Реактивы и антисыворотки, необходимые для них, весьма дороги и выпускаются ограниченным числом западных фирм. Кроме того, химически они выявляют только инсулин, не являясь маркерами собственно ионов цинка. Наконец, перечисленные выше методы, оценивая содержание инсулина в В-клетках, не позволяют судить о способности клеток депонировать синтезированный гормон с помощью ионов Zn2+, поскольку его содержание ими не оценивается.
Нами ставилась задача — разработать способ гистохимического выявления инсулина и одновременно ионов Zn2+ в панкреатических В-клетках с тем, чтобы оказалось возможным оценивать не только содержание инсулина в В-клетках, но и одновременно ионов Zn2+. Это позволило бы дополнительно судить о способности клеток депонировать, а не только синтезировать инсулин.
Предлагаемый способ количественной оценки содержания депонированного инсулина в окрашенных на инсулин В-клетках панкреатических островков поджелудочной железы основан на формировании окрашенного в красный цвет комплекса <^п2+-дитизон», выявляемого в панкреатических островках срезов ткани поджелудочной железы с помощью темнополевой микроскопии путем окраски В-клеток двумя путями: 1) введением раствора дифенилтиокарбазона (дитизона) животным внутривенно с последующей микроскопией препаратов замороженной поджелудочной железы; 2) окраской парафиновых или замороженных срезов поджелудочной железы раствором дитизона. Методом спектрального анализа подтверждено, что образующиеся в В-клетках ярко-красные гранулы химически являются комплексом <^п2+-дитизон» и имеют тот же спектр поглощения, равный 580 нм, что и синтезированный химическим путем дитизонат цинка [17]. Поскольку ионы Zn2+ в В-клетках находятся в связанном с инсулином состоянии, образуя депоформу гормона, данный метод одновременно позволяет судить и о содержании инсулина в клетках. Удаление дитизоната цинка из В-клеток сопровождается и удалением инсулина, связанного с цинком в виде депоформы, о чем свидетельствует полное отсутствие инсулина в В-клетке, выявляемое высокоспецифичными гистохимическими методами [17].
Материалы и методы исследования
В опытах использованы 14 беспородных кроликов массой 2480-3060 г. Животным внутривенно вводился водно-аммиачный раствор дитизона («MERCK», ФРГ), приготовленный следующим образом: 200 мг дитизона вносится в колбу с притертой пробкой, содержащую 25 мл дистиллированной воды, добавляется 0,2 мл 25 %-ного раствора аммиака, затем смесь встряхивается в течение 10 мин на водяной бане при температуре +70оС. После этого раствор охлаждался и медленно вводился внутривенно из расчета 45-50 мг/кг. Точная концентрация устанавливалась путем вычета нерастворившего-ся порошка дитизона, оставшегося на фильтре после его высушивания. Извлеченная поджелудочная железа замораживалась в криостате, после чего замороженные срезы толщиной 4-5 мкм исследовались в темном поле микроскопа.
Результаты исследования
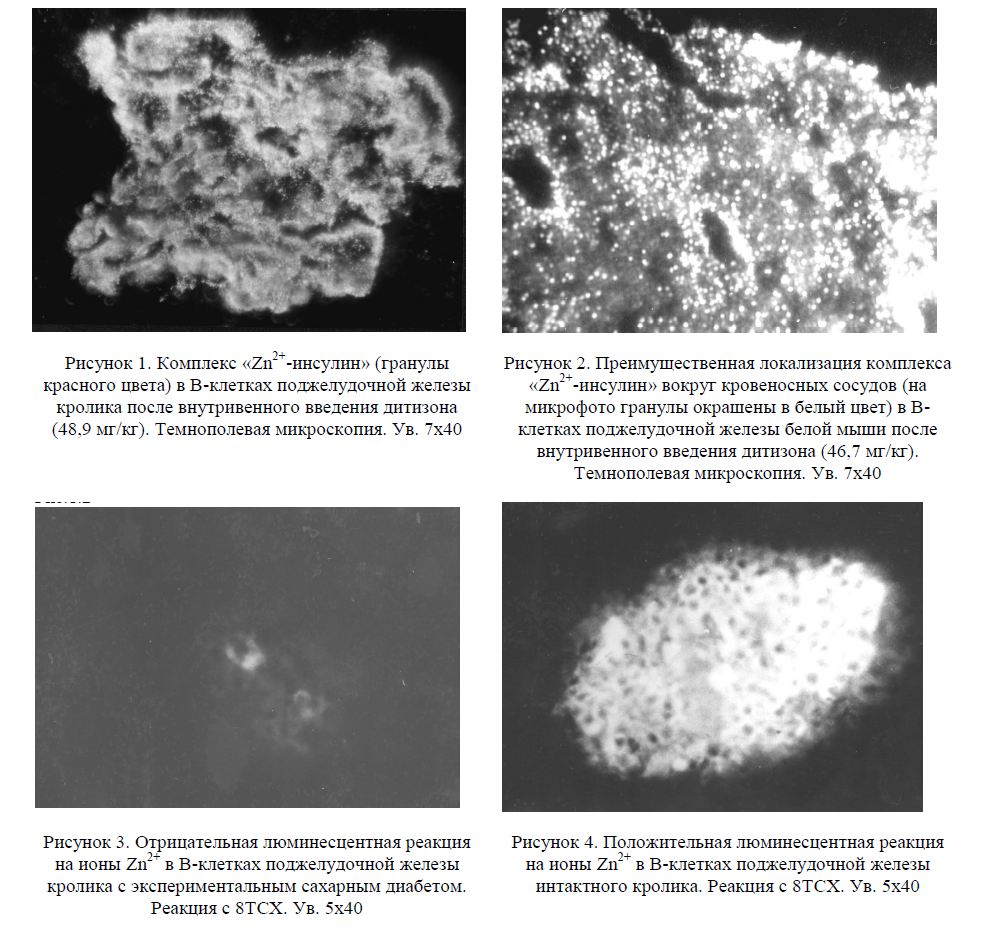
В поле зрения видны островки, содержащие обильную ярко-красную зернистость, особенно плотно располагающуюся вокруг стенок кровеносных сосудов, т.е. там, где концентрируется наибольшее количество депонированного инсулина (рис.1, 2), тогда как в В-клетках поджелудочной железы животных с экспериментальным диабетом зернистость полностью отсутствовала, как и ионы Zn2+ (рис.3), по сравнению с резко положительной реакцией на цинк в препаратах интактных животных (рис.4). Данная зернистость является комплексом <^п2+-дитизон», что подтверждено результатами спектрального анализа [17]. Интенсивность окраски можно оценить количественно путем фотометрии, с получением количественных данных в относительных единицах [15].
Этим же раствором можно окрашивать срезы замороженной ткани поджелудочной железы, не вводя его внутривенно, а нанося на срез на 2 минуты, после чего раствор дитизона смывается со среза дистиллированной водой. Однако качественные результаты такой окраски всегда уступают результатам, полученным способом, описанным выше: гистотопография комплекса в этом случае выявляется хуже.
Таким образом, полученные результаты свидетельствуют о том, что с помощью данного гистохимического метода в панкреатических В-клетках можно выявлять инсулин в комплексе с ионами Zn2+, что позволяет судить как о содержании инсулина в клетке, так и, по содержанию ионов Zn2+, о способности ее к депонированию гормона. Локализация ионов Zn2+ в цитоплазме В-клеток в точности повторяет расположение инсулина [3,15,17]. Практически всегда наблюдается строгий параллелизм между содержанием депонированного инсулина и ионов Zn2+, и лишь в двух случаях он может нарушаться. Это наблюдается, если ионы Zn2+ искусственно вымываются из В-клеток либо если они связаны с введенными извне хелаторами — производными дитиокарбаминовой кислоты. В этих крайне редко встречающихся случаях параллелизм нарушается, т.е. инсулин в клетке сохраняется, но реакция на цинк бывает отрицательной в результате его отсутствия или его конкурентного связывания с солями дитиокарбаминовой кислоты, которая, не снижая количества ионов Zn2+ в В-клетках, не дает возможности выявления его с помощью маркеров на цинк.
References
- Okamoto K. Experimental pathology of diabetes mellitus // Tohoku Journal of Exper. Medicine. — 1975. — 61. — Suppl. 1-2. — P. 1-61.
- Meyramov G.G., Meyramova A.G. Zn as Cause of Diabetes Induced by Chelators and as Cause of its Prevention // DIABETES. The Journal of American Diabetes Association, USA. — 2002. — 51. — № 6. — P. 591-592.
- Lapin W.I., Meyramov G.G., Korchin W.I., Satosin Table of contents of zinc and insulin in B-cells of small islands of Langergans at an experimental alloxanic diabetes // Of Patholog. Phisiol. experim.therap. — 1973. — № 4. — P. 36-39.
- Okamoto K. Experimental pathology of diabetes mellitus // Diabetes Mellitus: Theory and Practice. — New York. — 1970.256-264.
- Okamoto K., Kawanishi H. Submicroscopic histochemical demonstration of intracellular reactive zinc in B-cells of pancreatic islets // Endocrinol. Jap. — 1966. — 13. — № 3. — P. 305-318.
- BozhevolnovЕ.А., Serebrjakova G. V.8-п-tozilaminokhinolinovy luminescent reagent on zinc and cadmium // The Chemical reagents and preparations. — Мoscow, 1961. — 36-12.
- Meyramov G.G., Meyramova R.G. The High Specifical Histochemical Method Revealing of Zn-ions in B-cells of Isolated Pancreatic islets // DIABETES. The Journal of American Diabetes Association. — 1991. — 40. — Suppl. 1. — P. 65.
- Meyramov G.G., Meyramova A.G. 8-PTSQ as Fluorescent Reagent for Reve aling of Zn-ions in B-cells and as Diabetogenic Chelator //ACTA DIABETOLOGICA. The European Diabetes Journal. — 2003. — — 2003. — Vol. 40. — № 1. —57.
- Kvistberg D., Lester G., Lasarov A. Staining of Insulin with Aldehydefuchsin // Journal Histochem and Cytochem. — 1966. —Vol. — P. 609-611.
- Meyramov G.G., Niedderer H. The Histofunctional Method Appreciating of Functional State of Isolated Pancreatic B-cells in the Tissue of Culture // Diabetes Research. and Clinical Practice. The Journal of International Diabetes Federation. Amsterdam-New York, — Vol. 5. — P. 228.
- Wohlrab F., Dorsche H., Krautschick I., Schmidt S. On the specifity of the Insulin staining by Victoria Blue 4R // Histo-chem J. — 1985. — 17. — P. 515-518.
- Meyramova A.G., Kikimbaeva A.A., Meyramov G.G. Victoria 4 Method Staining of Insulin in B-cells of Isolated Pancreatic Islets // ACTA DIABETOLOGICA. The European Diabetes Journal. <<SPRINGER». — 2003. — 40. — № 4. — P. 208.
- Schiebler T.H., Schiessler S. Uber den Nachweis von Insulin mit den metachromatisch reagie- renden Pseudoisocyaninen // Histochemie. — 1959. — 1. — S. 445-465.
- Coalson R.E. Pseudoisocyanin staining of insulin and specifity of emperical islet cell stain // Stain Technol. — 1966. — № 2.
- 121-129.
- Meyramov G.G., Iusupbekova G.T., Meyramova R.G. Gistoflyuorimetrical method of determination of maintenance of insulin in pancreatic B-cells // Of Problem of endocrinology. — 1987. — № 5. — 49-51.
- Meyramov G.G., Kikimbaeva A.A., Meyramova A.G. Fluorescent Histochemical method Staining of Insulin in B-cells of Isolated Pancreatic islets by Diethylpseudoisocyanine Chloride // ACTA DIABETOLOGICA. The European Diabetes Journal. — 2005. — Vol. 42. — № 1. — P. 66.
- LasarisYa.A., MeyramovG.G.К выяснению роли блокирования цинка в патогенезе дитизонового диабета // OfProblemofendocrinology. — 1974. —Vol. — № 5. —P. 90-94.