Криоконсервация овариальной ткани является альтернативным методом сохранения генетического материала животных. В данном исследовании мы сравнили жизнеспособность овариальных фолликулов витрифицированной ткани яичника овец c 4,5М диметильсулфоксидом (DMSO) и 5М пропандиолом (PROH). После гистологического анализа процент морфологически нормальных фолликулов криосохраненной ткани составил: с 1,5 М DMSO ̶ примордиальных - 39,8%; первичных - 30,4 % и вторичных - 19,6 %; 1,5М PROH - 48,8%; 37,1% и 24,9%, а в контрольной группе - 95,8%; 92,9 % и 89,6%, соответственно. Таким образом, установлено, что использование 5М PROH оказывает более эффективное действие на жизнеспособность овариальных фолликулов при витрификации, чем использование 4,5М DMSO.
Введение Генетические ресурсы животных представляют ценный и стратегически важный капитал любой страны, так как они связаны с решением проблемы обеспечения населения страны продовольствием, промышленности – сырьем. Для решения данной проблемы в развитых странах мира проводятся интенсивные научные исследования по сохранению и рациональному использованию как культурных, созданных на основе искусственного отбора и подбора пород домашних животных, так и аборигенных пород и популяций животных, сформировавшихся в течение многих столетий на базе естественного отбора и народной селекции.
Сохранить генетический материал и репродуктивный потенциал можно не только за счет выделения и сохранения отдельных яйцеклеток и получаемых из них эмбрионов, но и путем криоконсервации самой функциональной (кортикальной) ткани яичника, технология которой так же включает методы медленного замораживания [1,2,3] и витрификации [4,5,6,7]. Медленное замораживание остается наиболее широко используемым методом в клинике. Более низкие концентрации криопротектантов используются в составе крипротекторов для медленного замораживания, что снижает риск токсического и осмотического повреждения клеток, но следует учитывать, что это не предотвращает образование кристаллов льда, которое приводит к уменьшению выживаемости клеток во время замораживания [8]. Витрификация считается относительно новым методом замораживания, о нем были опубликованы статьи как об эффективном альтернативном методе для криосохранения тканей яичников различных видов, в том числе мыши [9,10], крысы [11], свиньи [12], козы [13], овец [14, 15], обезьяны [16] и человека [17, 18]. Данный метод сочетает в себе быструю скорость замораживания и большую концентрацию криопротектантов в составе витрификационных растворов, которые быстро обезвоживают клетки при этом, предотвращая образование кристаллов льда [8].
С точки зрения криобиологии задача ученых состоит в повышении выживаемости овариальной ткани после криоконсервации. В связи с этим, целью нашего исследования является изучение влияния различных криопротекторов: 4,5М диметильсулфоксида (ДМСО) и 5 М пропандиола (PROH) на выживаемость тканей яичников при витрификации.
Материалы и методы Реагенты. Все реагенты, использованные в данном исследовании были куплены от Sigma-Aldrich (Германия).
Коллекция кортикальной ткани 30 яичников 2,5 годовалых овец аборигенной Чуйской популяции были взяты путем забоя животных, транспортировались в лабораторию при 37оС в фосфатно-солевом буфере Дюльбекко (DPBS). Яичники освободили от связок и промыли несколько раз в PBS с антибиотиками (пенициллина, стрептомицин). После снятия макроскопических данных удаляли мозговую часть яичника, а кортикальную часть разделили на мелкие кусочки c размером 0,5х0,5х1 см.
Экспериментальный план Полученные кусочки овариальной ткани поделили на три главные экспериментальные группы: группа I, криопротектор 4,5М диметилсульфоксид (ДМСО) и группа II, криопротектор 5М пропандиол (PROH); группа III, контрольная, не подвергалась воздействию криопротекторов и не витрифицировалась;
Витрификация и нагревание овариальной ткани
Яичники были витрифицированы по методу Lane et al. (1999). Образцы эквилибрировали в следующих витрификационных растворах:
Группа I - 1,125 М и 2,25 М DMSO на фосфатно-солевом буфере Дюльбекко образцы эквилибрировали по 10 минут, затем в витрификационном растворе (VS) – 4,5 М DMSO на фосфатно-солевом буфере Дюльбекко в течение 5 мин;
Группа II - 1,25 М и 2,5 М PROH на фосфатно-солевом буфере Дюльбекко по 10 минут; затем в витрификационном растворе (VS) – 5,0 М PROH на фосфатно-солевом буфере Дюльбекко в течение 5 мин. После этого образцы из криозащитной среды переносили в соломинку (straws, IMV technologies емкостью 0,5 см3). Соломинки заполняли в соответствии с требованиями IETS. Свободный конец соломинки запаивали и затем погружали в жидкий азот и хранили в сосудах Дьюара в течение одной недели. Для размораживания, витрифицированные образцы в соломинках 5 сек. держали в атмосферном воздухе при комнатной температуре, затем помещали на 25оC водяную баню. Для удаления криопротекторов проводили обратную эквилибрацию в растворах с понижающейся концентрацией криопротектора с добавлением сахарозы (Sigma, USA).
Гистологическая обработка Свежие и витрифицированные образцы овариальной ткани фиксировали в 10% формалине в течение 24 часов, дегидратировали и заключали в парафиновые блоки. С каждого образца делали серийные срезы толщиной 5 мкм, окрашивали гематоксилин-эозином и по Ван Гизону по стандартной методике. Исследование полутонких и гистологических препаратов осуществляли с помощью светового микроскопа при увеличениях объектива х20 их40. Микрофотосъемку осуществляли с помощью микроскопа Zeiss Axiostar plus, «Видеотест морфология». Осуществляли анализ гистологических срезов, изучая только фолликулы с видимым ядром для исключения повторного счета одного и того же фолликула в анализируемом срезе. Количество нормальных и дегенеративных фолликулов выражали в процентах по отношению к общему числу фолликулов в образцах.
Результаты исследований В ходе морфологического исследования изучалась морфология примордиальных, первичных и вторичных фолликулов в овариальной ткани и была проведена морфологическая оценка их качества. Микроскопический анализ окрашенных гематоксилин эозином и Ван Гизоном препаратов свежей ткани показали неповрежденную морфологию примордиальных и первичных фолликулов с плотным контактом между ооцитом и окружающими гранулезными клетками, а также между соседними гранулезными клетками (Рис. 1a и b). Большинство вторичных фолликулов свежей ткани показали ооциты с агранулярной цитоплазмой и центрально расположенным ядром окруженной несколькими слоями гранулезных клеток и хорошо организованный текальный слой. В ооцитах фолликулов наблюдалось однородное распределение цитоплазмы (Рис. 1c).
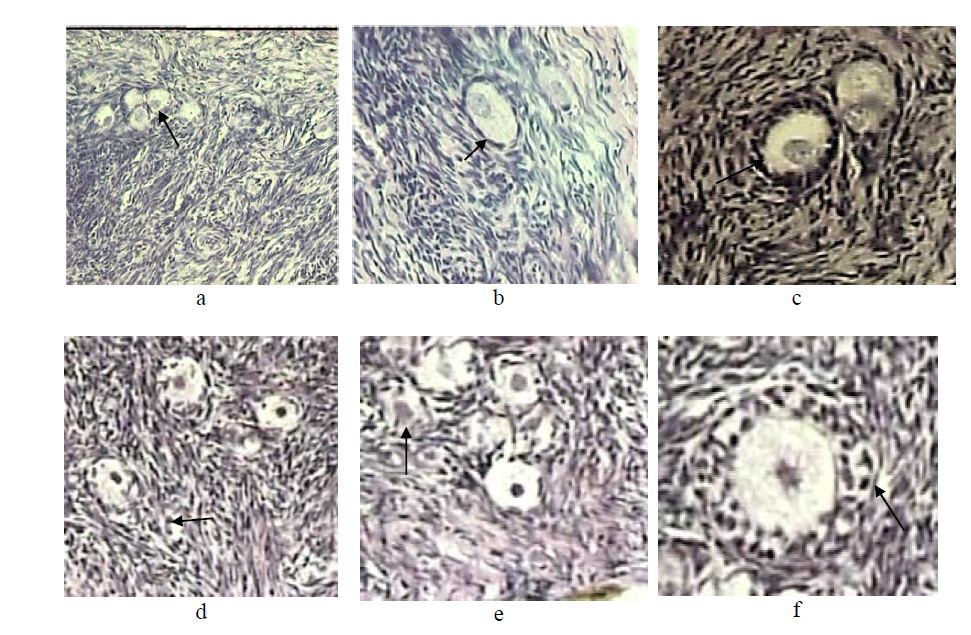
Рис 1. Представленные микрофотографии фиксированной овариальной ткани: свежие (a, b,c) и витрифицированные ткани (d,e,f). Свежая овариальная ткань показала примордиальные (а), первичные (b), вторичные (c), фолликулы со здоровым ооцитом и плотным компактным слоем гранулезных клеток. После витрификации морфология гранулезных клеток различного класса фолликулов главным образом были сохранены (d-f); однако, нечасто, повреждение включало сморщенных (d, стрелка) или вакуолизированных ооцитов (e, стрелка), а также наблюдалось неправильное пространство между фолликулами и стромой (f, стрелка). Увелечение х20, х40.
Морфологический анализ сохранности примордиальных и первичных фолликулов во фрагментах овариальной ткани витрифицированных двух групп показали некоторые повреждения. Были обнаружены сморщенные (Рис. 1. d,e,g,h) и вакуолизированные ооциты, а также неправильное пространство между фолликулами и стромой (Рис. 1f, стрелка). Во всех группах свежей и витрифицированной ткани с использованием различных криопротекторов белочная оболочка ткани была плотной и компактной стромой.
Таблица 1 - Относительное количество (%) морфологически нормальных фолликулов в овариальной ткани яичников овец после замораживания и оттаивания при использовании различных криопротекторов.
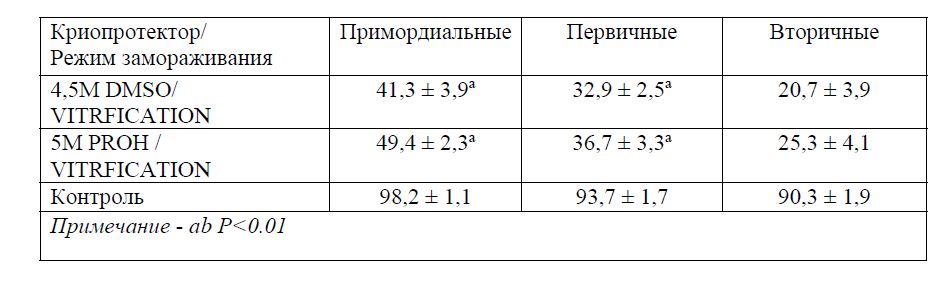
Сопоставляя данные, представленные в таблице 1, следует отметить, что количество морфологически нормальных примордиальных фолликулов в двух группах 4,5М DMSO 41,3 ± 3,9a и 5М PROH 49,4 ± 2,3a витрифицированной овариальной ткани выше по сравнению первичными 32,9 ± 2,5a , 36,7 ± 3,3a и вторичными 20,7 ± 3,9, 25,3 ± 4,1 фолликулами. Данный факт, по всей видимости, можно объяснить тем, что примордиальные фолликулы имеют небольшие размеры, клеточную стадию деления (профаза 1-го мейотического деления), низкую метоболическую активность, отсутствие zona pellucida, монослой клеток гранулезы. Это, очевидно и определяет устойчивость популяции данных клеток к действию криоповреждения.
Заключение Проведенные исследования показали, что процентное соотношение морфологически нормальных фолликулов в витрифицированной группе с использованием 5М PROH было выше, чем 4,5 DMSO. Криоконсервация овариальной ткани позволяет сохранить примордиальные и первичные фолликулы содержащимися в них незрелых ооцитов (примордиальные и первичные фолликулы). Для оплодотворения такие фолликулы должны пройти стадию созревания in vivo или in vitro. Поэтому в будущем не исключается возможность использования метода in vitro культивирования овариальных фолликулов из криоконсервированных фрагментов ткани яичника для всестороннего исследования размороженных образцов.
Литература
- Hovatta O. Methods for cryopreservation of human ovarian tissue//Reproductive 2005. - Online Vol.10.-P. 729–734.
- Isachenko V, Isachenko E, Reinsberg J, Montag M, van der Ven K, Dorn C,Roesing B & van der Ven H. Cryopreservation of human ovarian tissue: comparison of rapid and conventional freezing// Cryobiology. – 2007. – Vol. 55.- Р. 261–268.
- Jin S, Lei L, Shea LD, Zelinski MB, Stouffer RL & Woodruff Markers of growth and development in primate primordial follicles are preserved after slow cryopreservation // Fertility and Sterility. - 2010. – Vol. 93.- Р. 2627–2632.
- Li YB, Zhou CQ, Yang GF, Wang Q & Dong Y. Modified vitrification method for cryopreservation of human ovarian tissues//Chinese Medical Journal. –2007.- Vol.120.–Р. 110– 114.
- Huang , Mo Y., Wang W., Li Y., Zhang Q. & Yang D. Cryopreservation of human ovarian tissue by solid-surface vitrification// European Journal of Obstetrics, Gynecology, and Reproductive Biology. – 2008. – Vol.139. – Р.193–198.
- Быстрова О.В., Калугина Ф.С., Цыбатова Е.В. Способы восстановления фертильности у онкобольных // Практическая онкология. Т.10. № 4. С. 245–253.
- Huang , Mo Y., Wang W. et al.Criopreservation of human ovarian tissue by solid- surface vitrification //Eur J Obstet Gynecol Reprod Biol. 2008. V. 139. № 2. Pp. 193–198.
- Vajta G. Are programmable freezers still needed in the embryo laboratory? Review on vitrification Reproductive Biomedicine. -2006. -Online Vol.12. –Р.779–796.
- Wang X, Catt S, Pangestu M & Temple-Smith P. Live offspring from vitrified blastocysts derived from fresh and cryopreserved ovarian tissue grafts of adult mice//Reproduction.- 2009.- Vol.138.- Р.527–535.
- Fatehi R., Ebrahimi B., Shahhosseini M., Farrokhi A., Fathi R. Effect ovarian tissue vitrification method on mice preantral follicular development and gene expression//Theriogenology 81. –2014.- Р.302–308.
- Deng X., Zheng H., Yu X., Yu H., Zhang C., Chao L., Li R. & Liu W. Cryopreserved ovarian tissues can maintain a long-term function after heterotopic autotransplantation in rat// - 2009.- Vol.138.- Р.519–525.
- Gandolfi , Paffoni A., Papasso Brambilla E., Bonetti S., Brevini TAL & Ragni G. Efficiency of equilibrium cooling and vitrification procedures for the cryopreservation of ovariantissue: comparative analysis between human and animal models// Fertility and Sterility. – 2006. – Vol.85.- Р.1150–1156.
- Santos R.R., Tharasanit T., Van Haeften T., Figueiredo J.R., Silva J.R. & Van den Hurk R. Vitrification of goat preantral follicles enclosed in ovarian tissue by using conventional and solid-surface vitrification methods//Cell and Tissue – 2007. - Vol.327. – Р.167–176.
- Al-aghbari A.M. & Menino A.R. Survival of oocytes recovered from vitrified sheep ovarian tissues//Animal Reproduction Science. – 2002. – Vol. 71.- Р.101–110.
- Courbiere , Odagescu V., Baudot A., Massardier J., Mazoyer C., Salle B. & Lornage
- Cryopreservation of the ovary by vitrification as an alternative to slow-cooling protocols// Fertility and Sterility. – 2006. - Vol.86.- Р.1243–1251.
- Ting A.Y., Yeoman R.R., Campos J.R. & Zelinski M.B. Morphological and functional preservation of pre-antral follicles after vitrification of macaque ovarian tissue in a closed system//Hum.reprod. – 2013.- Vol.0.- Р.1–13.
- Keros V., Xella S., Hultenby K., Pettersson K., Sheikhi M., Volpe A., Hreinsson J. & Hovatta Vitrification versus controlled-rate freezing in cryopreservation of human ovarian tissue// Human Reproduction. – 2009.- Vol.24.- Р. 1670–1683.
- Zhou XH., Wu YJ., Shi J., Xia Y.X. & Zheng S.S. Cryopreservation of human ovarian tissue: comparison of novel direct cover vitrification and conventional vitrification//Cryobiology.– 2010. – Vol.60. – Р.101–105.