Авторами статьи проведены эксперименты по определению чувствиительности и специфичностиразрабатываемого метода ПЦР для диагностики пастереллеза.
Введение
Пастереллез – контагиозная инфекционная болезнь животных многих видов, характеризующаяся при остром течении септическими явлениями, крупозным воспалением легких, плевритом, отеками в различных областях тела, а при подостром и хроническом течениях гнойно-некротизирующей пневмонией, поражением глаз, суставов, молочной железы и геморрагическим энтеритом [1, 2, 3].
По данным многих исследователей, пастереллез различных животных имеет широкое распространение и препятствует развитию отрасли [4, 5, 6, 7]. Известно, что в нашей стране в последние годы отмечается широкое распространение пастереллеза сайгаков, увеличение очагов инфекции, что обостряет эпизоотическую ситуацию по этому заболеванию [8, 9]. Циркулирующие в природе возбудители участвуют в эпизоотологии болезни сельскохозяйственных животных, поэтому мониторинг природных очагов бактериальных патогенов является одной из основных мер предотвращения эпизоотий зооантропонозов.
По мнению многих ученых, микроб проявляет себя от крайне ослабленного при пастереллоносительстве до сильновирулентного возбудителя болезни, так как обычно вызывает опустошительные эпизоотии, нанося чрезвычайный ущерб [10,11,12]. От безысходности в такой ситуации большинство исследователей склонны утверждать причиной в основе развития пастереллеза различные предрасполагающие факторы, особенно метеофакторы, прежде всего температуру и влажность окружающей среды, снижающие естественную резистентность макроорганизма. Однако с внезапным появлением и очень быстрым ("молниеносным") развитием заболевания обычно первыми гибнут самые активные, упитанные и сильные животные. Издавна так называемый "парадокс вирулентности" возбудителя пастереллеза, когда в природе восприимчивые организмы заражаются легко и быстро, а в экспериментах при естественных путях инфицирования далеко не всегда возможно вызвать заболевание [13], не находит точного объяснения. При этом известно, что утрата ила же восстановление вирулентности и, как правило, капсулы, капсульного антигена (К-антигена), а также иммуногенности пастерелл сопровождается диссоциацией их микробной клетки, выявляемой по изменению колоний (S-, М-, R- формы и SR- или RS- переходные формы) [14]. Условия этого процесса, особенно по части восстановления биологических свойств пастерелл, почти не изучены. Однако в целях своевременного диагностирования зачастую необходима оперативность, поэтому наиболее востребованными на сегодняшний день является молекулярногенетические методы, прежде всего потому, что направлены непосредственно на изучение вирулентность ДНК капсульных антигенов микроорганизмов, присутствующих в организме животных, что позволяет своевременно и с высокой точностью оценить эпизоотологическую ситуацию в животноводстве.
Наличие фундаментальных исследований нуклеиновых кислот пастерелл, а также работ по геносистематике этих организмов позволяет сделать вывод о возможности применения методов биотехнологии для решения проблем, связанных с пастереллезом [15].
Одним из главных достоинств ПЦР является чрезвычайно высокая чувствительность и специфичность. После определения основных параметров разрабатываемого метода ПЦР для диагностики пастереллеза животных, были проведены эксперименты по определению чувствительности и специфичности данного метода.
Материалы и методы исследований
Работа выполнялась в 2014-2015 гг. в лаборатории противобактериозной биотехнологии Казахского национального аграрного университета, в учебно-научно- диагностической лаборатории Казахстанско-Японского инновационного центра.
Выделение нуклеиновых кислот из штамма Pasteurella multocida 90 проводили с помощью коммерческих наборов PureLink Genomic DNA Mini Kit. Набор предназначен для выделения геномной ДНК с высоким выходом и чистотой из самых разнообразных типов образцов. Набор позволяет выделять геномную ДНК из крови, тканей, клеток, слюны, бактерий, мазков и пятен крови, формалин-фиксированных парафиновых тканей (FFPE).
Метод выделения основан на фиксации ДНК на кремневой основе в центрифужной пробирке. Для выполнения выделения ДНК требуется выполнение этапов центрифугирования. Набор включает все необходимые реагенты, буферы для промывок, протеиназу К, РНКазу, колонки и пробирки.
Ход работы: Бактериальную суспензиюпастерелл центрифугировали. Затем ресуспендировали клеточный осадок в 180 мкл PureLink™ буфером. Добавили 20 мкл Протеиназы К для лизирования клетки. Все хорошо перемешивали кратким встряхиванием. Инкубировали пробирку при 55°С, периодически встряхивая на вортексе до лизиса (от 30 минут до 4 часов). Добавили 20 мкл RNase А к лизату, хорошо перемешали с помощью вортекса и инкубируют при комнатной температуре в течение 2 минут. Добавили 200 мкл PureLink™ GenomicLysis/BindingBuffer и хорошо перемешивали на вортексе, чтобы получить гомогенный раствор. Добавили 200 мкл 96-100% этанола к лизату. Все хорошо перемешали путем встряхивания в течение 5 секунд для получения гомогенного раствора. Далее очистку ДНК произвели по протоколу набора.
В наших экспериментах для выявления чувствительности ПЦР использовали различные разведения ДНК бактерии от 500 нг до 0,05 пг.
Для определения специфичности ПЦР использовали штаммы Escherichia coli, Salmonelladublin, Salmonella typhimurium, Listeria monocitogenes, Brucella abortus, Mycobacterium bovis, Mycobacterium paratuberculosis, Lysteria monocytogenes. В качестве положительного контроля при постановке ПЦР использовали ДНК Pasteurellamultocida штамм 90, в качестве отрицательного контроля использовали деионизированную воду.
Полимеразную цепную реакцию проводили в амплификаторе Еppendorf (Германия) серии «Mastercyclernexus», ранее описанными условиями амплификации.
Результаты исследования и их обсуждение
В работе Nagai S, чувствительность метода ERIC-ПЦР для диагностики пастереллеза с использованием праймеров на участок toxA гена достигала всего 25 пг. Порог чувствительности метода геномных «отпечатков пальцев» ПЦР в работах индийских ученых составил 1-10 фг. Чувствитеьность метода геномных «отпечатков пальцев» на порядок выше. Метод ПЦР разработанный Saxena MK, etal.при диагностике пастереллеза позволяет выявлять ДНК пастерелл в количестве 500 нг-50 фг в пробе.
Таким образом, по литературным данным, порог чувствительности различных модификаций метода ПЦР для выявления ДНК Pasteurella multocida варьирует в пределах 50 пг-50 фг.
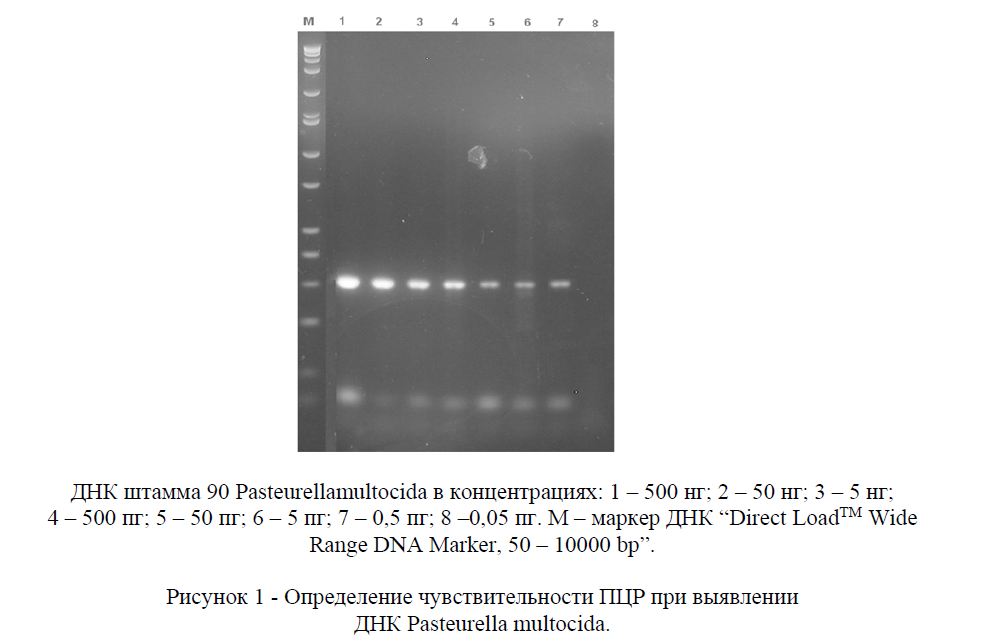
Как видно из рисунка 1 чувствительность метода ПЦР составила 0,5 пг ДНК Pasteurella multocida в пробе. Результаты экспериментов показали, что отработанный метод ПЦР обладает высокой чувствительностью.
Результаты наших исследований по определению чувствительности не уступают аналогичным работам зарубежных ученых. Значение порога чувствительности 0,5 пг в пробе и сокращение времени проведения диагноза повышают диагностическую ценность отработанного метода.
Результаты исследований по определению специфичности ПЦР показал, что ПЦР- продукт размером 372 п.о. нарабатывался только в пробах, содержащих ДНК Pasteurella multocida.
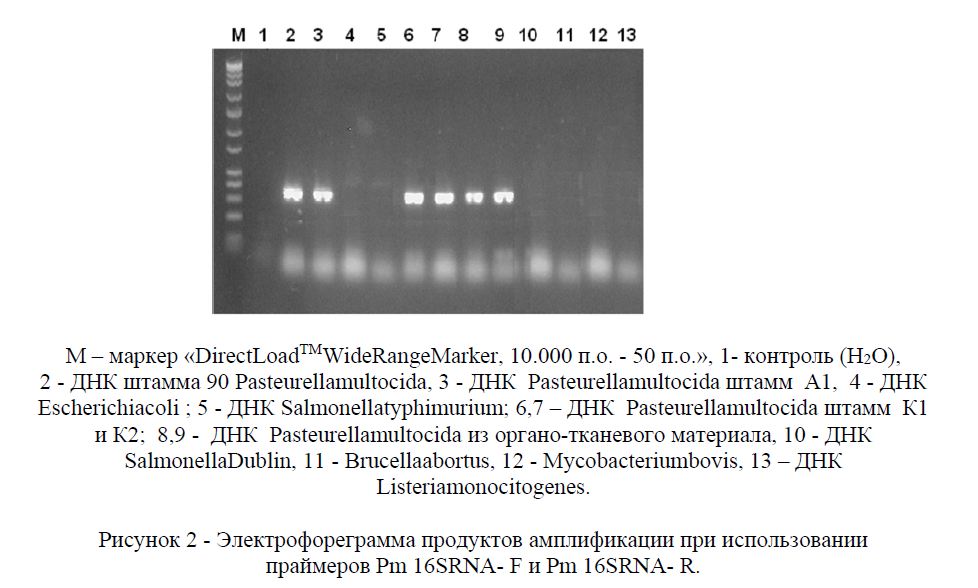
Как видно из рисунка 2 только в пробах, содержащих ДНК Pasteurellamultocida нарабатываются специфические продукты реакции размером около 372 п.о. (2-4, 9, 11-14). Отрицательные результаты были получены при использовании в качестве матриц ДНК Escherichia coli (4), Salmonella typhimurium (5), Listeria monocitogenes (13), Mycobacterium bovis (12), а также при использовании в качестве матриц ДНК Salmonella Dublin, Brucella abortus. Отсутствие каких-либо продуктов амплификации наблюдается и с деионизированной водой (1).
Выводы
Таким образом, результаты проведенных экспериментов показывают высокую чувствительность и специфичность разработанного метода ПЦР.
Литература
- Шегидевич Э.А., Федотов В.Б., Крючков В.Я. Серотиповой состав Пастерелламультоцида // Труды ВИЭВ. – М., 1983. – Т. – С.15-19.
- Масимов К.А. Значение пастерелл (Р.multocida) при остром респираторном синдроме парагриппа-3 у телят в откормочных хозяйствах промышленного типа: автореф...канд. вет.наук. – М., 1982. – 29 с.
- Gautam R., Kumar A.A., Singh V.P., Singh V.P., Dutta T.K., Shivachandra S.B. Specific identification of Pasteurellamultocida serogroup-A isolates by PCR assay// Res Vet Sci.- 2004. – Vol.3. –Р.179-85.
- Масимов Н.А. Пастереллез животных: Лекция // Моск. Гос. Акад. вет. медицины и биотехнологии им. К.И.Скрябина. – М., 1995. – 12с.
- Сосов Р.Ф. Пастереллез // Эпизоотология. - М.:Колос, 1974. - С.4-5.Rapports. de L| Office Inretnational des EpisootiesSessingenerale de mai,1979.- Р. 12-14.
- Джупина С.И., Колосов А.А. Особенности эпизоотологии, клинического проявления и диагностики пастереллеза в Новосибирской области // Профилактики и лечение болезней крупного рогатого скота. - 1992. - № - С.15-22.
- Салимов В.А., Жаров А.В. // Ветеринария. - 2007.-№ – С. 14 -15.
- Намет А.М. Иммунопрофилактика пастереллеза лошадей: автореф. докт. вет. наук. –Алматы, 2006. –3 с.
- Кожаев А.Н. Поливалентная вакцина против пастереллеза сельскохозяйственных животных: автореф. … канд. вет. наук. – Алматы, 2008. – 3 с.
- Борисенкова А.Н. Рекомендации по диагностике, профилактике и мерам борьбы с пастереллезом птиц: технологические процессы // Госагропром СССР. ВНИВИП. - Л., - 25 с.
- Пустовит Г.Л., Федотов Н.И., Кучеренко Л.А. Некоторые особенности эпизоотологии и течения пастереллеза свиней // В кн.: Инфекционные и инвазионные болезни с.-х. животных и птиц. – Одесса, 1983. – С.15-18.
- Луницын В.Г. Пастереллоносительство у пантовых оленей, некоторых видов грызунов и птиц в Горном Алтае // НИИ пушного звероводства и кролиководства. – – Т. 30. – С.160-168.
- Чоенбаев З.Н., Сарымсаков Е.С. О заболеваемости лошадей пастереллезом // Профилактика и меры борьбы с инфекционными и незаразными болезнями с.-х. животных в Казахстане. – Алма-Ата, 1984. – С.137-140.
- Meijer A., Kwakkel G.J., DeVries A., Schouls L.M., Ossewaarde J.M. Species Identification of Pasteurellamultocida by Analysing Restriction Fragment Length Polymorphism of the 16S – 23S rRNA Spacer Region.// J ClinMicrobiol. - 1998. . Vol. 37. - Р. 87 -
- Ralph D., McClelland M. Arbitrary Primed PCR Methods for Studying Bacterial Molecular Bacteriology.Protocols and Clinical Applications. Totowa: Humana Press. - 1998. - Р. 83 - 102.