В данной работе объектом исследований являлись семена, цветы, листья, стебли, т.е. вся наземная часть растения Alhagi pseudalhagi (верблюжья колючка), собранные в фазу цветения (май) и плодоношения (сентябрь) в окрестностях города Шымкента. Лекарственные свойства верблюжьей колючки известны давно, однако в официальной медицине она практически не применяется, так как до сих пор не выявлено действующее начало этого растения и не проведены соответствующие испытания его фармакологической активности.
Введение
Флавоноиды растений в последнее время становятся объектом пристального внимания ученых в связи с тем, что они, как показывают медико – биологические исследования, являются сильнодействующими физиологически активными веществами [1]. Известно, что многие димерные производные проявляют более высокое физиологическое действие, чем исходные соединения, в частности, очень эффективно, с этой точки зрения, соединение ароматических колец в полициклическую систему: дифенил более физиологически активен, чем бензол, фенантрен и антрацен – чем дифенил, многие бифлавоноиды – чем исходные флавоноиды [2,3,4]. Практический интерес представляют продукты димеризации флавоноидов, которые, судя по литературным данным, достаточно легко получить электрохимическим синтезом и которые имеют высокие характеристики физиологической активности. Наиболее детально процесс электрохимической димеризации, его механизм и кинетика описаны в работе [5], где определены оптимальные условия синтеза и даны рекомендации для подбора условий проведения процесса.
Цель работы
Цель проведенных в представленной работе экспериментов - добиться максимальной се- лективности процесса электродимеризации, получить димеры на основе ороксилина, 3- метилкверцетина, изорамнетина и кемиферида - флавоноидов, выделенных из Alhagi pseudal- hagi с максимальным выходом и, по возможности, исследовать физиологическую активность полученных продуктов. Для этого было проведено 7 серий опытов по исследованию влияния различных факторов на процесс димеризации.
Результати исследований
Растворитель и фоновый электролит выполняют очень важную функцию в электрохимическом эксперименте. Применение неводных растворителей значительно расширило разнообразие возможных электрохимических реакций, так как многие соединения окисляются (или восстанавливаются) труднее, чем вода и поэтому могут быть модифицированы в более широкой области потенциалов.
Таблица 1.Факторы, влияющие на процесс димеризации
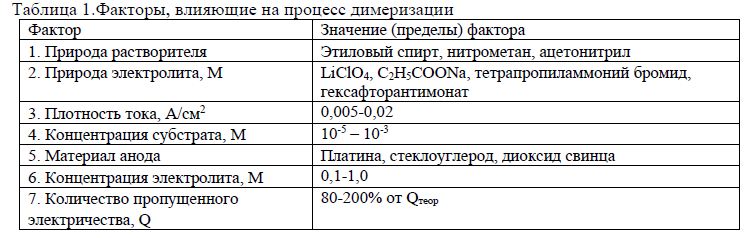
Чтобы избежать экспериментальных трудностей, подбирали растворители с высокой диэлектрической постоянной, которые при температуре опыта находятся в жидком состоянии, с низким давлением пара, полярные и неполярные, протонные и апротонные. При выборе электролита учитывали такие его свойства, как растворимость, электрохимическая и химическая инертность. Результаты опытов по изучению влияния природы растворителя и электролита представлены в таблице 2.
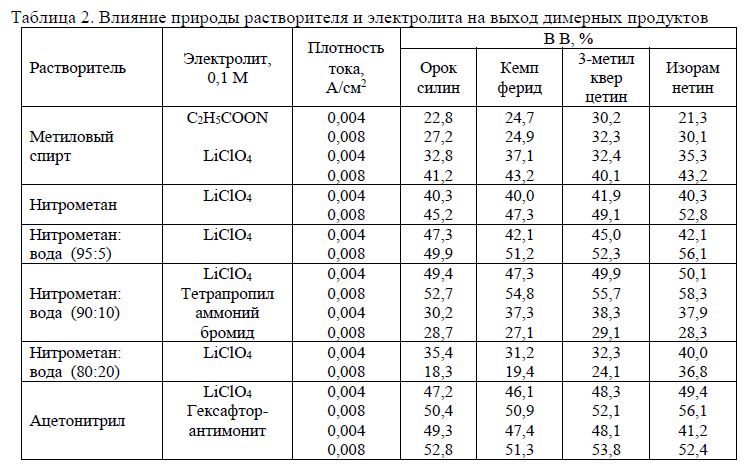
Из представленных результатов следует, что наименьшие выходы получены в среде метилового спирта, так как здесь наряду с основной реакцией протекают побочные реакции метоксилирования и образования димерных метоксипроизводных. Более приемлемыми следует считать растворители нитрометан и аценонитрил с добавкой LiCIO в качестве электролита. Низкие выходы в присутствии тетрапропиламмония объясняются тем фактом, что все галогениды достаточно легко окисляются в анодной области и потому возможно протекание побочных реакций.
В хорошем соответствии с данными поляризационных исследований и изучения физико- химических свойств флавоноидов находятся результаты по изучению влияния количества воды в составе реакционной среды на выход: с повышением содержания воды от 0 до 10% выходы димерных продуктов возрастают на 7-10%, достигая максимум при содержании воды 10%, при этом механизм окисления флавоноидов не меняется, число электронов на каждой стадии приблизительно равно 1.
При содержании воды 20% и выше выход целевых продуктов резко снижается, на вольтамперных кривых наблюдается резкий рост тока, количество электронов возрастает на каждой стадии до 3-5, что говорит о смене механизма реакции. При этом образуется большое количество смолообразных продуктов. Поэтому для дальнейших исследований выбрали систему нитрометан : вода (90 : 10) ∙ LiCIO.
Таблица 2. Влияние природы растворителя и электролита на выход димерных продуктов
При внедрении результатов многих электрохимических синтезов в производство возникает сложная проблема – рациональный подбор электродных материалов, свойства которых определяют направление, скорость, экономику и конструктивное оформление этих процессов. К свойствам анодных материалов предъявляются особо сложные, порой трудно совместимые требования: каталитическая активность, устойчивость при анодной поляризации и в окислительных средах, высокая электропроводность, хорошие механические свойства и, желательно, невысокая стоимость. Всем этим требованиям, кроме последнего, удовлетворяют аноды из группы платиновых металлов, которые по каталитическим, электрохимическим и коррозионным свойствам значительно превосходят все остальные. Однако их дороговизна и дефицитность обуславливают необходимость подбора более дешевых материалов, обладающих, тем не менее, вышеперечисленными свойствами.
В таблице 3 представлены результаты исследований влияния материала анода на выход димерных продуктов при электроокислении флавоноидов.
Таблица 3. Влияние материала анода на выход димерных продуктов электроокисления флавоноидов в среде нитрометан : вода (90:10) + 0,1 М LiClO4
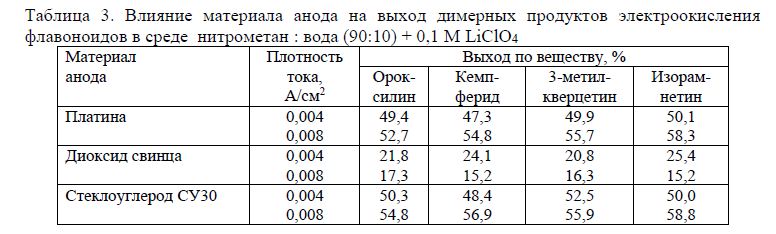
Из полученных данных видно, что на диоксиде свинца выходы димерных продуктов самые низкие. Для объяснения этого факта был исследован состав побочных продуктов электроокисления флавоноидов: оказалось, что на диоксиде свинца с высокой эффективностью идет реакция гидроксилирования. Это объясняется наличием на поверхности РbО2 активных частиц ОНадс, которые легко вступают в реакцию с радикалами флавоноидов с образованием гидроксипроизводных; причем, чем выше плотность тока, тем легче они образуются.
После изучения влияния всех факторов и математической оптимизации процесса по методу Розенборка выход димеров составил: 8-8-биороксилина - 67,4%, 8-8-бикемпферида - 69,5%, 8-8-би-3 метилкверцетина - 67,8%, 8-8-биизорамнетина -75,4%.
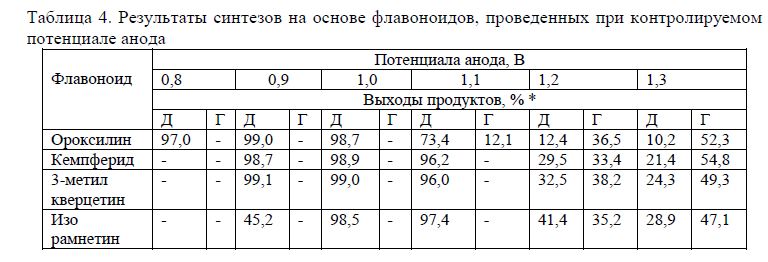
В результате проведения математической оптимизации процесса димеризации и экспериментальной проверки полученных результатов выход димерных продуктов достиг в среднем 70%. С целью повышения выхода, а также для наработки данных для составления схемы реакции был проведен ряд синтезов при контролируемом потенциале анода. Полученные результаты представлены в таблице 4.
Таблица 4. Результаты синтезов на основе флавоноидов, проведенных при контролируемом потенциале анода
Выводы
В КазНИИ онкологии и радиологии (Алматы) проведены медико-биологические испытания синтезированных соединений на белых беспородных мышах, 8-8-би-3- метилкверцетин в дозе 320 мг/кг дает высокие показатели радиопротекторного действия: процент выживаемости составил 81,3 при средней продолжительности жизни 17,7 дня, ФИД- 2,3, доза 80 мг/кг обусловила 50% выживаемости при средней продолжительности жизни 13,1 дня, ФИД-1,4.
Литература
- Синельников Н.А. Лекарственные растения. - М.:Медицина.-1965, с.20
- Балжай А., Шутый З.У. Фенольные соединения растительного происхождения.- М.: Мир, 1977-375с.
- Борлоу Р. Введение в химическую фармакологию. - М., 1987.-173 с.
- Халецкий А.М. Фармацевтическая химия. - Л.: Медицина, 1998.- 423 с.
- Надиров К.С. Электросинтез на основе госсипола, лагохилина и некоторых флованоидов // Диссертация на соискание ученой степени док.хим.наук. Алматы: ИОКЭ, 2000. 269с.