В данной статье представлены результаты исследований по определению оптимальных параметров культивирования рекомбинантных штаммов A/NYMC X-217 (H3N2) и B/NYMC BX-49 вируса гриппа в куриных эмбрионах. Установлено, что максимальное накопление вирусов отмечается при следующих условиях культивирования: возраст куриных эмбрионов - 9-11 суток при заражении в аллантоисную полость, заражающая доза вируса – 1000-10000 ЭИД50, температура и продолжительность инкубации – (34 ± 0,5) ºС и 48 часов, соответственно. При соблюдении указанных параметров культивирования можно стабильно получать высокоактивный вируссодержащий материал с инфекционной и гемагглютинирующей активностью, а также содержанием гемагглютинина не менее 7,0 lg ЭИД50/см3, 1:256 и 7,0 мкг/мл, соответственно, что вполне пригодно для приготовления трехвалентной инактивированной сплит-вакцины против сезонного гриппа.
Введение
В течение весьма длительного времени грипп остается серьезной проблемой для здоровья людей, вызывая ежегодные эпидемии, во время которых заболевает до 10% всего населения планеты, а во время возникающих время от времени гриппозных пандемий это число может возрастать в 4-6 раз. Кроме того, практически все эпидемии гриппа сопровождаются увеличением смертности [1]. Гриппозные эпидемии наносят экономический ущерб, исчисляемый в миллиардах долларах США.
Основной стратегией борьбы против гриппа является вакцинация. В настоящее время в мировой практике вакцинопрофилактики применяются три типа инактивированных вакцин: цельновирионные вакцины, расщепленные (сплит) вакцины и субъединичные вакцины. ИЗ этих трех видов гриппозных вакцин, цельновирионная вакцина содержит весь набор антигенов актуальных штаммов вирусов гриппа, иммуногенность их высокая, но из-за большого количества антигенов в их составе эти вакцины самые реактогенные и процент возникновения нежелательных реакций после их введения максимальный. Поэтому эти вакцины имеют возрастные ограничения к использованию. Субъединичная вакцина содержит только поверхностные антигены (НА и NА) вирусов гриппа, что обеспечивает хорошую иммуногенность и минимум нежелательных реакций на ее введение (аллергия к компонентам вакцины, например, к белку куриных яиц) [2]. Сплит-вакцины характеризуются значительно меньшим риском побочных реакций, предположительно в связи с разрушением пространственной структуры вируса. Преимущество сплит-вакцин в том, что они содержат как наружные, так и внутренние антигены вируса гриппа, при этом они избавлены от самого главного недостатка цельновирионных вакцин – наличия токсинов. Сплит-вакцины можно применять детям с 6-месячного возраста, они рекомендованы для предотвращения гриппа у беременных женщин. По сути дела, сплит-вакцины представляют собой «золотую середину» в профилактике гриппа, поскольку по уровню побочных реакций аналогичны субъединичным вакцинам, а по иммунологической эффективности – цельновирионным. Профилактическая эффективность вакцин этого класса колеблется в интервале от 75 до 96%. Сплит и субъединичные вакцины можно использовать для вакцинации лиц с иммунными дефектами, беременных и кормящих женщин; допускается их введение на фоне иммуносупрессивной терапии [3].
Состав вакцин ежегодно меняется для того, чтобы обеспечить максимальную защиту от "дикого" вируса. В зависимости от прогнозов ВОЗ о том, какой тип вируса будет циркулировать в следующем сезоне, в вакцину включают разные антигены. Обычно в состав современных вакцин включают 3 вида вирусных антигенов – два вида типа А и один вид типа В.
До настоящего времени исследования, нацеленные на разработку сезонной трехвалентной гриппозной вакцины для здравоохранения, в Казахстане не проводились, и поэтому существует реальная угроза биологической безопасности страны в случае пандемии гриппа. В НИИПББ для решения данной проблемы, ведутся работы по созданию трехвалентной сплит-вакцины против сезонного гриппа. Отработка условий культивирования вакцинных вирусов с целью их накопления является важным шагом на пути разработки вирусных вакцин. Как известно куриные эмбрионы (КЭ) в настоящее время являются основным субстратом для культивирования гриппозных вирусов. Доказана высокая эффективность использования КЭ по сравнению с различными культурами клеток (MDCK, Vero, HeLa, ФЭК), позволяющих получить высокоактивное вирусное сырье, пригодное для производства инактивированных вакцин с избежанием дорогостоящей процедуры концентрирования [4]. Наилучшим образом адаптированные к этой системе штаммы ВГП дают в КЭ достаточно высокие титры (около 104-105 гемагглютинирующих единиц на 1 эмбрион). Кроме того, эмбрион, изолированный от внешней среды не требует создания специальных стерильных условий, что также повышает ценность их использования.
В отношении параметров культивирования вирусов гриппа (ВГ) в зависимости от штаммовой принадлежности и степени их адаптированности к биологической системе в литературе приводятся разноречивые данные. В большинстве своем, штаммы ВГ культивируются на КЭ в возрасте 10-13 суток, инфицируются в аллантоисную полость в дозах 100-10000 ЭИД50 и инкубируются при температурах 34-38 ºС. Как видно, регламенты культивирования штаммов ВГ в КЭ колеблется в достаточно широких пределах, что вынуждает многих производителей противогриппозных вакцин, определять параметры культивирования новых вакцинных штаммов вирусов гриппа с целью приготовления надежных и высокоэффективных вакцин [ 5, 6 ].
В этой связи целью настоящих исследований являлось определение оптимальных параметров культивирование рекомбинантных штаммов A/NYMC X-217 (H3N2) и B/NYMC BX-49 для получения высокоактивного вируссодержащего материала (ВСМ), необходимого для разработки технологии изготовления сезонной трехвалентной инактивированной сплит-вакцины против сезонного гриппа.
Материалы и методы
Вирусы гриппа и куриные эмбрионы. Для оптимизации культуральных свойств вирусов гриппа А и В использованы следующие штаммы вируса гриппа (согласно рекомендации ВОЗ);
- рекомбинантный штамм NYMC X-217 (NIBSC code: 12/100), полученный в NIBSC (Великобритания) методом обратной генетики из штаммов A/Victoria/361/2011 (H3N2) и А/PR/8/34 (H1N1), соотношение генов 6:2;
- рекомбинантный штамм NYMC BX-49 (NIBSC code: 11/244), полученный в NIBSC (Великобритания) методом обратной генетики из штаммов B/Texas/06/2011 (линия Ямагата) и BX-38-1P-1 (B/Lee/40-подобный высокоурожаемый реассортантный /Panama/45/90 PA и NS гены), соотношение генов 1:1:6, пассажный уровень 7, гемагглютинирующая активность 1:512;
- развивающиеся куриные эмбрионы (РКЭ) из АО «Алель Агро» (Алматинская область, Казахстан).
Оптимизация параметров культивирования вирусов. С целью определения дозы заражения рекомбинантных штаммов A/NYMC X-217 (H3N2) и B/NYMC BX (ВГ) инфицирование проводили в аллантоисную полость КЭ в дозах от 1 до 1000000 и от 1 до 100000 ЭИД50, соответственно..
Для определения оптимального возраста, температуры и сроков инкубирования инфицированных КЭ заражали 9, 10, 11, 12, 13 - суточные КЭ в дозе 1000 ЭИД50 и инкубировали при температурах (32 ± 0,5) ºС, (34 ± 0,5) ºС, (36 ± 0,5) ºС, (38 ± 0,5) ºС в течение 24, 48, 72, 96 часов. Уровень накопления вируса оценивали путем титрования в КЭ, постановкой реакции гемагглютинации (РГА) и одиночной радиальной иммунодиффузии (ОРИД).
Определение инфекционной активности вирусов. Инфекционную активность определяли титрованием вируса в КЭ по общепринятому методу [7]. С этой целью готовили десятикратные разведения вирусной суспензии на физиологическом буферном растворе (ФБР) от 10-1 до 10-10. Каждым разведением вирусного материала заражали по 4 КЭ в аллантоисную полость по 0,2 мл. Культивирование КЭ проводили при температуре 34 ± 0,5 ºС, относительной влажности воздуха 55 ± 5%, в течение 2 сут. Наличие вируса в КЭ после охлаждения определяли капельным методом в РГА. Титр вируса вычисляли по методу L. Reed и H. Muench и выражали в log10 ЭИД50/мл согласно [8].
Определение гемагглютинирующей активности вирусов. Гемагглютинирующую активность вирусов определяли по общепринятой методике в РГА с использованием 1 % взвеси эритроцитов петуха [7].
Определение концентрации гемагглютинина в ОРИД. Определение концентрации гемагглютинина в ВСМ проводили методом одиночной радиальной иммунодиффузии (ОРИД) в соответствии с [9].
Статистическая обработка. Определяли среднеарифметические значения исследуемых параметров, а также их стандартную ошибку. Достоверность различий между показателями определяли с использованием статистической программы GraphPad Prism 6 (GraphPad Software, Inc., La Jolla, CA, USA). Значение Р < 0,05 считали значимым.
Результаты и обсуждения
Доза инфицирования КЭ. Для определения оптимальных параметров культивирования рекомбинантных штаммов A/NYMC X-217 (H3N2) и B/NYMC BX-49 вируса гриппа в КЭ проведены исследования по изучению уровня накопления вируса при различных дозах инфицирования. При этом использовали для штамма A/NYMC X-217 (H3N2) от 1 до 1000000 ЭИД50 и для штамма B/NYMC BX-49 от 1 до 100000 ЭИД50. Результаты проведенных исследований представлены на рисунке 1.
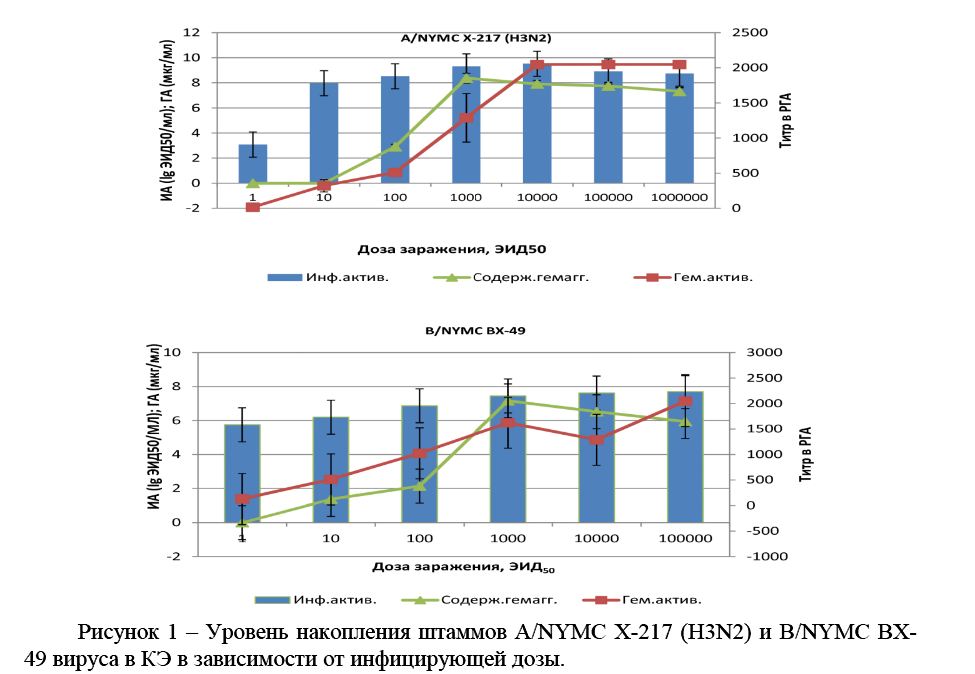
Рисунок 1 – Уровень накопления штаммов A/NYMC X-217 (H3N2) и В/NYMC BX- 49 вируса в КЭ в зависимости от инфицирующей дозы.
Из данных рисунка 1 видно, что штаммы A/NYMC X-217 (H3N2) и В/NYMC BX-49 со всеми испытанными дозами способны накапливаться в КЭ в достаточно высоких титрах. Максимальные значения инфекционной и гемагглютинирующей активности вируса были получены при использовании дозы для штамма A/NYMC X-217 (H3N2) в пределах от 1000 до 10000 ЭИД50 и В/NYMC BX-49 от 1000 до 10000 ЭИД50 при этом установлено зависимость уровня накопления вируса от дозы заражения. С увеличением дозы вируса от 1 до 10000 ЭИД50 (Р < 0,05) в КЭ отмечается рост титров как инфекционной и гемагглютинирующей активности, так и количественного содержания гемагглютинина. В дальнейшем с увеличением дозы заражения не наблюдалось роста инфекционной, гемагглютинирующей активности или содержания гемагглютинина. Так же установлена очень высокая степень корреляции между значениями титров вируса гриппа штаммов A/NYMC X-217 (H3N2) и В/NYMC BX-49 по РГА и ОРИД, коэффициент корреляции r = 0,9 и r = 0,8, соответственно.
На основании вышеизложенного, с учетом наивысшего значения инфекционной, гемагглютинирующей активности и содержания гемагглютинина в качестве оптимальной дозы заражения КЭ для штаммов A/NYMC X-217 (H3N2) и В/NYMC BX-49 принята доза в интервале 1000-10000 ЭИД50, так как дальнейшее увеличение дозы заражения не приводило к статистически достоверному (Р > 0,05) увеличению активности вируса. Полученные нами результаты согласуются с данными ряда авторов [10, 11, 12].
Температура инкубации вирусов. В следующих сериях опытов определяли уровень накопления штаммов A/NYMC X-217 (H3N2) и B/NYMC BX-49 вируса гриппа в зависимости от температуры инкубирования инфицированных КЭ. В опытах использовали 10 сут КЭ, которым вводили по 0,2 мл вируссодержащего материала из каждого штамма A/NYMC X-217 (H3N2) и B/NYMC BX-49 вируса гриппа в дозе 1000 ЭИД50. Дальнейшее культивирование вирусов проводили по методике, указанной в разделе «Материалы и методы». Инфицированные КЭ инкубировали при температурах 32, 34, 36, 38 ºС и относительной влажности воздуха (60 ± 5) % в течение 48 час. После инкубирование проводили сбор АЖ для определения инфекционной, гемагглютинирующей активности и содержание ГА.
Результаты проведенных исследований представлены на рисунке 2.
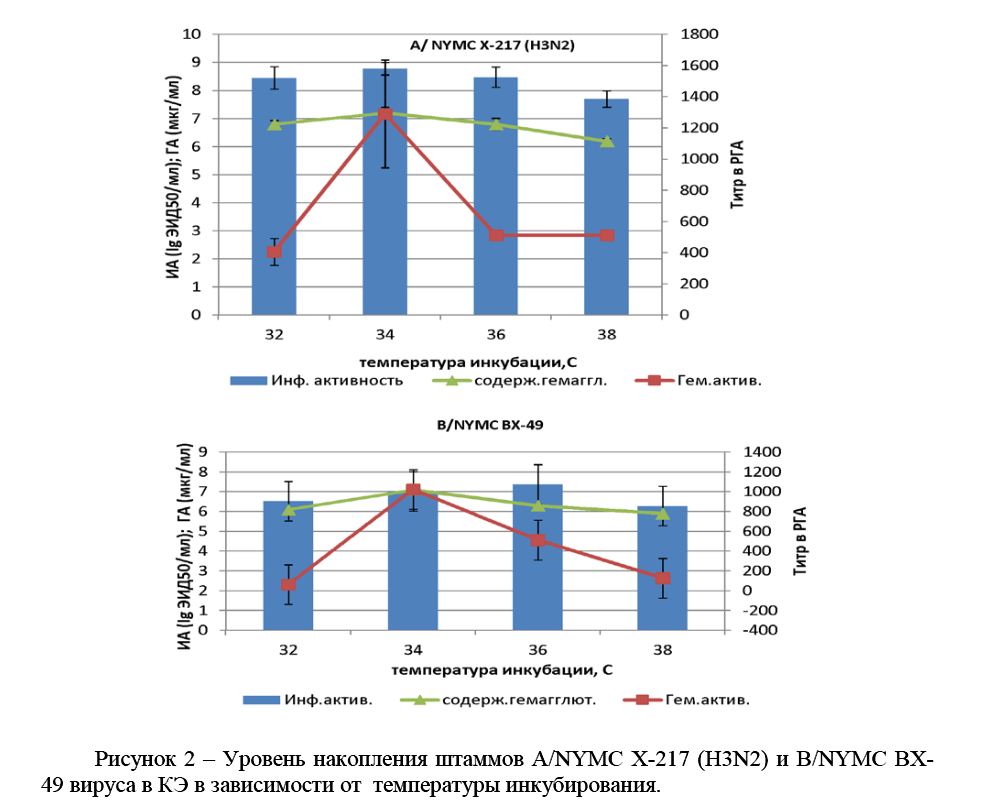
Рисунок 2 – Уровень накопления штаммов A/NYMC X-217 (H3N2) и В/NYMC BX- 49 вируса в КЭ в зависимости от температуры инкубирования.
Данные рисунка 2 свидетельствуют о высоком уровне репродукции штаммов A/NYMC X-217 (H3N2) вируса гриппа вне зависимости от температуры инкубирования. Статистический анализ показал достоверность результатов (Р < 0,05), максимальное накопление вируса происходит при температуре 34 °С и ориентируясь на экономичность и технологичность производственного процесса, в качестве оптимальной температуры инкубирования для штаммов A/NYMC X-217 (H3N2) и В/NYMC BX-49 вируса гриппа в КЭ выбрана температура (34 ± 0,5) °С. Корреляционный анализ показал что, средний коэффициент корреляции (r=0,6) отмечен между значениями титров РГА и ОРИД вируса гриппа штамма A/NYMC X-217 (H3N2) и очень высокий коэффициент корреляции (r=0,9) штамма В/NYMC BX-49. Исследуемые штаммы ВГ обладали высокой репродуктивностью в КЭ при температуре культивирования (34 ± 0,5) ºС, что согласуются с литературными данными [13,14].
Возраст КЭ для инфицирования. По данным, представленным в литературе [5, 6], и результатам собственных исследований на репродукцию вируса гриппа (ВГ), в определенной степени влияет возраст РКЭ. С целью определения уровня накопления вируса в зависимости от возраста КЭ нами проведены следующие серии исследований. С этой целью инфицировали КЭ 9, 10, 11, 12, 13 сут возраста в дозе 1000 ЭИД50. После инкубирования в течение 48 час при температуре (34 ± 0,5) °С проводили сбор АЖ и инфекционную активность вируса определяли методом титрования в КЭ, гемагглютинирующую активность вируса определяли в реакции гемагглютинации и содержание гемагглютинина определяли по методу ОРИД. Результаты проведенных исследований приведены в рисунке 3.
Рисунок 3 – Уровень накопления штаммов A/NYMC X-217 (H3N2) и В/NYMC BX- 49 вируса гриппа в РКЭ в зависимости от возраста КЭ.
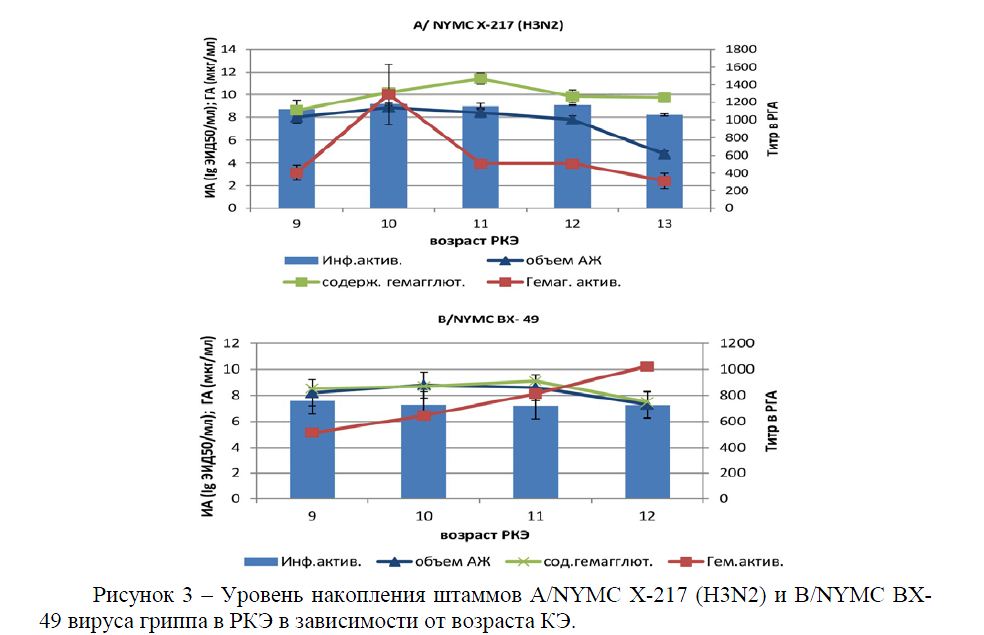
Из данных рисунка 3 следует, что уровень репродукции двух штаммов A/NYMC X- 217 (H3N2) и В/NYMC BX-49 вируса гриппа вне зависимости от возраста КЭ находится на высоком уровне: инфекционная активность от (7,20 ± 0,14) до (9,16 ± 0,12) lg ЭИД50/см3; гемагглютинирующая от 1:322 ± 86,42 до 1:1290 ± 345,45; содержание ГА от
(7,53 ± 0,9) до (11,43 ± 0,49) мкг/мл; достоверность результатов (Р < 0,05). При этом репродукция вируса в 12-13 сут КЭ приводит к снижению объема ВАЖ и к ухудшению ее качества. Показано очень слабая корреляция (r=0,2) между значениями титров ВГ по РГА и ОРИД штамма A/NYMC X-217 (H3N2) и слабая отрицательная корреляция (r=-0,5) между гемагглютинирующей активности и содержанием гемагглютинина. Таким образом, по результатам проведенных исследований для выращивания штаммов A/NYMC X-217 (H3N2) и В/NYMC BX-49 рекомендуются КЭ 9-11-сут возраста, что согласуется с литературными данными [10, 15, 16, 17].
Срок культивирования вирусов в КЭ. Заключительным этапом в исследованиях по оптимизации условий культивирования штаммов A/NYMC X-217 (H3N2) и B/NYMC BX- 49 вируса гриппа было определение оптимального срока культивирования вируса в КЭ.
Для этой цели КЭ 10-сут возраста инфицировали вирусами гриппа в дозе 1000 ЭИД50 и инкубировали при температуре (34 ± 0,5) °С. Через 24, 48, 72 и 96 часов инфицированные эмбрионы охлаждали при 4 ± 1 °С в течение 12 – 14 час и собирали АЖ для определения инфекционной, гемагглютинирующей активности и содержание ГА накопленного вируса. Результаты исследований представлены в рисунке 4
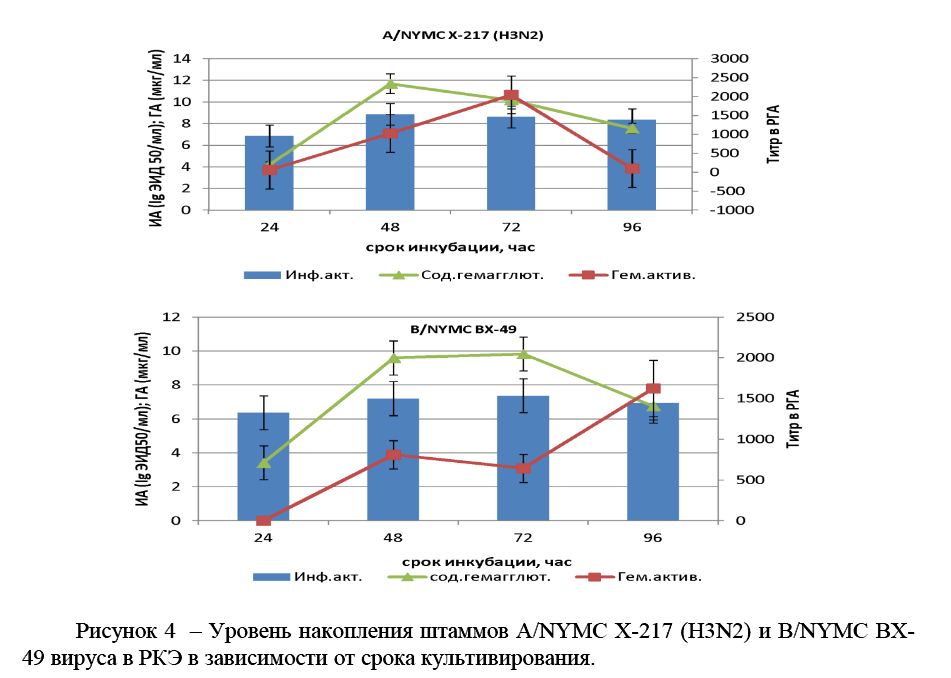
Рисунок 4 – Уровень накопления штаммов A/NYMC X-217 (H3N2) и В/NYMC BX- 49 вируса в РКЭ в зависимости от срока культивирования.
Из данных рисунка 4 видно, что при инфицировании 10-сут КЭ штаммами A/NYMC X-217 (H3N2) и В/NYMC BX- 49 наивысшее накопление вирусов отмечается на 48-96 ч инкубирования. Установлена средняя степень корреляции (r=0,7) для штамма A/NYMC X- 217 (H3N2) и слабая степень корреляции (r=0,3) для штамма В/NYMC BX - 49 между значениями титров ВГ по РГА и ОРИД. В целях сокращения продолжительности технологического процесса в качестве оптимального срока был выбран режим с 48 ч инкубации. На основе проведенного сравнительного анализа полученных результатов с данными научной литературы можно сделать вывод, что срок инкубирования 48 является оптимальной для вируса гриппа [10, 16].
Представленные результаты показывают, что при оптимизации параметров культивирования рекомбинантных штаммов A/NYMC X-217 (H3N2) и В/NYMC BX-49 вируса гриппа в КЭ достигнуты высокие показатели активности, которые не имели между собой значимой разницы. Наиболее значимым преимуществом нашей работы является определение накопления гемагглютинина в ОРИД в качестве дополнительного критерия оценки. ОРИД позволяет характеризовать качество инактивированной гриппозной вакцины (ИГВ) по концентрации ГА (в мкг/мл) в вакцинном препарате. В то же время ОРИД обладает большой точностью и воспроизводимостью, меньшей зависимостью результатов от условий постановки эксперимента, что позволяет охарактеризовать строго количественно все компоненты поливалентных гриппозных вакцин. Последнее обстоятельство чрезвычайно важно для практики производства и контроля ИГВ и их дальнейшего совершенствования [18]. Таким образом, было показано, что содержание гемагглютинина, определенная методом ОРИД, находится в пределах от 7,0 мкг/мл, что укладывается в допустимые ВОЗ пределы.
Таким образом, в результате проведенных исследований получены необходимые данные по оптимальным параметрам культивирования рекомбинантных штаммов A/NYMC X-217 (H3N2) и В/NYMC BX- 49. Следует отметить, что параметры другого рекомбинантного штамма NIBRG - 121хр (Н1N1), входящего в состав трехвалентной вакцины против сезонного гриппа, были установлены в наших ранних исследованиях [12].
Выводы
На основании проведенных исследований установлены оптимальные условия культивирования рекомбинантных штаммов A/NYMC X-217 (H3N2) и В/NYMC BX-49 в КЭ, включающие возраст КЭ, заражающую дозу вирусов, температуру и продолжительность инкубации, соблюдение которых позволяет получать вируссодержащую суспензию с инфекционной и гемагглютинирующей активностью не менее 7,0 lg ЭИД50/см3 и 1:256, соответственно, и содержанием ГА не менее 7,0 мкг/мл. Достигнутая активность вирусов достаточна для приготовления трехвалентной инактивированной сплит-вакцины против сезонного гриппа, отвечающей требованиям ВОЗ.
Литература
- Гендон Ю.З. Инактивированная расщепленная гриппозная вакцина Ваксигрипп // Вакцинация. – 2000. - № 11. – С. 12 –
- Петров Р.В., Хаитов Р.Н., Некрасов А.В., Иванова А.С., Пучкова Н.Г. Гриппозная вакцина нового поколения – Гриппол // Сборник трудов 5-го Конгресса «Современные проблемы аллергологии, иммунологии и иммунофармокологии». – Москва, 2002. - Т. 1, - С. 134-179.
- Таточенко В.К. О вакцинации против гриппа // «Лечащий Врач». -2001.- № 8 .- С. 10-12.
- Zhao X, Zhou D. Optimization of culture condition for cultivation of influenza virus A on MDCK cell // Wei Sheng Yan Jiu. - 2014;43(2):210-2.
- Кыдырбаев Ж.К., Табынов К.К., Мамадалиев С.М., Молдагулова Н.Б., Кожамкулов Е.М. Параметры культивирование вируса гриппа птиц А/домашний гусь/Павлодар/1/05 (H5N1) в куриных эмбрионах // Вестник сельскохозяйственной науки Казахстана. – 2007. - № 10. - С .49-51.
- Кыдырбаев Ж.К., Табынов К.К., Мамадалиев С.М., Рыскельдинова Ш.Ж. Параметры культивирование вируса гриппа птиц A/крачка/Южная Африка/61 (H5N3) в куриных эмбрионах для разработки инактивированной вакцины // Вестник Кыргызского НИИ животноводства, ветеринарии и пастбищ им. А. Дуйшеева. – Бишкек - № 1. - С. 243-248.
- 2002. WHO manual on animal influenza diagnosis and surveillance. Geneva: World Health Organization.
- Reed L J, Muench H. 1938. A simple method of estimating fifty percent endpoints. Am J Hyg, 27: 493–497.
- Palmer D F, Dowdle W R, Coleman M T, et 1975. Advanced laboratory techniques for influenza diagnosis. Immun Ser, 6: 25–45.
- Ершебулов З.Д., Абдураимов Е.О., Рыскельдинова Ш.Ж., Кыдырбаев Ж.К., Мамадалиев С.М., Кожамкулов Е.М., Табынов К.К., Асанжанова Н.Н., Жугинисов К.Д., Таранов Д.С. Определение оптимальных параметров культивирования рекомбинантного штамма А /Аstana RG/5:3/2009 // Биотехнология. Теория и практика. - 2010.- № 4. - С. 75 – 79.
- Кишкенбаева Д.О., Абдураимов Е.О., Жугунисов К.Д., Таранов Д.С., Ершебулов З.Д. Определение оптимальной условий культивирования изолята вируса гриппа лошадей выделенного в Жамбылской области // Вестник науки КазАту им. С.Сейфуллина.- -№ 2 (69).- С. 41- 49.
- Табынов К.К., Мамбеталиев М.А., Ажибаев А.Ж., Бурашев Е.Д., Азанбекова М.А. Оптимизация условий культивирования рекомбинантного штамма NIBRG-121хр вируса гриппа на куриных эмбрионах // Актуальные проблемы и перспективы биологической безопасности. - Гвардейский,2012. - С. 152-158.
- Егоров Ю., Медведева Т.Е., Полежаев Ф.И., Александрова Г.И., Гендон Ю.З. Особенности получения и характеристика холодоадаптированного варианта вируса гриппа А/PR/8/34 //Acta virol. – 1984. - 28:19-25.
- Табынов К.К., Мамбеталиев М.А., Булатов Е.А., Абсатова Ж.С., Копоченя А.А. Параметры культивирования референс-вируса гриппа NIBRG-121 на развивающихся куриных эмбрионах SPF // Тез. докл. междунар. конф.» Противогриппозные вакцины нового поколения». - Санкт-Петербург, 2009.- С. 78-79.
- Tabynov K, Kydyrbayev Z, Sansyzbay A, Khairullin B, Ryskeldinova S, Assanzhanova N, Kozhamkulov and Inkarbekov D. Immunogenic and Protective Properties of the First Kazakhstan Vaccine against Pandemic Influenza А (Н1N1) pdm09 in Ferrets // Virologica sinica. - 2012. - № 27 (6):345-352.
- Ewasyshyn E., Sabina L.R Allantoic fluid protease activity during influenza virus infection // Acta virol. – 1986. - 30:109-118.
- Wang Maoliang, Yan Jiaxin, lin Qiao sing mikropeptidnyh cards and monoclonal antibodies for analysis of antigenic variation of influenza A virus strains isolated in China from 1972 to 1983 // Acta virol. – 1986. - 30:97-102.
- Кастрикина Л.Н., Бижанов Г.И., Лонская Н.И., В.Ф. Попов В.Ф. Изучение стабильности инактивированной гриппозной вакцины в процессе хранения // Вопросы вирусологии. – 1990. - № 1. – С. 68-70.