В статье на основании литературных источников и собственных исследований приведены результаты исследований по выбору оптимального метода выделения ДНК Pasteurellamultocida из биологического материала.
В результате выбора оптимальных методов выделения ДНК Pasteurellamultocida из биологического материала, определили, что все использованные в работе методы выделения ДНК вполне приемлемы для экстракции геномной ДНК Pasteurellamultocida, но наибольшее количество ДНК выделено с помощью ФХЭ с гуанидином. Отношение оптической плотности (Е260/Е280) полученных препаратов ДНК Pasteurellamultocida имело средние значение 1,7 > 0,04. Несмотря на многоступенчатость и продолжительность анализа в сравнении с новыми высокочувствительными и простыми в исполнении методами выделения ДНК, этот метод является оптимальным для выделения аналитических количеств ДНК в случаях, когда нет большого потока исследований.
Введение
К настоящему времени в арсенале исследователей имеется довольно большой набор методов экстракции и очистки ДНК, причем эти методы продолжают совершенствоваться и модифицироваться применительно к новым объектам исследования. В связи с разнообразием живых объектов универсальных методов выделения ДНК не существует. Использование того или иного метода выделения ДНК диктуется, во-первых, спецификой изучаемого материала, а во-вторых, тем, какая преследуется цель: получение суммарной, ядерной, хлоропластной ДНК или других ее препаратов[1]. Метод выделения ДНК должен быть относительно простым, хорошо воспроизводимым и давать возможность быстрого получения достаточных количеств удовлетворительно очищенных препаратов ДНК. Выход ДНК зависит от природы исходного материала и обусловлен содержанием ДНК в данной ткани, а также наличием и характером примесей, препятствующих очистке ДНК. В любом случае ДНК должна содержать минимальное количество примесей полисахаридов и белков (не более 2—3%),что отражается на такназываемых спектральных характеристиках препаратов А260/А280 приблизительно равное 1,8.[2].
Целью и задачей наших исследований, являлось подбор оптимальных вариантов выделения ДНК Pasteurellamultocida из биологического материала.
Материалы и методы
Исследования проводились в лаборатории «Молекулярной биологии и генной инженерии вирусов» НИИПББ НЦБ РК, лаборатории противо бактериозной биотехнологии Казахского национального аграрного университета, филиале Костанайская НИВС.
- Метод фенол-хлороформной экстракции (ФХЭ) с предварительной обработкой протеиназой К. Клеточный осадок ресуспендировали в 300 мкл раствора № 1 (100 мМтрис-HCl рН 8,0, 10 мМ ЭДТА, 2 мг/мл лизоцима) и инкубировали 60 мин при 37°С. Добавляли 50 мкл раствора № 2 (8% додецилсульфат натрия (SDS) и 50 мкл протеиназы К (2 мг/мл). Хорошо перемешивали и инкубировали при 42°С 60 мин. Затем добавляли 200 мкл фенола и 200 мкл хлороформа, интенсивно перемешивали и центрифугировали 10 мин при 12 000 об/мин. Верхнюю фазу переносили в чистую пробирку, не затрагивая нижнюю фазу и интерфазу. Проводили повторную экстракцию 400 мкл хлороформа. К водной фазе добавляли 40 мкл ЗМ ацетата натрия (рН 5,4) и 800 мкл 96% этилового спирта, тщательно перемешивали. Инкубировали в течение ночи при — 20°С. ДНК осаждали центрифугированием 15 мин при 12 000 об/мин. Осадок промывали 400 мкл 75% этилового спирта, сушили при 37°С в течение 15 мин и растворяли в 30 мкл воды[3].
- Метод фенол-хлороформной экстракции с гуанидином. К клеточному осадку добавляли 250 мкл лизирующего буфера (6 М GuHCl, 40 мМтрис-HCl рН 6,4, 36 мМ ЭДТА) и тщательно перемешивали. Смесь прогревали 5 мин при 65°С и добавляли 125 мкл фенола и 125 мкл хлороформа. Далее выделяли так же, как и при ФХЭ с протеиназой К.
- Метод сорбции ДНК на силикагеле. В пробирки емкостью 1,5 мл с клиническими образцами вносили по 250 мкл лизирующего раствора (6 М GuHCl, 40 мМтрис-HCl рН 6,4, 36 мМ ЭДТА) и тщательно перемешивали на вортексе. Прогревали пробирку 5 мин при 65°С, тщательно перемешивали на вортексе до полного растворения материала. Добавляли 20 мкл ресуспендированного на вортексе сорбента (Silica S-5631, "Sigma"), хорошо перемешивали и отстаивали 7—9 мин. Сорбент осаждали на микроцентрифуге в течение 30 сек. Отбирали супернатант и добавляли по 400 мкл отмывочного раствора (4 М GuHCl, 40 мМтрис-HCl рН 6,4), перемешивали на вортексе до полного ресуспендирования сорбента, осаждали на микроцентрифуге в течение 30 сек. и отбирали супернатант. Повторяли процедуру отмывки еще раз. Осадок промывали 70% этиловым спиртом и высушивали в термостате при 56°С в течение 10 мин. Добавляли 100 мкл элюирующего буфера (80 мМNaOH, 0,5 мМ ЭДТА), тщательно ресуспендировали и помещали в термостат при 56°С на 10 мин, затем добавляли 5,3 мкл раствора 1 М трис-HCl рН 6,4 и встряхивали на вортексе. Суспензию осаждали на микроцентрифуге при 10 000 об/мин в течение 1 мин. Супернатант содержал очищенную ДНК[4,5].
Выделение ДНК другим методом проводили с применением лизирующего буфера, содержащего гуанидина гидрохлорид. Авторы опубликованных в литературе протоколов используют разные хаотропные агенты, предпочтительно применяются гуанидинатиоционат (GuaSCN) или гуанидина гидрохлорид (GuaHCl), рекомендуемый диапазон рабочих концентраций которых от 1M до 4M для GuaSCN и 6-8M для GuaHCl[6].
Результаты исследований
При выборе оптимальных методов выделения ДНК Pasteurellamultocida, учитывали некоторые особенности строения бактериальной клетки. Стенки грамотрицательных бактерий, к которым относится Pasteurellamultocida, более сложные по химическому составу, чем у грамположительных, в них содержится значительное количество липидов, связанных с белками и сахарами в сложные комплексы — липопротеиды и липополисахариды.
В нашем исследовании мы сравнили несколько способов выделения ДНК Pasteurellamultocida.
В первых двух методах для удаления белков применяли комбинацию растворителей фенол – хлороформ, которая является сильным средством депротеинизации. При перемешивании клеточного лизата и фенола формируются две фазы. ДНК находится в верхней (водной) фазе, а денатурированные белки — в нижней (органической) фазе [6]. Водный экстракт переносится в чистую пробирку, и нуклеиновая кислота была осаждена 3М ацетатом натрия, с последующим промыванием осадка в спирте (100, 70% этанол).Методы с использованием фенол-хромосомной экстракции достаточно просты, недороги, обеспечивают стабильность препарата ДНК в процессе хранения, но их недостатком является тот факт, что фенол и хлороформ – токсичные соединения и требуют утилизации после использования[7].
В качестве лизирующих агентов использовали додецилсульфат натрия (SDS), ЭДТА и лизоцим. Анионные детергенты, к которым относитсяSDS в буферных растворах дезорганизуют двухслойные липидные образования мембран, разрушают нековалентные связи и стабилизируют белки, тем самым разрушаются липидно-белковые комплексы мембран, при этом ДНК экстрагируется в буфер [8]. Конечный размер получающихся фрагментов ДНК зависит от двух основных факторов: действия клеточных нуклеаз и механического разрушения ДНК в процессе выделения. Применение додецилсульфата натрия не только депротеинизирует бактериальную клетку, но также подавляет активность нуклеаз. ЭДТА и лизоцим разрыхляют наружную мембрану, ингибируют нуклеазы – разрушают клеточную стенку.
Клеточные белки удаляли обработкой протеолитическим ферментом – протеиназой К, который эффективно инактивирует нуклеазы, будучи устойчивым при этом к денатурирующим (SDS, мочевина), хелатирующим (ЭДТА) и сульфгидрильным агентам. Активация этого фермента более чем в 7 раз в присутствии мочевины и SDS обусловлена главным образом денатурацией белков-субстратов в этих условиях. Данная протеаза работает в широком диапазоне рН (4-12). Денатурирующие агенты повышают доступность пептидных связей белков для протеиназыК[9].
При выделении ДНК методом сорбции на силикагеле также использовали гуанидин гидрохлорид. Силиконовый матрикс связывает ДНК в присутствии высоких концентрацийхаотропных солей, таких как гуанидингидрохлорид, которые разрушают гидрофобные взаимодействия. По определению исследователей, метод имеет два преимущества: дешевизнасиликон диоксида и универсальность протокола для широкого приложения для очистки ДНК [10].1 мл/г силикон диоксида способен связатьдо 3-4,5 мкг ДНК и в таком состоянии стабильность ДНК сохраняется до 12 месяцев. Очевидно, что количество используемого силикагеля зависит от предполагаемого количестваДНК в исходном материале; ДНК отделяется от силикагеля при понижении концентрациисоли, а также быстрым центрифугированием (10 сек.); либо ДНК может быть отмыта небольшим объемом (от 5 мкл) воды, облегчить элюцию можно нагреванием. Предлагаемыйметод прост, быстр и экономичен, не требует специальных колонок и оборудования, чтоделает его привлекательным при большом объеме образцов в экспериментах. Силикагельвключается во многие коммерческие наборы экстракции ДНК.
Начальные условия были одинаковыми для всех методов, так как выделение проводилось из одного образца, разделенного на 6 равных частей. Для того чтобы свести к минимуму ошибку при наборе материала, исследование повторяли 3 раза и за количество ДНК принимали среднее значение.
После выделения ДНК Pasteurellamultocida вышеперечисленными методами проводили качественный и количественный анализ образца. Электрофорез проводили в 0,8 % агарозном геле в ТАЕ-буфере. Наибольшее количество ДНК выделяется с помощью ФХЭ с гуанидином и ФХЭ с предварительной обработкой протеиназой К. Отношение оптической плотности (Е260/Е280) полученных препаратов ДНК Pasteurellamultocida имело среднее значение 1,65 n=03,)0.Р4езу(льтат качественного анализа полученного препарата ДНК представлен на электрофореграмме (рисунок 1).
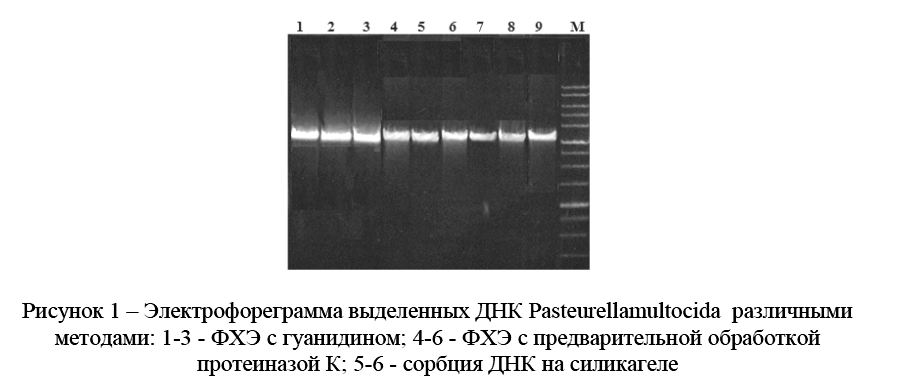
Рисунок 1 – Электрофореграмма выделенных ДНК Pasteurellamultocida различными методами: 1-3 - ФХЭ с гуанидином; 4-6 - ФХЭ с предварительной обработкой протеиназой К; 5-6 - сорбция ДНК на силикагеле
По чувствительности ФХЭ превосходит методы сорбции на силикагеле. Методы, основанные на ФХЭ, дают хороший выход ДНК, но очень трудоемки. Еще одним отрицательным фактором в них является токсичность фенола и хлороформа, что требует наличия вытяжного шкафа в лаборатории, где эти методы применяются.
В таблице 1 представлены результаты типичного эксперимента по выделению ДНК стабилизированной трилоном Б цельной крови молоднякакрупного рогатого скотаметодом ФХЭ с гуанидином (таблица 1).
Таблица 1 - Результаты выделения ДНК цельной крови крупного рогатого скота
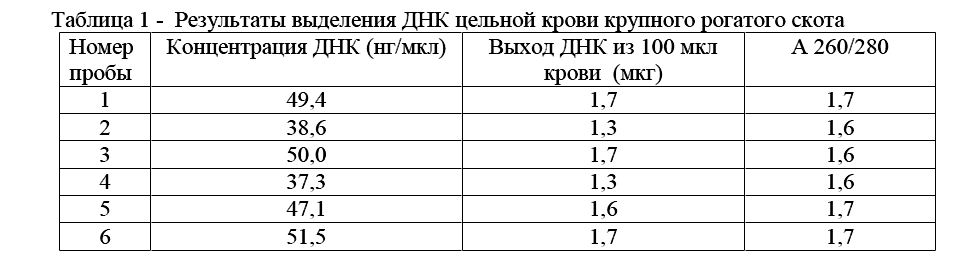
В данном эксперименте ДНК выделяли из 6-ти проб крови от разных животных. Выход ДНК варьировал в диапазоне 1,3 - 1,7 мкг из 100 мкл крови. Для определения чистоты выделенной ДНК её осаждали этанолом, растворяли в воде и определяли отношение оптических плотностей на 260 нм и280 нм с использованием спектрофотометра Pro RNA/DNA Calculator «GenQuant». Отношение А260/А280 близкое к 1,8 указывает на то, что ДНК обладает высокой чистотой.
Выводы
В результате исследований по выбору оптимальных методов выделения ДНК Pasteurellamultocida выяснили, что все использованные в работе методы выделения ДНК вполне приемлемы для экстракции геномной ДНКPasteurellamultocida, но наибольшее количество ДНК выделено с помощью ФХЭ с гуанидином. Отношение оптической плотности (Е260/Е280) полученных препаратов ДНК Pasteurellamultocida имело средние значение 1,7 > 0,04. Несмотря на многоступенчатость и продолжительность анализа в сравнении с новыми высокочувствительными и простыми в исполнении методами выделения ДНК, этот метод является оптимальным для выделения аналитических количеств ДНК в случаях, когда нет большого потока исследований.
Литература
- Ведерников В. Е. Сравнительная характеристика способов экстракции нуклеиновых кислот. Журнал "Лаборатория" №4,2012, с.14-15;
- Рябушкина Н., Омашева М.Е., Галиакпаров Н. Специфика выделения ДНК израстительных объектов. Биотехнология. Теория и практика. № 2, 2012.с. 13;
- Jose Antonio Amigot, Montserrat Torremorell, Carlos Pijoan «Evalution of techniques for the detection of toxigenic Pasteurellamultocida strains from pigs» Direct RAPD Evaluation of Bacteria without Conventional DNA Extraction// J. Clin. Microbial. - 2008. - 29 р.
- Евтыхова Е.Б., Мукантаев К.Н., ТурсуновК., Сытник И.И., Карибаев Т.Б., Хасенов Б.Б., ШустовА.Б. Метод выделения ДНК и тест-система ПЦР в реальном временидля диагностики лейкоза крупного рогатого скота. Биотехнология. Теория и практика. № 2 2012, С 78 -84.
- X., G. K. Nair, V. Jayaprakasan, M. MiniandT. V. Aravindakshan 2007. Nucleic acid based differentiation of Pasteurellamultocida serotypes. The Internet Journal of Veterinary Medicine, 2 (2): 85-89.
- Townsend, M., A. J. Frost, C. W. Lee, J. M. Papadimitriou and H. J. S. Dawkins, 1998. Development of PCR Assays for Species and Type-Specific Identification of Pasteurellamultocida Isolates. J. Clinical Microbiol., 36 (4): 1096–1100
- Hopkins B.A., Huang T.H.M. & Olson L.D. (1998). Differentiating turkey post- vaccination isolates of Pasteurellamultocida using arbitrarily primed polymerase chain Avian Dis., 42, 265-274.
- Kumar A. A, Shivachandra S. B, Biswas A, Singh V. P, Singh Vijendra P, Srivastava K (2004). Prevalent serotypes of Pasteurellamultocida isolated from different animal and avian species in India. Vet. res. Commun 28:657-667
- Townsend M., Dawkins H.J., Papadimitriou J.M. (1997). REP-PCR analysis of Pasteurellamultocida isolates that cause hemorrhagic septicemia. Res Vet Sci 63:151-5.
- Townsend, John Boyce, Jing Y. Chung, Alan J. Frost, and Ben Adler (2001). Genetic organization of Pasteurellamultocida cap loci and development of multiplex capsular PCR typing system. J. Clinical Microbiol., 39: 924-929.