Рассматриваются повышения жизнеспособности спящих зимующих почек груши при криоконсервации и снижения периода подготовки к замораживанию. Опыты по оптимизации методов криосохранения проведены с почками при естественной влажности и подсушенными до 30% содержания влаги. Испытано влияния криопротекторов и способов предобработки почек на жизнеспособность после замораживания. Выявлено следующие подходящие криопротекторы для замораживания и жизнеспособности спящих почек груши – PVS3, PVS4, ИББР-1.
Введение Одним из способов сохранения генофонда является криосохранение покоящихся почек древесных растений. При этом сводится к минимуму возможность возникновения сомаклональных вариантов, что важно, когда необходимо сохранить целостность клона с уникальной комбинацией генов, как в случае плодовых культур. Первое сообщение о замораживании веток древесных растений в жидком азоте было сделано Sakai в 1960 году. Ветки шелковицы (Morus), ивы (Salix) и тополя (Populus) были заморожены при сверхнизкой температуре без ущерба только в том случае если охлаждение проводилось медленно. Растительный материал до погружения в жидкий азот должен быть предварительно охлажден по крайней мере до -30°С [1,2]. Позже были разработаны методы, в результате которых отмечено от 80% до 100% восстановления жизнеспособности криоконсервированных покоящихся почек Malus, Amelanchier, Crataegus, Sorbus и Prunus. Методика была протестирована на других объектах, в том числе крыжовнике, смородине, шелковице, некоторых сортах яблони, абрикоса, черешни и вишни, персика и 11 других видах семейства Rosaceae [3]. Другим фактором является влажность почек перед замораживанием. В частности, высокая выживаемость почек яблони может быть достигнута при влажности 25-30% , а груши – около 41% [4].
Материалы и методы Для создания криобанка гермоплазмы использованы почки холодостойких древесных растений умеренного климата – груши. Закаленные холодом ветки растений, после снижения температуры окружающей среды до -10°С и ниже, обезвожены до содержания влаги 30% и затем заморожены со скоростью 1°С/час до – 25°С, оставлены при такой температуре на 24 часа, а затем погрузили в жидкий азот – 196ºС. Контроль размораживания проведена при комнатной температуре. Восстановление роста осуществлено методом окулировки глазка с почкой на подвой или микроклональным размножением размороженной почки на искусственных питательных средах. [5].
С целью повышения жизнеспособности при криоконсервации и снижения периода подготовки почек к замораживанию поставлен ряд экспериментов по оптимизации криосохранения спящих зимующих почек.
После снижения температуры окружающей среды до – 10ºС или ниже (январь, февраль), проведён сбор древесных черенков со спящими почками в Помологическом саду Института плодоводства и виноградарства.
Для проведения опытов по замораживанию спящих почек определяли влажность образцов во влагомере KERN MLB 50-3. Часть черенков были помещены для высушивания в климо камеру с температурой –5ºС до снижения влажности почек до 30%, потеря влаги определяется 2 раза в неделю. Другая часть черенков не было высушена. Опыты по оптимизации методов криосохранения проведены с почками при естественной влажности и подсушенными до 30% содержания влаги.
Рисунок 1 - Предобработка криопротекторами в криопробирках
Черенки нарезали на сегменты с одной почкой размером 2 см, расположенной в середине, и помещены в криовайлы (2-5 сегментов). Пакеты и криовайлы вынули из жидкого азота и перенесели на 24 часа в холодную комнату с температурой +4oC. Сегменты с почками достали из криовайлов, промыли дистиллированной водой и поместили в чашки Петри во влажную камеру на 2-5 суток.
Результаты исследований и обсуждение
В Зарубежных исследованиях показано, что покоящиеся почки акклиматизированных к холоду яблонь могут восстанавливать рост после криоконсервации с высоким процентом выживания (80-100%), при использовании метода контролируемого высушивания и медленного замораживания с последующим погружением в жидкий азот [6]. В наших исследованиях выявлено, что наиболее подходящие криопротекторы для замораживания спящих почек груши являются – PVS3, PVS4, ИББР-1 (жизнеспособность почек составила 100%), а также криопротектор Towill (жизнеспособность почек составила 66%).
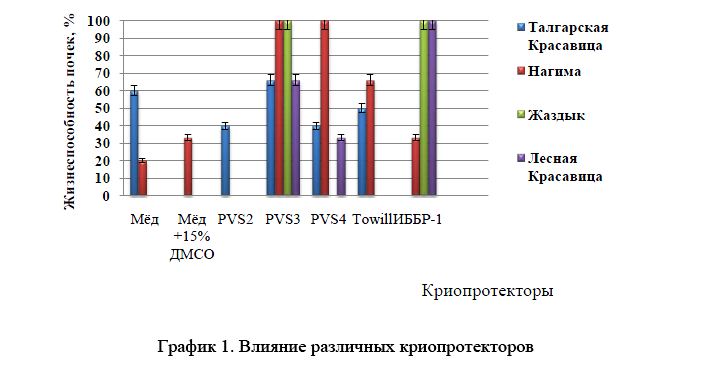
График 1. Влияние различных криопротекторов
Литература
- Sakai A. Survival of the Twig of Woody Plants at –196 o 1960. С. 393-394.
- Towill LE, Forsline PL, Walters C, Waddell JW, Laufmann Cryopreservation of Malus germplasm using a winter vegetative bud method: results from 1915 accessions. CryoLetters 2004. С.323-334.
- Chang Y, Reed Extended alternating-temperature cold acclimation and culture duration improve pear shoot cryopreservation. Cryobiology 2000. С. 311-322.
- Suzuki M, Niino T, Akihama T, Okai Shoot formation and plant regeneration of vegetative pear buds. Japan Soc Hort Sci 1997. С.29-34.
- Chang Y, Reed Preculture conditions influence cold hardiness and regrowth of Pyrus cordata shoot tips after cryopreservation. HortScience 2001. С.1329-1333.
- (Seufferheld M.J., Fitzpatrick J., Walsh T.M., Stushnoff C. Cryopreservation of dormant buds from cold tender taxa using a modified vitrification procedure // 28th Annual Meeting. - Cryobiology. – 1991. – V.28(6). – P.576.)