В статье представлены результаты клонального микроразмножения растений груши. Изучено влияние минерального состава питательных сред и влияние регуляторов роста в различных концентрациях на микроразмножение груши. Наиболее эффективные питательные среды для размножения груши являются Мурасиге-Скуга и среда PRS .
Введение Современные методы биотехнологии позволили значительно повысить эффективность клонирования растений. Исследования в области культивирования соматических тканей привели к разработке принципиально новых методов размножения – клональное микроразмножение. В сущности, эти методы аналогичны вегетативному способу размножения и различаются лишь тем, что весь процесс протекает в условиях in vitro [1].
Главное условие клонального микроразмножения – получение растений, полностью сохраняющих генетическую однородность. Поэтому для этих целей предпочтительнее использовать культуру апексов (меристематических верхушек), т.к. в условиях in vitro они являются генетически стабильными, и пролиферирующие ткани всегда остаются диплоидными [2].
Клональное микроразмножение является эффективным способом вегетативного размножения, позволяющим быстро тиражировать отдельные генотипы, получать оздоровленный материал и, главное, сокращать сроки селекционного процесса [3,4].
Методы исследования Объектами исследования являлись 5 сортов груши: Талгарская Красавица, Жаздык, Нагима, Любимица Клаппа и Лесная Красавица. Оптимизацию условий клонирования производили путем отчленения меристематических верхушек, терминальных и латеральных почек и посадки их на искусственные питательные среды. При этом проводили подбор минерального состава питательных сред, ауксинов, цитокининов и других регуляторов роста, способствующих введению эксплантов в культуру, пролиферации побегов.Вычисление апексов и пересадка при культивировании проводилась в ламинарных боксах предварительно стерилизованных кварцевой или бактериальной лампами.
Микроклональное размножение проводили в термостатируемых комнатах при освещённости 40 μmol m-2s-1, 16-ти часовом фотопериоде, при температуре +25оС. Питательные среды разливали в культуральные посуды и автоклавировали при давлении 1 атм. 30 мин. Повторность опытов 5-10-ти кратная. Наблюдения и учёт проводили ежемесячно. Учитывали состояние и число образовавшихся побегов. Коэффициент размножения средний за 1 пассаж для каждого генотипа высчитывали по формуле:
P= a/b·c
a – количество вновь образовавшихся побегов
b – количество побегов высаженных для размножения c – количество пассажей
Микроклональное размножение проводили в термостатируемых комнатах при освещённости 40 μmol m-2s-1, 16-ти часовом фотопериоде, в температуре +23+25оС [5].
Результаты и их обсуждение Важным фактором, имеющим значение для успешного микроразмножения, является гормональный состав питательной среды и вид экспланта. Решающую роль в этом играют концентрации и сочетание фитогормонов.
Наблюдения показали, что асептические побеги груши через 7—10 дней после посадки на ростовые питательные среды начинали активно расти. На (таблице 1) приведены результаты развития эксплантов сорта Талгарская Красавица на основе питательной среды МС, содержащей различное количество БАП, ИМК, и ГК.
Таблица 1 - Развитие эксплантов груши сорта Талгарская Красавица на средах с различным сочетанием концентраций стимуляторов роста
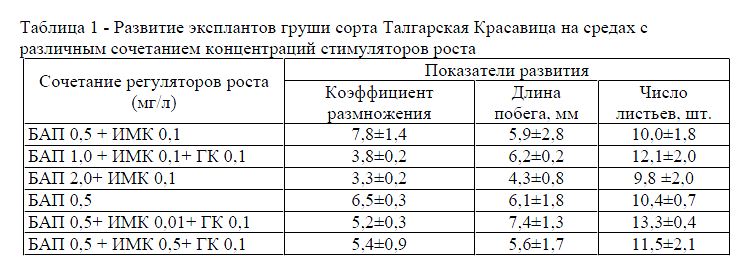
Среди использованных сочетаний регуляторов роста наибольшую степень размножения (6,5±0,3) отмечали в присутствии в среде сочетания БАП 0,5 мг/л. Минимальная степень размножения проявилась при сочетании регуляторов роста БАП 2,0+ ИМК 0,1 (3,3±0,2). На рост побегов в длину существенное влияние оказало сочетание БАП 0,5+ ИМК 0,01+ ГК 0,1 мг/л. Данный вариант обеспечивал развитие длинных побегов, пригодных к укоренению. Средняя длина побегов в варианте составила 7,4 мм (табл. 2).
На этапе микроразмножения использовали среды : Мурасиге и Скуга (MS), Ллойда и Маккоуна (L&M), и Pear Rootstock medium (PRS). На коэффициент размножения побегов груши оказали влияние два фактора – состав питательных сред и генотип. На среде МС (контроль) максимальный коэффициент размножения был у сорта Лесная Красавица коэффициент размножения в среднем составил (5,2). На среде PRS высокая степень пролиферации отмечена у сортов Талгарская Красавица в среднем (7,2), Нагима (6,1) На среде (L&M) наиболее высокий коэфициент размножения был у сортов Талгарская Красавица (6,6) и Любимица Клаппа (4,4), (таб.2).
Таблица 2 - Коэффициент размножения у эксплантов различных сортов груши в зависимости от минерального состава питательных сред
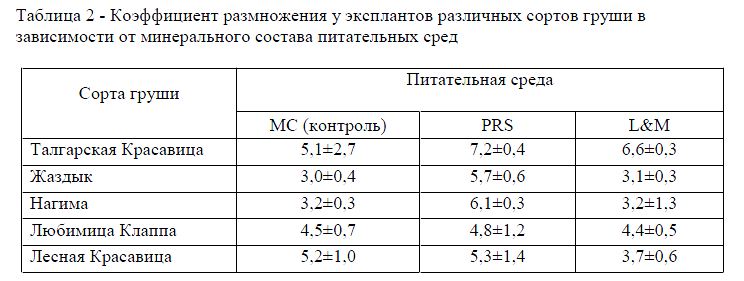
Наибольший рост побегов в длину был отмечен на среде PRS у сортов Талгарская Красавица, Лесная Красавица и Любимица Клаппа. (рис.1)

Рисунок 1 – Микроклональное размножение груши
Таким образом, для большинства сортов груши среды PRS и МС оказались оптимальными. На питательной среде PRS были получены лучшие результаты по таким показателям, как коэффициент размножения и длина побегов. Эта среда была пригодна для культивирования побегов без частого субкультивирования (табл.2).
Литература
- Высоцкий В.А. Клональное микроразмножение плодовых растений и декоративных кустарников / В. А. Высоцкий // Микроразмножение и оздоровление растений в промышленном плодоводстве и цветоводстве. Мичуринск, 1989. − С.
- Расторгуев С.Л. Культура изолированных тканей и органов в селекции плодовых растений – Мичуринск : изд-во МичГАУ, 2009. – 170с.
- Niedz RP, Evens TJ (2007) Regulating plant tissue growth by mineral nutrition. In Vitro Cell Dev Biol- Plant 43: 370-381
- А. В. Верзилин, Д. В. Иванов, Ю. В. Трунов // Использование биотехнол. методов для решения генет.-селекционных проблем. – Мичуринск, 1998. – С. 63-66.
- Bell RL, Reed BM (2002) In vitro tissue culture of pear: Advances in techniques for micropropagation and germplasm preservation. Acta Hort 596: 412-418