Бурая ржавчина является опасным заболеваниям пшеницы. В настоящем исследовании внимание было обращено на часть эффективных генов устойчивости к бурой ржавчине – Lr9, Lr10, Lr22а, Lr24, Lr29, Lr32, Lr68 а также комплекс генов Lr19/Sr25, Lr26/Sr31/Yr9/Pm8, Lr37/Yr17/Sr31, Lr35/Sr39 и Lr34/Yr18. В результате молекулярного скрининга установлено, что линия L286 является носителем пяти эффективных Lr-генов (Lr22a, Lr29, Lr34, Lr35, Lr68), включающие APR-гены возрастной устойчивости (Lr22a, Lr34 и Lr68), а у линии L372 идентифицировано 4 гена (Lr24, Lr29, Lr35, Lr37) и у сорта Жетысу идентифицирован 1 Lr-ген (Lr22a). Полученные результаты используются в Казахстане для создания устойчивых к бурой ржавчине сортов пшеницы с применением MAS-селекции.
Введение
Основным критерием высокого уровня продовольственной безопасности является устойчивое воспроизводство зерна, масла и других сельскохозяйственных продуктов. Регион Центральной Азии является одним из важнейших мировых производителей пшеницы, которая выращивается на площади 15 млн. га. На этой территории в последние годы получила распространение бурая ржавчина пшеницы Puccinia recondita f. sp. tritici, которая наносит серьезный экономический ущерб, снижая и качество зерна. В связи с этим, одной из главных задач агропромышленного комплекса Казахстана является повышение урожайности и качества стратегически важных сельскохозяйственных культур. Использование генетически устойчивых сортов является наиболее эффективным, экономически и экологически надежным методом контроля болезней, позволяющим снизить или элиминировать применение фунгицидов и свести к минимуму потери урожая от ржавчины [1].
В научной литературе имеется обширная информация о генах устойчивости пшеницы к возбудителю бурой ржавчины. К настоящему времени в каталоге генов пшеницы имеется информация о 68 Lr-генах [2]. Однако одной из основных проблем недолгой эффективности большинства Lr-генов является появление вирулентных рас патогена, которые способны преодолеть устойчивость. Вследствие этого многие из известных Lr-генов устойчивости становятся неэффективными [3].
В каталоге 36 Lr-генов интрогрессированы в вид Triticum aestivum от других видов злаков. Ген Lr9 перенесен Sears в мягкую пшеницу от Aegilops umbelulata в 1961 г. [4]. Ген Lr9 локализован в хромосоме 6В и имеется у сортов Transfer, Abe, Arthur 71, Riley 67, Oasis. В Казахстане в популяции возбудителя бурой ржавчины вирулентность к этому гену отсутствует или встречается очень редко. Агрессивных к нему рас и биотипов нет, ген высокоэффективен [3]. Ген Lr10 изолирован у гексаплоидной пшеницы и расположен на хромосоме 1AS. Он кодирует белок типа CC-NBS-LRR с N-терминал доменом. При экспрессии в трансгенных растениях пшеницы, Lr10 обеспечивает повышенную устойчивость к бурой ржавчине. Lr10 имеет сходство с RPM1 в Arabidopsis thaliana и и устойчив к генам аналогам в рисе и ячмене, но не тесно связаны с другими Lr-генами пшеницы [5]. Источником генов Lr19, Lr24, Lr29 явился пырей Agropyron elongatum (Thinopyrom elongatum). Очень редко появляющиеся вирулентные патотипы пока агрессивностью не обладают и угрозы для носителей этого гена не представляют [6,7,8]. Ген устойчивости Lr22a интрогрессирован от Aegilops tauschii на 2DS хромосому мягкой пшеницы. Ген Lr22a обеспечивает возрастную устойчивость (APR) к бурой ржавчине [9]. Источником гена Lr26 является рожь Secale cereale [10]. Ген Lr26 интрогрессирован в хромосому 1B. Ген Lr32 трансформирован от Aegilops tauschii на 3DS хромосому гексаплоидной пшеницы, что обеспечивает устойчивость к бурой ржавчине на уровне проростков [11]. Небольшая группа генов устойчивости к бурой ржавчине, такие как Lr34 и Lr46, известна как «slow rusting genes» [12]. Они обеспечивают длительную и неспецифическую устойчивость взрослых растений, но их эффект более ограничен, чем у расаспецифических генов. Наблюдался плейотропный эффект между Lr46 и Yr29, также «slow rusting gene» к желтой ржавчине. Ген Lr34 расположен на коротком плече хромосомы 7D, недалеко от локуса Xgwm295. Lr34 тесно связан с локусом некроза листья (LTN), также возможно, что фенотип LTN может иметь плейотропный эффект самого Lr34 [12]. Ген Lr35 происходит от Aegilops speltoides. Ген Lr35 интрогрессирован 2B хромосому пшеницы. Lr35 был переведен в гексаплоидную пшеницу сорта Marquis от Aegilops speltoides. Ген расположен на сегменте 2S хромосом А. speltoides и транслоциривался к 2В хромосомы пшеницы. Транслоцируемый сегмент является носителем гена против стеблевой ржавчины Sr39 и adult-plant гиперчувствительный геном устойчивости к бурой ржавчине Lr35 [13]. Источником гена Lr37 является Aegilops ventricosa. Этот ген идентифицирован Барианой и Макинтошем в 1991 г. и локализован в 2AS хромосоме. Носители этого гена поражаются в ювенильной фазе растений, но проявляют возрастную устойчивость. Длинный хромосомный фрагмент (25-38 сМ), содержащий три гена устойчивости к ржавчине был транслоцирован между короткими плечами 2NS хромосомы от Triticum ventricosum в 2AS хромосомы мягкой пшеницы. Этот сегмент включает три гена устойчивости к болезням: Lr37, Yr17 и Sr38 устойчивости к бурой, желтой и стеблевой ржавчине, соответственно. Фрагмент 2NS впервые интрогрессирован у сорта пшеницы VPM1, а затем он был переведен в другие коммерческие сорта, как Madsen и Thatcher [14]. Группа ученых из СИММИТ в сорте пшеницы Parula идентифицировали APR-ген Lr68 у Parula(FKN/3/2*Frontana//Кения350AD. 9C.2/Gabo55 /4/Bluebird/Chanate), и он локализован на длинном плече хромосомы 7B. Ранее был назван как LrP. Выявлены молекулярные маркеры, фланкирующие ген Lr68, которые могут быть использованы в маркерной селекции. Сорт Parula создан учеными CIMMYT в 1981 году, который объединяет также APR-генов устойчивости как Lr34 и Lr46. Возможно, происхождение Lr68 гена является бразильский сорт Frontana [15].
Однако на большое количество идентифицированных Lr-генов одной из основных проблем их недолгой эффективности является появление вирулентных рас патогена, которые способны преодолеть устойчивость. Вследствие этого многие из известных генов устойчивости становятся неэффективными. Особая опасность бурой ржавчины обусловлена способностью патогена к мутации и быстрой смене генераций, что ускоряет расообразовательный процесс [16]. Тем не менее, четыре гена устойчивости, Lr34/Yr18, Lr46/Yr29, Sr2/Yr30, Lr68 и Lr67/Yr46, обеспечивают частичную, но длительную устойчивость [17]. Эти гены способствуют замедленному типу развития ржавчины и являются эффективными ко всем расам патогена. Дополнительное действие этого типа гена приводит к повышению устойчивости до уровня иммунности. Поэтому необходимо продолжать поиск источников новых доноров устойчивости к бурой ржавчине пшеницы.
Поэтому необходим поиск источников новых генов устойчивости к ржавчине пшеницы. Для того чтобы с большей надежностью контролировать болезнеустойчивость, очень важно иметь в распоряжении молекулярные маркеры, сопряженные с этим признаком. В настоящем исследовании внимание было обращено на часть эффективных генов устойчивости к бурой ржавчине – Lr9, Lr10, Lr22а, Lr24, Lr29, Lr32, Lr68 а также комплекс генов Lr19/Sr25, Lr26/Sr31/Yr9/Pm8, Lr37/Yr17/Sr31, Lr35/Sr39 и Lr34/Yr18, которые идентифицировали в процессе молекулярного скрининга гермоплазмы пшеницы.
Материалы и методы
Материалами исследований являются сорта и перспективные линии мягкой озимой пшеницы; Жетысу, L286 Алмалы/Обрий, L372 Алматинская полукарликовая /Прогресс. Анализ устойчивости образцов пшеницы к видам ржавчины проводили на полевом стационаре Казахского НИИ земледелия и растениеводства. Оценку развития болезни желтой и бурой ржавчиной проводили в фазу молочно-восковой спелости по принятой в CIMMYT методике, определяя инфекционный тип (в баллах) и степень поражения (%) [18] Коллекции образцов пшеницы высевали во всех фитопатологических опытах на делянках площадью 1 м2 в трехкратной повторности. Выделение геномной ДНК из растительного материала осуществлено из проростков пшеницы на основе CTAB метода выделения геномной ДНК, с использованием 5–дневных проростков по методике C.R.Riede, J.A.Anderson, [19]. Для идентификации носителей генов устойчивости использован метод полимеразной цепной реакции (ПЦР) в соответствии с протоколом X.M.Chen et al. [20]. В качестве положительного контроля при идентификации генов использованы образцы пшеницы, в которых гены устойчивости идентифицированы, а в качестве отрицательного контроля – ddH2O или образцы, в которых гены устойчивости не выявлены. Амплификация проведена в амплификаторе Mastercycler (Eppendorf, Германия), программы амплификации выбраны в зависимости от идентифицируемого Lr–гена устойчивости (Таблица 1–2). Объем реакционной смеси для ПЦР составлял 10 мкл и содержал 1,0 мкл 10× буфер, 1,0 мкл 2,5 mM dNTP, 0,2 мкл 10 микромоль каждого праймера, 0,2мкл 5 Unit Taq-полимеразы, 6,4 мкл MQ-H2O, 1 мкл 20 нг/мкл ДНК. Для выявления носителей генов устойчивости Lr9, Lr10, Lr19/Sr25, Lr22a, Lr24, Lr26, Lr29, Lr32, Lr34/Yr18, Lr35/Sr39, Lr37/Yr17/Sr38, Lr68 использованы SSR, STS, SCAR, CAPS маркеры J13, F1.2245Lr10-6/r2, GbF/R, WMS296, J91/2, iag95, Lr29F/R18, Xbarc135, csLV34, Sr39#50, VENTRIUP/LN2, csGS, соответственно. Для разделения фрагментов амплифицированной ДНК электрофорез осуществляли в 2 %-м агарозном или 8 % полиакриламидном геле (ПААГ) в ТВЕ-буфере (45 мМ трис-борат, 1мМ EDTA, pH-8) [20].
Таблица 1 – Источники гена, локализация в хромосоме и последовательность праймеров к Lr-генам устойчивости
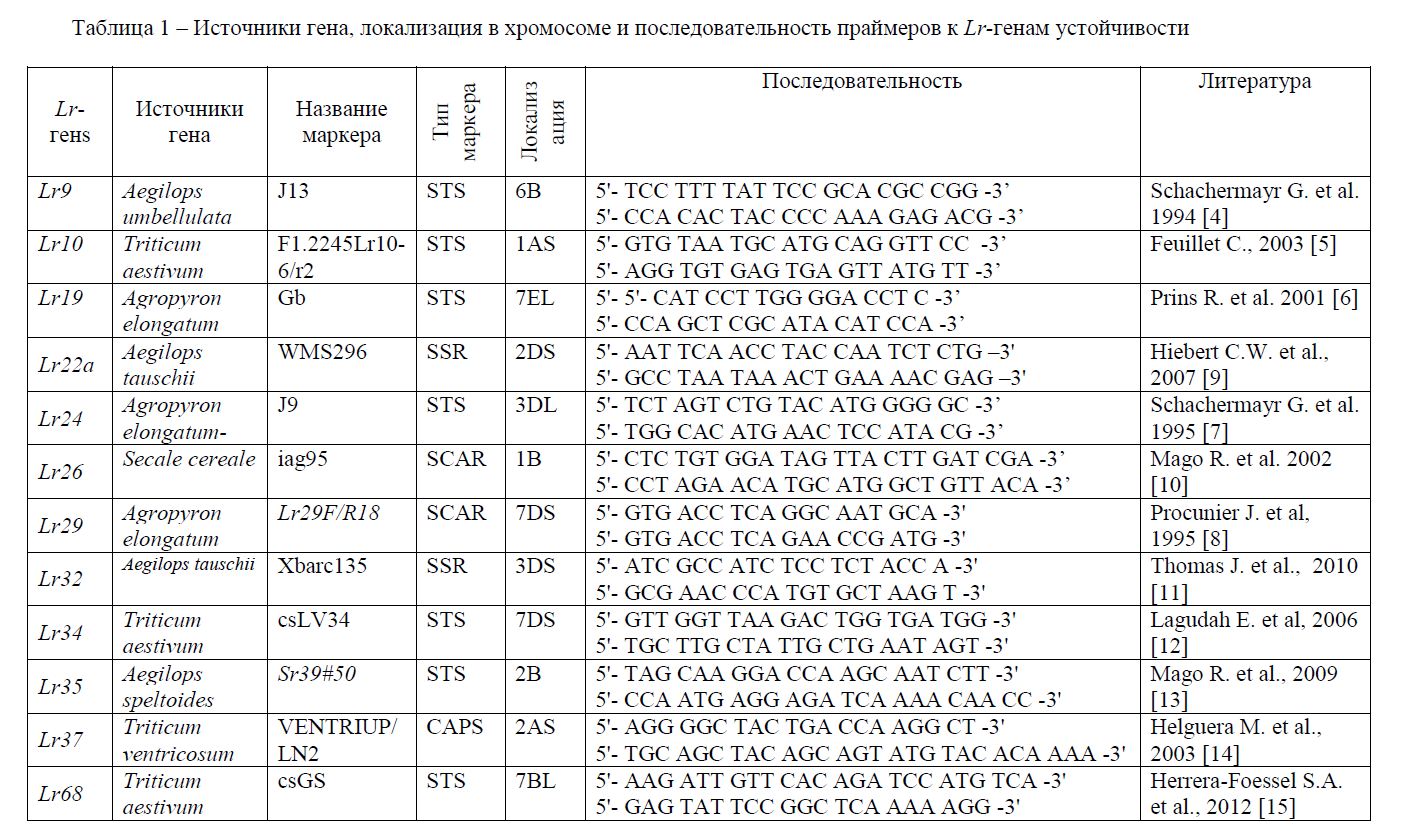
Таблица 2 – Протоколы для проведения полимеразной цепной реакции с использованием праймеров к соответствующим Lr-генам устойчивости
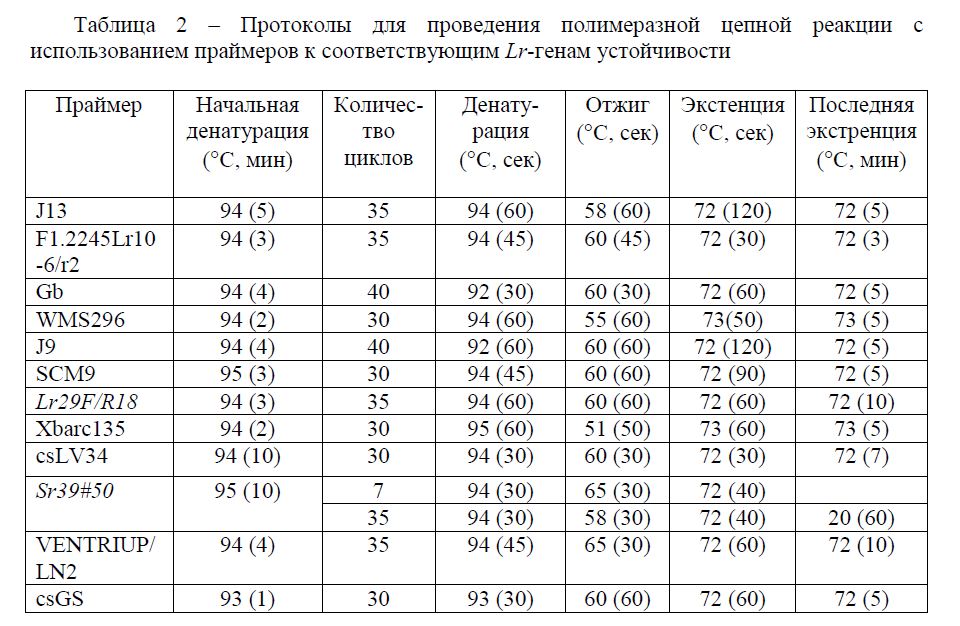
Результаты исследований Известно, что ген возрастной устойчивости APR ген Lr22a локализован на хромосоме 2DS, источником гена является Aegilops tauschii, тестерней линией является TC*6/RL5404 (RL6044). Для идентификации носителей гена Lr22a проводили ПЦР, с использованием SSR маркера WMS296 [9]. В качестве положительного контроля при идентификации носителей генов использована изогенная линия сорта Тэтчер (RL6044), в которой идентифицирован ген устойчивости Lr22а, а в качестве отрицательного контроля – ddH2O. В результате ПЦР–анализа фаргмент ДНК, характерный для носителей гена Lr22a размером 121 и 131 п.н., формировался у сорта Жетысу и линии L286 (Рисунок 1).
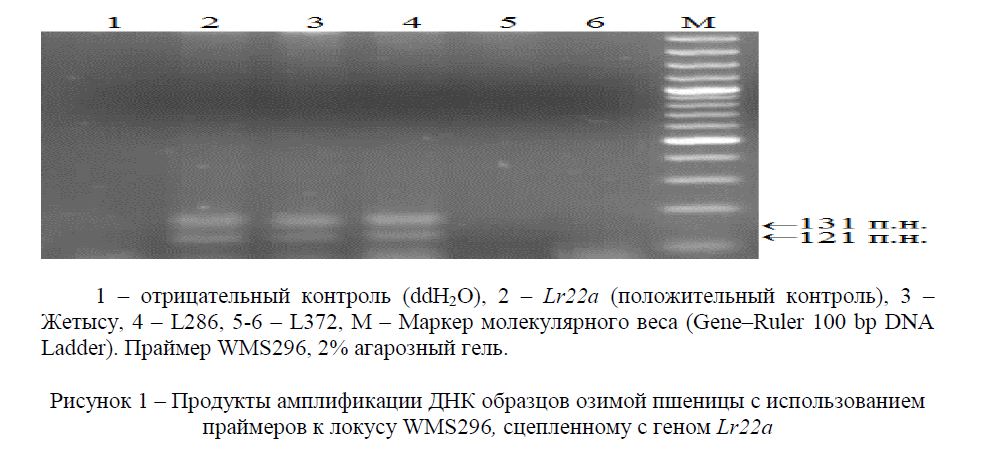
Рисунок 1 – Продукты амплификации ДНК образцов озимой пшеницы с использованием праймеров к локусу WMS296, сцепленному с геном Lr22а
Ген Lr24 локализован на хромосоме 3 DL, источником гена является Agropyron elongatum, тестерной линией является сорт Thatcher TC*6/Agent (RL6064). Для идентификации носителей гена Lr24 проводили ПЦР амплификацию с использованием праймеров STS J91/2 [7]. В качестве положительного контроля при идентификации носителей Lr–генов использованы изогенные линии сорта Thatcher и российский сорт Лавина, в которых идентифицирован ген устойчивости Lr24. В качестве отрицательного контроля – ddH2O. В результате ПЦР–анализа показано, что фрагмент ДНК, характерный для носителей гена Lr24 размером 280 п.н. формировался у линии L372 (Рисунок 2).
Продукты характерного фрагмента амплификации отсутствовали у сорта Жетысу и линии L286.

Рисунок 2 – Продукты амплификации ДНК образцов озимой пшеницы с использованием праймеров к локусу J9, сцепленному с геном Lr24
Для поиска гена Lr29 использованы праймеры SCAR маркера Lr29F/R18. Ген Lr29 локализован на хромосоме 7 DS, источником гена является Agropyron elongatum, тестерной линией является TC*6/CS7AG#11 RL6080 [8]. На рисунке 3 представлены результаты электрофореза продуктов ПЦР, отражающие наличие или отсутствие в исследуемых образцах гена Lr29. ПЦР–анализ показал что фрагмент ДНК, характерный для носителей гена Lr29 размером 900 п.н. формировался у линий L286 и L372. Продукты характерного фрагмента амплификации отсутствовали у сорта Жетысу.
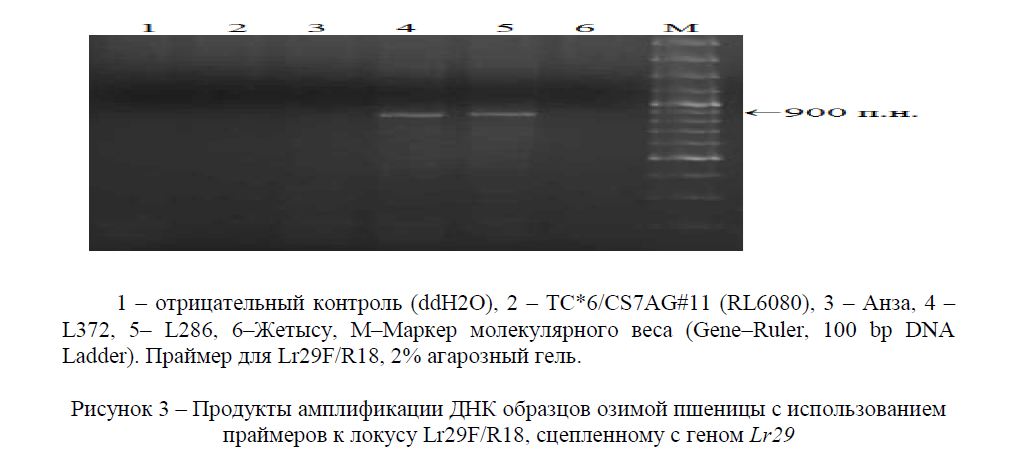
Рисунок 3 – Продукты амплификации ДНК образцов озимой пшеницы с использованием праймеров к локусу Lr29F/R18, сцепленному с геном Lr29
Ген Lr34 локализован на хромосоме 7DS, тестером является линия TC*6/PI58548 RL6058. Ген Lr34 сцеплен с APR геном устойчивости к желтой ржавчине Yr18 [175]. Для идентификации носителей гена Lr34 проводили с использованием STS маркера csLV34
[12]. В качестве положительного контроля при идентификации носителей генов использована изогенная линия сорта Thatcher (RL6058), в котором идентифицирован ген устойчивости Lr34 сцепленый с геном Yr18. На рисунке 4 показаны результаты ПЦР– анализа потенциальных носителей генов Lr34/Yr18 c использованием маркера csLV34. На электрофореграмме показано, что линия L286 и изогенная линия сорта Thatcher RL6058 формировали продукта амплификации размером 150 п.н., что указывает на наличие у них генов Lr34/Yr18.
1 – Изогенная линия Lr34 TC*6/PI58548 (RL6058), положительный контроль, 2-5 – Avocet S, отрицательный контроль, 6– Жетысу, 7 – L286, 8 – L372, М– Маркер молекулярного веса (Gene–Ruler, 100 bp DNA Ladder). Праймер csLV34, 2% агарозный гель.

Рисунок 4 – Продукты амплификации ДНК образцов озимой пшеницы с использованием праймеров к локусу csLV34, сцепленному с геном Lr34/Yr18
Ген Lr35 сцеплен с геном устойчивости к стеблевой ржавчине Sr39 и локализован на хромосоме 2В, источником гена является Aegilops speltoides L., тестерной линией является сорт Thatcher RL5711. Гены устойчивости к бурой и стеблевой ржавчине Lr35/Sr39 трансформированы от Aegilops speltoides L. [13]. Для идентификации носителей гена Lr35 проводили ПЦР амплификацию с использованием праймеров STS Sr39#50. В качестве положительного контроля при идентификации носителей Lr-генов использованы изогенные линии Sr39 RL5711 Kerber. В качестве отрицательного контроля – ddH2O. В результате ПЦР–анализа показано, что фрагмент ДНК, характерный для носителей гена Lr35 размером 250 п.н. формировался у изогенной линии Sr39 RL5711 Kerber, L286 и L372 (Рисунок 5). Продукты характерного фрагмента амплификации отсутствовал у сорта Жетысу.

Рисунок 5 – Продукты амплификации ДНК образцов озимой пшеницы с использованием праймеров к локусу Sr39#50, сцепленному с геном Lr35/Sr39
Ген Lr37 локализован на хромосоме 2AS, источником гена является Triticum ventricosum, тестером является линия VPM1. Ген Lr37 сцеплен с генами устойчивости к желтой и стеблевой ржавсине Yr17 и Sr38. Для идентификации носителей гена Lr37 проводили ПЦР амплификацию с использованием CAPS праймеров LN2/Ventriup [14]. В качестве положительного контроля использован американский сорт Madsen с идентифицированным геном устойчивости Lr37, а в качестве отрицательного контроля – ddH2O. ПЦР–анализ, представленный на рисунке 13, свидетельствует о формировании амплифицированных продуктов, характерных для носителей генов Lr37/Yr17/Sr31 размером 262 п.н., у линии L372 и Madsen. У остальных образцов продукты амплификации отсутствовали.

Рисунок 13 – Продукты амплификации ДНК образцов озимой пшеницы с использованием праймеров к локусу VENTRIUP/LN2, сцепленному с геном Lr37
Для поиска гена Lr68 использованы праймеры STS маркера csGS [15]. Ген Lr68 локализован на хромосоме 7BL [15], источником гена Lr68 является бразилский сорт Frontana, тестерным сортом Parula. На рисунке 14 представлены результаты электрофореза продуктов ПЦР, отражающие наличие или отсутствие в исследуемых образцах гена Lr68. ПЦР–анализ показал что фрагмент ДНК, характерный для носителей гена Lr68 размером 375 п.н. формировался у линий L286 и у сорта Parula. Продукты характерного фрагмента амплификации отсутствовали у сорта Жетысу и L372.
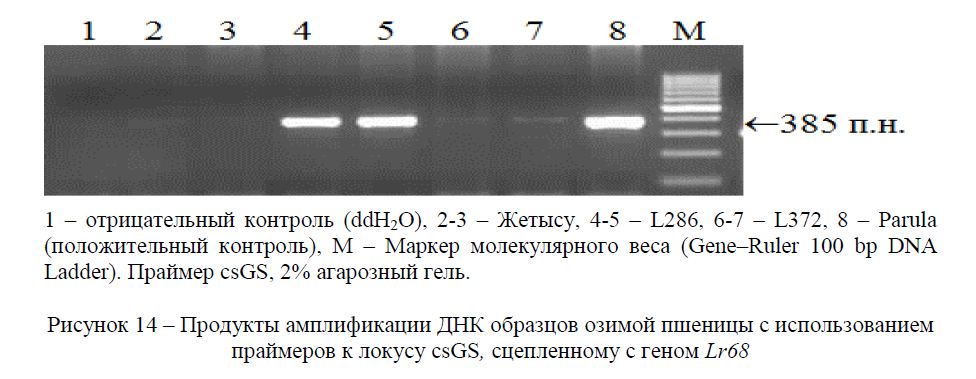
Рисунок 14 – Продукты амплификации ДНК образцов озимой пшеницы с использованием праймеров к локусу csGS, сцепленному с геном Lr68
В таблице 12 представлены обобщенные результаты ПЦР–анализа с использованием молекулярных маркеров, сцепленных с генами устойчивости Lr22a, Lr24, Lr29, Lr34/Yr18, Lr35/Sr39, Lr37/Yr17/Sr38 и Lr68.
У линии L286 обнаружены пять эффективных Lr-генов, включая гены Lr22a, Lr29, Lr34, Lr35, Lr68 (Таблица 12). Известно, что APR ген Lr34 очень широко распространен у коммерческих сортов пшеницы. Известно, что комплекс генов Lr34 и Lr68 относится к генам с длительным развитием ржавчины, “slow rusting genes”, которые обеспечивают длительную и неспецифическую устойчивость взрослого растения. По данным Колмера [21], ген остается эффективным в контроле бурой ржавчины более 30 лет. По–видимому, этим объясняется стабильная полевая устойчивость к ржавчине этой линии на инфекционном фоне.
Хотя у линии L372 идентифицировано 4 гена (Lr24, Lr29, Lr35, Lr37), этот образец характеризуются умеренно–восприимчивой реакцией (20MS) на патоген. В сорте Жетысу идентифицировано 1 ген (Lr22a), однако он не обеспечивает устойчивость к популяции патогена и в полевых условиях сорт поражается на 30MS бурой ржавчиной.
Заключение
В результате молекулярного скрининга установлено, что линия L286 является носителем пяти эффективных Lr-генов (Lr22a, Lr29, Lr34, Lr35, Lr68), включающие APR-гены возрастной устойчивости (Lr22a, Lr34 и Lr68), которые обеспечивают устойчивую реакцию на патоген (тип реакции 0–R). У линии L372 идентифицировано 4 гена (Lr24, Lr29, Lr35, Lr37), которые, являясь проростковыми генами, менее эффективно защищают пшеницу от патогена; линия характеризуется умеренно-восприимчивым типом реакции, 30MS. У сорта Жетысу идентифицирован 1 Lr- ген (Lr22a), на стадии взрослого растения этот сорт проявляет умеренно-восприимчивый и восприимчивый тип реакции, 40MS-S. Полученные результаты используются в Казахстане для создания устойчивых к бурой ржавчине сортов пшеницы с применением MAS-селекции.
Литература
- Маркелова Т.С. Иммунологические основы и методы создания исходного материала пшеницы для селекции на устойчивость к болезням в Поволжье: дис. … док. с- х. наук: 06.01.11. – Саратов, 2007. – 44 с.
- McIntosh A., Dubcovsky J., Rogers J., Morris C., Appels R., Xia X. Catalogue of gene symbols for wheat: 2010 supplement // http://www.shigen.nig.ac.jp/wheat/ komugi/genes/macgene 2010.
- Кохметова А.М., Сапахова З.Б., Маденова А.К., Есенбекова Г.Т. Идентификация носителей генов устойчивости к желтой Yr5, Yr10, Yr15 и бурой ржавчине Lr26, Lr34 на основе молекулярного скрининга образцов пшеницы // Биотехнология. Теория и Практика. – 2014. – №1. – С. 71-78 DOI: 11134/btp.1.2014.10.
- Schachermayr G., Siedler H., Gale M.D., Winzeler H., Winzeler M., Keller IdentiWcation and localization of molecular markers linked to the Lr9 leaf rust resistance gene of wheat // Theoretical and Applied Genetics. – 1994. – № 88. – Р. 110–115.
- Feuillet C., Travella S., Stein N., Albar L., Nublat A., Keller B. Map-based isolation of the leaf rust disease resistance gene Lr10 from the hexaploid wheat (Triticum aestivum ) genome. Proc. of the National Academy of Sciences of the United States of America. – 2003, – 100(25). – P. 15253–15258.
- Prins, , Groenewald, J.Z., Marais, G.F., Snape, J.W., Koebner, R.M.D. AFLP and STS tagging of Lr19, a gene conferring resistance to leaf rust in wheat // Theoretical and Applied Genetics. –2001. – № 103: – Р. 618–624.
- Schachermayr , Messmer M.M., Feuillet C., Winzeler H., Winzeler M., Keller B. Identification of molecular markers linked to the Agropyron elongatum–derived leaf rust resistance gene Lr24 in wheat // Theoretical and Applied Genetics. – 1995. – № 90. – Р. 982- 990.
- Procunier J.D., Townley-Smith T.F., Fox S., Prashar S., Gray M., Kim W.K., Czarnecki E., Dyck P.L. RAPD/DGGE markers linked to leaf rust resistance genes Lr29 and Lr25 in wheat (Triticum aestivum ). // Journal of Genetics and Breeding. – 1995. – 49. – P. 87-92.
- Hiebert C.W., Thomas J.B., Somers D.J., McCallum B.D., Fox S.L. Мicrosatellite mapping of adult-plant leaf rust resistance gene Lr22a in wheat // Theoretical and Applied – 2007. – 115. – P. 877–884.
- Mago R., Spielmeyer W., Lawrence G.J., Lagudah E.S., Ellis J.G., Pryor Identification and mapping of molecular markers linked to rust resistance genes located on chromosome 1RS of rye using wheat-rye translocation lines // Theoretical and Applied Genetics.– 2002. – Vol. 104(8). – P. 1317-1324.
- Thomas , Nilmalgoda S., Hiebert C., McCallum B., Humphreys G., DePauw R. Genetic markers and leaf rust resistance of the wheat gene Lr32 // Crop Science. – 2010. – № 50.– Р. 2310-2317.
- Lagudah E.S., McFadden H., Singh R.P., Huerta-Espino J., Bariana H.S., Spielmeyer
- Molecular genetic characterization of the Lr34/Yr18 slow rusting resistance gene region in wheat // Theoretical and Applied Genetics. – 2006. – Vol. 114(1). – P. 21-30
- Mago , Zhang P., Bariana H.S., Verlin D.C., Bansal U.K., Ellis J.G., Dundas I.S. Development of wheat lines carrying stem rust resistance gene Sr39 with reduced Aegilops speltoides chromatin and simple PCR markers for marker-assisted selection // Theoretical and Applied Genetics. – 2009. – 124. – P.65-70.
- Helguera , Khan I.A., Kolmer J., Lijavetzky D., Zhong-qi L., Dubcovsky J. PCR assays for the Lr37-Yr17-Sr38 cluster of rust resistance genes and their use to develop isogenic hard red spring wheat lines // Crop Science. – 2003. – № 43. – P. 1839-1847.
- Herrera-Foessel S.A., Singh R.P., Huerta-Espino J., Rosewarne G.M., Periyannan S.K., Viccar , Calvo-Salazar V., Lan C., Lagudah E.S. Lr68: a new gene conferring slow rusting resistance to leaf rust in wheat // Theoretical and Applied Genetics. – 2012, – Vol.124. P. 1475-1486.
- Кохметова А.М., Седловский А.И., Тюпина Л.Н., Есенбекова Г.Т., Идентификация гермоплазмы пшеницы, устойчивой к ржавчине с использованием генетических и молекулярных маркеров // Бюллетень Никитского ботанического сада. – Выпуск 99. – С. 41-45.
- Lagudah E.S. Molecular genetics of race non-specific rust resistance in whaet // Euphytica. 2011. – 179. – Р. 81-91.
- Peterson R.F., Campbell A.B., Hannah A.E. A diagrammatic scale for estimating rust intensity on leaves and stems of cereals // Canadian Journal of – 1948. – Vol. 26 – P. 496-500.
- Riede R. and Anderson J.A. Linkage of RFLP markers to an aluminum tolerance gene in wheat // Crop Science. – 1996. – Vol. 36. – P. 905-909.
- Chen X.M., Line R.F., Leung H. Genome scanning for resistance gene analogs in rice, barley, and wheat by high resolution electrophoresis // Theoretical and Applied Genetics –– Vol.97. – P. 345-355.
- Kolmer J.A. Genetics of resistance to wheat leaf rust // Annu. Rev. Phytopathology. –
- –34(1). – P. 435-455.