В статье представлены результаты введения в асептическую культуру in vitro различных сортов груши. Объектами исследований являлись - спящие почки и активно растущие побеги сортов груши Нагима, Талгарская Красавица, Лесная Красавица, Жаздык и Шыгыс. Испытано влияния различных стерилизующих агентов с разными концентрациями и экспозициями. Наиболее эффективным и менее опасным стерилизующим веществом оказался гипохлорид натрия «Белизна» в соотношении 1:5 с экспозицией 5 минут.
Введение
При проведении биотехнологических исследований, связанных с культурой in vitro, важным этапом является стерилизация исходного растительного материала, взятого из природных условий, так как его поверхностные ткани, заражены грибами и их спорами, а также бактериями. Известны работы по культуре in vitro листовых эксплантов плодовых и ягодных культур [1,2]. Однако у сортов груши, такие исследования в нашем регионе не проводились. Для стерилизации листовых эксплантов плодовых культур используют 0,1%-ный раствор сулемы, время экспозиции варьирует от 2 до 10 минут [3], а также перекись водорода, спирт, гипохлорид натрия и другие [4].
Материалы и методы
Объектами исследований являлись - спящие почки и активно растущие побеги сортов груши Нагима, Талгарская Красавица, Лесная Красавица, Жаздык и Шыгыс.
Введение в культуру in vitro проводили в два периода: первый – инициация роста побегов из спящих почек черенков груши. После прохождения периода покоя в январе- марте, второй – в период активного роста этих культур в май-июнь месяцы. Собрали черенки зимних почек груши из Помологического сада НИИ плодоводства и виноградарства. Собранные черенки с почками промыли в мыльным растворе в проточной воде в течение часа. Промыли 3 раза в стерильной воде. Погрузили в стерилизующие агенты (Рисунок 1). В ходе работы подбирали стерилизующие агенты и оптимальные способы обработки для введения растений в асептическую культуру. Поскольку стандартная процедура дезинфекции растительного материала при введении их в культуру in vitro включает использование растворов ртутьсодержащих веществ, таких как диацид, необходимо было подобрать менее опасные стерилизующие агенты. В связи с этим была изучена эффективность использования различных стерилизующих веществ, для ингибирования роста сапрофитной микрофлоры при введении растений в асептическую культуру. Инициацию роста у почек проводили путём проращивания в 50% растворе макро- и микроэлементов по Мурасиге и Скугу с добавлением 1 мг/л гибберелловой кислоты, рН 5,6. Отросшие побеги и верхушки активно растущих побегов с меристематической зоной отмывали в мыльном растворе, ополаскивали дистиллированной водой и погружали в стерилизующий агент с различной концентрацией и экспозицией, затем промывали 3 раза в стерильной воде. Спящие почки сортов груши Нагима, Талгарская Красавица, Лесная Красавица, Жаздык и Шыгыс поставили в раствор 1/2МС + 2-5мг/л ГК на проращивание.
Выделенные апексы стерилизовали от сапрофитной микрофлоры и высаживали на питательную среду Мурасиге-Скуга.

Рисунок 1 – Стерилизующие агенты
В культуру in vitro вводили меристематические верхушки размером 0,2-0,4 см, которые изолировали из развивающихся почек, освобождая их от покровных тканей, что обеспечивало достаточно эффективную стерилизацию. В качестве стерилизующих агентов использовали 0,2 % раствор ртути HgCl2 с экспозициями 3 и 4 минуты, 5% гипохлорид натрия «Доместос» в соотношении 1:2 с экспозицией 3 минут, «Доместос» в соотношении 1:5 с экспозицией 15 мин., раствор гипохлорид натрия «Белизна», содержащий гипохлорид натрия, «Белизна» 1:2 с экспозицией 3 мин., «Белизна» 1:5 с экспозицией 5 мин., «Деохлор» 1% 5 мин., чистящие средства «Vanish» без разведения 15 мин., «Мистер Мускул» без разведения. В работах Harvey A.E., Grasham J.L. [5] применение 5,25% гипохлорита натрия и 3% перекиси водорода оказалось эффективным для поверхностной стерилизации годичных стеблей.
Результаты и их обсуждения
Выраженные побегообразования хорошо выросли у сортов Нагима и Лесная Красавица (Рисунок 2).
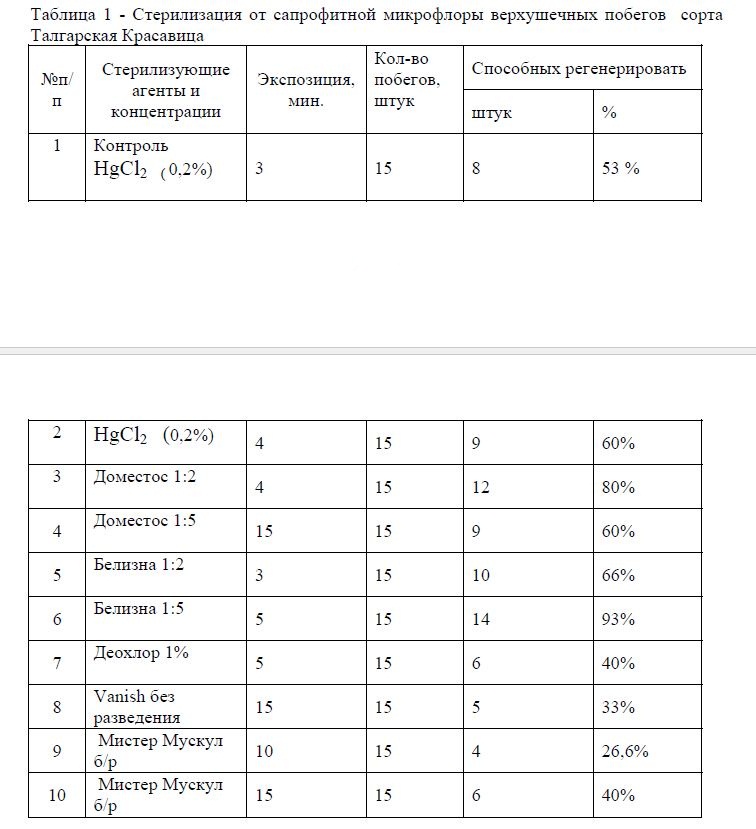
В результате эксперимента установлено, что наиболее оптимальными стерилизующими агентами верхушек побегов груши при введении в асептическую культуру являются обработка: а) Белизна 1:5 с экспозицией 5 мин. выход стерильных эксплантов составил при этом 93%; б) Доместос 1:2 с экспозицией 4 минуты, выход стерильных эксплантов составил при этом 80% ; в) Доместос 1:5 с экспозицией 15 минут жизнеспособных эксплантов составило 60% (Таблица1).
Использование остальных стерилизующих агентов как Деохлор 1 %, Мистер Мускул, Vanish без разведения приводило к некрозу побегов и их к гибели от бактериальной и грибковой инфекции. В этом случае у некоторых эксплантов проявились признаки грибковой инфекции, такие как потемнение основания побега и листьев, а также помутнение питательной среды, что приводило к гибели побегов. Вероятно, поверхностная стерилизация первичных эксплантов способствовала освобождению их от грибковой инфекции, но была малоэффективна против инфекции бактериальной.

Рисунок 2- Проращивание побегов из спящих почек груши
Таблица 1 - Стерилизация от сапрофитной микрофлоры верхушечных побегов сорта Талгарская Красавица
Выводы:
В наших исследованиях было установлено, что из всех испытанных стерилизующих агентов лучшим стерилизующим и менее опасным являлся гипохлорид натрия «Белизна» в соотношении 1:5 с экспозицией 5 минут.
Литература
- Высоцкий В.А. Регенерация плодовых и ягодных растений в культуре каллусной ткани, пыльников, листовых и стеблевых эксплантов// Садоводство и виноградарство. –2008. − № – С. 17-20.
- Орлова С.Ю. Особенности размножения сортов вишни различного происхождения в культуре in vitro / С. Ю. Орлова, А. А. Юшев // Плодоводство на рубеже XXI века : Матер. междунар. конф., посвящ. 75- летию со дня образования Белорусского НИИ плодоводства – Минск, 2000. – С. 27-28.
- Шорникова Д. Г. Совершенствование технологии размножения редких садовых растений в культуре in vitro и оценка их потенциала устойчивости к абиотическим стрессорам. дис. ... канд. с.-х. наук / Д. Г. Шорников. – М., 2008. – 192 с
- Верзилин А. В. Д. В. Иванов, Ю. В. Трунов // Использование биотехнол. методов для решения генет.-селекционных проблем. – Мичуринск, 1998. – С. 63-66.
- Harvey E., Grasham J.L. Procedures and media for obtaining tissue culture of 12 conifer species // Can. J. – 1969. – Bot. 47, N. 4. – Р. 547-549.