Для мониторинга за пораженными растениями, особенно при латентной инфекции, не выявляемой при визуальном осмотре, необходимы высокочувствительные методы диагностики вирусов картофеля. Одним из основных этапов создания диагностикумов является накопление вирусной инфекции в тест-растениях. В результате исследований установлено, что PVX успешно накапливается на 15-е сутки в растениях D. stramonium при нанесении инфекционного сока на фильтровальную бумагу в продольный разрез стебля растения, а в растениях Nicotiana tabacum X-вирус — на 30-е сутки при инокуляции карборундом. Изучено цитоанатомическое влияние вирусов на поражённое растение табака. В клетках хлоренхимы, пораженных вирусами растений, наблюдалось уменьшение размеров ядра, увеличивались размеры вакуолей, измельчались хлоропласты. По мере разрушения клеток происходила некротизация тканей. В клетках появлялись кристаллы в виде рафидов.
Введение
PVX, или крапчатая мозаика, — один из наиболее распространенных вирусов картофеля. На многих сортах картофеля вирус не вызывает видимых симптомов, поэтому остается незамеченным. В зависимости от патогенности штамма, вирус может наносить разный вред: слабопатогенные штаммы могут снижать урожай на 12 %; сильнопатогенные — на 45 %. Снижение урожайности даже при отсутствии симптомов может достигать 10 %, при мозаике — 45 % [1]. Вирус также может поражать белену, паслен черный, дурман, томат и табак. Идентифицировать вирус можно только лабораторными методами. Распространяется вирус преимущественно при механических контактах с поврежденными растениями, при резке картофеля, через сельскохозяйственные орудия и механизмы при сельскохозяйственных работах (опрыскивание, окучивание и др.). Увеличиваются потери урожая при совместном заражении с вирусами PVY и PVA.
В настоящее время очень актуальна проблема мониторинга вирусных инфекций, результативность которого может быть достигнута только в том случае, когда методы диагностики станут доступны для региональных и производственных лабораторий и будут широко применяться в повседневной практической работе [2]. Для контроля за пораженными растениями, особенно при латентной инфекции, не выявляемой при визуальном осмотре, необходимы высокочувствительные методы диагностики вирусов картофеля. Одним из основных этапов его создания является накопление вирусной инфекции в тест-растениях.
Исследования проводились на базе лаборатории биотехнологии кафедры защиты и карантина растений КАТУ им. С.Сейфуллина в рамках бюджетного грантового финансирования МОН РК по проекту «Создание банка отечественных штаммов вирусов картофеля для производства высокочувствительных диагностических штаммов».
Целью наших исследований была отработка оптимальных параметров инокуляции тест-растений и накопление X-вируса картофеля.
Материалы и методы
Основным объектами исследований были тест-растения табака (Nicotiana tabacum), дурмана (Datura stramonium), моноинфицированные X-вирусом растения картофеля сорта Артемис № 43.
Для инокуляции тест-растений были использованы несколько вариантов. При механическом переносе инокуляция проводилась путем растирания тканевого экстракта по верхней стороне листа тест-растения с помощью мелкозернистого абразива — карборунда. Абразив напыляли на поверхность листа перед натиранием или добавляли в инокулюм. После натирания инокулированную поверхность листа промывали водопроводной водой. Использованы были также методы инфильтрации инфекционного сока в листовую пластинку (шприцом без иглы под давлением, нанесение инфекционного сока на фильтровальную бумагу в продольный разрез стебля растения, прививка в расщеп (прививка верхушек моноинфицированных растений Solanum tuberosum (привой) к Datura stramonium (подвой), укол инфекционного сока в проводящую систему).
При оценке тест-растений на зараженность изучаемым вирусом картофеля применяли коммерческие иммуноферментные тесты. Для определения вирусной инфекции использовался метод двойного наслоения антител («сэндвич-вариант» ИФА). При проведении данного варианта ИФА применялись диагностические наборы для определения вирусов картофеля ГНУ Всероссийский НИИ картофельного хозяйства им. А.Г.Лорха РАСХН (п. Коренево) [3]. Срезы тканей растений картофеля делали с помощью салазочного микротома, окуляр-микрометром определялись длина устьиц, размеры клеток хлоренхимы [4; 56–103].
Обсуждение результатов
Первоначальным этапом создания иммуноферментной диагностической тест-системы для детекции вирусной инфекции является накопление отдельных вирусов в тест-растениях с целью получения высокоочищенного вирусного препарата.
Известно, например, что для накопления Х-вируса картофеля можно использовать растения Datura stramonium, Chenopodium, Nicotiana tabacum, Homphrena и др. [5, 6]. Из нескольких видов и сортов растений, использованных при изучении способов оптимальной инокуляции и накопления вирусной инфекции, нами были отобраны для работы дурман, картофель сорта Артемис и табак сорта Самсун, иммунный к ВТМ и мучнистой росе.
В лаборатории биотехнологии растений кафедры защиты и карантина растений КАТУ им. С.Сейфуллина были высеяны семена тест-растений и определена их лабораторная всхожесть (табл. 1).
Лабораторная всхожесть семян тест-растений
Т а б л и ц а 1
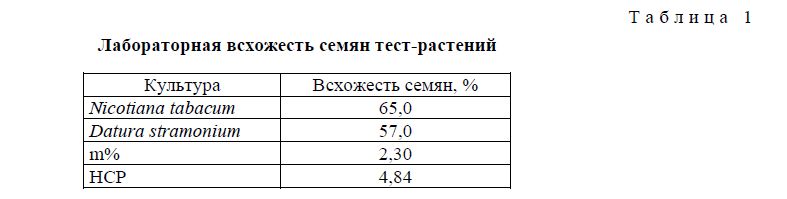
Согласно данным таблицы 1, лабораторная всхожесть изучаемых видов растений находилась в пределах 57–65 % (рис.1).
Рисунок 1. Определение лабораторной всхожести семян тест-растений
На тест-растениях, зараженных штаммом PVX, через две недели появлялись ярко выраженные симптомы в виде крапчатой пятнистости, морщинистости листьев, первичной и вторичной некротизации.
На молодых листьях образовывалась светло-зеленого цвета мозаика, т.е. пятна разной интенсивности, величины и формы. В проведённых нами цитоанатомических исследованиях было выявлено, что в клетках эпидермиса листьев, поражённых PVX, наблюдалось измельчение клеток. На срезах листьев, поражённых вирусной инфекцией, заметно уменьшение количества слоёв столбчатой и губчатой паренхимы. Объём межклеточников губчатой хлоренхимы снижался, палисадные клетки укорачивались, некоторые теряли свою вертикальную ориентацию, при этом мезофилл уплотнялся, толщина листа уменьшалась. В клетках хлоренхимы, пораженных вирусами растений картофеля, наблюдалось уменьшение размеров ядра, увеличивались размеры вакуолей. Размеры хлоропластов в поражённых вирусами листовых пластинках измельчались. Количество хлоропластов в клетках снижалось по сравнению с клетками здоровых растений, подобные изменения наблюдались нами и при изучении поражения растений PVY [7]. По мере разрушения клеток происходила некротизация тканей. В клетках появлялись кристаллы в виде рафидов.
Патологические изменения происходили и в жилках листьев, наблюдалось их недоразвитие, утолщение клеточных оболочек, измельчение клеток колленхимы. На некоторых растениях в процессе старения пятна постепенно исчезали, таким образом вирус переходил в латентную, бессимптомную форму.
Как известно, для выделения вирусов картофеля из растений-накопителей обычно используются листовой материал [4]. Поэтому на этапе накопления вирусной инфекции важно получить максимум вегетативной массы растений за короткий период.
В этой связи из полученных ботанических сеянцев, в соответствии с рисунком 2, была выращена рассада тест-растений и проведена их пикировка.

Рисунок 2. Пикировка рассады D. stramonium
Далее, в соответствии с рисунком 3, проводили изучение способов инокуляции тест-растений различными вирусами картофеля.
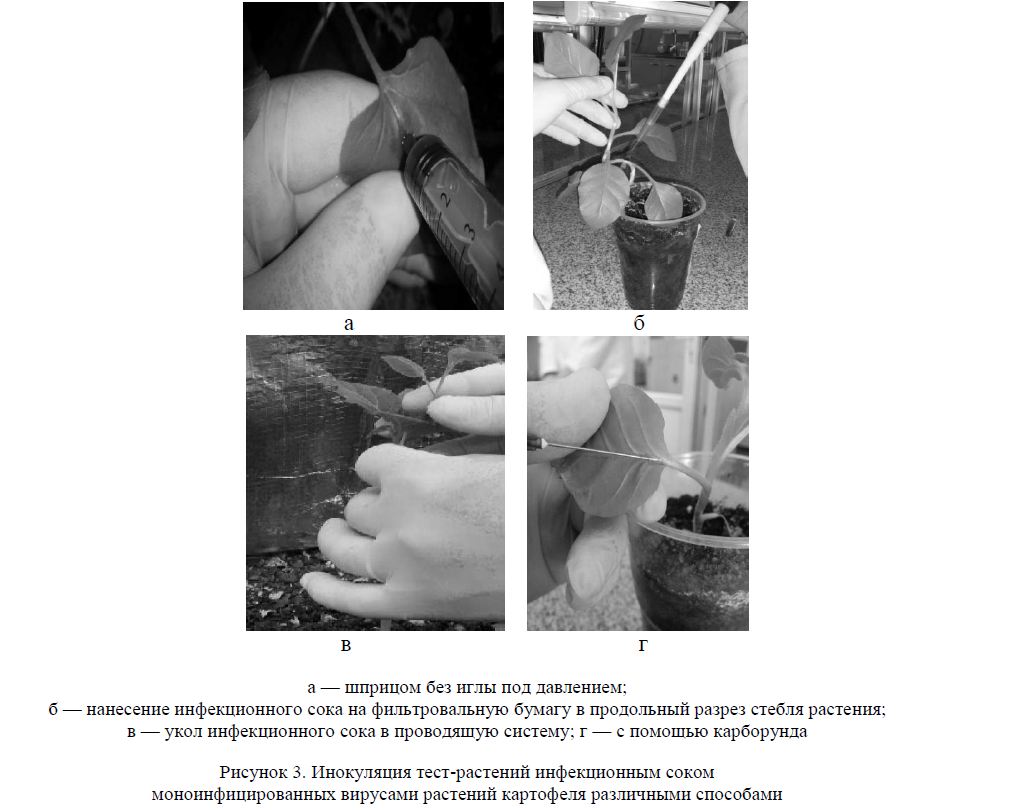
Рисунок 3. Инокуляция тест-растений инфекционным соком моноинфицированных вирусами растений картофеля различными способами
После инокуляции тест-растений изучали динамику накопления вирусов картофеля на 15–40-е сутки. Следует отметить, что листовые пробы, использованные для проверки вирусной инфекции в разные сроки, хранились при +4°С и были протестированы одновременно. Исходная относительная концентрация изучалась в «сэндвич-варианте» ИФА в единицах оптической плотности (экстинции) — о.е. (табл. 2).
Т а б л и ц а 2
Динамика накопления Х-вируса картофеля в успешно инокулированных тест-растениях, «сэндвич-вариант» ИФА
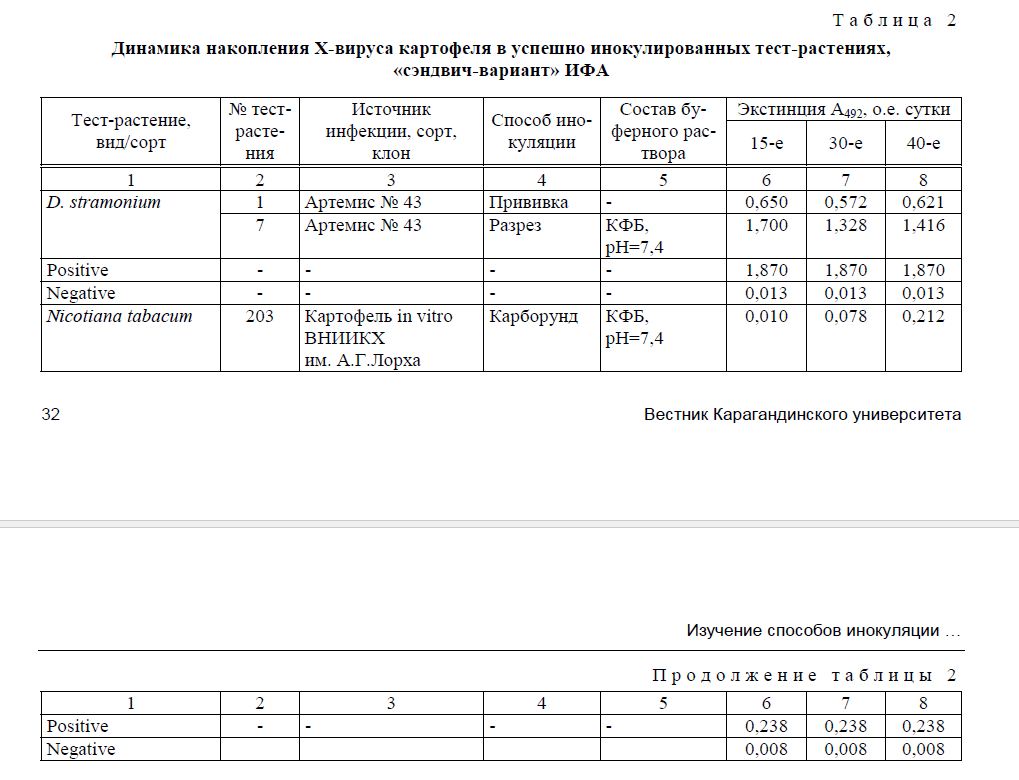
Как видно из данных таблицы, растения Nicotiana tabacum при механической инокуляции карборундом накапливали вирусную инфекцию на 30-е сутки.
Известно, что основным показателем, влияющим на выход вирусного препарата, является титр вируса в инфекционном соке тест-растения.
В этой связи на заключительном этапе наших исследований определялся рабочий титр PVX в инфекционном соке инокулированных тест-растений Datura stramonium и Nicotiana tabacum в «сэндвич-варианте» ИФА (табл. 3).
Т а б л и ц а 3
Результаты изучения рабочих титров вирусов картофеля в инокулированных тест-растениях в «сэндвич-варианте» ИФА

Как видно из таблицы 3, наиболее высоким титром со специфическими антителами в ИФА обладал сок растения-накопителя PVХ — D. stramonium.

Рисунок 5. Инокуляция в разрез стебля растения D. stramonium c cимптомами PVХ на 15-е сутки
Как видно из рисунков 3 и 4, растения Datura stramonium были успешно заражены PVХ при использовании обоих способов инокуляции: прививкой и в разрез стебля. Однако на варианте с прививкой (рис. 4) симптомы начинали появляться уже через неделю на нижних листьях растения как и в случае с прививкой картофеля инфицированного PLRV к дурману (рис. 5), и затем уже на 30-е сутки — на верхних листьях отросшего под привоем побега. Изменение окраски нижних листьев D. stramonium может быть связано с оттоком органических веществ привоя к подвою. В случае инокуляции PVХ в разрез стебля, в соответствии с рисунком 4, симптомы уже проявлялись на 5-е сутки на молодых листьях нового побега, что подтверждалось также высокой экстинцией в ИФА в данный период.
Выводы
На основании проведенных исследований необходимо сделать следующие выводы:
- Установлено, что PVX успешно накапливается на 15-е сутки в D. stramonium при нанесении инфекционного сока на фильтровальную бумагу в продольный разрез стебля растения. В растениях Nicotiana tabacum X-вирус накапливается на 40-е сутки при инокуляции карборундом.
- Действие вирусов на поражённое растение табака проявлялось в уменьшении размеров клеток покровных тканей, изменением их структуры. В клетках хлоренхимы, пораженных вирусами растений, установлено уменьшение ядер, увеличение размеров вакуолей, измельчение хлоропластов. По мере разрушения клеток происходит некротизация тканей листьев, появляются кристаллы в виде рафидов.
Список литературы
- Амелюшкина Т.А., Семешкина П.С. Защита семенных посадок картофеля от вирусных болезней // Защита и карантин растений. — 2011. — № 3. — С. 21–23.
- Гнутова Р.В. Серология и иммунохимия вирусов растений. — М.: Наука, 1993. — 301 с.
- Симаков Е.А., Усков А.И., Варицев Ю.А. Новые технологии производства исходного оздоровленного материала в элитном семеноводстве картофеля: рекомендации. — М.: Агропромиздат, 2000. — 76 с.
- Паушева З.П. Практикум по цитологии растений. — М.: Агропромиздат, 1988. — 270 с.
- Николаева О.В. Современные иммунологические методы в массовой диагностике вирусов растений: обзорная информация. — М.: Наука, 1986. — 52 с.
- Бобкова А.Ф., Чирков С.Н. Применение иммуноферментного анализа для диагностики вирусных заболеваний картофеля: обзор // Сельскохозяйственная биология. — 1983. — № 5. — С. 32–35.
- Хасанов В.Т., Муранец А.П., Оразбаева Г.К., Букаев А. Инокуляция, накопление и идентификация вируса PVY картофеля в тест-растениях Nicotiana tabacum // Вестн. КАТУ им. С.Сейфуллина. — 2012. — № 4 (75). — С. 31–36.