Успех лечения злокачественных опухолей во многом зависит от точной диагностики. Для верификации диагноза в онкологии используются различные методы, наиболее современными из которых являются молекулярно-биологические.
Первый генетический маркер опухоли — филадельфийская хромосома (Ph) — был описан в 1960 г. Эта хромосома была обнаружена исследователями, работавшими в Филадельфии, Novell и Hungerford, в метафазных пластинках, полученных при культивировании клеток крови пациентов с хроническим миелолейкозом. Измененная хромосома представляла собой результат делеции примерно половины длинного плеча хромосомы 22 пары [1].
Филадельфийская хромосома (Ph) обнаруживается более чем у 90 % больных хроническим миелолейкозом (ХМЛ) как взрослых, так и детей. Образуется она вследствие реципрокной, или сбалансированной, транслокации между хромосомами 9 и 22 пар — t (9;22)(q34; q11). При этом хромосома 9 пары повреждается в локусе q34, где локализован онкоген ABL, а 22 хромосома — в точке q11, где находится ген BCR (breakpoint cluster region). В результате транслокации на 22 хромосоме образуется новая патологическая последовательность ДНК, ген BCR-ABL, белковый продукт которого характеризуется повышенной тирозинкиназной активностью, как большинство известных онкопротеинов. Интересно, что в тех случаях, когда у больных ХМЛ обнаруживаются нетипичные хромосомные изменения или нормальный кариотип, BCR-ABL ген выявляется в клетках костного мозга и периферической крови пациентов. Другим известным заболеванием, при котором выявляется эта транслокация, является острый лимфобластный лейкоз (ОЛЛ). При этой форме лейкоза филадельфийская хромосома выявляется у 5 — 10 % детей с ОЛЛ. Ph-хромосома у больных ОЛЛ, как и при ХМЛ, образуется вследствие реципрокной транслокации t (9;22)(q34; q11) и цитогенетически не отличима при этих заболеваниях [2].
Для исследования ДНК наиболее часто применяются цитогенетический анализ, Southern-блот и полимеразная цепная реакция (ПЦР). ПЦР (polymerase chain reaction, PCR), безусловно, завоевала звание «чемпиона» методик молекулярной медицины, поскольку позволяет выявлять ничтожно малые количества фрагментов ДНК [3]. В настоящем исследовании для определения патологического гена BCR-ABL в крови пациентов, больных лейкозом, был использован этот анализ.
Целью настоящего исследования явилось выявление филадельфийской хромосомы методом ПЦР у больных различными формами лейкозов, проживающих в Карагандинской области.
Материалы и методы
Материалом для наших анализов были периферическая кровь и костный мозг пациентов, обследовавшихся в гематологическом отделении областной клинической больницы г. Караганды.
Выделение РНК. Выделение РНК из крови и костного мозга осуществляли с применением комплекта «Рибо-золь» и сорбента универсального. Биологический материал обрабатывали лизирующим раствором, а затем промывали дважды отмывочными растворами. РНК экстрагировали растворами фенола и хлороформа, затем промывали 70 %-ным этанолом. Полученную таким образом РНК растворяли в буфере ТЕ. Конечный объем составлял 50 мкл.
Реакция обратной транскрипции. При постановке этой реакции использовали набор реагентов «PEBEPTA-L». Для этого в пробирку с DTT лиофилизированным добавляли 125 мкл RT-mix и тщательно перемешивали на вортексе. К полученному раствору добавляли 6 мкл ревертазы (MMLV), перемешивали на вортексе. Вносили в микропробирки по 10 мкл готовой реакционной смеси, добавляли по 10 мкл РНК-пробы в пробирку с реакционной смесью. Осторожно перемешивали. Затем ставили пробирки в амплификатор (термостат) при 370С на 30 минут. Полученную в реакции обратной транскрипции кДНК разводили в 2 раза ДНК-буфером для последующей постановки реакции амплификации.
Постановка реакции амплификации. Для амплификации искомых фрагментов ДНК ставили 3 индивидуальные реакции для выявления патологических генов а3-е1, а3-е12 и а3-е19 в режиме, рекомендованном производителем наборов реагентов «Амплисенс». Использовали ПЦР смесь 1, содержащую праймер для выявления искомой транслокации. Смесь 2, содержащая буфер, набор дезоксирибонуклеотидтрифосфатов, Taq-полимеразу и бромфеноловый синий, наносилась поверх смеси 1.
Электрофорез ДНК. Электрофоретический анализ продуктов ПЦР проводили в агарозном геле с применением комплекта реагентов «ЭФ», вариант 300. Использовали 1,5 %-ную агарозу, трисборатный буфер (ТБЕ), концентрированный, с бромидом этидия. Напряженность электрического поля составляла 100 в/см2 [4].
Трис-боратный буфер, входящий в состав данного комплекта, обеспечивает хорошее разделение фрагментов ДНК и имеет значительную буферную емкость, не требующую его рециркуляции. Бромид этидия — флуоресцирующий и интеркалирующий в ДНК краситель, позволяющий визуализировать ДНК.
По окончании электрофореза агарозный гель фотографировали и анализировали с помощью компьютерной системы TotalLab.
Результаты и обсуждение
Нами исследованы образцы крови 40 пациентов гематологического отделения Карагандинской областной клинической больницы с различными формами лейкозов, такими как хронический миелолейкоз, миелопролиферативное заболевание, первичный миелофиброз, острый лимфолейкоз, идиопатический лимфолейкоз. У двух пациентов проанализированы образцы костного мозга. Районы проживания объектов исследования: города Караганда, Темиртау, Жезказган, населенные пункты Шетского, Каркаралинского, Казыбекбийского районов и др., характеризующиеся неблагоприятной экологической обстановкой. Возраст пациентов составлял от 23 до 70 лет.
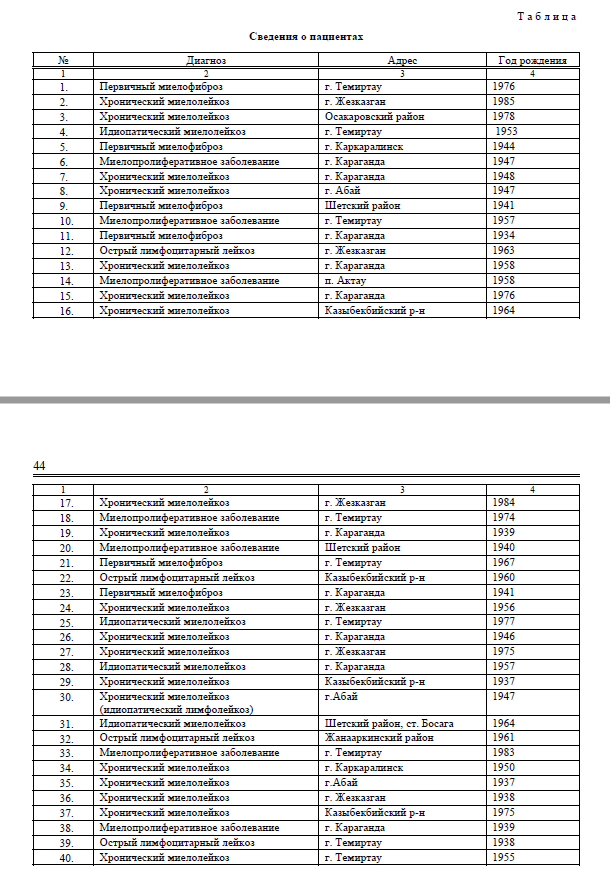
Данные о пациентах приведены в таблице.
Сведения о пациентах
Т а б л и ц а
РНК выделяли из сыворотки описанных выше пациентов, для чего венозную кровь центрифугировали, осаждали форменные элементы, отбирали супернатант — плазму. Для выделения РНК использовали сорбент универсальный. С полученными из образцов крови и костного мозга пациентов молекулами РНК ставили реакцию обратной транскрипции, используя фермент ревертазу. Время ревертазной реакции составляло 30 минут, температура 37 °С. По окончании с полученной кДНК ставили полимеразную цепную реакцию, количество циклов которой составляло 42. Поскольку в наших исследованиях применялся аппарат с матричным регулированием температур «Терцик МС2», использовали минеральное масло. В каждом эксперименте ставили реакции с положительными и отрицательными контрольными образцами. Положительный контрольный образец использовали для выявления фрагментов амплифицированных ДНК. Отрицательный контрольный образец применяли для исключения ложноположительных результатов. Детекцию продуктов амплификации осуществляли процедурой электрофореза в 1,5 %-ном агарозном геле. Применяли трисборатный буфер для электрофореза. Агарозный гель просматривали на трансиллюминаторе, фотографировали. Для точного определения размеров амплифицированных фрагментов ДНК картину электрофореза анализировали при помощи компьютерной системы TotalLab. Каждый раз использовали маркер молекулярного веса с фрагментами ДНК известного размера для сравнения размеров полученных амплифицированных сегментов нуклеиновых кислот.
Проведенные исследования обнаружили 12 случаев возникновения искомой нереципрокной транслокации фрагмента длинного плеча 9 хромосомы на длинное плечо 22 у 40 пациентов, больных описанными формами лейкозов, что составило 30 % всех исследованных образцов биологического материала.
Фотография электрофореза исследуемого патологического гена BCR-ABL, выявленного у одного из исследованных пациентов с диагнозом «хронический миелолейкоз», приведена на рисунке 1.
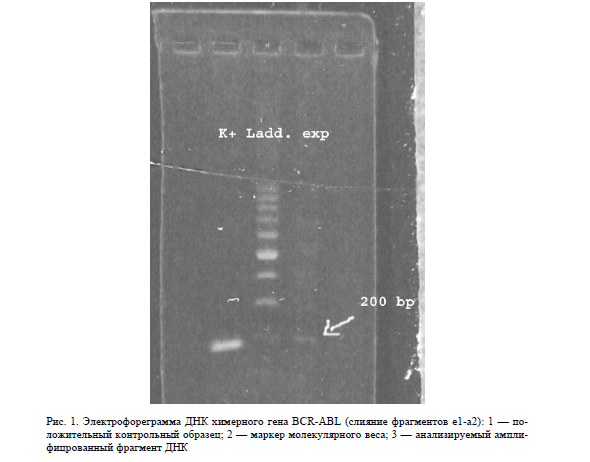
Рис. 1. Электрофореграмма ДНК химерного гена BCR-ABL (слияние фрагментов e1-a2): 1 — положительный контрольный образец; 2 — маркер молекулярного веса; 3 — анализируемый амплифицрованный фрагмент ДНК
Из рисунка видно, что выявляется специфический транскрипт, соответствующий химерному гену BCR-ABL (слияние фрагментов e1-a2), размером примерно 200 пар оснований. Транскрипт соответствует белку p185.
В результате исследований выявлены различные транскрипты, соответствующие гену BCR-ABL, образовавшемуся в результате слияния фрагментов 9 и 22 пар хромосом. Обнаружено слияние фрагментов e1-a2, е2-а2. У одного пациента с диагнозом «миелопролферативное заболевание» обнаружено сразу 2 транскрипта, образованных слиянием различных фрагментов указанных хромосом, размерами 400 и 500 п.н. Транскрипты соответствовали белкам p185–190.
Картина электрофореза ДНК, выделенной из крови другого пациента с хроническим миелолейкозом, приведена на рисунке 2. Данная электрофореграмма обработана с помощью компьютерной системы TotalLab, что позволяет с высокой точностью определить размеры выявленных фрагментов ДНК.
Анализ фотографии электрофореза, представленной на рисунке 2, позволил обнаружить у данного пациента фрагмент ДНК исследуемого гена BCR-ABL размером 220 п.н., что доказывает наличие в этом случае транскрипта, образованного слиянием фрагментов e2-a2. Данная патология соответствует синтезу белка р190. Ген G6PD использовали в качестве положительного контрольного образца.
Полученные данные согласуются с литературными, в которых исследователями обнаруживались подобные транслокации в локусах р22 хромосомы 9 и q23 хромосомы 22 [5]. Кроме того, белок аналогичного размера, обусловленный возникновением химерного гена BCR-ABL, обнаруживали в результате выявления инверсии в хромосоме 3 [6].
Дальнейшие исследования предполагают анализы костного мозга на предмет обнаружения искомой транслокации t (9;22) у пациентов с лейкозами. Будут проведены также исследования детей с различными формами лейкозов, наблюдающихся в Карагандинском областном детском онкогематологическом центре.

Рис. 2. Электрофореграмма ДНК химерного гена BCR-ABL (слияние фрагментов e2-a2): 1 — маркер молекулярного веса; 2 — анализируемый амплифицрованный фрагмент ДНК; 3 — положительный контроль — ген G6PD
Кроме того, будут исследованы образцы крови и костного мозга пациентов с описанными формами лейкозов с целью выявления других форм транслокаций в режиме «Real-time», а также для определения чувствительности анализа при исследованиях различных биологических проб.
На основании полученных данных можно сделать вывод о том, что у пациентов, больных различными формами лейкозов (как острых, так и хронических), обнаруживается патологический ген BCR-ABL, обусловленный транслокационным слиянием различных фрагментов хромосом 9 и 22.
Список литературы
- Мельник А.И., Мельник В.А., Цыба Л.Н., Глущенко Э.Н. Клиническая характеристика хронического миелобластного лейкоза у детей раннего возраста // Актуальні питання педагогіки, експериментальної та кліничної медицини / Республіканська збірка наукових праць. — Донецьк, 1995. — С. 243–242.
- Vieira L., Sousa A.C., Matos P., Marques B., Alaiz H., Ribero M.J., Braga P., da Silva M.G., Jordan P. Three-way tranclocation involves MLL, MLLT3, and a novel cell cycle control gene, FLJ10374, in the pathogenesis of acute myeloid leukemia with t (9;11;19)(p22; q23; p13.3) // Genes Chromosome Cancer. 2006 May;45(5):455–469.
- Глик Б., Пастернак Дж. Молекулярная биотехнология. Принципы и применение. — М.: Мир, 2002. — 589 с.
- Залетаев Д.В., Кулешов Н.П. Молекулярная диагностика наследственной патологии / Сб. науч. тр. МОНИКИ. — М., 1995. — С. 133–139.
- Scholl , Schlenk R.F., Eiwen K., Dohner H., Frohling S., Dohner K., AML Study Group The prognostic value of MLL-AF9 detection in patients with t (9;11)(p22; q23)-positive acute myeloid leukemia // Haematologica. 2005 Dec;90(12):1626–1634.
- Han J.Y., Theil K.S. The Philadelphia chromosome as a secondary abnormality in inv (3)(q21q26) acute myeloid leukemia at diagnosis: confirmation of p190 BCR-ABL mRNA by real-time quantitative polymerase chain reaction. // Cancer Cytogenet. 2006 Feb; 165(1): 70–74.