Нами проведен сравнительный анализ результатов вакцинации у 254 детей с хроническими болезнями почек (ХБП). Установлено, что при стандартной вакцинации поствакцинальный иммунитет лучше сохранен у детей с 1-2 стадиями ХБП (61,5 и 41,3% соответственно). При ХБП 3 стадии снизился до 37,5%, 4 стадии – 27,9 и 5 стадии до 18,9%. Повторная вакцинация детей с 1-4 стадиями ХБП в двойной дозе по схеме 0-1-6 мес. сопровождалось формированием достаточного поствакцинального иммунитета. Тогда как дети, на гемодиализе вакцинированные четырехкратно в двойной дозе по сравнению с детьми получившие иммуномодулятор на фоне вакцинации показали малоэффективный результат.
Вирусный гепатит В остается одной из самых актуальных и социальных проблем здравоохранения во всем мире, включая Казахстан. Несмотря на существенный прогресс в профилактике гепатита В, достигнутый за последние годы, распространенность этой инфекции снижается медленно и остается по-прежнему достаточно высокой. Результаты стандартной вакцинации пациентов с хронической болезнью почек (ХБП), остаются низкими и неудовлетворительными 1,2. Кроме того, ответ на вакцинацию у пациентов с почечной недостаточностью имеет тенденцию к снижению, а у пациентов с терминальной почечной недостаточностью (ТПН) становятся отрицательными в течение первых 6-12 мес. начала лечения гемодиализом (ГД)
3. Разработаны различные стратегии для улучшения иммунного ответа на вакцинацию среди пациентов с ХБП: изменение схемы, дозы вакцинации, техника введения и разработка новой вакцины 4,5. У больных с уремией вследствие свойственного им иммунодефицита, эффективность вакцинопрофилактики гепатита В оказалась существенно ниже, несмотря на иммунизацию двойной дозой вакцины (обычно 40 мкг) при четырехкратном введении по схеме 0-1-2-6 месяцев [6,7]. Поэтому с целью оптимизации результатов вакцинации у пациентов с ХБП рекомендуется проведение ранней вакцинации с применением препаратов стимулирующих иммунный ответ, поскольку депрессия иммунитета выявляется уже на начальной стадии почечной недостаточности 8.
Цель исследования: оценка эффективности различных схем вакцинации гепатита В у детей с различными стадиями ХБП. Материалы и методы исследования. Нами проведено обследование 254 детей с различными стадиями ХБП, получавших лечение в отделениях нефрологии и гемодиализа гг. Алматы и Астаны. Возраст пациентов находился в диапазоне от 1 до 18 лет, и в среднем составил 11,74,10 лет. Среди пациентов, включенных в исследование, преобладали мальчики 128 (50,4%). В структуре заболеваний, приведших к ХБП, преобладали врожденные аномалии мочевыводящей системы 117 (46%), хронический гломерулонефрит выявлен у 100 (39,3%) детей, нефрит Шенлейн-Геноха у 16 (6,3%), наследственный нефрит у 7 (2,8%), люпус-нефрит у 3 (1,2%), тубулоинтерстициальный нефрит у 5 (2%), хронический пиелонефрит у 4 (1,6%) и диабетическая нефропатия (ДН) у 2 (0,8%).
По формуле Шварца был произведен расчет скорости клубочковой фильтрации (СКФ) с распределением детей на стадий ХБП 9. В 1 стадию ХБП вошли 26 (10,2%) детей с уровнем креатинина сыворотки 44,45,5 мкмоль/л, соответственно СКФ до 14511,7 мл/мин. 63 (24,8%) пациента с креатинином 72,515,4 мкмоль/л и снижением СКФ до 78,215,7 мл/мин во 2 стадию. В 3 стадии 32 пациента с уровнем креатинина 118,552,1 мкмоль/л и снижением СКФ до 47,615,8 мл/мин. У пациентов с 4 стадией (22/8,7%) уровень креатинина достоверно различался по сравнению с 1-3 стадиями ХБП и составил 287,787 мкмоль/л (р0,05), со снижением СКФ до 19,310 мл/мин. Достоверно значимые различия по уровню креатинина (853,1251 мкмоль/л) и значительному снижению СКФ (7,01,87 мл/мин) были характерны для больных на ГД с 5 стадией ХБП. Дети с ХБП 5 стадией получали заместительную почечную терапию программным гемодиализом (ПГД) в период 2002-2008 годы в отделениях гемодиализа гг. Алматы и Астаны. Процедура гемодиализа проводилась по стандартной программе 3 раза в неделю по 3,5-4 часа с продолжительностью ПГД от 1 до 74 мес., в среднем 11,912,5 мес.
детей были вакцинированы ранее стандартно в одинарной дозе по схеме 0-1-6 мес. Повторная вакцинация проведена детям (62) при снижении титра протективных антител 10 мМЕ/мл или отрицательном ответе вакциной ЭнджериксВ. Детям с ХБП 2-4 стадией трехкратно по схеме 0-1-6 мес. в двойной дозе, с ХБП 5 стадией четырехкратно в двойной дозе по схеме 0-1-2-6 мес. внутримышечно. На гемодиализе 11 детей из 27 были вакцинированы для стимуляции иммунного ответа в комбинации с иммуномодулятором Левамизолом в дозе 1 мг/кг однократно per os после каждого сеанса гемодиализа в течение 4-х мес.
Определение маркеров вирусных гепатитов В, С: HBsAg, aнтиHBcore IgM, анти-НВ core total (суммарный), анти-HBs количественный, HBeAg, анти-НВе и aнти-HCV выполняли методом иммуноферментного анализа на автоматическом анализаторе ABBOT с применением тест-систем этой же фирмы каждые 6 мес.
Контроль за динамикой титра анти-HBs при вакцинации проводилась через 1 мес., 3 мес., 6 мес., 6-12 мес., 12-24 мес. и более 24 мес. ДНК ВГВ и РНК ВГС подтверждали ПЦРдиагностикой.
Результаты исследования. В ходе исследования установлено, что 85 (33,4%) детей были инфицированы HBV, наибольший процент приходиться на детей на ГД – 56 (50,5%).
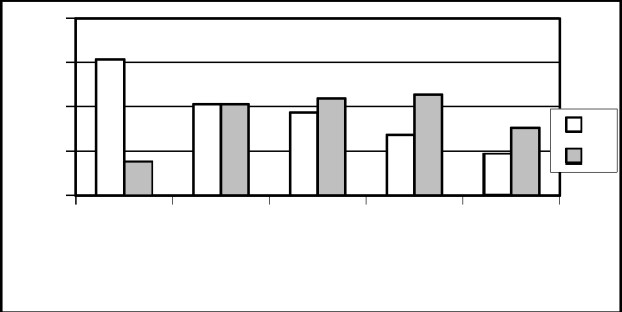
При анализе поствакцинального иммунитета установлено, что у (34,2%) из 170 есть поствакцинальный иммунитет. При рассмотрении по группам выявлено, что иммунитет от HBV лучше сохранен у детей с 1 группой (16/61,5%) и 2 стадией ХБП (26/41,3%). По мере прогрессирования почечной недостаточности отмечалось снижение поствакцинального иммунитета: при 3 стадии ХБП – присутствовал у 12(37,5%), 4 стадии – у 6(27,9%), а при ХБП 5 стадии (на гемодиализе) только у 21(18,9%) (рисунок 1).
С целью уточнения динамики титра анти-HBs мы
 80 61,5
80 61,5
60
40
41,341,337,43,8 45,5
27,3
5
30,6
проанализировали в сравнительном аспекте стандартно и повторно вакцинированных детей с различными стадиями ХБП.
86 (33,8%) детей вакцинированных стандартным методом с различными стадиями ХБП сохранили поствакцинальный
15,4
20
0
18,9
е… иммунитет (таблица 1).
Однако с тенденцией к понижению поствакцинального
н…
иммунитета в динамике. Если при исследовании исходный титр анти-HBs у больных с 1 стадией ХБП (16) составлял 220,0234,5
мМЕ/мл, то через 36 мес. титр антител снизился до 62,068,9
ХБП 1 ХБП 2 ХБП3 ХБП 4 ХБП 5
мМЕ/мл (р0,001). При ХБП 2 стадии (26) титр был 205,8205
ст. ст. ст. ст. ст
мМЕ/мл, через 36 мес. снизился до 47,655,9 мМЕ/мл, у детей с
3 стадией (12) анти-HBs в начале исследования составили 140,2159,9 мМЕ/мл, то через 36 мес. 39,790 мМЕ/мл (р0,001).
Рисунок 1 – Частота поствакцинального иммунитета у детей с ХБП
Таблица 1. Динамика титра анти-HBs у детей с ХБП вакцинированных стандартным методом
|
Стадии ХБП |
Пол м/д |
Динамика титра анти-HBs |
|||||
|
ч/з 1 мес. |
ч/з 3 мес. |
ч/з 6 мес. |
ч/з 12 мес. |
ч/з 24 мес. |
ч/з 36 мес. |
||
|
1 |
10/6 |
220,0234,5 |
201,7219,3 |
157,7157,88 |
116110,2 |
90,694,2 |
62,068,9 |
|
2 |
11/ 15 |
205,8205 |
180,8179,8 |
153,9154,4 |
121,3125 |
81,585 |
47,655,9 |
|
3 |
5/7 |
140,2159,9 |
118,2152,4 |
97,2131,9 |
76,9123 |
61,9112 |
39,790 |
|
4 |
3/4 |
108,21125 |
84,299,0 |
66,686,0 |
50,267,6 |
34,755,1 |
6,186,68 |
|
5 |
9/12 |
175,9200 |
138,8173 |
103149 |
71,2124 |
40,181 |
11,526 |
Значительное снижение титра протективных антител было характерно для детей с ХБП 4 и 5 стадиями. При 4 стадии титр антител снизился с 108,21125 мМЕ/мл до 6,186,68 мМЕ/мл (р0,001), при 5 стадии с 175,9200 мМЕ/мл до 11,526 мМЕ/мл (р0,001).
Таким образом, по мере прогрессирования ХБП титр протективных антител, у детей вакцинированных стандартно, сопровождался прогрессивным снижением их уровня, что повышает риск инфицирования HBV в будущем.
Анализ повторно вакцинированных против HBV детей (62) показал, что почти все дети сформировали достаточный поствакцинальный иммунитет против гепатита В (серопротекция) (таблица 2).
При ХБП 2 стадии титр антител составил 671,1162 мМЕ/мл, через 36 мес. оставался на достаточно высоком уровне 433,3157 мМЕ/мл, с 3 и 4 стадиями титр был в пределах 424,0269 и 427,6261 мМЕ/мл соответственно и в динамике 270,1243 и 272,7250 мМЕ/мл. Тогда как поствакцинальный иммунитет у детей на ГД достоверно различался при сравнении вакцинированных бези с применением иммуномодулятора Левамизола.
У детей (16) которым проводилась вакцинация четырехкратно (0-1-2-6 мес.) в двойной дозе без иммуномодулятора титр антител сопровождался значительным снижением в динамике с 472,3290 мМЕ/мл до 11,5120 мМЕ/мл (р0,001). Тогда как дети, получившие Левамизол в течение 4-х мес. после каждого сеанса гемодиализа, показали достаточный уровень анти-HBs после вакцинации (987,933,6 мМЕ/мл) с незначительным снижением в динамике (842,777,8 мМЕ/мл).
Таблица 2. Динамика титра анти-HBs у детей с ХБП повторно вакцинированных
|
Стадии ХБП |
Пол м/д |
Динамика титра анти-HBs |
|||||
|
ч/з 1 мес. |
ч/з 3 мес. |
ч/з 6 мес. |
ч/з 12 мес. |
ч/з 24 мес. |
ч/з 36 мес. |
||
|
2 |
9/4 |
671,1162 |
619,6162 |
572,2176 |
522,4174 |
480,5 178 |
433,3 157 |
|
3 |
10/3 |
424,0269 |
396,7265 |
371,7269 |
326,0260 |
289,6 247 |
270,1243 |
|
4 |
4/5 |
427,6261 |
394,4265 |
351,5269 |
313,6236,3 |
271,1 260 |
272,7 250 |
|
5 без левамизол а |
7/9 |
472,3 290 |
402,2 262 |
335,6 227 |
280,3 200 |
210,3 166 |
11,5 120 |
|
5 с левамизолом |
6/5 |
987,9 33,6 |
989,030,1 |
971,341,2 |
941,864,2 |
912,9 71,3 |
842,7 77,8 |
Больные с ХБП в додиализной стадии (1-4) стандартно вакцинированных имели тенденцию к снижению защитного уровня антител. Тогда как проведение вакцинации трехкратно в удвоенной дозе способствовало длительному сохранению поствакцинального иммунитета на достаточно высоком уровне. Заключение. Результаты вакцинации детей на гемодиализе показали, что при стандартной вакцинации титр быстро снижался до отрицательной. Тогда как вакцинация в комбинации с иммуномодулятором оказалась намного эффективной в отличие от четырехкратной вакцинации в двойной дозе без стимуляции иммунного ответа. Снижение или отсутствие поствакцинального иммунитета у детей на гемодиализе обусловлено вторичным иммунодефицитом, характерного для больных с уремией.
Таким образом, с целью оптимизации результатов вакцинопрофилактики гепатита В у больных с ХБП необходимо проведение максимально ранней вакцинации. Для повышения эффективности вакцинации против гепатита В при ТПН рекомендуется использование препаратов, стимулирующих иммунный ответ. Комплексный подход к профилактике гепатита В в отделениях ГД позволит существенно уменьшить распространенность этой инфекции, а также повысить эффективность заместительной терапии ТПН.
Список литературы:
- CDC. Recommendations for preventing transmission of infections among chronic haemodialysis patients//MMWR. – 2001.
- Chaabane NB, Loghmari H, Melki W, Hellara O, Safer L, Bdioui F, Saffar H. Chronic viral hepatitis and kidney failure// Presse Med. – 2008. – Vol. 37(4 Pt 2). – Р. 665-78.
- Lacson E, Teng M, Ong J, Vienneau L, Ofsthun N, Lazarus JM. Antibody response to Engerix-B and Recombivax-HB hepatitis B vaccination in end-stage renal disease//Hemodial. Int. – 2005. – Vol.9. – Р. 367-75.
- Weinstein T, Chagnac A, Boaz M, Ori Y, Herman M, Zevin D, et al . Improved immunogenicity of a novel third-generation recombinant hepatitis B vaccine in patients with end-stage renal disease//Nephron Clin Pract. – 2004. – Vol. 97. – Р.67-72.
- McNulty CA, Bowen JK, Williams AJ. Hepatitis B vaccination in predialysis chronic renal failure patients a comparison of two vaccination schedules// Vaccine. – 2005. – Vol.23. – Р. 4142-7.
- Girndt M., Kohler H. Hepatitis В Virus Infection Hemodialysis Patients// Seminars in Nephrology. – 2002. – Vol.4. – Р.340-350.
- Bruguera M., Cremada M., Rodicio J.L. et al. Immunogenecity of a yeast-derived hepatitis В vaccine in hemodialysis patients//Am J Med. – 1989. – Vol. 87. – Р.30-32.
- Shahnaz Sali, Seyed M Alavian, Behzad Hajarizadeh. Effect of levamisole supplementation on hepatitis B virus vaccination response in hemodialysis patient//Nephrology. – 2008. – Р.14401797.
- National Kidney Foundation. K/DOKI clinical practice guidelines for chronic kidney diseases: evaluation, classification and stratification//Am. J. Kidney Dis. – 2002. – Vol.39 (suppl. 1). – Р.S17S31.