Введение. В последние годы рак предстательной железы (РПЖ) становится наиболее распространенным злокачественным новообразованием у мужчин, занимая лидирующее положение в развитых странах мира. Ежегодно в мире выявляется более 900 тысяч больных РПЖ, а более 250 тыс. умирает *1,2,3+. Аналогичная тенденция к росту заболеваемости и смертности РПЖ наблюдается и в Республике Казахстан (РК). Так в 2001 г. с впервые жизни установленным диагнозом РПЖ взято на учет 534 (3,6 %000) мужчин, а в 2011 г. - 835 (4,8 %000), при высоких динамических показателях смертности: в 2001г. - 296 (2,0 %000), а в 2011 г. - 407 (2,4 %000) мужчин [4,5].
Также в РК остается достаточно высоким удельный вес больных с III-IV стадией заболевания. Так например в 2001г. III-IV стадия выявлена у 76,1% больных РПЖ, а в 2011 г. у 63,3% больных *4,5+. Из-за с поздней диагностики и большим числом пациентов с местнораспространенными и диссеминированными формами РПЖ, лучевая терапия (ЛТ) по-прежнему остается основным специализированным видом локального лечения в большинстве случаев РПЖ *6,7,8+. Также ЛТ является методом выбора при локализованных формах РПЖ, в определенной степени конкурирующим с радикальной простатэктомией. При этом следует учитывать, что ЛТ не вызывает столь серьезных осложнений, как хирургическое вмешательство и качество жизни больных, практически не страдает.
Внедрение методик высокотехнологичного облучения, т.к. CRT, IMRT, IGRT, VMAT, DART, SRT с использованием многолепестковых коллиматоров линейных ускорителей в последнее время значительно потеснило оперативное лечение, т.к. отдаленные результаты обоих методов лечения стали приблизительно одинаковы, но ЛТ не вызывает столь серьезных осложнений, как хирургическое вмешательство *6,7,8,9,10,11+.
Среди всех гормонально зависимых опухолей злокачественные опухоли простаты считаются наиболее чувствительными к гормональной терапии (ГТ). Она является единственным эффективным лекарственным методом лечения РПЖ, позволяющим добиться стойкой ремиссии заболевания у большинства больных РПЖ при любой стадии процесса в самостоятельном или комбинированном (с ЛТ или операцией) режимах [6,8,12].
Однако до настоящего времени не существует единой точки зрения на проведение гормонального лечения при опухолях предстательной железы. Выбор метода кастрации, целесообразность использования антиандрогенов на фоне хирургической или медикаментозной кастрации по-прежнему остается дискутабельными. А назначение ГТ по схеме - максимальная андрогенная блокада (МАБ) совместно с облучением общепринятой во многих онкологических клиниках, рядом авторов до сих пор считается малоэффективным *13,14,15+.
Таким образом, проблема лечения РПЖ по-прежнему остается актуальной задачей в современной онкологии и урологии. Несмотря на комплексный подход в лечении больных с данной патологией, прогноз для этой группы больных часто остается весьма неблагоприятным, особенно при местно-распространенных и диссеминированных формах. Поэтому необходим поиск новых терапевтических режимов, которые должны увеличивать частоту непосредственного ответа, выживаемость и качество жизни.
Цель исследования - повышение эффективности лечения рака предстательной железы за счет оптимациии методик гормоно- и лучевой терапии.
Материалы и методы. Контролируемое клиническое исследование проведено на 60 пациентах с местнораспространенным раком предстательной железы (С61 по МКБ-10), без оперативного лечения, которые были разделены на две группы в зависимости от методики лучевой терапии. 1-я группа (основная) -30 (50,0%) больных РПЖ. Им проведена конформная лучевая терапия в комбинации с ГТ по МАБ. 2-я группа (контрольная) - 30 (50,0%) больных РПЖ. Им проведена конвенциальная лучевая терапия на фоне ГТ по МАБ. Распределение больных в группах в зависимости от возраста, стадии заболевания представлены в таблице 1. Как видно из представленных данных возраст больных колебался от 54 до 72 лет, при среднем возрасте 61,8±6,1 лет.
Таблица 1 Клиническая характеристика больных раком предстательной железы.
|
Группы |
Средний возраст (годы) |
Стадия |
|||
|
STIII |
STIV |
||||
|
T3N0M0 |
T3N1M0 |
T4N0M0 |
T4N1M0 |
||
|
1-я /п=30/ |
63,5±5,9 |
12 (40,0±8,9%) |
6 (20,0±7,3%) |
3 (10,0±5,4%) |
9 (30,0±8,3%) |
|
2-я /п=30/ |
60,1±6,6 |
15 (50,0±9,1%) |
3 (10,0±9,4%) |
3 (10,0±5,4%) |
9 (30,0±8,3%) |
|
ИТОГО /п=60/ |
61,8±6,3 |
27 (45,0±6,4%) |
9 (15,0±4,6%) |
6 (10,0±3,8%) |
18 (30,0±5,9%) |
Стадирование осуществляли в соответствии с рекомендациями Международного противоракового Союза по системе TNM (2007). С 3-й стадией заболевания
- T3N0M0 было всего 27 (45,0%) больных из них 12 (40,0%) в 1-й группе и 15 (50,0%) во 2-й группе. С 4-й стадией процесса было всего 33 (55,0%). Из них с T3N1M0 6 (20,0%) и 3 (10,0%) больных, с T4N0M0 3 (10,0%) и 3 (10,0%) больных, с T4N1M0 9 (30,0%) и 9 (30,0%) в 1-й и 2-й группах соответственно (таблица 1).
У всех больных диагноз РПЖ был подтвержден морфологически, на основании гистологического исследования биопсийного материала после проведенной тонкоигольчатой биопсии из 6 точек под контролем ТРУЗИ.
В соответствии с общепризнанной международной гистологической классификацией опухолей предстательной железы и системой морфологической оценки степени злокачественности (grade) по Gleason (1977), мы разделили все гистологические типы опухоли в соответствии между показателем суммы по Gleason и степенью дифференцировки аденокарциномы (G): Gleason score 2-4 - G1; Gleason score 5-6 - G2; - Gleason score 7-10 - G3-4.
Как видно из представленных данных рисунка 1, больных с высокой степенью дифференцировки (G1) всего было 12 (20,0%) , с умеренной степенью дифференцировки (G2) 33 (55,0%), Пациентов с низкой степенью дифференцировки или отсутствие дифференциации (G3-4) было 15 (25,0%).
25,0 20,0
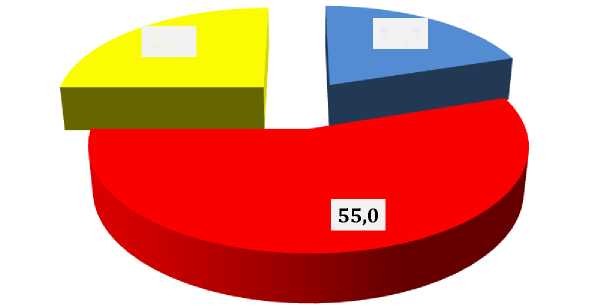
Распределение больных РПЖ по степени дифференцировки
- G1 (Gleason 2-4)
- G2 (Gleason 5-6)
- G3-4 (Gleason 7-10)
Рисунок 1 Распределение больных раком предстательной железы в зависимости от степени дифференцировки опухоли и числа Gleason
При этом больных дифференцировки 6 (20,0%) больных,дифференцировки (G2)с высокой степенью(G1) было пос умеренной степеньюбыло 15 (50,0%) и 18 (60,0%)больных, пациентов с низкой степенью дифференцировки или отсутствие дифференциации (G3-4) было 9 (30,0%) и 6 (20,0%) соответственно в 1-й группе и 2-й группе соответственно (таблица 2).
|
Группы |
G1 (Gleason 2-4) |
G2 (Gleason 5-6) |
G3-4 (Gleason 7-10) |
|
1-я группа |
6 (20,0±7,3%) |
15 (50,0±9,1%) |
9 (30,0±8,3%) |
|
2-я группа |
6 (20,0±7,3%) |
18 (60,0±8,9%) |
6 (20,0±7,3%) |
|
Итого |
12 (20,0±5,1%) |
33 (55,0±6,4%) |
15 (25,0±5,5%) |
Таблица 2 Распределение больных раком предстательной железы в испытуемых группах в зависимости от степени дифференцировки опухоли (Gleason)
Таким образом, представленные клинические данные свидетельствуют о сопоставимости их по основным клиническим признакам, таким как возраст, стадия заболевания, гистологическая структура опухоли.
Предлучевая подготовка к проведению конформной ЛТ (КФЛТ) проводилась в несколько этапов с применением VCT Light Speed GE и рентгеновского симулятора "Acuity CBCT". Она включала в себя: 1) подготовка пациента, за 3 часа до процедуры употребить не более 100 мл воды за час опорожнение мочевого пузыря. С контрастированием прямой кишки водорастворимым контрастом; 2) симуляция на "AcuityCBCT" c вынесением опорной точки и боковых проекций; 3) создание идентичных условий (укладка на ровной поверхности с совпадением опорных меток) на аппаратеМСКТ, получение КТ срезов области подлежащей облучению с шагом в 2,5 и 5,0 мм., Перенос в систему дозиметрического планирования данных в формате DICOM; 4) контурирование мишени и критических органов на компьютерной системе планирования ECLIPSE, реконструкция объемного 3-D виртуального изображения анатомических структур, попадающих в зону облучения (мочевой пузырь, прямая кишка, спинной мозг), а также самой опухоли и лимфоузлов зон ее возможного метастазирования; 6) дозиметрическое планирование с формированием полей облучения MLC; 7) оценка планов с помощью гистограмм доза -объем (DVH), и выбор оптимального варианта; 8) во время первой укладки верификация плана на симуляторе и линейном ускорителе с корректировкой параметров плана облучения; 8) контроль качества с помощью портальной визуализации на системе "Portalvision"; 9) проведение сеансов КФЛТ. Сама КФЛТ проводилась в РОД 2,5 Гр 28 фракций до СОД 70 Гр на линейных ускорителях «Clinac 600 C/D или 2100 C/D».
ГТ по МАБ проводилась препаратами агонистами ЛГРГ (золадекс 3,6 мг или 10,8 мг, диферелин 3,75 мг или 11,25 по схеме) + бикалутамид 100-150 мг ежедневно. После окончания курса гормонолучевой терапии ГТ продолжалась до 2-х лет.
Динамическая оценка результатов лечения проводилась по объему опухоли полученных при трансректальном ультразвуковом исследовании (ТРУЗИ), и определение концентрации общего и свободного ПСА в сыворотке крови. Непосредственную эффективность лечения анализировали согласно рекомендациям ВОЗ (1979) *16+, а отдаленные результаты с использованием актуриального моментного методу расчета по Kaplan E.L., Meier P. (1958) [17].
Результаты и обсуждение. В результате применения ЛТ по методике конформного облучения в 3-D режиме в комбинации с гормонотерапией по МАБ у больных РПЖ в 1-й группе отмечен ОЭ у всех 30 (100,0%) больных, что было статически значимо выше аналогичных показателей 2-й группы на 30,0%, где ОЭ был отмечен у 21 (70,0%) больных (p<0,05). При этом у 20 (66,7%) больных основной группы отмечалась полная регрессия (ПР) процесса, чтобы было достоверно выше на 46,7% аналогичных показателей контрольной группы, где ПР была достигнута всего лишь у 6 (20,0%) больных (р<0,05). Количество частичных регрессий в 1-й и 2-й группах составило 10 (33,3%) и 15 (50,0%) соответственно, и статистически не отличалось между собой. Прогрессирование заболевания в процессе лечения не отмечено ни у одного пациента обеих групп (таблицу 3).
|
Группы |
Непосредственная эфе |
активность лечения абс. ч. |
(%) |
|
|---|---|---|---|---|
|
ОЭ |
ПР |
ЧР |
СТ |
|
|
1-я группа /п=30/ |
30 (100,0) |
20 (66,7±8,6%) |
10 (33,3±8,6%) |
- - |
|
2-я группа /п=30/ |
21 (70,0±8,3) |
6 (20,0±7,3) |
15 (50,0±9,1%) |
9 (30,0±8,3) |
|
*р |
р>0,05 |
р<0,05 |
р>0,05 |
р>0,05 |
|
Примечание - *р вероятность ошибки между 1-й и 2-й группами соответственно. |
||||
Таблица 3 - Непосредственные результаты терапии у больных раком предстательной железы
Мониторинг динамического изменения среднего уровня ПСА до начала проведения гормонолучевой терапии показал, что особых различий в количественных показателей в испытуемых группах не было.
Контрольные измерения уровня ПСА через 1 месяц после проведенного гормоно- и лучевого лечения, показал значительное снижение данного показателя у всех больных. Однако наибольшее снижение зафиксировано в 1-й группе больных получивших КФЛТ на фоне ГТ по МАБ до 2,1 нг/мл, при статической значимой разнице в 1,8 нг/мл в сравнении со 2-й группой больных, получивших стандартную ЛТ и ГТ по МАБ, где данный показатель составил 3,9 нг/л (p<0,05) (таблица 4).
Дальнейшее наблюдение за этими пациентами через 3 и 6 месяцев также показало, что средний уровень ПСА снижался до нормальных величин в обеих группах, но при этом наименьший показатель отмечался в 1-й группе до 1,8 нг/мл и 0,9 нг/мл, что было достоверно меньше железы в испытуемых группах аналогичных показателей 2-й группы на 1,6 нг/мл и 1,5 нг/мл, где они составили 3,4 нг/мл и 2,4 нг/мл соответственно (р<0,05).
|
Группы |
Средний уровень ПСА нг/мл Средний объем опухоли см3 |
|||
|
До гормонолучевой терапии |
После гормонолучевой терапии |
|||
|
через 1 месяц |
через 3 месяца |
через 6 месяцев |
||
|
1-я /п=15/ |
25,4±2,6 нг/мл 12,7±2,1 см3 |
2,1±1,3 нг/мл 3,7±2,5 см3 |
1,8±0,8 нг/мл 1,7±0,9 см3 |
0,9±0,3 нг/мл 0,7±0,1 см3 |
|
2-я /п=15/ |
26,7±3,1 нг/мл 11,5±2,4 см3 |
3,9±0,9 нг/мл 4,7±2,1 см3 |
3,4±1,1нг/мл 3,3±1,3 см3 |
2,4±0,8нг/мл 1,7±0,3 см3 |
|
*р |
р>0,05 |
р>0,05 |
р<0,05 |
р<0,05 |
|
Примечание - |
р вероятность ошибки между 1-й и 2-й группами соответственно. |
|||
Проведенный мониторинг степени регрессии среднего объема опухоли по данным ультразвукового исследования через 1 месяц после проведенной гормонолучевой терапии в обеих группах показал, что в сравнении с первоначальным объемом отмечался значительный регресс опухоли в обеих группах. Более чем в 3 раза в 1-й группе и более чем в 2 раза во 2-й Таблица 4 - Динамическое изменение среднего объема группе, до 2,1 см3 и 3,9 см3 соответственно (таблица 4).
В то же время контрольные результаты через 3 и 6 месяцев после окончания лечения показали, что наибольшая регрессия опухолевого процесса был отмечена в 1-й группе, где средний объём опухоли составил после гормонолучевого лечения 1,7 см3 и 0,7 см3, что было статистически значимо меньше на 1,6 см3 и 1,0 см3, показателей 2-й группы, где они составили соответственно 3,3 см3 и 1,7 см3 (р<0,05).
Анализ побочных эффектов лучевой терапии показал, что наиболее часто встречаемыми лучевыми реакциями были лучевой цистит и ректит. Однако у больных, получавших ЛТ по методике конформного облучения, эти реакции носили менее интенсивный характер, и возникали значительно позже, чем у больных, получивших стандартную конвенциальную лучевую терапию. При этом все возникшие лучевые реакции и осложнения купировались стандартными лекарственными средствами.
Расчет отдаленных результатов лечения показал, что наблюдаемая общая 36-месячная выживаемость, рассчитанная одномоментным методом по Kaplan-Meier составила в 1-й группе 71,9±2,1%, что достоверно превышало аналогичные показатели 2-й группы на 14,0%, где они составили 57,9±2,9 % соответственно (p<0,05) (рисунок 2).
Как видно из рисунка 2 одно- и двух летняя выживаемость также была всегда выше в группе больных, получивших конформную лучевую и гормонотерапию, в сравнении с контрольной группой, составляя 90,2% и 82,9%, и статически значимо превышая на 9,3% и 11,3%, аналогичные показатели 2-й группы, где они составляли 80,9% и 71,6% соответственно (р<0,05). Медиана общей наблюдаемой выживаемости составила в 1-й и 2-й группах 57,5±1,3 и 53,1±1,7 месяцев соответственно, при статически значимой разнице в 4,4 месяца (p<0,05).
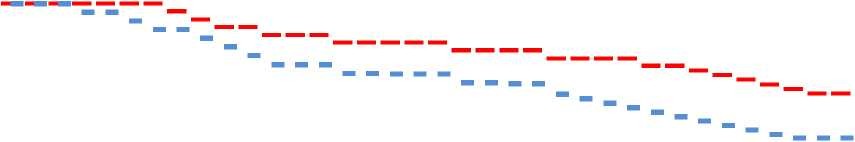
месяцы
Общая выживаемость по Kaplan-Meier у больных РПЖ — 1-я группа 2-я группа
Рисунок 2 Общая наблюдаемая 3-х летняя выживаемость больных РПЖ в испытуемых группах.
Заключение. Таким образом, применение конформной лучевой терапии в комбинации с гормонотерапией по МАБ при раке предстательной железы позволил достичь 100,0% объективного эффекта, при 70,0% полных регрессий, что было статически значимо выше на 30,0% и 50,0% соответственно, таких же показателей контрольной группы, где лечение проводили стандартным методом. При этом 36-месячная выживаемость у этих больных составила 71,9 %, статически значимо превышая аналогичные показатели контрольной группы на 14,0% (p<0,05).
СПИСОК ЛИТЕРАТУРЫ
- American Cancer Society: Cancer Facts and Figures 2009.
- Parking D.M., Bray F., Pisani F., Pisani P. Global cancer statistics, 2005 //CA Cancer J. Clin. 2009. V. 59, № 2. P. 74 108.
- Aus G., Abbou C.C., Bolla M. et al. European Association of Urology Guidelines on Prostate Cancer //Prostate Cancer.pdf. Accessed November, 2005.
- Абдрахманов Ж.Н., Позднякова А.П., Филиппенко В.И. Показатели онкологической службы Республики Казахстан за 1999 год (статистические материалы). Алматы, 2012. 108 с.
- Нургазиев К.Ш., Сейтказина Г.Д., Байпеисов Д.М. и др. Показатели онкологической службы Республики Казахстан за 2011 год (статистические материалы). Алматы, 2000. 78 с.
- Hanks G.E., Pajak T.F., Porter A. et al. Phase III trial of long-term adjuvant androgen deprivation after neoadjuvant hormonal cytoreduction and radiotherapy in locally advanced carcinoma of the prostate: the Radiation Therapy Oncology Group Protocol 92-02 //J. Clin Oncol. 2003. Vol.21. P.3972-3978.
- Гранов А.М., Метелев В.В., Карелин М.И. и соавт. Лучевая терапия в онкоурологии //Лучевая терапия в онкогинекологии и онкоурологии. СПб.: Фолиант, 2002. С. 178-233.
- Аль-Шукри С.Х., Ткачук В.Н. Опухоли мочеполовых органов. СПб.: Питер, 2000. С.266-287.
- Gerald J.Kutcher Intensity modulalated radiation therapy. A clinical