Нестероидные противовоспалительные препараты (ППВПjявляются наиболее часто применяемыми в ревматологии, хотя долгосрочное их применение связано со спектром неблагоприятных эффектов, прежде всего, с поражением слизистой оболочки (СО) гастродуоденальной зоны (ГДЗ) .
Количество осложнений и смертей, связанных с приемом НПВП, экономические затраты на их лечение с каждым годом растут. При длительном приеме НПВП патологические изменения в СО ГДЗ часто рецидивируют, что определяет необходимость проведения профилактики в течение всего периода лечения пациентов.
В данной статье описаны факторы риски возникновения, тактикавведение и профилактика, немедикаментозное и медикаментозное лечение НПВП – гастропатии.
Специфические особенности НПВП-гастропатий.
В 1986 г. S.H. Roth впервые предложил термин НПВП- гастропатия для обозначения повреждений желудка у пациентов с ревматоидным артритом [2]. Все НПВП, независимо от их химического строения, лекарственной формы и способа введениямогут вызывать язвы, гастрит, гастропатию и перфорацию [3,4]. У больных, принимающих НПВП, риск желудочно-кишечных кровотечений (ЖКК) возрастает в 3-5 раз, прободений язв - в 6 раз, риск смерти от осложнений, связанных с поражением желудочнокишечного тракта (ЖКТ) - в 8 раз. До 40-50% всех случаев острых ЖКК бывают обусловлены приемом НПВП [5]. При эндоскопическом исследовании эрозивно-язвенные поражения (ЭЯП) СО ГДЗ (сопровождающиеся диспепсией или бессимптомные) обнаруживаются у 40% больных, длительно принимающих НПВП [6].
НПВП в основном получают больные с патологией суставов, при которых боль и воспаление являются основными клиническими проявлениями. В ревматологической практике они используются длительно и в высоких дозах. Эти препараты до настоящего времени сохраняют важное значение в лечении ревматоидного артрита (РА), анкилозирующего спондилоартрита (АС), остеоартроза (ОА), подагры и т.д. [9].
Важным является выбор фармакологических препаратов с минимальными коэффициентами риска и отсутствием побочных действий. Вопросы безопасности применения НПВП особенно важны у пожилых, у лиц с желудочнокишечными, сердечно-сосудистыми или почечными факторами риска. Поэтому проблема снижения неблагоприятного действия НПВП важна для таких групп населения [10,11].
Термин «НПВП-гастропатия» в данной формулировке в Международной классификации болезней 10-го пересмотра (МКБ-10) отсутствует [12]. Однако, побочные действия на СО ГДЗ некоторых лекарств отражены в МКБ-10 в соответствующей рубрике под определенным кодом: салицилаты (Y45.1), производные пропионовой кислоты (Y45.2), другие нестероидные противовоспалительные лекарственные средства (Y45.3) (таблица 1).
Таблица 1 - Л екарственные средства, оказывающие неблагоприятные реакций при терапевтическом применении (М КБ-10). Y45 - Аналгезирующие, жаропонижающие и противовоспалительные средства
Y45.0 - Опиоидные и родственные аналгезирующие средства
Y45.1 - Салицилаты
Y45.2 - Производные пропионовой кислоты
Y45.3 - Другие нестероидные противовоспалительные лекарственные средства [NSAID]
Y45.4 - Противоревматические средства
Y45.5 - Производные 4-аминофенола
Y45.8 - Другие аналгезирующие, жаропонижающие и противовоспалительные средства
Y45.9 - Аналгезирующие, жаропонижающие и противовоспалительные средства неуточненные
Комбинируя различные рубрики классификации МКБ-10 (таблица 2), можно поставить диагноз как НПВП- индуцированной гастропатии, так и НПВП-ассоциированной диспепсии [12].
Таблица 2 - Болезни желудка и дв енадцатиперстной кишки (МКБ-10).
К25 - Язва желудка
К26 - Язва двенадцатиперстной кишки
К27 - Пептическая язва неуточненной локализации К28 - Гастроеюнальная язва
К29 - Гастрит и дуоденит
К30 - Функциональная диспепсия
K92.0-K92.2- желудочно-кишечное кровотечение
Примеры формулировки диагноза:
- – «НПВП-гастропатия: язва желудка, осложненная кровотечением» (K25, K92, Y45.3),
- – «НПВП-гастропатия: язва ДПК, связанная с приемом ацетилсалициловой кислоты (АСК), диспепсия» (К26, К30, Y45.1).
Обезболивающие, противовоспалительные и жаропонижающие эффекты являются результатом способности НПВП ингибировать ферменты циклооксигеназы (ЦОГ), которые катализируют превращение арахидоновой кислоты в простагландины [13,14].
Развитие НПВП-ассоциированных ЭЯП кишки обусловлены 2 механизмами - непосредственным повреждением СО ГДЗ в результате локального раздражающего действия лекарств и системным ингибированием ключевого фермента ЦОГ в каскаде метаболизма арахидоновой кислоты, которая является предшественником простагландинов, простациклинов и тромбоксанов. Данный фермент имеет два изомера - ЦОГ-1 и ЦОГ-2 [15].
Угнетение активности ЦОГ-1 вызывает нарушение синтеза простагландинов в СОЖ, в то время как подавление активности изомера ЦОГ-2 определяет противовоспалительный эффект НПВП. Снижение цитопротекторного эффекта и нарушение функции тромбоцитов при ингибировании ЦОГ-1, служат факторами, способствующих высокой частоте повреждений СО ГДЗ и развитию ЖКК [16].
ЦОГ-2 преимущественно участвует в процессах воспаления и канцерогенеза. Ингибирование ЦОГ-2 подавляет также некоторые воспалительные медиаторы, участвующие в прогрессировании атерогенеза и ишемического повреждения миокарда, что приводит к изменению баланса между антитромботическим простациклином и протромботическим тромбоксаном А2, увеличивая риск тромбоза [17,18].
НПВП приводят к снижению кровотока в СОЖ, уменьшению выработки желудочной слизи и бикарбонатов, стимуляции секреции соляной кислоты и продукции пепсиногена, усилению апоптоза и десквамации эпителиальных клеток, изменениям гастродуоденальной моторики, повышению образования свободных радикалов, фактора некроза опухолей, увеличению хемотаксиса нейтрофилов [4].
Риск развития ЭЯП СО ГДЗ зависит и от того, какой именно препарат из группы НПВП был выбран для лечения. Так, относительный риск возникновения НПВП-гастропатии при приеме ибупрофена составляет 1,19, пироксикама - 1,66, диклофенака 1,73, напроксена - 1,83 [19]. Наиболее безопасными ЛС среди неселективных (неспецифических) ингибиторов ЦОГ-1 и ЦОГ-2 являются ацеклофенак, ибупрофен, диклофенак, а наиболее токсичными - индометацин и кеторолак [20,21].
Патологически, НПВП-индуцированная гастропатия развивается при дозе, которая ингибирует выработку простагландинов и усиливает перистальтику желудка, таким образом, вызывая увеличение проницаемости СО, инфильтрацию нейтрофилами и образование свободных радикалов, в конечном счёте, вызывая поражения желудка [22].
В качестве главного классификационного признака НПВП [21,23] используется селективность в отношении ЦОГ (таблица 3).
Таблица 3 - Классификации НПВП
Неселективные (неспецифические) ингибиторы ЦОГ-1 и ЦОГ-2: ацеклофенак, ацетилсалициловая кислота, диклофенак, ибупрофен, кетопрофен, кеторолак, набуметон, напроксен, пироксикам, сулиндак
Препараты с преимущественным влиянием на ЦОГ-2: мелоксикам, нимесулид
Коксибы (специфические ингибиторы ЦОГ-2): вальдекоксиб, целекоксиб, эторикоксиб
С целью снижения риска возникновения НПВП-гастропатии разрабатываются новые лекарственные средства, которые обладали бы селективным ингибирующим действием на ЦОГ-2 и не влияли бы на активность ЦОГ-1. Всемирная организация здравоохранения определила эти препараты (коксибы) как новый подкласс селективных НПВП [24]. Исследования VIGOR (Vioxx [rofecoxib] in Gastrointestinal Outcomes Research) и CLASS (Celecoxib Longterm Arthritis Safety Study) подтвердили снижение частоты возникновения НПВП-гастропатии при приеме рофекоксиба и целекоксиба [25,26,27].
Известны и другие селективные ингибиторы ЦОГ-2, не относящиеся к коксибам. В их число входят мелоксикам, этодолак, нимесулид, а также НПВП, содержащие оксид азота, при приеме которых поражения ГДЗ встречаются реже, чем при приеме пироксикама и напроксена [27]. Результаты исследования CLASS продемонстрировали, что через 6 мес. риск развития осложнений составил 0,76% на фоне целекоксиба и 1,45% - на фоне неселективных НПВП, язв - 2,08 и 3,54% соответственно [27].
Такие факторы риска как пожилой возраст, наличие сопутствующих заболеваний (например, язвенная болезнь, гастроэзофагеальная рефлюксная болезнь, стриктура пищевода, системный склероз с поражением пищевода и желудка, цирроз печени, заболевания сердечно-сосудистой системы), длительное применение НПВП, инфекция Helicobacter pylori (H. pylori), курение и хронический алкоголизм, а также другие применяемые одновременно лекарственные препараты повышают вероятность развития НПВП-индуцированной гастропатии и эпизодов осложнений [28].
Относительный риск (ОР) возникновения ЭЯП ГДЗ у пациентов, принимающих НПВП, составляет 3,7, а у пожилых больных он увеличивается до 13,2. При наличии в анамнезе ЯБ и пожилого возраста больных этот риск увеличивается в 17 раз [29]. У больных в возрасте старше 60 лет при назначении доз, превышающих стандартные в 1,5 раза, риск развития НПВП-гастропатии возрастает в 2,8 раза, а при тройном превышении стандартных доз он увеличивается уже в 8 раз [30].
Наибольший риск отмечается в период с 30-го по 50-й день приема препаратов, но при назначении индометацина максимальный риск смещается к 7-14 дню приема [31]. Комбинации НПВП с другими ЛС также повышаютриски развития НПВП-ассоциированных осложнений. [32].
Как неселективные, так и селективные НПВП СОХ-2 связаны с повышенным риском возникновения осложнений со стороны ЖКТ. Однако риск для неселективных НПВП значительно выше [33].
При возникновении на фоне приема НПВП язвы и/или ЖКК показано тестирование на наличие инфекции H.рylori, а при ее выявлении - проведение курса эрадикационной терапии. Однако, эрадикация H.pylori не снижает полностью риск рецидива гастропатии, поэтому при необходимости продолжения приема НПВП следует использовать дополнительные методы профилактики [34].
Комитетом Американского колледжа гастроэнтерологов было опубликовано руководство по предупреждению развития НПВС-зависимых язвенных осложнений, в котором несколько изменены факторы желудочно-кишечного риска и подход к их стратификации (таблица 4) [35].
Таблица 4 - Рекомендации ACG НПВС- в принимающих НПВП, является классификация Lanza (1993 г.), основанная на балльной оценке патологии, выявляемой при эндоскопическом исследовании [36] (таблица 5)
Единой общепринятой классификации НПВП- индуцированных гастропатий нет. Наиболее известной классификацией ЭЯП СО ГДЗ, возникающих у пациентов,
|
Высокий риск |
Умеренный риск |
Низкий риск |
|
1. В анамнезе осложненная язва |
1. Возраст >65 лет |
Нет факторов риска |
|
2. Множественные (≥2) факторы риска |
2. Высокая доза НПВС |
|
|
3. В анамнезе неосложненная язва |
||
|
4. Сопутствующий прием АСК (включая малые дозы), кортикостероидов или антикоагулянтов |
Таблица 5
|
Количество баллов |
Эндоскопическая картина |
|
0 |
отсутствие эрозий и геморрагий |
|
1 |
единичные эрозии и геморрагии |
|
2 |
от 2 до 10 эрозий или подслизистых геморрагий |
|
3 |
более 10 эрозий или подслизистых геморрагий |
|
4 |
язвы - глубокие повреждения СО желудка более 5 мм в диаметре |
Эндоскопическая классификация Lanza score поражения СО ГДЗ
Специфические особенности НПВП-гастропатий [5,37]:
- мало- или безсимптомное течение (80%);
- отсутствие четкой связи между клиническими проявлениями и эндоскопически выявляемых язв.
- острые множественные эрозий и/или язвы (40-60%) СО ГДЗ;
- преимущественная локализация в СОЖ антрального отдела (80%);
- отсутствие локального воспаления и гистологических признаков гастрита (60-70%);
- выявление инфекций H.pylori (50-60%);
- манифестация осложнений (до 60% — кровотечение, реже — перфорация язвы, стеноз привратника);
- заживление язв при отмене НПВС.
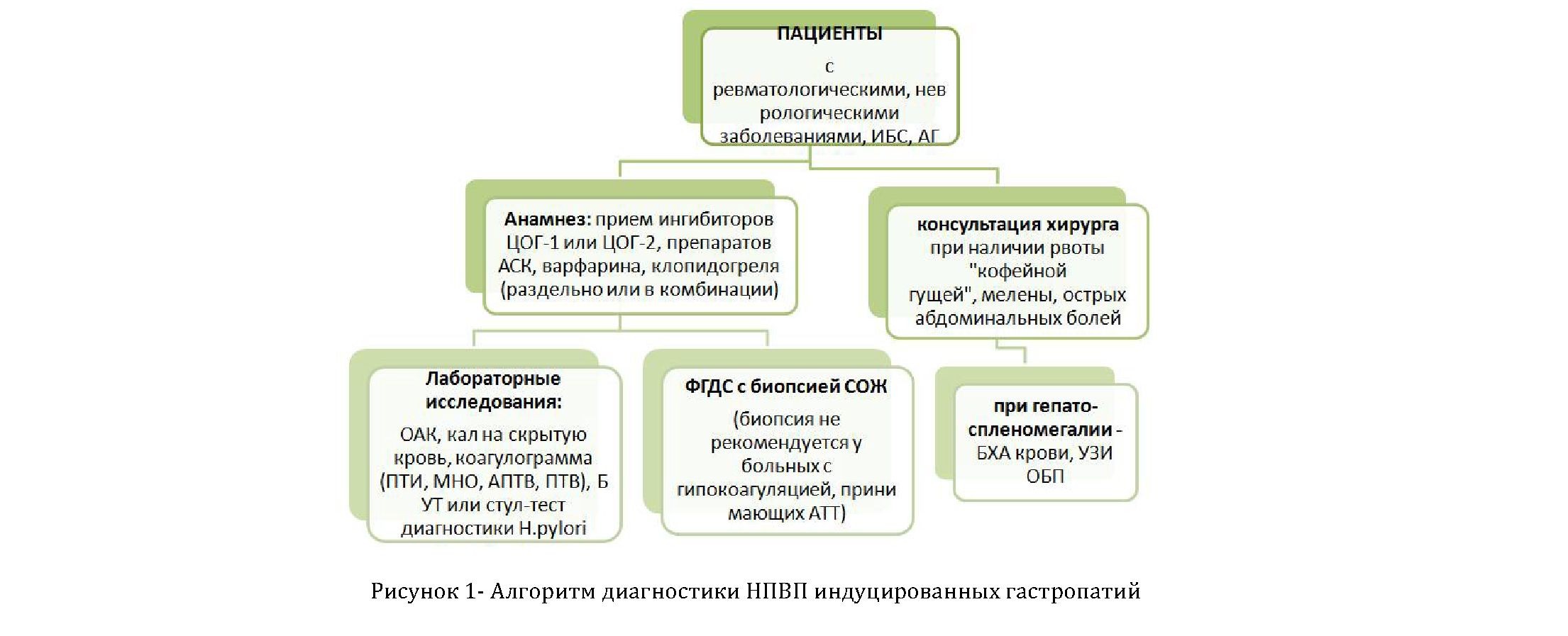
Дифференциальный диагноз и обоснование дополнительных исследований представлены в таблице 6.
Лечение НПВП-гастропатии представляет собой трудную задачу, поскольку полная отмена НПВП без назначения кислотосупрессивных препаратов не приводит к заживлению язв и эрозий у 60% пациентов в течение ближайших 1-3 месяцев.
Тактику лечения и профилактики НПВП-гастропатии уловно можно разделить на 2 стратегии: комбинации НПВП с гастропротективными препаратами и использование селективных ингибиторов ЦОГ-2. К основным гастропротективным средствам относят аналоги простагландина (ПГ), антисекреторные препараты - ингибиторы протонной помпы (ИПП), блокаторы Н2- рецепторов и антациды.
Цели терапии:.
- купирование клинических симптомов,
- эпителизация дефектов слизистой оболочки,
- повышение качества жизни пациентов
- достижение полной ремиссии заболевания
- профилактика рецидивов и развития осложнений
- предупреждение прогрессирования заболевания Основные задачи лечения:
- снижение активности кислотно-пептического фактора;
- нормализация секреторно-моторной функции желудка;
- повышение защитных свойств СОЖ и слизистой оболочки ДПК;
- эрадикация H.рylori.
Задачи врача:
- Оценить риск осложнений сердечно-сосудистых заболеваний.
- Оценить риск ЭЯП ГДЗ, их осложнений (кровотечения, перфорации).
- Осуществлять практические мероприятия.
Опираясь на клинические и эпидемиологические исследования, эксперты утвердили тактику максимальной степени достоверности:
- всем больным, у которых ранее подтверждена пептическая язва, при приеме НПВП необходимо назначать профилактическое лечение;
- во всех случаях требуется его проведение при наличии двух факторов риска (иными, чем пептическая язва в анамнезе); если больные принимают неселективные НПВП, такое лечение может быть целесообразным и при наличии одного фактора риска.
Немедикаментозное лечение и общие мероприятия включают:
- при обострении - полупостельный режим;
- питание полноценное и разнообразное;
- режим питания дробный, до 6 раз в сутки, малыми порциями;
- ограничение механических и химических раздражителей ЖКТ, стимуляторов желудочной секреции, веществ, длительно задерживающихся в желудке;
В ревматологической практике алгоритм лечения больных с НПВП-гастропатией предполагает решение вопроса об отмене аспирина и других неселективных НПВП или их замене селективными ингибиторами ЦОГ-2. После перевода больного на селективные ингибиторы ЦОГ-2 назначаются ИПП в стандартных дозах курсом от 4 до 8 недель, а при ЭЯП ГДЗ - двойных доз ИПП. При ассоциации с инфекцией Н. pylori рекомендуется проведение эрадикационной терапии [38].
Наиболее эффективными препаратами при лечении ЭЯП ГДЗ являются ИПП, которые угнетая активность Н+К+АТФ- азу, блокируют синтез соляной кислоты. В результате происходит снижение уровня базальной и стимулированной секреции. Это выгодно отличает ИПП от блокаторов Н2 - рецепторов, которые блокируют лишь один из множества механизмов секреции соляной кислоты.
Назначение Н2-блокаторов и синтетического аналога простагландина мизопростола является менее эффективной терапией. Многие положения, которые определяют лечение НПВП-индуцированного поражения гастродуоденальной области, имеют подтвержденный уровень доказательности [39].
При установлении синергического воздействия НПВП и инфекции H.pylori в этиопатогенезе ЭЯП СО ГДЗ, перед началом лечения НПВП, целесообразно провести эрадикационную терапию в соответствии с рекомендациями и положениями консенсуса Маастрихт-V (2015) [38]
Терапия первой линия (14 дней):
Таблица 6 - Дифференциальная диагностика НПВП гастропатий
|
Нозологии |
Клинические симптомы |
Лабораторно-инструментальные признаки |
|
НПВП гастропатий |
Больные ревматическими заболеваниями, патологией периферической нервной системы, ИБС, АГ принимающие НПВП, препрараты АСК, антикоагулянты; У 80% больных клинические симптомы патологии ГДЗ отсутствуют |
ФГДС - множественные эрозивно-язвенные поражения СО чаще антрального отдела желудка; Гипохромная железодефицитная анемия при кровотечении; в кале - положительная реакция на скрытую кровь; (+) тесты на H.pylori (50-60%) |
|
Стрессовые эрозии и язвы ГДЗ |
Больные с тяжелыми травмами, массивными ожогами, сепсисом, в состоянии шока, перенесшие операции, инфаркт миокарда. Боли в мезо- и эпигастрии различной интенсивности не связанные с приемом пищи, рвота «кофейной гущей», мелена, признаки анемии. |
ФГДС - острые эрозии и острые язвы в теле и кардиальном отделе желудка. Гипохромная железодефицитная анемия при кровотечении; в кале - положительная реакция на скрытую кровь |
|
Язвенная болезнь ДПК |
Больные чаще мужчины молодого возраста, астенического телосложения; боли в пилородуоденальной зоне поздниеболи через2-3 часа после еды, ночные, «голодные», стихают после приема еды, молока |
ФГДС - Язвенный дефект ДПК, Гипохромная железодефицитная анемия при кровотечении; в кале - положительная реакция на скрытую кровь (+) тесты на H.pylori (70-85%) |
|
Язвенная болезнь желудка |
Пациенты среднего и пожилого возраста; одинаково наблюдаются как у мужчин так и у женщин; симптомы желудочной и кишечной диспепсии; боли в эпигастрии «ранние» - через-1-1.5 ч после еды, уменьшаются после рвоты, плохой аппетит, потеря веса |
ФГДС - Язвенный дефект чаще на малой кривизне желудка окруженный воспалительным валом, (+/-) реакция на скрытую кровь в кале, (+) тесты на H.pylori 50-60% |
- 3-х компонентная схема: [ИПП 40 мг + амоксициллин 1000 мг + кларитромицин 500 мг] х 2 раза в сутки (УД А, сильная рекомендация)
- Квадротерапия без висмута: [ИПП 40 мг + амоксициллин 1000 мг + кларитромицин 500 мг + нитромидазол 500 мг] х 2 раза в сутки
- Квадротерапия с висмутом: [ИПП 40 мг + амоксициллин 1000 мг + кларитромицин 500 мг + висмута трикалия дицитрат 240 мг] х 2 раза в сутки УД С.Класс рекомендаций: сильнаяреко мендация
Терапия второй линии (14 дней):
- 3-х компонентная схема:
ИПП+амоксициллин+фторхинолон (УД С)
Классрекомендаций:слабаярекомендация.
- Квадротерапия без висмута: [ИПП 40 мг + амоксициллин 1000 мг + кларитромицин 500 мг + нитромидазол 500 мг /или тетрациклин 200 мг (2 таб)] х 2 раза в суткиУД А.Класс рекомендаций: сильнаярекомендация У
- Квадротерапия с висмутом: [ИПП 40 мг + амоксициллин 1000 мг + висмута трикалия дицитрат 240 мг] х 2 раза в сутки + левофлоксацин 500 мг х 1 раз в сутки [40,41].
Мероприятия, позволяющие повысить эффективность лечения [38]:
- Назначение дважды в день удвоенной дозы ИПП по сравнению.
- Увеличение продолжительности эрадикационной терапии до 10-14 дней.
- Добавление к стандартной тройной терапии висмута трикалия дицитрата в дозе 240 мг 2 раза в сутки.
- Добавление к стандартной тройной терапии пробиотика Saccharomyces boulardii (энтерол по 250 мг 2 раза в сутки).
- Подробное инструктирование пациента и контроль за точным соблюдением назначенного режима приема лекарственных средств.
НПВП-индуцированная гастропатия часто имеет бессимптомное течение и может манифестировать ЖКК, что диктует необходимость профилактического назначения гастропротективных препаратов. [42,8].
Алгоритм профилактики НПВП - гастропатии включает:
- Своевременное выявление больных с высоким риском ЭЯП ГДЗ.
- Назначение селективных ингибиторов ЦОГ-2.
- Профилактическое назначение в стандартных (лучше в удвоенных) дозах ИПП или блокаторов Н2- рецепторов гистамина.
- При инфекции H.pylori проведение эрадикационной терапии.
Заключение
Адекватная оценка факторов риска НПВП-ассоциированной гастропатии, выбор оптимального терапевтического режима для больного с учетом факторов риска и нежелательных эффектов лекарственных средств, создание в необходимых случаях «прикрытия» в виде назначения ИПП позволяют снизить риск возникновения тяжелых ЭЯП ГДЗ и предотвратить развитие ЖКК, нередко приводящих к летальным исходам.
СПИСОК ЛИТЕРАТУРЫ
- Conaghan PG. A turbulent decade for NSAIDs: update on current concepts of classification, epidemiology, comparative efficacy, and toxicity // Rheumatology International. - 2012. - №32(6). - Р. 1491-1502. doi:10.1007/s00296-011-2263-6
- Roth SH.Nonsteroidal anti-inflammatory drug gastropathy. We started it--can we stop it? // Arch Intern Med. - 1986. - №146(6). - Р. 1075-1076.
- Каратеева А.Е. Рациональное применение нестероидных противовоспалительных препаратов в клинической практике // Современная ревматология. - 2015. - №1. - С. 4-23.
- Koffeman AR, Valkhoff VE, Çelik S, et al. High-risk use of over-the-counter non-steroidal anti-inflammatory drugs: a population-based cross-sectional study // The British Journal of General Practice. - 2014. - №64(621). - Р. 96-103.
- В.Т.Ивашкин, А.А.Шептулин, Е.К.Баранская, А.С.Трухманов, Т.Л.Лапина Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению эрозивно-язвенных поражений желудка и двенадцатиперстной кишки, вызванных нестероидными противовоспалительными препаратами // РЖГГК. - 2014. - №6. - С. 89-94.
- Ким В.А. НПВП-гастропатия и роль простагландинов в ее возникновении, профилактике и лечении // Эксперим. клин. гастроэнтерология. - 2008. - №8. - С. 84-91.
- Пахомова И.Г. НПВП-индуцированные поражения желудочно-кишечного тракта: проблемы, особенности и пути решения // Consilium Medicum. - 2009. - № 2. - С. 71-76.
- Lanas A. A review of the gastrointestinal safety data - a gastroenterologist's perspective // Rheumatology. - 2010. - Vol.49, Suppl.2. - P. 3-10.
- Евсютина Ю.В.,Трухманов А.С. Гастропатия, индуцированная НПВП, - современные представления о механизмах развития, лечении и профилактике // РМЖ «Медицинское обозрение». - 2014. - №3. - С. 2214-2219.
- Каратеев А.Е., Насонов Е.Л. НПВП-ассоциированная патология ЖКТ: реальное состояние дел в России // Рус. мед. журн. - 2006. - № 15. - С. 1073-1078.
- RothS.H. Nonsteroidal anti-inflammatory drug gastropathy: new avenues for safety // Clin Interv Aging. - 2011. - №6. - Р. 125-131. Published online 2011 May 30. doi: 10.2147/CIA.S21107
- Конорев М.Р., Ковалева Л.Ф. Гастропатия, индуцированная нестероидными противовоспалительными препаратами: факторы риска, лечение, профилактика. - Минск: 2006. - 145 с.
- Карасёва Г. А.НПВП-индуцированная гастропатия: от понимания механизмов развития к разработке стратегии профилактики и лечения // Медицинские новости. - 2012. - №8. - С. 21-26.
- Haroutiunian S, Drennan DA, Lipman AG. Topical NSAID therapy for musculoskeletal pain // Pain Med. - 2010. - №11(4). - Р. 535-549.
- Rao P, Knaus EE. Evolution of nonsteroidal anti-inflammatory drugs (NSAIDs): cyclooxygenase (COX) inhibition and beyond // JPharmPharmSci. - 2008. - №11(2). - Р. 81-110.
- RothS.H. Nonsteroidal anti-inflammatory drug gastropathy: new avenues for safety // Clin Interv Aging. - 2011. - №6. - Р. 125-131. Published online 2011 May 30. doi: 10.2147/CIA.S21107
- Rouzer CA, Marnett LJ. Cyclooxygenases: Structural and functional insights // J Lipid Res. - 2009. - №50. - Р. 29-34.
- Rao P, Knaus EE. Evolution of nonsteroidal anti-inflammatory drugs (NSAIDs): cyclooxygenase (COX) inhibition and beyond // J Pharm Pharm Sci. - 2008. - №11(2). - Р. 81-110.
- Rouzer CA, Marnett LJ. Cyclooxygenases: Structural and functional insights // J Lipid Res. - 2009. - №50. - Р. 29-34.
- Richy F, Bruvere O., Ethgen O. et al. Time dependent risk of gastrointestinal complications induced by non-steroidal anti-inflammatory drug use: a consensus statement using a meta-analytic approach // Ann. Pheum. Dis. - 2004. - Vol.63. - P. 759-766.
- Lanza F., Chan F.К., Quigley E.et al. // Am. J. Gastroenterol. - 2009. - Vol.104. - Р.728-738,
- Wilder-Smith C.H., Robert J., Schindler D. Upper gastrointestinal tract mucosal injury by AZD3582. A COX-inhibiting nitric oxide donor and naproxen: a randomized, double-blind, crossover study in healthy subjects [Abstract] // Gut. - 2004. - Vol.53, Suppl.6. - P.36-47.
- Каратеев А.Е. Лечение и медикаментозная профилактика НПВП-гастропатии: основные положения // Фарматека. - 2006. - №6. - С. 5-10.
- NICE Guidelines: Acute upper gastrointestinal bleeding in over 16s: management. Available from https://www.nice.org.uk/guidance/cg141 Last accessed 15th September 2016.
- Драпкина О.М., Гацолаева Д.С. Справочник поликлинич. врача. - 2006. - Т.4, №8. - С.24-31.
- Hawkey C.I., Wight N.J. NSAIDs and gastrointestinal complications // LSC Life Science Communications. - London: 2001. - Р. 51-56.
- Bombardier C., Laine L., Reicin A. et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumathoid arthritis VIGOR Study Group // N. Engl. J. Med. - 2000. - Vol.343. - P.1520-1528.
- Silverstein F.E., Faich G., Goldstein J.L. et al. Gastrointestinal toxicity with cеlеcoxib vs nonsteroidal anti-inflammatory drugs for osteoarthritss and rheumatoid arthritis: the CLASS study: A randomized controlled study. Celecoxib Long-term Arthritis Safety Study // JAMA. - 2000. - Vol.284. - P.1247-1255.
- Chan F.K., To K.F., Wu J.C.Y. et al. A randomized double-blind trial to evaluate the gastroduodenal safety of oral meloxicam 7,5 mg once daily compared with oral piroxicam 20 mg once daily over a period of f our weeks in patients with osteoarthritis of the knee [Abstract] // Gut. - 2004. - V0l.53, Suppl.6. - P.119-127.
- Hawkey C.I., Wight N.J. NSAIDs and gastrointestinal complications // LSC Life Science Communications. - Lоndon: 2001. - P.51-56.
- Deepak L.B., Scheiman J., Abraham N.S. et al. ACCF/ACG/AHA 2008 Expert Consensus Document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use // Circulation. - 2008. - Vol.118. - P.1894-1909.
- Richy F, Bruvere O., Ethgen O. et al. Time dependent risk of gastrointestinal complications induced by non-steroidal anti-inflammatory drug use: a consensus statement using a meta-analytic approach // Ann. Pheum. Dis. - 2004. - Vol.63. - P.759-766.
- Lanas A., Garcia-Rodriguez L.A., Arroyo M.T. et al. Risk of upper gastrointestinal ulcer bleeding associated with selective cyclo-oxygenase- 2 inhibitors, traditional non-aspirin non-steroidal anti-inflammatory drugs, aspirin and combinations // Gut. - 2006. - Vol. 55(12). - P. 1731-1738.
- Lazzaroni M, Porro GB. Management of NSAID-induced gastrointestinal toxicity: Focus on proton pump inhibitors // Drugs. - 2009. - №69(1). - Р. 51-69.
- Malfertheiner P1, Megraud F2, O'Morain CA3 European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report // Gut. - 2016. - №66(1). - Р. 26-30.
- Bhatt DL, Scheiman J, Abraham NS, et al. American College of Cardiology Foundation Task Force on Clinical Expert Consensus DocumentsACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents // Circulation. - 2008. - №118(18). - Р. 1894-909.
- Lanza F.L. Endoscopic studies of gastric and duodenal injury after the use of ibuprofen, aspirin and other NSAIDs // Am.J.Med. -1984.- №7. - P. 19-24.
- Zidar N., Odar K., Glavac D. et al. Cyclooxygenase in normal human tissues - is COX-1 really a constitutive isoform, and COX-2 an inducible isoform? // Cellular Molecular Med. B. - 2009. - Vol. 13(9). - P. 3753-3763.
- Malfertheiner P1, Megraud F2, O'Morain CA3 European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report // Gut. - 2017. - №66(1). - Р. 26-30.
- Каратеев А.Е., Яхно Н.Н., Лазебник Л.Б. и др. Применение нестероидных противовоспалительных препаратов. Клинические рекомендации. - М.: ИМА пресс, 2009. - 167 с.
- Gatta L., Vakil N., Vaira D., et al. Global eradication rates for Helicobacter pylori infection: systematic review and meta- analysis of sequential therapy // BMJ. - 2013. - №347. - Р. 458-467.
- Feng L., Wen M.Y., Zhu Y.J., et al. Sequential therapy or standard triple therapy for helicobacter pylori infection: an updated systematic review // Am.J.Ther. - 2016. - №23. - Р. 880-893.
- Зборовская И.А. Гастропатии, индуцированные нестероидными противовоспалительными препаратами: клиническое значение, лечение, профилактика: Методическое пособие для практических врачей. - Волгоград: 2005. - 16 с.