Поиск и создание новых физиологически активных веществ из растительного сырья считается наиболее актуальным и перспективным для получения лекарственных препаратов самого различного назначения. В этом отношении особый интерес представляют алкалоиды, занимающие уникальное место среди природных соединений благодаря их огромному структурному многообразию, высокой физиологической активности и широкому спектру действия. Так, на основе алкалоида лаппаконитина из некоторых видов растений рода Aconitum (аконит) создан препарат «Аллапинин», который рекомендован для применения в медицинской практике для лечения нарушения сердечного ритма [1-2].
Флора Казахстана в своем составе насчитывает более ста видов алкалоидоносных растений. Среди последних наибольшие запасы представлены такими, как акониты (Aconitum), живокост (Delphinium), василистник (Thalictrum), различные виды лютиковых [3].
Растения рода Thalictrum (Василистник) семейства Ranunculaceae (Лютиковые) широко распростронены по всему земному шару и издавна применяются в народной медицине.
Из 9 видов Василистника, произрастающих на территории Казахстана, исследовано 7: Thalictrum alpinum L., Thalictrum flavum., Thalictrum foetidum L., Thalictrum isopyr., Thalictrum longip., Thalictrum minus., Thalictrum simplex L. Алкалоиды Thalictrum обнаруживают широкий спектр физиологической активности [4].
В данной работе нами изучено растение Thalictrum foetidum L. (василистник вонючий), собранное в Каркаралинском районе Карагандинской области в фазе цветения. Из надземной части растения Thalictrum foetidum L. методом хлороформной экстракции получили суммы экстрактивных веществ. В результате колоночной хроматографии суммы экстрактивных веществ выделили алкалоида глауцин.
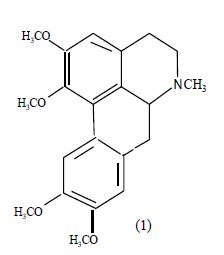
В спектре ПМР-'Н (II) проявляются сигналы протонов четырех метоксильных групп при 3.59,
3.87, 3.93, 3.94 м.д. (ЗН), а также N-метильных групп при 2.93 м.д. в виде синглета. В области ароматических протонов Н-3, Н-8, Н-11 наблюдаются однопротонные синглеты при 6.56- 6.78 и 8.00 м.д.
При действии на глауцин (1) вторичных аминов в присутствии параформа при умеренном нагревании протекает региоселективное аминометилирование, приводящее к образованию аминопроиз-водных (2-4).
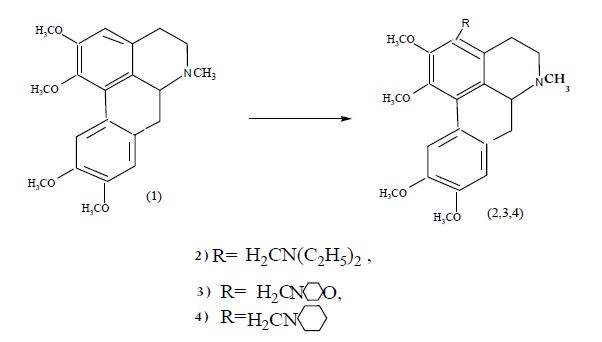
В ПМР-спектре (2) проявляются сигналы протонов (N -(СН2 СН3)2 группы при 2.18 м.д., четырех метоксильных групп при 3.87, 3.98, 3.99, 3.94 м.д. (3Н), а также N-СН — при 3.0 м.д. в виде синглета. Были изучены антигрибковая и фагоцитарная активность диэтиламинометилглауцина и морфолинометилглауцина.
Антигрибковая активность. В результате испытаний установлено, что диэтиламинометилглау-цин и морфолинометилглауцин проявляют умеренную антигрибковую активность. Умеренно-выраженное антигрибковое действие к грибковому штамму Trichophyton men. проявил диэтиламино-метил глауцин. В отношении Penicillium citrinum эти вещества проявили слабую активность. Также эти вещества проявили слабую антигрибковую активность к грибковым штаммам Aspergillus niger и Aspergillus flavus.
Фагоцитарной активность — установлена только для 2 веществ: диэтиламинометил- и морфо-линометилглауцины. Эти вещества в низкой концентрации (0,01мг/мл) оказывают стимулирующее, а в высокой (1 мг/мл) — супрессирующее воздействие на фагоцитоз. Таким образом, диэтиламиноме-тил- и морфолинометилглауцины оказывают выраженное стимулирующее фагоцитозное действие.
Материалы и методы исследования
Для колоночной хроматографии использовали прокаленный А2Оз\(Пст.активности), для ТСХ -пластинки Silufol UV-254 и Silicagel оп А1ишіпиш, 20Х., проявитель — пары йода. Температуру плавления определяли на приборе ВоеЙиш. ИК-спектры снимали на Фурье-спектрофотометре Vektor-22 в КВг. Спектры ЯМР1 Н и13С получены на спектрометрах Вгикег АС 200 [рабочие частоты 200.13 (1Н) и 50.32 МГц (13С)] и Вгикег DRX 500 [рабочие частоты 500.13 (1Н) и 125.76 МГц (13С)] для 5 %-ных растворов СБС1з или СБзОБ.
Хлороформная экстракция: 900г надземной части воздушно-сухого сырья смачивали 5 %-ным раствором соды и исчерпывающе экстрагировали хлороформом. Хлороформный экстракт взбалтывали с 5 % -ным раствором серной кислоты. Кислый раствор промывали хлороформом, затем при охлаждении подщелачивали содой и алкалоиды экстрагировали хлороформом. Получили 12 г (1,3 %) суммы экстрактивных веществ (от веса воздушно-сухого сырья). При колоночной хроматографии на
оксиде алюминия в соотношении сумма: носитель 1:70 с применением в качестве элюента смеси гек-
сан-этилацетат выделили 0,03г алкалоида глауцина. Т.пл 115-117°С.
ИК- спектр (КВг v, см-1): 846, 950, 975, 1005, 1121, 1161, 1200, 1228, 1318, 1392, 1440, 1535, 1595, 1600, 2850, 2930, 2958.
Взаимодействие глауцина с диэтиламином и параформом
0,1 г (0,23 ммоль) глауцина растворили в абсолютном хлороформе, добавили 0,17 мл (0,36 ммоль) диэтиламина и 0,082 г (0,27 ммоль) параформа. Реакционную смесь выдержали в течение трех часов при нагревании до 50 °С.Затем обработали водой и экстрагировали хлороформом. Хлороформный слой сушили сульфатом натрия и упаривали. Остаток хроматографировали на колонке с окисью алюминия в соотношении сумма-носитель (1:20). При элюировании смесью гексан: этил-ацетат (1:3) получили 3-диэтиламинометилглауцин (2) с т.пл. 122-124 °С, выход (0,195г) 85 %.
ИК-спектр (КВг v, см 616, 760, 806, 957, 1001, 1032, 1086, 1100(-СН2), 1121, 1161, 1230, 1253, 1298, 1332, 1375 (СН3), 1511 (С-Аг), 1596 (С-N (С2Щ2), 1611 (С=С), 2830(N -СН3) 2994(ОСЩ, 3164.
ПМР-спектр (200МГц, СБСЬ, 5, м.ді/Гц): 2.18 (с., N -(СН СН3) 2, J =7,2); 3.0(3Н, с., N-СНз) 3.40 (2Н, тр., J=6, Н-5), 3.87, 3.98,3.99,3.94 (ЗН, с, ОСН3), 6.98, 7.0, 7.20 (1Н, с, Н-3, Н-8, Н-11).
Взаимодействие глауцина с пиперидином и параформом
0,1 г глауцина растворили в абсолютном хлороформе, добавили 0,17 мл пиперидина и 0,082 г па-раформа. Реакционную смесь выдержали в течение трех часов при нагревании до 50° С. Затем обработали водой и экстрагировали хлороформом. Хлороформный слой сушили сульфатом натрия и упаривали. Остаток хроматографировали на колонке с окисью алюминия в соотношении сумма-носитель (1:20). При элюировании смесью гексан: этилацетат (1:5) получили кристаллическое вещество с т.пл. 124-126° С, выход 75 %.
ИК-спектр (КВг v, см 614, 806,846,950, 1001, 1030, 1085, 1110(-СН2), 1121, 1161, 1200, 1228, 1259, 1298, 1332, 1392, 1510 (С-Аг), 1590 (С-Ы), 1637 (С=С), 1758, 2824 (N-Ob), 2958 (ОСН3), 3000.
ПМР-спектр (200МГц, СБСЬ, 5, м.дЛ/Гц): 3.0, (ЗН, с., N-СЩ, 3.35 (2Н, тр., J =6, Н-5), 3.87, 3.96,3.99,4.0 (ЗН, с, ОСН3), 6.79, 6.98, 7.1, 7.23 (1Н, с, Н-3, Н-8, Н-11).
Взаимодействие глауцина с морфолином и параформом
0,3 г (0,68) глауцина растворили в абсолютном хлороформе, добавили 0,399 мл (5,9 ммоль) мор-фолина и 0,137 г (0,045 ммоль) параформа. Реакционную смесь выдержали в течение трех часов при нагревании до 50°С.Затем обработали водой и экстрагировали хлороформом. Хлороформный слой сушили сульфатом натрия и упаривали. Остаток хроматографировали на колонке с окисью алюминия в соотношении сумма-носитель (1:20). При элюировании смесью гексан: этилацетат (1:3) получили кристаллическое вещество с т.пл. 119-122 °С, выход 88 %.
ИК- спектр (КВг v, см 595, 869, 894, 1034, 1045, 1098, 1186 (-СН2), 1224, 1377 (СН3), 1563 (С-N), 1964, 2149, 2428, 2593, 2774 (Ч-СН3), 2810-2945 (ОСН3).
ПМР-спектр (200МГц, СБС13, 5, м.ді/Гц): 2.99, (ЗН, с., N -СН3), 3.33 (2Н, тр., J =6, Н-5), 3.81. 3.99, 4.0,4.01 (ЗН, с, ОСН3), 6.51, 6.98, 7.05, 9.00 (1Н, с, Н-3, Н-8, Н-11).
Результаты исследований антигрибковой активности
Материалы и методы. Объектом исследования служили 2 образца веществ на наличие противогрибковой активности.
Маркировка (название) образцов: 1. О-А — диэтиламинометилглауцин, 2. G-М морфолиноами-нометил глауцин. Препаратом сравнения служил антигрибковый препарат нистатин.
Изучение антигрибковой активности веществ проводилось по отношению к грибам Aspergillus niger. Aspergillus flavus, Trichophyton mentagraphytos, Epidermophyton fioccosum, Penicillium citrinum методом дисков.
Культуры грибов выращивали на плотной среде (Сабуро) рН-5,6 ±0,2 при t 37 и 28° С, в зависимости от особенностей роста грибов, в течение 48 часов. Культуры разводили 1/1000 изотоническим раствором натрия хлорида и засевали в чашки Петри со средой Сабуро по методу «сплошного газона». На подсушенную поверхность среды накладывали стерильные диски, на которые наносили растворы исследуемых веществ (10 мкг) в виде капли (разведение 1:10 в этиловом спирте). В чашки помещали также контрольные стандартные диски с антигрибковым препаратом нистатином. Посевы инкубировали в термостате в течение 48 часов при температуре от 20 до 25°С.
Антигрибковая активность оценивалась по диаметру зон задержки роста культуры грибов. Сплошной рост на чашке оценивали как отсутствие антигрибковой активности. Статистическую обработку проводили методами параметрической статистики с вычислением средней арифметической и ее стандартной ошибки.
Результаты исследований. Установлено, что практически все представленные образцы проявляют умеренную противогрибковую активность (табл.2). Умеренно-выраженное противогрибковое действие к Trichophyton mentagraphytos проявил диэтиламинометил глауцин. В отношении Penicillium citrinum все вещества проявили слабую активность. Также все образцы проявили слабую антигрибковую активность к грибковым штаммам Aspergillus niger и Aspergillus flavus. Результаты исследования антимикробной активности образцов приведены в таблице 2.
Результаты исследований фагоцитарной активности
Материалы и методы. Объектом исследования служил О-А — диэти-ламинометилглауцин и морфолиноаминометилглауцин
Скринииговое исследование влияния веществ на фагоцитарную активность клеток проведено в цельной крови. 100 мкл гепаринизированной венозной крови (20 ЕД гепарина на 1 мл крови) вносили в лунку иммунологического планшета и инкубировали с 50 мкл раствора испытуемого вещества в течение 15 минут в термостате при 37° С. Затем вносили суточную культуру (концентрация 20 микробных тел на клетку, штамм) в объеме 50 мкл в лунки с кровью. Вновь инкубировали образцы в термостате при 37° С в течение 15 минут. После этого содержимое лунки переносили на обезжиренное спиртом предметное стекло и в течение 20 минут термостатировали при 37°С в условиях влажной камеры. Затем мазки высушивали на воздухе в вертикальном положении, проводили гемолиз эритроцитов дистиллированной водой в течение 3 минут, после чего высушенные мазки фиксировали 30 минут в смеси Никифорова и окрашивали азур-эозином в течение 10 минут. При микроскопировании (увеличение 10x40, масляная иммерсия) подсчитывали количество фагоцитирующих нейтрофилов (фагоцитарный индекс) на 200 фагоцитов и количество стафилококков, поглощенных одним нейтро-филом (фагоцитарное число).
Сухое вещество массой 2 мг с учетом известной его растворимости разводили в физиологическом растворе, или в 0,4 мл 96 %-ного спирта, до полного растворения и доводили до 2 мл физиологическим раствором. Конечная концентрация испытуемых веществ составила 1 мг/мл. Контролем служили мазки крови, инкубированной с физиологическим раствором. Вещества тестировались в концентрации 0,1 и 1 мг/мл. Препараты сравнения иммунал и левамизол. Каждое вещество в одной концентрации тестировалось в трех определениях. Статистическую обработку результатов проводили методами параметрической статистики с вычислением средней арифметической (М) и ее стандартной ошибки (т). Результаты скринингового исследования приведены в таблице 3.
В результате исследования установлено, что диэтиламинометилглауцин в обеих изученных дозах проявляет выраженные фагоцитозстимулирующие свойства.
Морфолиноаминометилглауцин проявляет дозозависимое влияние на фагоцитоз нейтрофилов, т.е. относится к группе модуляторов исследуемого процесса. Он в низкой концентрации (0,01мг/мл) оказывает супрессирующее воздействие на фагоцитоз.
Список литературы
1 Юнусов С.Ю. Алкалоиды. — Ташкент, 1974. — С. 320.
1 АриповаХ.Н. Итоги исследования алкалоидоносных растений. — Ташкент, 1993. — 220 с.
2 Горяев М.И., Круглыхина Г.К., Сатдарова Э.И., Куринная Н.В., Шабанов И.М., Пояков П.П. Материалы к изучению алкалодоносности флоры Казахстана и некаторых районов Средней Азии // Химия природных соединений: Тр. хим. наук. — 2000. — Т. 4. — С. 112-122.
3 Садритдинов Ф.С., Курмуков А.Г. Фармакология растительных алкалоидов и их применение в медицине. — Ташкент: Медицина, 1980.