Из работ [1-18] о применении Pt, Ru и Pt-Ru катализаторов в реакции дегидрирования, селективного каталитического окисления (СКО) метана, парокислородной конверсии СН4, паровой конверсии метана, разложения углеводородов и аммиака остается неясным оптимальное соотношение благородных элементов в Pt-Ru катализаторах и концентрация их на носителях.
Ранее нами в работе [19,20] исследовались низкопроцентные (0,05-1,0вес.%) Pt-Ru/2%Се/(q+a)-Al2O3 катализаторы с различным соотношением Pt к Ru в процессе СКО метана в синтез-газ при малых временах контакта. Найдены оптимальные условия подготовки катализаторов для проведения процесса. Установлено, что при временах контакта 3,0-4,0мс конверсия метана изменяется от 96 до 100%, селективность по водороду - 100%, по СО - 95%-100%. При атомном соотношении Pt:Ru ~ 2:1 либо ~ 1:1 наблюдаются максимальные 100% степени превращения метана при селективности по Н2 и СО 100% и при суммарном содержании благородных металлов в составе катализатора 0,2 – 1,0 вес.%.
Целью данной работы явилось исследование процессов парокислородной конверсии, парового риформинга и термического разложения метана на оптимальных составах катализатора.
Экспериментальная часть
Для исследований была приготовлена серия Pt-Ru катализаторов на 2%Ce/(θ+α)Al2O3 с общим содержанием металлов 0,2% и 1,0% с атомным соотношением Pt:Ru~2:1. Катализаторы готовились путем последовательного нанесения элементов на (θ+α)-Al2O3 (100-200 мкм, Sуд=57,7 м2/г) из водных растворов солей металлов Ce(NO3)3×6H2O, Ru(OH)Cl3, и H2PtCl6×6H2O методом капиллярной пропитки по влагоемкости с последующим прогревом на воздухе при 873К 3 часа.
Активность катализаторов в реакции СКО, паровой, парокислородной конверсии и термического разложения СН4 определяли в проточной установке при атмосферном давлении в кварцевом микрореакторе с внутренним диаметром 4,5 мм по методике [2]. Навеска катализатора 10 мг тщательно перемешивалась с порошком кварца (размер частиц 0,2 мм в соотношении 1:43, высота слоя 20 мм), а сверху в реактор добавлялись частицы более крупного кварца (1¸2 мм) до общей высоты слоя 70 мм.
Анализ исходной смеси и продуктов реакции проводили с использованием хроматографа «Хроматэк Кристалл 5000.1» с программным обеспечением «Хроматэк Аналитик 2,5» на капиллярной колонке, заполненной фазой состава 20% гептадекана на диатомитовом носителе с детектором по теплопроводности, снабженного автоматическим газовым дозатором, подключенным непосредственно к установке по окислению метана в синтез-газ. Отбор проб проводился автоматически через 60 секунд после начала реакции.
Катализаторы предварительно восстанавливались смесью Н2+Ar (40:60, об.%) при 1173К со скоростью потока 60 мл/мин в течение 1 часа, либо испытывались невосстановленные образцы, прогретые на воздухе. После продувки системы инертным газом (Ar) в течение 30 мин со скоростью 50 мл/мин, для парокислородной конверсии СН4 подавалась исходная реакционная смесь состава: СН4:О2:Н2О:Ar=2,0:1,0:2,0-4,0:93,0-95,0 (%); в случае паровой конверсии: СН4:Н2О:Ar=3,99:3,6-42,74:86,46-53,27 (%); в реакции СКО:СН4:О2:Ar=2,0:1,0:97,0 (%); а при термическом разложении:СН4:Ar = 4,0:96,0 (%); при температуре 1123К и объемной скорости (V) от 510.103 до 1 047.103 ч-1 при времени контакта (t) от 3,4.10-3 до 7,0.10-3 с. Испытания проводились в течение 100-600 минут до установления показателей процесса.
Результаты и их обсуждение
В первой серии опытов исследовался невосстановленный в Н2 0,16%Pt+0,04%Ru катализатор на (θ+α)Al2O3, модифицированный 2%Ce в процессе паровой конверсии СН4 при варьировании концентрации паров воды Н2О (%) в реакционной смеси при температуре 1123К, V =628-1 047*103ч-11. В таблице 1 приведены количество подаваемой Н2О (%), концентрация продуктов реакции, соотношение H2/CO, конверсия СН4, селективность по Н2 и СО на 60 минуте анализа.
Из данных таблицы видно, что при взаимодействии реагирующих веществ в соотношении 3,99% СН4 + 92,54-86,46% Ar + 3,6-9,55% Н2О с V=628-663*103 ч-1, концентрация водорода на выходе составляла 3,9% и 3,0% без выделения СО и СО2, при этом конверсия СН4 составляла 63,2-65,0%, а селективность по Н2 – 30,2-38,6%.
Далее при увеличении количества добавляемой Н2О в реакционную смесь до 12,99% повышалась концентрация выделяемого Н2 до 3,7%, появлялось СО – 1,75%, при этом соотношение H2/CO=2,1 и обнаружены следы СО2 – 0,0025%, повышалась конверсия СН4 до 80,0%, селективность по Н2 и по СО до 38,6% и 54,8%.
При дальнейшем увеличении количества добавляемой Н2О от 15,72% до 19,92% концентрация Н2 резко увеличилась до 11,97%, концентрация СО колебалась в пределах 1,15%-1,4%, при этом соотношение Н2/СО=10,4 и 8,55, обнаружены следы СО2. Конверсия СН4 и селективность по Н2 повышались до максимальных 100% значений, а селективность по СО равнялась 28,82% и 35,08%.
Увеличение добавляемой концентрации Н2О от 23,72% до 34,32% приводило к уменьшению концентрации Н2 до 9,0%, концентрации СО падала до 1,45-0,8%, при этом соотношение Н2/СО изменялось от 6,2 до 11,25, обнаружены следы СО2. Максимальное 100% значение конверсии СН4 наблюдалось в этих условиях, селективность по Н2 падала 75,18%, а по СО понижалась от 36,34% до 20,05%.
Обогащение парами Н2О исходной реакционной смеси до 42,74% приводило к уменьшению концентрации Н2 и СО до 7,2% и 0,2%. При этом соотношение Н2/СО=36, также обнаружены следы СО2, понизилась конверсия СН4, селективность по Н2 и по СО, соответственно, до 80,7%, 74,53% и 6,2%.
Таблица 1 – Влияние концентрации паров воды в паровой конверсии СН4 на невосстановленном 0,16%Pt+0,04%Ru/2%Се/(q+a)-Al2O3 катализаторе
|
Н2О, (%) |
СН4:Н2О |
[H2], % |
[CO], % [CO] |
[CO2], % |
H2/CO |
XCH4, % |
SH2, % |
SCO, % |
|
3,6 |
1:1 |
3,9 |
0 |
0 |
- |
63,2 |
30,2 |
- |
|
9,55 |
1:2,3 |
3,0 |
0 |
0 |
- |
65,0 |
38,6 |
- |
|
12,99 |
1:3,2 |
3,7 |
1,75 |
0,0025 |
2,1 |
80,0 |
38,6 |
54,8 |
|
15,72 |
1:3,9 |
11,97 |
1,15 |
0,0025 |
10,4 |
100,0 |
100,0 |
28,82 |
|
19,92 |
1:4,9 |
11,97 |
1,4 |
0,025 |
8,55 |
100,0 |
100,0 |
35,08 |
|
23,72 |
1:5,9 |
9,0 |
1,45 |
0,03 |
6,2 |
100,0 |
75,18 |
36,34 |
|
34,32 |
1:8,6 |
9,0 |
0,8 |
0,005 |
11,25 |
100,0 |
75,18 |
20,05 |
|
42,74 |
1:10 |
7,2 |
0,2 |
0,0025 |
36,0 |
80,7 |
74,53 |
6,2 |
|
Анализ продуктов на 60 минуте процесса. 0,16%Pt+0,04%Ru/2%Се/(q+a)-Al2O3 катализатор, Тр=1123К. Исходная реакционная смесь: 3,99%СН4 + 86,46-53,27%Ar + 3,6-42,74% Н2О, V=628 -1 047*103 ч-1, τ= 5,7-3,4 мс |
||||||||
Таким образом, в паровой конверсии СН4 максимальное значение по Н2 (11,97%) со следами СО достигалось при соотношении СН4:Н2О=1:3,9 и 1:4,9, а при меньшем или большем соотношении показатели процесса ухудшались.
Далее нами было проведено исследование восстановленного в смеси Н2+Ar катализатора состава 0,8%Pt+0,2%Ru на носителе в реакции парокислородной конверсии СН4 в зависимости от изменения температуры и концентрации паров воды.
В таблице 2 приведены условия проведенных экспериментов, концентрации веществ на выходе из реактора, изменение конверсии СН4, селективности по Н2 и СО, соотношение H2/CO для процесса парокислородной конверсии СН4 при соотношениях СН4:О2 = 2:1, СН4:Н2О = = 1:1 и СН4:Н2О=1:2 в зависимости от температуры реакции.
Таблица 2 – Изменение концентрации продуктов, конверсии метана, селективности по H2 и CO и соотношения H2/CO в зависимости от изменения температуры эксперимента на 0,8%Pt+0,2%Ru/2%Се/(q+a)- Al2O3 катализаторе
|
Условия опыта |
Т, К |
СН2, % |
ССО, % |
ССО2, % |
ХСН4, % |
SH2, % |
SCO, % |
H2/CO |
|
2,0%СН4+ СН4:Н2О=1:1; |
1023 |
1,1 |
0,3 |
0 |
97,5 |
28,2 |
15,4 |
3,6 |
|
1073 |
2,0 |
0,6 |
0 |
98,75 |
50,6 |
30,4 |
3,3 |
|
|
1123 |
4,0 |
2,0 |
0 |
100,0 |
100,0 |
100,0 |
2,0 |
|
|
1173 |
3,0 |
0,6 |
0 |
100,0 |
75,0 |
30,0 |
5,0 |
|
|
2,0%СН4+ СН4:Н2О=1:2; |
1023 |
1,0 |
0,116 |
0,0125 |
62,4 |
40,16 |
13,9 |
8,6 |
|
1073 |
2,69 |
0,5 |
0,0125 |
81,2 |
83,02 |
46,2 |
5,3 |
|
|
1123 |
3,99 |
1,28 |
0,0125 |
100,0 |
100,0 |
96,5 |
3,1 |
|
|
1173 |
3,99 |
1,3 |
0,0225 |
100,0 |
100,0 |
97,7 |
3,06 |
|
|
2,0%СН4+1,0%О2+2,0-4,0%Н2О+93,0-95,0%Ar, СН4:О2=2:1, СН4:Н2О=1:1 и 1:2, V=900*103 ч-1, τ=4,0мс. |
||||||||
Видно, что при температуре 1023К конверсия СН4 при равномсоотношении СН4:Н2О=1:1 равна 97,5%, при избытке паров воды СН4:Н2О =
=1:2 62,4%, а с повышением температуры реакции до 1073К соответственно увеличивается до 98,75% и 81,2%. Начиная с 1123К и при 1173К достигается максимальное значение – 100%. Селективность по Н2 и по СО соответственно увеличивается с повышением температуры от 28,2% и 15,4% до 100% при 1123К, но уменьшается при 1173К до 75,0% и 30,0%. С увеличением температуры реакции при соотношении СН4:Н2О=1:2 повышается селективность по Н2 и по СО от 40,16% и 13,9% до 100,0% и 97,7% при 1173К, а также выделяется малое количество СО2 (ССО2 =0,0125%).
Таким образом, в парокислородной конверсии метана с увеличением температуры происходило постепенное повышение превращения СН4 до максимального 100% значения. Более предпочтительным процессом по превращению метана является парокислородная конверсия СН4 (СН4:Н2О=1:1), т.е. добавление в реакционную систему малых количеств кислорода (1,0%) и паров воды (2,0%), способствующее окислительной конверсии метана.
В следующей серии опытов исследовался невосстановленный в Н2 0,16%Pt:0,04%Ru катализатор на (θ+α)Al2O3, модифицированной 2%Ce, в процессах СКО СН4, парокислородной конверсии СН4 и термического разложения СН4. Проведено определение влияния температуры реакции на превращение метана.
На рисунке 1 показано сравнение процессов СКО СН4, парокислородной конверсии СН4 и термического разложения СН4 по превращению СН4 в температурном интервале 1023-1173К. Видно, что при температуре 1023К для данных процессов конверсия СН4 находится в пределах от 50% до 62,4%, т.е. в СКО - 59,3%, парокислородной конверсии – 62,4% и в термическом разложении СН4 - 50%. С увеличением температуры процессов до 1073К наблюдалось повышение конверсии СН4 до 68%, 81,2% и 78,7%, соответственно. При дальнейшем увеличении температуры до 1123К и 1173К наблюдались максимальные 100% превращения СН4 для процессов СКО и парокислородной конверсии СН4, а для термического разложения превращение СН4 составляло 83,75%.
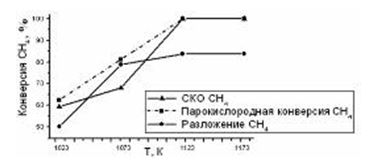
Рисунок 1 – Изменение конверсии СН4 в реакциях СКО, парокислородной конверсии и термиченского разложения СН4. Данные по конверсии СН4 определялись на 60 минуте анализа
В СКО метана при относительно низких температурах (1023К) превращение СН4 не высокое (выше превращения СН4 в термическом разложении, но ниже превращения метана в парокислородной конверсии СН4), но с увеличением температуры происходило постепенное повышение превращения СН4 до максимального 100% значения.
В процессе термического разложения при всех температурах превращение СН4 не превышает соответствующих значений в парокислородной конверсии и СКО СН4,где максимальное значение составляет 83,75%.
Таким образом, при температурах от 1023К до 1123К более предпочтительным процессом по превращению метана является парокислородная конверсия СН4 с соотношением СН4:Н2О=1:1 на катализаторе с атомным соотношением Pt-Ru~2:1 вне зависимости от количественного содержания металлов (0,2% и 1,0%), т.е. добавление в реакционную систему малых количеств кислорода и паров воды способствуют окислительной конверсии метана.
СПИСОК ЛИТЕРАТУРЫ
1 Попова Н.М., Досумов К. Катализаторы селективного окисления и разложения метана и других алканов. – Алматы: Наука, 2007. – С. 203.
2 Павлова С.Н. и др. // Кинетика и катализ. – 2004. – Т.45. – №4. – С. 622.
3 Садыков В.А. и др. // Кинетика и катализ. – 2005. – Т.46. – №2. – С. 243.
4 Арутюнов В.С., Крылов О.В. Окислительные превращения метана. – М.: Наука, 1998. – С. 350.
5 Кипнис М.А., Волнина Э.А., Самохин П.В. // XVIII Менделеевский съезд по общей и прикладной химии. – М., 2007. – Т. 3. – С. 185.
6 Петрова Н.В., Шкребко О.А., Явич А.А. // XVIII Менделеевский съезд по общей и прикладной химии. – М., 2007. – Т. 3. – С. 213.
7 Антонова Н.А. Автореф. дис. на соиск уч. степ. канд. хим. наук, ИОКЭ АН КазССР. – Алма-Ата, 1988. – С. 24.
8 Кипнис М.А., Волнина Э.А., Нелюба Т.Ю. // XVIII Менделеевский съезд по общей и прикладной химии. – М., 2007. – Т. 3. – С. 184.
9 Liang Y., Zhang H., Zhong H., Zhu X. // J. Catal, 2006. – V.238. – P.468.
10 Ефимов М.Н. и др. // XVIII Менделеевский съезд по общей и прикладной химии. – М. 2007. – Т. 3. – С. 351.
11 Сокольский Д.В. и др. // Известия АН КазССР. – 1970. – №6. – С. 72.
12 Кузора Т.В. // Известия АНКазССР. – Алма-Ата. – 1971. – №6. – С. 14-18.
13 Сокольский Д.В. и др. // Известия АН КазССР. – 1973. – №5. – С. 29.
14 Dossumov K., Salakhova R.Kh., Popova N.M., Tungatarova S.A., et al // III Intern. Conf. Catalysis: Fundamentals and Application, Novosibirsk. – 2007. OP-II-4. – P. 125.
15 Попова Н.М. и др. // Кинетика и катализ. – 1997. – Т. 38. – №5. – С. 749.
16 B. Li, S. Kado, Y. Mukainakano, M. Nurunnabi, T. Miyao, S. Naito. K. Kunimori. // Applied catalysis A: General. – 2006. – V. 304. – P. 62-71.
17 Mukainakano Y., Yoshida K., Okumura K., Kunimori K., Tomishige K. // Catalysis Today. – 2008. – V. 132. – P. 101-108.
18 G. Jones, J. G. Jakobsen, S.S.Shim, J. Kleis. // Journal of Catalysis. 2008. – V. 259. – P. 147-160.
19 Досумов К., Попова Н.М., Байжуманова Т.С., Тунгатарова С.А. // Нефтехимия. 2009. (в печати).
20 Досумов К., Попова Н.М., Байжуманова Т.С., Тунгатарова С.А. // Известия НАН РК. – 2009. (в печати).