Топлива на основе керосина применяются в воздушном и наземном военном транспорте, гражданской авиации и в паре с кислородом в ракетоносителях типа «Союз» и «Молния». Топливо «керосин Т-1» является сложной смесью более чем 260 алифатических и ароматических углеводородов, включая переменные концентрации потенциальных ядов, типа бензола, n-гексана, ксилолов, нафталены (ПАУ, изомеры n-пропилбензена, триметилбензена) /1/. Ранее нами было показано, что длительное поступление в организм крыс «керосина Т-1» сопровождается активацией монооксигеназной системы печени в начальные сроки воздействия и последующим её угнетением /2/. Снижение содержания и активности цитохрома р450 и гибель гепатоцитов могут являться следствием активации процессов ПОЛ, которые, как известно, являются универсальным неспецифическим звеном в развитии большинства патологических изменений в клетках. Перекисное окисление мембранных фосфолипидов играет важную роль в поддержании нормальной физиологической активности клетки, являясь необходимым, например, для синтеза простагландинов, лейкотриенов. В то же время, неконтролируемая липопероксидация может приводить к повреждению мембран, выражающемуся в нарушении белок-липидных и липид-липидных взаимодействий, ингибированию активности ферментов, изменению избирательной проницаемости мембран для ионов и т.д. Для проверки предположения о роли процессов ПОЛ в развитии патологических изменений в печени крыс при длительном воздействии «керосином Т-1» было исследовано содержание в органе продуктов ПОЛ (ГПЛ и МДА), и факторов антиоксидантной защиты (восстановленный глутатион, GSH).
МАТЕРИАЛЫ И МЕТОДЫ
В эксперименте были использованы нелинейные белые половозрелые крысы весом 175 – 200 грамм. Животные были разделены на следующие группы: I группа – контрольные животные; II – VI группы – животные, подвергавшиеся ингаляционному воздействию паров керосина Т-1 3 часа в дозе 6 мг/л в течение 1, 4, 8, 16 и 30 дней соответственно, VII – XI группы – контрольные животные для каждой точки эксперимента. Животных помещали в специальную камеру объемом 70,7 л на 3 часа. Забой животных осуществляли под эфирным наркозом, кусочки печени помещали в холодный 0,05 М трис-НСl буфер (рН 7) с добавлением 0,1 М КСl и 0,9 мМ ЭДТА и с помощью гомогенезатора Поттера приготавливали 10% гомогенат. Об интенсивности процессов ПОЛ судили по концентрации МДА /3/ и уровню гидроперекисей липидов /4/ в гомогенате, содержание глутатиона определялипо йодометрической реакции. Полученные результаты обрабатывали общепринятыми методами информационной статистики, достоверность различий оценивали по критерию Стьюдента.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рисунке 1 и 2 представлены результаты исследования первичных продуктов ПОЛ – гидроперекисей липидов (ГПЛ) и вторичного продукта – малонового диальдегида (МДА) в гомогенате печени крыс, подвергавшихся ингаляционному воздействию «керосина Т-1» в течение 1,4, 8, 16 и 30 дней.
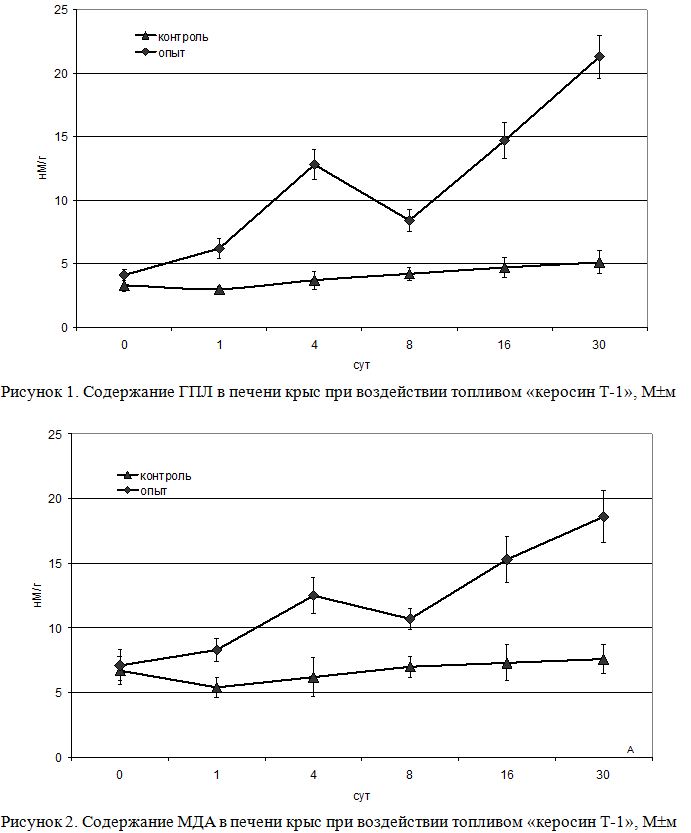
Видно, что содержание ГПЛ и МДА в печени интоксицированных животных резко возрастало на 4 сутки после воздействия по сравнению с контролем соответственно в 3,5 (Р≤0,01) и 2,0 (Р≤0,05) раза. На 8 сутки эксперимента, наоборот, происходило достоверное снижение содержания первичных и вторичных продуктов ПОЛ в 1,5. В дальнейшем (на 16 и 30 сутки эксперимента) вновь наблюдалось повышение уровня ГПЛ и МДА в печени интоксицированных крыс. При этом содержание ГПЛ и МДА на 16 сутки превышало контрольный уровень в 3,0 (Р<0,01) и в 2,0 (Р≤0,01) раза, а на 30 сутки - в 2,4 (Р≤0,001) и 4,0 (Р≤0,001) раза.
Длительная интоксикация животных керосином Т-1 приводила не только к активации ПОЛ, но и к значительным изменениям антиоксидантной защиты клеток. Определение содержания восстановленного глутатиона – одного из факторов антиоксидантной системы клеток, выявило его мобилизацию в первые сутки после ингаляционного воздействия керосином Т-1 (рисунок 3). Установлено, что уровень восстановленного глутатиона в печени интоксицированных крыс на 1 сутки возрастал почти в 1,5 раза по сравнению с контролем.
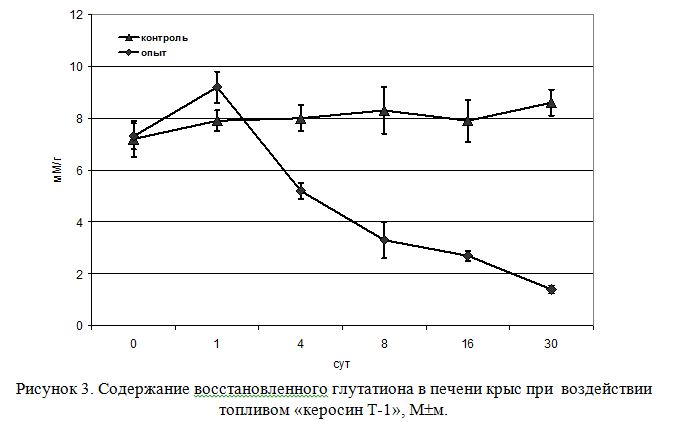
Однако после 4 суток ингаляции керосином Т-1 содержание восстановленного глутатиона резко уменьшалось ( практически в два раза, Р≤ 0,01) и продолжало снижаться по мере увеличения продолжительности воздействия ксенобиотика. Так, на 8 сутки эксперимента уровень GSH в печени снижался почти в 2,0 раза (Р ≤0,05), на 16 сутки – в 3,0 раза (Р≤0,01), а на 30 суткам - в 6,5 раз (Р≤0,001).
Наблюдаемое на 4 сутки после ингаляционного воздействия керосином Т-1 увеличение ГПЛ и МДА в печени крыс является, вероятно, следствием индукции ферментов микросомального окисления и в частности цитохрома Р450. Известно, что в процессе ферментативных реакций с участием цитохрома Р450 происходит образование активных форм кислорода и усиление процессов липопероксидации в мембранах микросом /5/. Ранее нами было показано, что именно на 4 сутки ингаляционного воздействия керосина Т-1 приходится пик активации монооксигеназ, увеличение содержания цитохрома Р450 в печени интоксицированных крыс /2/. В то же время, наблюдаемое на 4 сутки эксперимента увеличение содержания первичных и вторичных продуктов ПОЛ может быть связано со снижением уровня восстановленного глутатиона, который, как показывает наше исследование, резко падает в этот период. Дальнейшее увеличение содержания продуктов ПОЛ в печени интоксицированных крыс также, по-видимому, связано с истощением восстановленного глутатиона. Известно, что восстановленный глутатион (GSH) является неотъемлемым компонентом реакций, катализируемых глутатионпероксидазой, субстратами которой являются первичные продукты ПОЛ, особенно ГПЛ /6/. Доказано, что если в клетках имеет место снижение содержания восстановленного глутатиона во времени, то с большой степенью достоверности можно говорить об интенсификации ПОЛ, вызванной тем или иным фактором /5/. Кроме того, GSH играет центральную роль в инактивации токсичных и реактивных продуктов (хинонов, семихинонов, эпоксиды и др), генерируемых в реакциях биотрансформации ксенобиотиков, в нашем случае компонентов керосина Т-1 /7/. Из литературы известно, что маркером поступления керосина в организм млекопитающих является нафтален – один из его компонентов, который гидроксилируется системой цитохрома Р450 до 1-нафтола /8/. В свою очередь 1-нафтол трансформируется в цитотоксичные 1,2-эпоксиды и 1,2- и 1,4-нафтохиноны /9, 10/. Снижение уровня GSH, таким образом, будет способствовать накоплению вышеуказанных цитотоксичных продуктов и, как следствие, интенсификации процессов ПОЛ, то есть усилению процессов липопероксидации.
Таким образом, в результате выполненного исследования было установлено, что длительное воздействие керосина Т-1 приводит к активации процессов перекисного окисления в печени, о чем свидетельствует высокий уровень ГПЛ и МДА и снижение восстановленного глутатиона в печени интоксицированных крыс. Истощение глутатиона приводит к усилению процессов липопероксидации и, вероятно, к накоплению токсичных метаболитов компонентов топлива, что также способствует развитию деструктивных изменений в печени.
ЛИТЕРАТУРА
- Zeiger E., Smith L. The first international conference on the environmental health and safety of jet fuel //Environmental health perspectives. – 1998. – vol.6, №11. – pp. 763 - 764
- Суворова М.А. Изучение монооксигеназной ферментной системы печени крыс при воздействии ракетным топливом керосин Т-1// Вестник КазНУ. Серия экологическая. – 2008. - №2(23). – С.43 -48
- Гаврилов В.Б., Мишкорудная М.И. спектрофотометрическое определение содержания гидроперекисей липидов в плазме крови // Лабораторное дело. – 1983. - №3. – С. 23 – 25
- Стальная И.Д., Граишвили Г.Г. Определение МДА с помощью тиобарбитуровой кислоты //Современные методы в биохимии. Под ред. В.Н. Ореховича. – 1977. – С. 66 – 68
- П.В.Гулак, Дубченко А.М., Зайцев В.В. Гепатоцит: Функционально-метаболические свойства. М.: Наука, 1985. - 272 с.
- J.Feher, G.Csomos and A.Vereckei. Role of free radical reactions in liver diseases // Free radicals and the liver. Springer-verlag. Berlin, 1992, pp. 1-13
- Lipid peroxidation and hepatocyte damage in the animal model and human patients. G.Poli, E.Chiarpotto et al //ibid. pp. 36-43
- Wilson AS, Davis CD, Williams DP, Buckpitt AR, Pirmohamed M, Park BK. Characterisation of the toxic metabolite(s) of naphthalene//Toxicology – 1996. - №114(3) – рр 233-42
- Buckpitt A.R., Bahnson L.S., Franklin R.B.Hepatic and pulmonary microsomal metabolism of naphthalene to glutathione adducts: factors affecting the relative rates of conjugate formation //J Pharmacol Exp Ther. – 1984. - № 231(2). – рр.291-300
- Buckpitt A.R., Warren D.L. Evidence for hepatic formation, export and covalent binding of reactive naphthalene metabolites in extrahepatic tissues in vivo // J Pharmacol Exp Ther. – 1983. - №225(1). – рр.8-16