В настоящее время одним из наиболее перспективных направлений в исследовании является использование растений для восполнения недостатка белка в рационе как человека, так и животных. Благодаря простоте выращивания, быстрым темпам роста и размножения, большому количеству легкоусвояемого белка, а так же содержание с своем составе витаминов, жирных кислот, микро и макроэлементов, делает микроводосроли спирулину и хлореллу лидерами данного направления.
Цель работы состояла в получении экстрактов микроводорослей Chlorella vulgaris и Spirulina sp и разработке на их основе биологически активных добавок к кормам рыб. Для решения этой цели были поставлены следующие задачи:
- Усовершенствование методики выращивания микроводорослей Chlorella vulgaris (штамм Т-4) и Spirulina sp
- Получение чистых культур и выделение чистых экстрактов Chlorella vulgaris (штамм Т-4) и Spirulina sp.
- 0пределение аминокислотного состава Chlorella vulgaris штамма Т-4.
- Разработка на основе полученных экстрактов биологически активных добавок в пищу декоративных видов рыб.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЙ
Для получения монокультуры микроводорослей цианобактерии культивировали на жидких средах в конических колбах, объемом 100 мл в люминаторе с круглосуточным освещением при температуре 26-28 градусов Цельсия. Продолжительность культивирования 30 дней. Для кульитивирования использовались среды Зарукка, Тамия, Еленкина и Чу-10.
Для выявления оптимального вида среды для каждой конкретной культуры проводили определение динамики прироста концентрации клеток ( в случае одноклеточных культур ), или прироста биомассы. 0пределение проводили через каждые 5 суток в процессе 30-дневного культивирования. В пробах просчитывали концентрацию клеток с помощью камеры Горяева. Для определения прироста биомасс все содержимое колбы наливали в стеклянные бюксы, упаривали при темп 105 градусов в течение 1 часа, сушили ночь над CaCl2 и взвешивали, повторяя эту операцию неоднократно для доведения до постоянного веса. Сухой вес биомассы определяли с точностью до 0,0001г. Для определения коэффициента размножения (КР), который использовался нами как критерий роста культур , пользовались следующей формулой
КР= м2/м1,
где м2 - сухой вес биомассы в конце опыта ( конечная концентрация клеток ), м1 - сухой вес посевного материала ( начальная концентрация клеток ).
Плотность клеток определяли на фотоэлектроколориметре, который использовали как нефелометр. Для снятия влияния зеленого цвета микроводорослей, измерение проводили при 540 и 590 нм, т.е. в зеленых лучах спектра.
Аминокислотный состав белков в среде определяли методом бумажной хроматогрфии. Культуральную жидкость микроводорослей упаривали при 45 0C на водяной бане с вентилятором. Сухой остаток растворяли в 70 проц спирте и наносили на полоски хроматографической бумаги. Параллельно с опытными растворами наносили пятна метчиков стандартных аминокислот. Сушили пятна с помощью фена. Хроматограммы разгоняли в системе растровителей БУВ. Окрашенные пятна лилового, сиреневого и фиолетового цветов располагались вдоль линии разгонки. Пятна вырезали и растворяли в 0,1 M CaCl2. Поглощение растворов измеряли на ФЭК при 420 нм. Полученные данные оптической плотности сопоставляли с калибровочными графиками, построенными по растворам соответствующих стандартных аминокислот
При статистической обработке результатов исследования рассчитывали среднюю арифметическую, ошибку средней арифметической.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ
Результаты культивирования и выделения спирулины и хлореллы
Спирулину выращивают в открытых и закрытых фотокультиваторах. Существуют проекты по выращиванию микроводоросли в больших открытых культиваторах на берегу крупных водоемов. Благодаря быстрому росту, водоросль дает протеина в 20 раз больше с единицы площади, чем соя и в 200 раз больше, чем говядина.
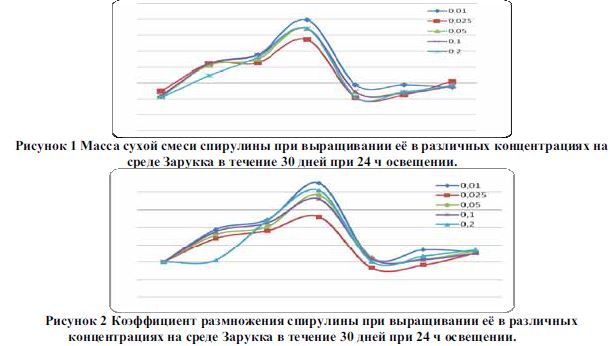
Нами были предприняты усилия по оптимизированию процесса выращивания спирулины Spirulina sp в лабораторных условиях. Для определения оптимальной концентрации и продолжительности выращивания спирулины, цианобактерии выращивали в различных концентрациях на среде Зарукка в течение 30 суток при 24 ч освещении. Через равные промежутки времени определяли массу сухой смеси (рисунок 1) и коэффициент размножения (рисунок 2).
По результатам экспериментов наибольший прирост наблюдался при выращивании спирулины в течении 15 суток. В это время можно собирать цианобактерии. Оптимальная концентрация для посадки спирулины составляет 0,01 мг/л.
Хлорелла - одноклеточная зеленая водоросль, получившая широкое распространение в качестве биологически активной добавки в корма рыб, домашних животных и птиц, пищевой добавки для людей и средства для очищения водоемов. Уникальность хлореллы заключается в том, что по содержанию витаминов хлорелла превосходит все растительные корма и культуры сельскохозяйственного производства.
Однако не все штаммы хлореллы имеют одинаковую ростовую активность и производительность. Зачастую для каждого штамма необходима отдельная обработка режимов культивирования. Минеральный состав питательной среды и барботация (продувка воздухом) является одним из существенных факторов повышения интенсивности ростовых процессов культур водорослей.
Нами было выделено несколько штаммов Chlorella Sp из различных биотопов Алматинской области. Для опытов был выбран штамм ГИ, который культивировали на средах Тамия, ЧУ-10, Еленкина и Фитцджеральда при барботации и без нее в течение 30 суток в люминостате (температура 23-25 °С и освещенность 2000 лк). Темпы роста определялись ежедневно фотоколориметрическим методом (длина волны 590 нм). Концентрацию клеток определяли по калибровочной кривой (рисунок 3).
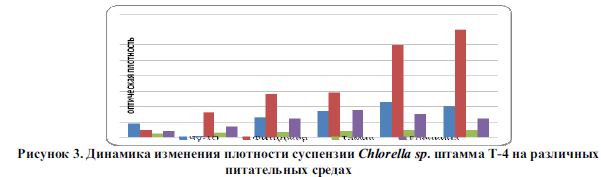
Полученные данные показали, что рост концентрации клеток хлореллы по мере увеличения срока культивирования на указанных средах, проходил с различной скоростью. На среде Тамия наибольшая концентрация клеток, равная 1х10 7 клеток/мл, достигался при непрерывном культивировании в течение 25 суток. Несколько большая плотность клеток получена при такой же продолжительности культивирования на середе ЧУ-10 , что составило 3,4 х 10 7 клеток\мл. Культивирование на среде Фитцджеральда дало ускоренное нарастание концентрации клеток хлореллы. Так, на 15-ые сутки культивирования в этом варианте опыта было определено 5,9 х 10 7 клеток/мл. При последующем увеличении сроков культивирования на этой среде до 20 суток концентрация клеток практически не менялась, что могло свидетельствовать о выходе кривой роста на «плато». Однако при последующем культивировании до 25 суток концентрация клеток вновь увеличилась в 2,5 раза, достигнув величины 14,7 х 10 7 клеток/мл. На 30-ые сутки рост хлореллы на среде Фитцджеральда не прекращался В результате проведенного опыта выяснено, что наиболее оптимальной средой для культивирования оказалась среда Фитцджеральда.
ЗАКЛЮЧЕНИЕ
Анализ результатов опытов с барботацией показал, что продувка воздухом оказала положительное влияние на рост хлореллы. Максимальная интенсивность роста в этих условиях наблюдалась на 20-ые сутки культивирования. Интенсивность роста хлореллы при барботации превышает рост без барботации примерно на 20-ый день опыта, где концентрация клеток достигает показателя 33,3х107 клеток/мл. Оптимальным сроком выращивания хлореллы при барботации является три недели, то есть 20-21 день. Таким образом, установлено, что для культивирования штамма ГИ Chlorella sp. Оптимальной средой оказалась среда Фитцджеральна, а барботация воздухом повышала рост водоросли.
Нами был определен аминокислотный состав штамма Т-4 Chlorella sp. Штамм выращивали на среде Фитцджеральда при барботации воздухом. Результаты определения аминокислотного состава представлены в таблице 1.
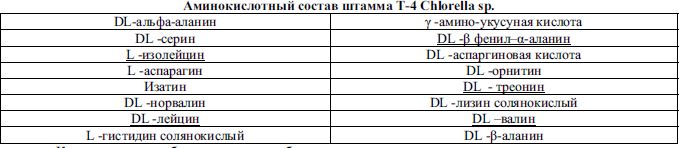
Как видно из таблицы, помимо общего спектра аминокислот, суспензия хлореллы содержит большинство незаменимых аминокислот. Это делает хлореллу уникальной белковой основой для приготовления кормов для рыб.
ЛИТЕРАТУРА
- Beijerinck M.W. Culturversuche mit Zoochlorella, Lichenengonidien und anderen niederen Algen // Bot. Zeit., 48, 47, Idem in: Verzamelde Geschriten van M.W. Beijerinck, 1921, № 2.
- Богданов Н.И. Способ культивирования микроводорослей на основе штамма «Chlorella vulgaris ИФР № С-111»: пат. Рос. Федерация № 2176667 / Н.И. Богданов, М.В. Куницын ; Бюл. № 34. - 2001.
- Акзамов А. Продуктивность микроводорослей, выращенных в различных условиях перемешивания без продувания углекислым газом // Физиолого-биохимические аспекты культивирования водорослей и высших водных растений в Узбекистане. Ташкент: Фан Уз ССР, 1976. - С. 92-93.
- Beijerinck M.W. Culturversuche mit Zoochlorella, Lichenengonidien und anderen niederen Algen // Bot. Zeit., 48, 47, Idem in: Verzamelde Geschriten van M.W. Beijerinck, 1921, № 2.
- Богданов Н.И. Способ культивирования микроводорослей на основе штамма «Chlorella vulgaris ИФР № С-111»: пат. Рос. Федерация № 2176667 / Н.И. Богданов, М.В. Куницын ; Бюл. № 34. - 2001.
- Акзамов А. Продуктивность микроводорослей, выращенных в различных условиях перемешивания без продувания углекислым газом // Физиолого-биохимические аспекты культивирования водорослей и высших водных растений в Узбекистане. Ташкент: Фан Уз ССР, 1976. - С. 92-93.
- Андреева В.М. Род CLORELLA. Морфология, систематика, принципы классификации / В.М. Андреева - Л.: Изд-во «Наука», Ленингр. отд., 1975. - 110 с.