Важной проблемой развития рыбного хозяйства РК является сохранение генофонда редких и исчезающих видов осетровых рыб и формирование представления о его изменениях в современных условиях. Первым этапом для достижения этого является генетическая паспортизация производителей, то есть выявление маркеров, позволяющих получить генетические характеристики особей, популяций и видов. Молекулярно-генетические методы обеспечивают наиболее точную и надежную идентификацию живых осетровых рыб. Для мониторинга генетической вариабельности искусственно размножаемых осетровых применяется метод стандартного ПЦР-анализа и метод RAPD-ПЦР (ПЦР со случайной амплификацией полиморфной ДНК), основанные на амплификации участков ДНК с помощью праймеров, определенной и произвольной нуклеотидной последовательности.
Цель данной работы - проведение молекулярно-генетического анализа полиморфизма выращиваемых осетровых рыб с целью определения пригодности отобранных особей для формирования ремонтно-маточного стада (РМС).
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЙ
Для проведения анализа были отобраны фрагменты плавников особей русского осетра 2-х летнего (33 образца) и 4-х летнего (80 образцов) возраста и годовиков сибирского осетра (35 образцов), выращенных в искусственных условиях. Образцы фиксировались в 96% этиловом спирте и маркировались с присвоением идентификационного номера. Кроме того, регистрировался возраст каждой особи (определяемый рыбоводом), размер и вес.
Выделение ДНК из фрагментов плавников осетровых рыб осуществлялось методом солевой экстракции. Для определения и подтверждения видовой принадлежности особи использовался набор праймеров, разработанный в Центре молекулярно-генетической идентификации осетровых при Всероссийском НИИ рыбного хозяйства и океанографии (ВНИРО) (Н. Мюге и др., 2008, Генетика 44 (7) с. 913-919). Приоритет ВНИРО в разработке ПЦР-системы идентификации осетровых и состав видоспецифичных праймеров защищены патентом РФ № 2332463 от 25 января 2007 г.
Анализ полиморфизма по микросателлитным локусам ядерной ДНК. Анализ проводился методом стандартной ПЦР, с применением амплификатора РТС-225 MJ Research (США). Реакционная смесь (25 мкл) для проведения полимеразной цепной реакции содержала 2,5 мкл 10-кратного буфера для Taq-полимеразы, 1 мкл 50mM MgCl2, 2 мкл смеси четырех дезоксирибонуклеозидтрифосфатов, по 10 пМ каждого из праймеров, 10 нг ДНК и 1,5 единицы Taq-полимеразы. Амплификацию проводят по следующей схеме: предварительное плавление ДНК - 950C (10 мин.), синтез ПЦР-продуктов (35 циклов): плавление - 950С (20 сек.), отжиг праймеров - 580С (15 сек.), синтез ДНК - 720С (15 сек.), финальная элонгация - 720С (5 мин).
Праймеры для микросателлитного анализа синтезировали согласно опубликованным данным [1, 2]. Было запланировано проведение анализа по пяти микросаттелитным локусам по разработанным методикам [1, 2, 3]: Праймеры для микросателлитного анализа:

Выполнен анализ контрольного региона мтДНК исследуемых образцов для определения видового состава и наличия русско-сибирского гаплотипа по методике, описанной Мюге и др. (2008 г). Анализ проводился с помощью метода стандартной ПЦР с использованием амплификатора MJ Research PTC-225 (США) и реагентов различных производителей (Диалат, Силекс, Fermentas и др.). ПЦР-смесь включала в себя 1х Taq-буфер (Силекс, Москва), 2,5 мM MgCl2, 2,5 мМ каждого dNTP (Диалат, Москва), 2,5-5 пM праймеров (согласно табл. 1), 2,8 мкл крезол-глицерина (3,5 мM крезоловый красный, 50% водный раствор глицерина), 2,5 ед. Taq-полимеразы (Силекс-М), 2 мкл раствора ДНК исследуемых образцов и деионизированная вода (milliQ) до конечного объема 15мкл. Условия проведения ПЦР были следующими: предварительное плавление при 95°С - 2 мин., синтез ПЦР-продуктов (35 циклов): плавление - 92°С (20 сек.), отжиг - 57°С (30 сек.), элонгация - 72°С (30 сек.), и финальная элонгация при 72°С - 10 минут. Праймеры использованные для видовой идентификации осетровых:
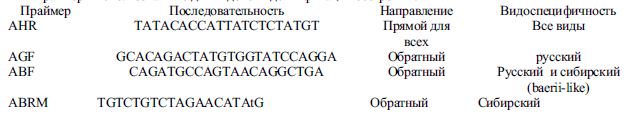
Секвенирование мт ДНК. Проведено прямое секвенирование гипервариабельного участка контрольного региона митохондриальной ДНК с целью выявления изменчивости, наследуемой по материнской линии. Секвенирование проводили на автоматическом секвенаторе ABI 3100 Genetic Analyzer (США) с использованием набора BigDye v.1.1. Секвенирование проводилось по стандартной методике [4, 5].
RAPD-ПЦР анализ. ПЦР анализ проводился с применением амплификатора РТС-225 MJ Research (США) и с использованием готовой смеси AmpliTaq Gold PCR Master Mix. Реакционная смесь, объемом 25 мкл состояла из 2,5 мкл ПЦР буфера, 2,5 мкл 2 мМ дНТФ (дезоксирибонуклеозидтрифосфатов), 0,25 мкл каждого праймера (100 нМ/мкл), 1 мкл Таq-полимеразы, 2 мкл разбавленной в 100 раз пробы ДНК и 16,5 мкл деионизованной воды. Условия ПЦР были следующими: первичная денатурация - 94°C (5 мин.) однократно, синтез ПЦР-продуктов (36 рабочих циклов) - 94°C (30 сек), 36°C (30 сек.), 72°C (1 мин.), финальная элонгация - 72°C (10 мин.) однократно. Осуществлено электрофоретическое разделение ДНК в 1,7 % агарозном геле. Для проведения горизонтального электрофореза ДНК использовали ТВЕ (трисборатный) буфер - 0,089М Трис, 0,089М борная кислота 0,002М ЭДТА. В буфер добавляют бромистый этидий до 0,5 мкг/мл для детекции нуклеиновых кислот. Раствор ПЦР-продукта смешивали с буфером для нанесения образца, содержащим в конечной концентрации 5-10% глицерина или 70% сахарозы и 0,025% краситель БФС (бромфеноловый синий). Электрофорез проводили в течение 20 минут при оптимальной напряженности электрического поля 10 В/см. Использовали камеру Е-2 «Хеликон» и источник питания «Эльф-4». Гели анализировали и фотографировали под ультрафиолетом в трансиллюминаторе.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ.
Анализ последовательностей D-петли митохондриальной ДНК (мтДНК). Анализ выявил наличие двух типов митохондриальной ДНК. Среди особей, маркированных как 2-х летние - 24 особи относятся к «русско-сибирскому» гаплотипу, и 7 особей были определены как представители «русского» гаплотипа митохондриальной ДНК. Среди особей, маркированных как 4х-летние, 2 особи имели «русско-сибирский» гаплотип, а остальные (78 особей) -«русский» гаплотип.
Секвенирование мтДНК. В связи с тем, что в каждой возрастной группе наблюдалась гетерогенность по наличию определенного гаплотипа, был проведен анализ нуклеотидной последовательности (секвенирование) контрольного региона мтДНК. Анализ последовательностей подтвердил присутствие всего двух типов нуклеотидных последовательностей этого высокополиморфного региона, соответствующих русскому и русско-сибирскому гаплотипам, причем особи с русским гаплотипом, маркированные как 4-х летние, и особи, маркированные как 2-х-летние, имели идентичную последовательность ДНК. Также идентична была последовательность у особей с «русско-сибирским» гаплотипом, вне зависимости от декларированного возраста. Проведенный анализ позволяет с высокой степенью достоверности сделать вывод, что все особи русского осетра принадлежат к потомству только двух самок - от одной самки получены четырехлетки, от другой - двухлетки.
Анализ полиморфизма по микросателлитным локусам ядерной ДНК. Проведен анализ по пяти микросателлитным локусам. Однако в связи с очевидной близкородственностью выборки статистический анализ проведен по двум локусам, имеющим наибольшее аллельное разнообразие в данных выборках.
На основании анализа электрофореграмм по каждому из локусов были выявлены аллели, характерные для исследуемых особей. Набор аллелей (от 1 до 4) был индивидуален для каждой особи. У отдельных особей этот набор мог совпадать. Также встречались особи, имеющие сходный состав аллелей, но различающиеся по количеству той или иной аллели. Поэтому учитывался так называемый доз-эффект, вычисляемый по различию в интенсивности свечения полос на каждой отдельной дорожке электрофореграммы. Для определения генотипа исследуемых особей было подсчитано количество аллелей по каждому из локусов в отдельности. В каждой возрастной группе (с учетом проведенной коррекции на основании анализа мтДНК) выявлен уровень полиморфизма, характерный для потомков одной пары производителей. То есть, при оплодотворении икры использовалась сперма только одного самца, либо, если использовалась смесь спермы нескольких самцов, то сперма остальных самцов не была фертильна. Таким образом, можно сделать вывод, что представленные для анализа особи в каждой из возрастных групп являются полными сибсами.
RAPD-ПЦР анализ. Для проведения анализа использовали праймеры А01, А05, А09 и В10. На основании спектрофотометрического анализа полученных растворов ДНК проводили разведение до конечной концентрации 2 мкг/мл. ПЦР выполняли по стандартной методике. На рис. 1 представлен пример RAPD-фингерпринта для ДНК русского и сибирского осетров с праймером А05.
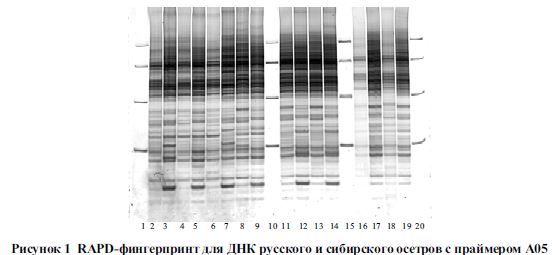
На электрофореграмме можно отметить сходные и отличные полосы-сигналы внутри вида и между видами. Использование различных праймеров показало, что внутри вида наблюдается незначительное различие по числу выявляемых полиморфных полос. Для каждого образца и каждого праймера выявлено более 20 полос в индивидуальных электрофоретических спектрах.
В результате обработки данных были получены дендрограммы по полиморфизму русских и сибирских осетров. На рис. 2 представлена дендрограмма полиморфизма ДНК с использованием праймера А09. Русские и сибирские осетры на дендрограмме находятся на значительном расстоянии друг от друга, но между двумя группами есть промежуточная группа особей, спектры которых перекрываются между собой, причем по всем четырем праймерам обнаруживается одна и та же закономерность: 2, 4 - русские осетры и 7,9,11 - сибирские осетры входили в промежуточную группу особей. Результаты RAPD-ПЦР анализов обрабатывали в программе BioNumerix.

ЗАКЛЮЧЕНИЕ
При проведении молекулярно-генетического анализа полиморфизма выращиваемых осетровых рыб с целью определения пригодности для создания ремонтно-маточного стада выявлено, что отобранные осетровые рыбы представляют собой близкородственных особей, как в выборке русского осетра, так и в выборке сибирского осетра. Все особи русского осетра принадлежат к потомству только двух самок - от одной самки получены четырехлетки, от другой - двухлетки. Таким образом, можно сделать вывод, что представленные для анализа особи сибирского и русского осетров в каждой из возрастных групп являются полными сибсами.
В связи с этим необходимо продолжить пополнение стада неродственными кроссами, чтобы повысить природный генетический полиморфизм формируемого РМС.
В результате анализа генетического полиморфизма методом RAPD-ПЦР, были отобраны и использованы в дальнейшей работе праймеры с нуклеотидной последовательностью: CAG-GCC-CTT-C - A01; AGG-GGT-CTT-G -A05; GGG-TAA-CGC-C - A09; CTG-CTG-GGA-C - B10. На основе полученных данных составлены дендрограммы, выявляющие генетический полиморфизм между видами русского и сибирского осетра и внутри этих видов. При анализе была выявлена группа особей занимающих по RAPD-ПЦР спектрам промежуточное положение между русскими (Acipenser gueldenshtaedtii) и сибирскими (A. baerii) осетрами.
ЛИТЕРАТУРА
- Zane et al., Isolation and characterization of microsatellites in the Adriatic sturgeon (Acipenser naccarii); 2002, Mol. Ecol. Notes, 2, 586-588.
- Welsh et al., Identification of microsatellite loci in lake sturgeon, Acipenser fulvescens, and their variability in green sturgeon, A. medirostris; Mol. Ecol. Notes, 3, 47-55.
- Henderson-Arzapalo, King TL., Novel microsatellite markers for Atlantic sturgeon (Acipenser oxyrinchus) population delineation and broodstock management; 2002, Mol. Ecol. Notes, 2, 437-439.
- Тимошкина Н.Н., А.Е.Барминцева, А.В.Усатов, Н.С.Мюге. Внутривидовой генетический полиморфизм русского осетра (Asipenser gueldenstaedtii) // Генетика - 2009. - №9. - С.1250-1259.
- Тимошкина Н.Н. Внутривидовой генетический полиморфизм русского осетра. дисс. канд.биол.наук, 2009.118 с.