Статья посвящена новому методу молекулярной диагностики — петлевой изотермической амплификации (LAMP). Рассматриваются компоненты, этапы данной реакции, методы визуализации продуктов амплификации, также описаны ее преимущества и недостатки. К преимуществам петлевой изотермической амплификации относятся простота, скорость, специфичность и чувствительность, экономическая эффективность. В отличие от полимеразной цепной реакции в методе LAMP используется четыре (шесть) праймера, что обеспечивает высокий уровень его специфичности. Автором подчеркнуто, что LAMP проводится в условиях постоянной температуры, т. е. для его осуществления не требуется такого дорогостоящего оборудования, как амплификатор. Для постановки LAMP можно использовать приборы на базе термоблока или водяную баню. Кроме того, в статье дана информация о возможности применения данного метода для диагностики бактериальных, вирусных инфекционных заболеваний. На данный момент разработано небольшое количество тест-систем для определения ДНК и РНК патогенов. Основным производителем тест-систем является компания Eiken Chemical.
Петлевая изотермическая амплификация (LAMP) является новым методом амплификации нуклеиновых кислот, который был разработан Tsugunori Notomi и его коллегами в 2000 г. [1]. Сущность данного метода заключается в удвоении участка ДНК с высокой специфичностью, эффективностью и скоростью в условиях постоянной температуры. При совмещении с обратной транскрипцией LAMP может с высокой эффективностью амплифицировать РНК последовательности. Данный метод основан на автоматическом цикле синтеза ДНК цепи со смещением при использовании ДНК-полимераз с высокой активностью смещения и четырех (шести) специально созданных праймеров. Четыре прай-мера сконструированы таким образом, чтобы быть нацеленными на шесть определенных регионов гена-мишени. Последние обозначаются как F3c, F2c и F1c на 3'-конце и В1с, В2с и В3с на 5'-конце. Различают внешние (Outer) и внутренние (Inner) праймеры. Первый внешний праймер F3 (Forward Outer Primer) состоит из F3 региона, который комплементарен F3c фрагменту гена-мишени. Второй внешний праймер В3 (Backward Outer Primer) состоит из В3 региона, который комплементарен В3с участку гена-мишени. Третий праймер — внутренний FIP (Forward Inner Primer) содержит F2 фрагмент на 3'-конце, который комплементарен F2c, а также такую же последовательность, как и F1c регион ДНК мишени на 5'-конце. Четвертый праймер BIP Backward Inner Primer также является внутренним и состоит из региона В2 на 3'-конце и такой же последовательности, как и В 1с регион на 5'-конце [2].
Этапы LAMP показаны на рисунке. В LAMP-реакции различают три этапа:
1) этап синтеза начального материала (starting material producing step);
2) этап циклической амплификации (cycling amplification step);
3) этап элонгации и рециклирования (elongation and recycling step).
Реакция протекает в изотермических условиях, так как денатурация цепей происходит за счет их смещения. Сама реакция инициируется внутренними праймерами, содержащими смысловые и бессмысленные последовательности ДНК мишени. При температуре 60 °С F2 регион внутреннего прай-мера FIP гибридизируется с мишенью, и цепь достраивается с помощью ДНК-полимеразы. Затем внешний праймер F3 присоединяется к F3с фрагменту мишени, и полимераза достраивает цепь, при этом смещая только что синтезированную последовательность. Смещенная цепь формирует петлеобразные структуры на 5'-конце, так как F1c участок гибридизируется с F1 регионом. На 3'-конце праймеры также гибридизируются с мишенью, и в итоге получается новая цепь с петлеобразными структурами на обоих концах. С такой, похожей на гантель ДНК начинается второй этап — цикл экспоненциальной амплификации. Цепи с несколькими инвертированными повторяющимися последовательностями ДНК мишени могут быть синтезированы благодаря повторениям процессов достраивания и смещения цепей [3].
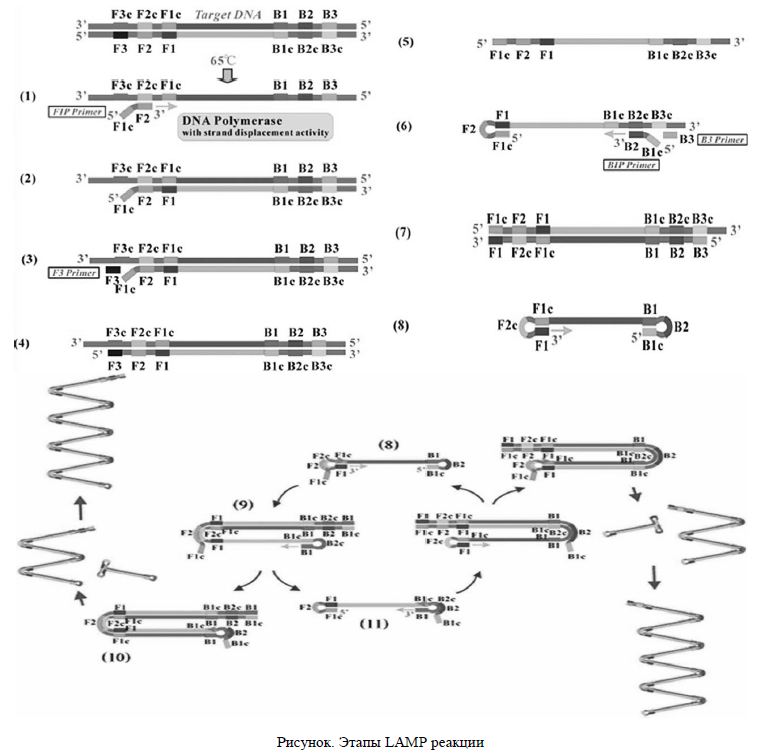
Цикл продолжается около 1 часа и приводит к образованию примерно 109 копий ДНК мишени. Конечный продукт реакции представляет собой цепи ДНК с петлями различной длины, состоящие из нескольких перевернутых, повторяющихся последовательностей оригинального ДНК-шаблона (структура похожа на цветную капусту).
Визуализация продуктов амплификации. Для визуализации конечного продукта LAMP-реакции могут использоваться несколько методов. Чаще всего применяется метод визуализации с помощью электрофореза в агарозном геле. Агарозный гель обрабатывают красителями, например, бромистым этидием или SYBR Green I. Так как конечный продукт состоит из цепей различной длины с многочисленными петлями ДНК, электрофорез в агарозном геле определяет продукты с минимальным количеством копий ДНК мишени в загрузочной лунке, которые выглядят как мазок на верхушке петли в основании геля. LAMP реакция позволяет синтезировать чрезвычайно большое количество ДНК. Добавление красителя SYBR Green I в реакционную пробирку дает возможность визуализировать продукты с помощью прибора для УФ просвечивания флуоресцирующих в свете или поглощающих свет объектов. Данный метод пригоден для полевых наблюдений, где лимитирующим фактором является электрофорез в агарозном геле. Другой способ предусматривает накопление большого количества побочных продуктов реакции. В LAMP-реакции образуется большое количество побочных продуктов, ионов пирофосфата, от которых в реакционной смеси получается белый осадок пирофосфата магния. Поэтому, определяя присутствие или отсутствие белого осадка, можно узнать, амплифицировалась ли ДНК. Так как в ходе реакции происходит возрастание плотности раствора, для определения её окончания можно использовать колориметрию [4].
Таким образом, нами были рассмотрены такие методы детекции продуктов LAMP, как визуализация продуктов реакции электрофорез + окрашивание бромидом этидия/нитратом серебра; флуоресцентная детекция в растворе интеркалирующими агентами (SybrGreen, PicoGreen, Yo-Pro-Iodide, PicoGreen) — Optigene и турбидиметрическая визуализация — образование нерастворимого пиро-фосфата, турбидиметрия + флуоресценция Calcein/Naphtol Blue с пирофосфатом магния — Eiken. Кроме того, могут быть использованы BART — турбидиметрия + люминесценция — 3М, электрохимическое определение продуктов, реакция биотин-СТР-продуктов с Nanogold-частицами, Surface Plasmon Resonance, флуоресцентно-меченые праймеры.
Преимущества LAMP-метода
- Простота. Изотермическая амплификация выполняется в один этап, легко визуализировать конечные продукты.
- Скорость. Конечные результаты анализа можно получить уже через 15-60 минут.
- Специфичность и чувствительность. Использование 4 или 6 праймеров обеспечивают высокую специфичность реакции, так как они узнают 6 или 8 последовательностей-мишеней. Многие исследователи сообщают о высокой чувствительностиLAMP до 6 копий искомого гена, что в 10 раз превышает чувствительность стандартной ПЦР.
- Экономическая эффективность. Не требуется специальных дорогостоящих реагентов и оборудования.
- Количество амплифицированных продуктов. В течение 15-60 мин приводит к образованию примерно 109-1010 копий ДНК мишени.
- Амплификация РНК. Метод подходит для амплификации РНК при добавлении обратной транскриптазы [5].
Реактивы и оборудование для LAMP
Для проведения данной реакции используется фермент Bst-полимераза, которая является большой субъединицей ДНК-полимеразы Bacillus stearothermophilus (Eiken, NEB, 3M). Оптимальная температура для данного фермента 60-65 °С. Данная реакция более специфична к последовательности матрицы, так как в ней участвуют 4-6 праймеров, нацеленных на многие ее звенья. Так же как и для любой реакции амплификации, должны быть ДНК-матрица и четыре дезоксирибонуклеотида, а также буфер, бетаин, сульфат магния.
Для постановки LAMP можно использовать приборы на базе термоблока (не требуется точного термоциклирования) или водяную баню, градуированную микроволновую печь. Отсутствие специальных дорогостоящих аппаратов также доказывает преимущества метода.
Использование LAMP для диагностики инфекций
Хотя LAMP был создан в 2000 г., его популярность стала расти только после широкого распространения вирусов лихорадки Западного Нила и тяжелого острого респираторного синдрома (ТОРС).
На сегодняшний день с помощью данного метода диагностированы возбудители таких вирусных заболеваний, как лихорадка денге [6], японский энцефалит [7], чикунгунья [8] (тропическая комариная лихорадка), лихорадка Западного Нила [9], тяжелый острый респираторный синдром — ТОРС [10], высокопатогенный «птичий грипп» (H5N1) [11].
Метод LAMP используют также для определения бактериальных инфекций. В настоящее время коммерциализированы тест-системы для следующих возбудителей: Salmonella, Legionella, Listeria, Esherichia coli, продуцирующая веротоксин, Campylobacter. В таблице 1 представлен список патогенов, диагностированных с помощью LAMP, с указанием ученых, разработавших методику их определения [2].
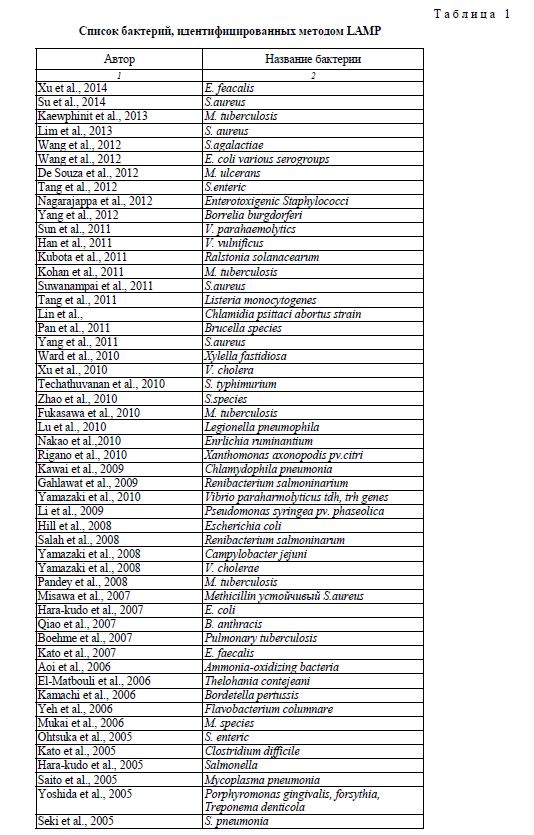

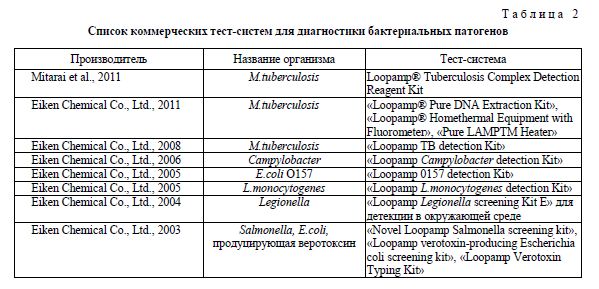
В настоящее время большое количество бактериальных патогенов диагностируется методом петлевой изотермической амплификации. Некоторые исследователи разработали коммерческие тест-системы, которые позволяют быстро и легко определять вид бактерии (табл. 2). Эти наборы содержат буфер, бетаин, дезоксирибонуклеотиды, праймеры, Bst-полимеразу, MgSO4 в соответствующих концентрациях. Готовые наборы для детекции M.tuberculosis, Campylobacter spp и т.д. коммерциализированы химической компанией Eiken (Eiken Chemical Co., Ltd) [2].
С помощью метода LAMP диагностируются не только бактериальные и вирусные патогены, но также и инфекции, вызываемые простейшими. Одним из таких патогенов является малярийный плазмодий. Так, Birgit Poschl и его коллеги провели сравнительный анализ следующих трех методов диагностики для обнаружения возбудителей малярии: микроскопия, вложенная полимеразная цепная реакция (nPCR) и LAMP. С этой целью в 105 образцах крови человека, собранных в Северном Таиланде, определяли наличие Plasmodium falciparum и Plasmodium vivax. Общее количество положительных образцов Plasmodium falciparum составило 57 (54 %), а Plasmodium vivax — 25 (24 %). В качестве эталона для сравнения был использован метод nPCR. Чувствительность LAMP для Plasmodium falciparum составила 100 %. Все nPCR-отрицательные образцы для данного возбудителя также были отрицательными при диагностике методами микроскопии и LAMP (специфичность 100 %). Для диагностики Plasmodium vivax методом микроскопии обнаружены 15 из 23 nPCR-положительных образцов (чувствительность 65 %), методом LAMP — 22 из 23 (чувствительность 96 %). Из 82 nPCR-отрицательных образцов микроскопия обнаружила два положительных образца (специфичность 98 %). Все 82 nPCR-отрицательные также были отрицательными по методу LAMP (специфичность 100 %). Использование как родоспецифичных, так и видоспецифичных наборов праймеров для LAMP давало одни и те же результаты во всех образцах. Следовательно, для диагностики видов Plasmodium в образцах крови данной популяции применение метода LAMP так же оправданно, как и nPCR. Кроме того, он надежнее, чем микроскопия [5].
Таким образом, нами были рассмотрены принцип, этапы и компоненты нового метода молекулярной диагностики — петлевой изотермической амплификации. Было выявлено, что данный метод имеет ряд преимуществ по сравнению с другими методами диагностики. Также был проведен краткий обзор литературы по использованию LAMP в диагностике вирусных, бактериальных инфекций и заболеваний протозойной этиологии. Из всего сказанного выше можно сделать вывод о том, что петлевая изотермическая амплификация является перспективным методом и требует дальнейших исследований по определению его эффективности в определении ДНК различных патогенов.
Список литературы
- Notomi T., Okayama H., Masubuchi H., Yonekawa T., Watanabe K., Amino N., Hase T. Loop-Mediated Isothermal Amplification Of DNA // Nucleic Acids Re— 2000. — Vol. 28, No. 12. — P. E63.
- Saharan P., Dhingolia S., Khatri P., Duhan J.S., Gahlavat S.K. Loop-mediated isothermal amplification (LAMP) based detection of bacteria: Review // African Journal of Biotechnology. — 2014. — 13. — P. 1920-1928.
- Lei Yan, Jie Zhou, Yue Zheng, Adam S. Gamson, Benjamin T. Roembke, Nakayama S., Herman O. Sintim. Isothermal amplified detection of DNA and RNA // Mol. BioSyst.— — No. 10. — P. 970-1003.
- http://aquavitro.org/2013/06/13/sredstva-diagnostiki-zabolevanij-ryb-molekulyarnaya-diagnostika/
- Pdschl B., Waneesorn J., Thekisoe O., Chutipongvivate S., Karanis P. Comparative diagnosis of malaria infections by microscopy, nested PCR, and LAMP in northern Thailand // TropMedHyg. — 2010. — 56-60.http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2912576/
- Parida M., Horioke , Ishida H., Dash P.K., Saxena P., Jana A.M., Islam M.A., Inoue S., Hosaka N., Morita K. Rapid detection and differentiation of dengue virus serotypes by a real-time reverse transcription-loop-mediated isothermal amplification assay // J. Clin. Microbiol. — 2005. — Vol. 43. — P. 2895-2903.
- Parida M.M., Santhosh S.R., Dash P.K., Tripathi N.K., Saxena P., Ambuj S., Sahni A.K., Lakshmana Rao P.V., Morita K. Development and evaluation of reverse transcription-loop-mediated isothermal amplification assay for rapid and real-time detection of Japanese encephalitis virus // Journal of Clinical Microbiology. — 2006. — 44. — P. 4172-4178.
- Parida M.M., Santhosh S.R., Dash P.K., Tripathi N.K., Lakshmi V., Mamidi N., Shrivastva A., Gupta N., Saxena P., Babu J.P., Rao P.V.L., Morita K. Rapid and Real-Time Detection of Chikungunya Virus by ReverseTranscription Loop-Mediated Isothermal Amplification Assay // Journal of Clinical Microbiology. — 2007. — 45. — P. 351-357.
- Parida M., Posadas G., Inoue S., Hasebe F., Morita K. Real-Time Reverse Transcription Loop mediated isothermal amplification for rapid detection of West Nile Virus // Journal of Clinical Microbiology. — 2004. — 42. — P. 257-263.
- Hong T.C., Mai Q.L., Cuong D. V., Parida M., Minekawa H., Notomi T., Hasebe F., Morita K. Development and evaluation of a novel loop-mediated isothermal amplification method for rapid detection of severe acute respiratory syndrome coronavirus // Journal of Clinical Microbiology. — 2004. — 42. — P. 1956-1961.
- Imai M., Ninomiya A., Minekawa H., Notomi T., Ishizaki T., Tu P.V., Tien N.T.K., Tashiro M., Odagiri T. Rapid diagnosis of H5N1 avian influenza virus infection by newly developed influenza H5 hemagglutinin gene-specific loop mediated isothermal amplification method // Virol. Methods. — 2007. — 141. — P. 173-180.