В статье разработан метод генотипирования группы крови, основанный на ПЦР в реальном времени. Он может быть использован в качестве дополнения к классическому серологическому способу. Данный метод определения группы крови человека, включающий генотипирование трех полиморфизмов гена АВО (261, 796 и 803), отличается тем, что генотипирование проводится методом полимеразной цепной реакции в режиме реального времени и позволяет определять группу крови АВ0 у населения Казахстана с точностью до 99,5 %. Проведение генетического тестирования аллелей гена АВО будет наиболее востребовано в центрах переливания крови в случае возникновения спорных ситуаций при стандартном определении группы крови.
Введение
Для безопасного переливания крови должны быть удовлетворены три основных условия. Во-первых, красные кровяные тельца должны быть совместимы по группе крови АВ0. Во-вторых, не допускается переливание резус-положительных эритроцитов резус-отрицательным реципиентам женского пола. В-третьих, эритроциты донора не должны иметь антигенов, вступающих в реакцию с любым клинически значимым антителом реципиента. Таким образом, возникает вопрос, существуют ли надежные и недорогие ДНК-методы для определения антигенов группы крови АВ0, удовлетворяющие эти условия, чтобы рассматривать их в качестве замены существующих серологических методов?
Известно, что ошибки при определении групповой принадлежности крови у реципиентов создают серьезные предпосылки для развития гемолитических осложнений при гемотрансфузионной терапии. Частота острых гемолитических осложнений в среднем составляет 1 на 25 тыс. трансфузий. Фатальные гемолитические осложнения встречаются с частотой 1 на 100 тыс. трансфузий. Несовместимость по группе АВ0 составляет примерно 83 % от всех фатальных острых гемолитических осложнений [1]. При этом летальность в результате несовместимых по системе АВ0 трансфузий составляет в Великобритании 1 на 10 случаев несовместимых трансфузий, в США — 1 на 18, в России — 1 на 3,9 [2, 3]. Летальность гемолитических осложнений в Казахстане неизвестна. Точный анализ частоты встречаемости острых гемолитических осложнений затруднен, поскольку в трансфузиологической практике, как в нашей стране, так и за рубежом ряд осложнений скрывается или маскируется под видом других диагнозов [4].
В настоящее время описано более 300 наследуемых антигенов, находящихся на поверхности эритроцитов, и характеризующих группы крови человека [5, 6]. Эти антигены были впервые выявлены после обнаружения антиген-специфичных антител, присутствующих в сыворотке крови человека. Около 50 из этих антигенов являются полиморфными в любой популяции земного шара. То есть альтернативные аллели представлены в популяции в большей степени, чем теоретически возможно. Некоторые из полиморфных антигенов являются клинически значимыми при переливании крови и могут приводить к гемолитической болезни плода (ГБП), а также другим побочным реакциям. Следовательно, безопасное переливание для большинства реципиентов зависит от корректного типирования больных и доноров в отношении фенотипа АВ0 и скрининга сыворотки пациентов на наличие клинически значимых антител, полиморфных среди местного населения. Например, определение антигена D (резус-фактора) обязательно среди доноров и реципиентов в популяциях, где он полиморфен, потому что именно он будет являться основной причиной ГБП и других побочных реакций. В странах Юго-Восточной Азии, где резус-отрицательный фенотип является редкостью, данная процедура необязательна [7].
Известно, что фенотип AB0 определяется экспрессией гена гликозилтрансферазы. Группы крови АВ0 у человека определяются тремя альтернативными вариантами гена гликозилтрансферазы (А, В, 0), расположенного на 9-й хромосоме. Эта система групп крови наследуется по множественному принципу, при котором действие различных вариантов одного гена проявляется в равной степени, независимо друг от друга. Попарное сочетание этих генов определяет одну из четырех групп крови. Ген АВО состоит из 7 экзонов размером от 28 до 688 п.н., с наибольшей кодирующей последовательностью в 7-м экзоне. Два последних экзона содержат 823 нуклеотида из 1062 и кодируют растворимую часть АВО гликозилтрансферазы, содержащую каталитический домен. На основании нуклеотидного полиморфизма, который детектируется в этом районе, к настоящему моменту описано большое число аллелей гена АВО [8-11]. Только те полиморфные замены, которые приводят к смене аминокислоты, являются критичными в определении активности и субстрат-специфичности глико-зилтрансферазы и, таким образом, ответственными за различные АВО-фенотипы. К настоящему моменту описано 26 несинонимичных замен в нуклеотидных последовательностях экзонов 6 и 7. За одним исключением, все они локализованы в 7-м экзоне. Однако надо отметить, что каждая популяция имеет свой уникальный набор аллельных вариантов генов, что усложняет разработку тест-систем, основанных на ДНК-анализе.
За последние 30 лет в медицине наблюдается тенденция к уменьшению количества предтранс-фузионных тестов и внедрение модифицированных тестов, основанных на агглютинации, например, таких как гелевый тест, которые могут проводиться сотрудниками лаборатории без длительного практического обучения, характерного для традиционных серологических методов. Несмотря на то, что эти тесты идеально подходят большинству реципиентов, некоторые пациенты имеют более высокий риск аллоиммунизации, например, при серповидно-клеточной анемии или талассемии, и, следовательно, нуждаются в более точном подборе донорской крови [12, 13].
Параллельно с упрощением процедуры предтрансфузионного тестирования долгое время проводились масштабные исследования по изучению генов, ответственных за образование групп крови [14]. В результате был разработан новый подход определения антигенов группы крови, основанный на определении последовательности ДНК, а не на реакции агглютинации. Основным недостатком ДНК-метода является то, что он не может обнаружить непосредственно присутствие или отсутствие антигена на поверхности эритроцитов. Несмотря на это, существует ряд клинических случаев, когда этот подход является востребованным. В настоящее время существует несколько способов ге-нотипирования гена ABO, непосредственно участвующего в формировании группы крови человека. К ним относятся секвенирование нуклеотидной последовательности гена, рестрикционный анализ, ДНК-анализ на чипах и некоторые другие методы, основанные на полимеразной цепной реакции (аллель-специфичная ПЦР, анализ кривых плавления, метод конкурирующих такман зондов). В настоящей работе предлагается использование метода полимеразной цепной реакции в режиме реального времени, который является наиболее быстрым, удобным и достаточно точным для применения в центрах переливания крови.
Следует отметить, что определение генетической структуры локусов, ответственных за экспрессию эритроцитарных антигенов, позволит избежать ошибок в определении групп крови, связанных с объективными трудностями при выполнении иммуногематологических исследований. Поэтому проведение генетического тестирования аллелей генов эритроцитарных антигенов будет наиболее востребовано в центрах переливания крови в случае возникновения спорных ситуаций при стандартном определении группы крови.
Материалы и методы
Сбор образцов осуществлялся на базе Научно-производственного центра трансфузиологии г. Астаны у лиц, которые являлись донорами крови. Кровь собирали на основе информированного согласия, также добровольцы заполняли анкету. У всех добровольцев были определены группы крови стандартным методом иммуноферментного анализа.
ДНК из образцов венозной крови выделяли классическим методом высаливания. Количественное содержание ДНК проводили на спектрофотометре Nanodrop 1000. Амплификация ДНК 6 и 7 эк-зонов гена ABO проводилась с сиквенс-специфичными праймерами, представленными в таблице. Общий объем реакционной смеси для ПЦР был равен 25 мкл и содержал 3,2 пмоль прямого и обратного праймеров, 10 нг геномной ДНК, 0,2 единицы фермента Taq Pol (Fermentas), 200 мкМ каждого из дезоксинуклеотидтрифосфатов (дНТФ), 1x буфер для ПЦР (Fermentas) и 2,5 мМ раствор MgCl2.
Протокол для ПЦР был следующим: 94 0C — 10 мин; затем 35 циклов, включающих в себя денатурацию при 94 °С, — 1 мин, отжиг при 55 °С — 1 мин, элонгация при 72 °С — 1 мин и заключительная элонгация при 72 °С — 7 мин. Продукты ПЦР детектировались в 1,5 % агарозном геле с добавлением бромистого этидия. Нуклеотидная последовательность продуктов определялась на генетическом анализаторе ABI 3730xl с тем же набором праймеров (Applied Biosystems, США). Полученные нуклео-тидные последовательности сравнивались с последовательностью NM_020469.2 (transferase A, alpha-1-3-N-acetylgalactosaminyltransferase; transferase B, alpha-1-3-galactosyltransferase). Для обнаружения полиморфизмов использовался программный пакет SeqScape V 2.6 (Applied Biosystems, США).

В общей сложности в исследовании приняли участие 500 добровольцев, из них 369 казахов. Изначально групповая принадлежность определялась с помощью обычного серологического метода в центре переливания крови. Фенотипы 369 образцов выглядели следующим образом: группа крови A (n=99), В (n=93), 0 (n=132) и АВ (n=45). Далее выделяли ДНК методом высаливания. В связи с тем, что подавляющее большинство нуклеотидных замен, приводящих к изменению АВО-фенотипа, локализованы в 6 и 7 экзонах гена АВО, было принято решение ограничиться секвенированием данных экзонов (см. рис.). Определение нуклеотидной последовательности проводилось методом прямого секвенирования с использованием сиквенс-специфичных праймеров. Так как в случае экзона 7 при использовании фланкирующих праймеров получался фрагмент более 600 п.н. (оптимальный для проведения реакции секвенирования), дополнительно были выбраны внутренние праймеры, которые использовались для амплификации двух перекрывающихся фрагментов, соответствующих 7-му экзону гена АВО. Детекция продуктов ПЦР перед секвенированием проводилась электрофоретически. По результатам сравнения полученных нуклеотидных последовательностей гена АВО с референтной последовательностью NM_020469.2 (transferase A, alpha-1-3-N-acetylgalactosaminyltransferase; transferase B, alpha-1-3-galactosyltransferase), находящейся в открытом доступе Национального центра биотехнологической информации США (http://www.ncbi.nlm.nih.gov/nuccore/NM_020469.2), отбирались наиболее информативные полиморфизмы для данной выборки. В результате было отобрано три полиморфизма гена АВО (261, 796 и 803), на которые были подобраны праймеры и конкурирующие зонды для проведения ПЦР в реальном времени.
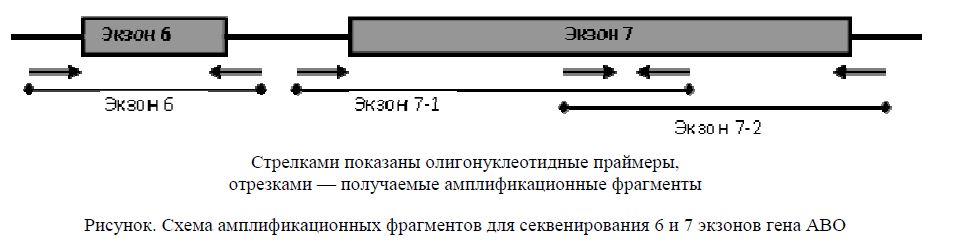
Рисунок. Схема амплификационных фрагментов для секвенирования 6 и 7 экзонов гена АВО
Далее, используя метод полимеразной цепной реакции в режиме реального времени, нами была определена групповая принадлежность по системе ABO у 369 человек с известной группой крови. Группа крови определялась следующим образом. Наличие делеции гуанина в 261 положении гена АВО (261 del) в гомозиготном состоянии приводит к однозначному определению группы крови 0. Среди гетерозигот по 261 del носители аллеля 796A как в гетеро-, так и в гомозиготной форме относятся к группе крови В, а носители аллеля 796С — к группе крови А, группа крови АВ в данном случае невозможна. При отсутствии делеции в 261 положении в гомозиготном состоянии группы крови определяются по наличию мутации C796A: генотип С/С — группа крови А и 0, генотип С/А и генотип А/А — группа крови В и АВ. В позиции 796 дикий тип (С) в показывает 0 либо А и на 100 % исключает АВ. Замена С на А на 100 % исключает группы 0 и А и показывает группу В. Гетерозигота С/А также на 100 % исключает 0 и А. В позиции 803 замена G на C на 100 % исключает 0 и А и показывает группу В.
Анализ результатов генотипирования полиморфизмов в образцах с известной группой крови показал, что точность определения группы крови человека методом ПЦР в реальном времени достигает 99,5 % (367 из 369 человек). В двух оставшихся случаях можно предположить наличие редких аллелей, которые маскируют группу крови. В одном случае гетерозиготный носитель делеции в 261 положении (261G/del-796С/С-803G/G), определенный нами как имеющий группу крови А, по результатам серологического исследования имел группу крови О. В данном случае ошибка может происходить из-за наличия нуклеотидной замены G802A. Во втором случае гетерозиготный носитель нуклео-тидной замены C796A (261G/G-796С/А-803G/G) определялся нами как имеющий группу крови АВ, хотя по стандартной методике он имел группу крови А. В то же время встречаемость таких образцов составила менее 1 % от общего количества правильно определенных групп крови. Таким образом, генотипирование трех полиморфизмов гена ABO (261, 796 и 803) является достаточным для идентификации основных генотипов АВО, встречающихся у населения Казахстана.
Таким образом, нами был разработан метод для генотипирования групп крови АВ0, основанный на ПЦР в реальном времени. Метод может быть использован в качестве дополнения к классическому серологическому способу определения группы крови. Данный способ определения группы крови человека, включающий генотипирование трех полиморфизмов гена АВО (261, 796 и 803), отличается в первую очередь тем, что генотипирование проводится методом полимеразной цепной реакции в режиме реального времени и позволяет определять группу крови АВ0 у населения Казахстана с точностью до 99,5 %.
В перспективе применение данной технологии определения группы крови позволит предотвратить развитие гемолитических осложнений при гемотрансфузионной терапии, что особенно актуально для больных анемией и другими аутоиммунными заболеваниями. Кроме того, разработанный метод позволит уменьшить риск неправильного подбора донора и последующего несоответствия групп крови при переливании.
Таким образом, изучение молекулярного полиморфизма генов человека дает возможность определять генетические детерминанты физиологических особенностей человека. В частности, способ определения группы крови человека методом ПЦР в реальном времени может быть использован в здравоохранении, в медицинских учреждениях различного профиля, в центрах переливания крови и диагностических центрах Республики Казахстан.
Список литературы
- Dunbar N.M., Ornstein D.L., DumontL.J. ABO incompatible platelets: risks versus benefit // Current opinion in hematology.— Vol. 19, № 6. — P. 475-479.
- Berseus O., Boman K., Nessen S.C., Westerberg L.A. Risks of hemolysis due to anti-A and anti-B caused by the transfusion of blood or blood components containing ABO-incompatible plasma // Transfusion. — 2013. — 53, Suppl.1. — P. 114-123.
- Izetbegovic S. Occurrence of ABO and RhD Incompatibility with Rh Negative Mothers // Materia socio-medica. — 2013. — Vol. 25, № 4. — 255-258.
- Колосков А. Как повысить иммунологическую безопасность гемотрансфузионной терапии? // Медицинская газета. Наука и практика. — 2006. — № 82. — 27 окт. — С. 12-15.
- Daniels G.L., Fletcher A., Garratty G. et al. Blood group terminology 2004: from the International Society of Blood Transfusion committee on terminology for red cell surface antigens // Vox Sang. — 2004. — Vol. 87. — P. 304-316.
- Daniels G.L., Flegel W.A., Fletcher A. et al. International Society of Blood Transfusion Committee on Terminology for Red Cell Surface Antigens: Cape Town report // Vox Sang. — 2007. — 92. — P. 250-253.
- Lin M. Taiwan experience suggests that RhD typing for blood transfusion is unnecessary in southeast Asian populations // Transfusion. — 2006. — 46, № 1. — P. 95-98.
- Yamamoto F., Clausen H., White T. et al. Molecular genetic basis of the histo-blood group ABO system // Nature. — 1990.
- 345. — P. 229-233.
- Patenaude S.I., Seto N.O.L., Borisova S.N. et al. The structural basis for specificity in human ABO(H) blood group biosynthesis // Nat. Struct. Biol. — 2002. — 9. — P. 685-690.
- Lee H.J., Barry C.H., Borisova S.N. et al. Structural basis for the inactivity of human blood group O2 glycosyltransferase // J. Biol. Chem. — 2005. — 280. — P. 525-529.
- Storry J.R., Carter V., Helberg A. et al. Pre-transplantation confirmatory ABO genotyping reveals a novel non-deletional O allele // Vox Sang. — 2008. — 95, Suppl.1. — P. 178.
- Vichinsky E.P., Earles A., Johnson R.A. et al. Alloimmunization in sickle-cell anemia and transfusion of racially unmatched blood // Engl. J. Med. — 1990. — Vol. 322. — P. 1617-1621.
- Josephson C.D., Su L.L., Hillyer K.L. et al. Transfusion in the patient with sickle cell disease. A critical review of the literature and transfusion guidelines // Transfus. Med. Rev. — 2007. — Vol. 21. — P. 118-133.
- Chapman J.F., Milkins C., Voak D. The computer crossmatch: a safe alternative to the serological crossmatch // Transfus. Med. — 2000. — 10. — P. 251-256.