В статье представлены и обсуждаются результаты применения различных методов создания инфекционного фона Pyricularia oryzae для проведения фитопатологической оценки устойчивости селекционных материалов риса к пирикуляриозу и отбора болезнеустойчивых сортов и линии риса. Экспериментальным путем установлено, что наиболее эффективным лабораторным методом создания инфекционного фона является инокуляция отрезки листьев растений риса фильтровальной бумагой, пропитанной конидиальной суспензией гриба и инокуляция отрезки листьев растений риса каплями конидиальной суспензии патогена.
Введение
Одним из опасных заболеваний риса во всем мире, в том числе и в Казахстане, является пирикуляриоз, вызываемый несовершенным грибом Pyricularia oryzae Br. et Cav. (синоним Magnaporthe grisea (Hebert) Barr) [1-4]. Впервые оно было описано в Японии в 1704 г., а его возбудитель – в 1896 г. Сейчас пирикуляриоз известен во всех районах возделывания риса [1]. Патоген поражает все надземные органы растения, что приводит к потере урожая на 30-60%, а в годы эпифитотий – на 80-100% [2-4].
В настоящее время по научной и экономической важности возбудитель пирикуляриоза риса P. oryzae возглавляет «Топ-10» грибных болезней растений. Эксперты подчеркивают экономическое значение этого гриба, так как он может буквально уничтожать рисовые поля, являющиеся основой для пропитания половины населения Земли [5]. Возбудитель P. oryzae образует фитотоксины – пирикулярин и α-пиколиновую кислоту, вызывающие у растений типичные симптомы заболевания. Устойчивые к пирикуляриозу сорта риса устойчивы и к действию этих токсинов [6].
Наиболее практичным и экономичным подходом в борьбе с пирикуляриозом риса является использование сортов, устойчивых к болезни. Определение устойчивости растений к патогену базируется на создании жесткого инфекционного фона и провокационных условий при возделывании культуры. Инфекционный фон может быть естественным и искусственным. При этом естественный инфекционный фон непостоянен и может варьиро-вать в пределах одного года и в разрезе отдельных лет, так как погодные условия не всегда благоприятствуют развитию, интенсивному размножению и распространению возбудителя болезни. В годы с умеренным и слабым развитием болезней гарантированную оценку болезнеустойчивости обеспечивает искусственное заражение растений, которое можно осуществлять как в полевых инфекционных питомниках, так и в условиях искусственного климата – теплицах и климатических камерах [6, 7].
В связи с этим, фитопатологии и селекционеры в своей работе в основном использует искусственный инфекционный фон для определения вирулентности гриба и отбора устойчивых сортов растений. Следовательно, изучение иммунологических свойств исходного и селекционного материала при искусственном заражении растений позволяет выявлять потенциальную и стабильную устойчивость сортообразцов, проводить своевременную браковку и отбор невосприимчивых форм на всех этапах селекции, что значительно ускоряет селекционный процесс, сокращая сроки выведения новых сортов культуры [8].
Успешная инокуляция может быть осуществлена при наличии ряда благоприятных условий [9]:
- оптимальная температура для прорастания спор, конидии или развития мицелия гриба;
- высокая влажность на поверхности листьев для прорастания спор;
- качество и интенсивность освещения;
- растения должны быть в достаточно восприимчивой физиологической стадии развития;
- инокулюм должен быть наиболее эффективно распределен на растении.
К настоящему времени разработаны различные способы и методы создания инфекционного фона возбудителем P.oryzae. Однако не все известные методы являются эффективными для оценки устойчивости сортов риса к болезни. Прежде чем провести массовый скрининг сортов риса на устойчивость, необходимо выбрать эффективного метода по созданию инфекционного фона, что сказывается на качестве проведения эксперимента. Кроме того, проведение фитопатологических и иммунологических исследований в Казахстане лимитируется отсутствием коллекции изолятов возбудителя пирикуляриоза, не разработанностью полевых и лабораторных методик оценки болезнеустойчивости с использованием современных методов.
Материалы и методы
В качестве инфекционного материала использована смесь из казахстанских изолятов возбудителя P. oryzae, которые выделены в 2013-2014 гг. и культивированы на картофельно-декстрозном агаре. Для приготовления суспензии культуру гриба с поверхности агара соскабливали шпателем и суспензировали в стерильной воде. Полученную суспензию фильтровали и разводили водой до необходимой концентрации. Для проведения инокуляции растений были использованы Твин 80 и желатин.
Эксперименты по созданию инфекционного фона пирикуляриоза риса проводили в тепличных и лабораторных условиях. Семена риса перед закладкой опыта в течение суток замачивали в воде с добавлением регулятора роста (0,2% янтарная кислота). В последующем семена раскладывали равномерно на дно чашки Петри с увлаженной фильтровальной бумагой и ставили в термостат на 3 сут, при температуре 28-30 °С. После 3 сут проростки растений риса посадили в пластмассовые горшки, заполненные смесью почвы. Следует отметить, что почву привезли из Кызылординской области.
На основании анализа литературных данных подобраны четыре метода инокуляции растений риса возбудителем P. oryzae, которые были использованы в данной работе:
- метод опрыскивания [2, 10, 11];
- смазывания листьев суспензией гриба [12];
- инокуляция отрезки листьев каплями суспензией гриба [13];
- инокуляция отрезки листьев фильтровальной бумагой пропитанной суспензией гриба [14].
Количество спор в суспензии (на 1 см2 площади колонии) определяли с помощью камеры Горяева по формуле:

Микроскопические работы проводили с помощью цифрового микроскопа (MC 300TS, Австрия), анализ микроскопических изображений проведен по компьютерной программе Motic Images 2000-1.3. Освещенность измеряли люксметром Ю-116.
Результаты и их обсуждение
В настоящее время наиболее распространенным и широко используемым методам создания инфекционного фона пирикуляриоза риса является «Метод опрыскивания». Основные результаты и подходы использования данного метода подробно отражены в разных литературах [2, 10, 11, 15]. Кроме этого существует другие методы, один из них
«смазывания листьев суспензией гриба». Согласно, данному методу отрезки листьев (2-3 см) риса раскладывали в чашки Петри с фильтровальной бумагой смоченной водой и поверхность каждого листа смазывали суспензией конидий гриба с помощью щетки. После заражения растений создавали влажную камеру с 12-часовым режимом освещения, при температуре 28 °С. Однако заражения не произошло на изучаемых образцах риса, даже через 5-6 сут отрезки листьев полностью пожелтели и засыхали. По данным отдельных ученых, указанный метод больше подходит для заражения взрослых растений, т.е. инокуляцию необходимо проводит в период трубкования (выход в трубку) [16]. В связи с этим, мы пришли к выводу, что данный метод неэффективен для определения ювенильной устойчивости сортов риса к болезни.
При использовании метода «Инокуляция отрезки листьев каплями суспензией гриба» получено положительные результаты. Изначально отрезки листьев (2-3 см) риса раскладывали в чашки Петри с фильтровальной бумагой смоченной водой и на поверхность каждого листа микропипеткой наносили по 4-7 капелл суспензии конидий гриба с добавлением желатина. Затем чашки Петри выдерживали при непрерывном освещении лампами дневного света в течение 24 ч. при температуре 24-27°C. Первые симптомы заражения на отрезках листьев проявились уже 4-5 сут после инокуляции, с начало в виде хлоротичных пятен, затем на 6-8 сут было отмечено некротичные пятна, а на 10 сут на пораженных участках образовались конидиальная спороношения гриба P. oryzae. Чтобы поддерживать уровень влажности воздуха в период инкубации и избегание высыхание листьев риса на фильтровальную бумагу периодически добавляли стерильную воду.
На основе полученных результатов, можно считать, что метод заражения каплями конидиальной суспензии патогена имеет ряд преимуществ. Во-первых, данный метод позволяет, определит патогенность гриба в контролируемой среде, т.к. эксперименты выполняются в лабораторных боксах, и поэтому нет риска распространения гриба. А во- вторых метод экономичен во времени, не требует много растительного материала, изолята гриба, много места в лаборатории. Кроме того, использование данного метода позволяет одновременно заразить одних и тех же образцов несколькими изолятами болезни. Результаты исследований показаны на рисунке 1.

Дальше проводили опыты с использованием другого метода «инокуляция отрезки листьев фильтровальной бумагой, пропитанной конидиальной суспензией гриба». При этом отрезки листьев (2-3 см) раскладывали в чашки Петри на поверхность 0,5% агара, приготовленного на 0,004% растворе бензимидазола. На поверхность каждого листа прикладывали фильтровальные бумаги, пропитанные суспензией гриба. Чашки Петри с инокулированными отрезками листьев помещали в затемненное место на 24-36 ч при температуре 25 °С, затем переносили на светоустановку с 12-часовым режимом освещения и температурой 22-25 °С и удаляли фильтровальные бумаги с поверхности каждого листа. В результате на инфицированных отрезках листьев через 4-5 сут проявлялись хлоротичные пятна, а на 6-8 сут – некротичные пятна. Как видно из данных рисунка 2, что на 10 сут на пораженных участках образовались конидиальная спороношения гриба P. оryzae, а отрезки листьев растений оставались зелеными. Этот метод является более удобным и воспроизводимым лабораторным методом из-за использования светоустановок и бензимидазола. Одна из важнейших свойств последнего – сохранять жизнеспособность изолированных листьев в течение 2-3 недель без изменения иммунологических свойств растений.

Результаты лабораторных экспериментов показали, что конидии пирикуляриоза риса можно поместить на растения разными способами. При этом дана характеристика к четырем методам заражения сортов риса возбудителем P. oryzae (суммировано в таблице 1).
Таблица 1 – Основные параметры методов заражения риса возбудителем P. Oryzae
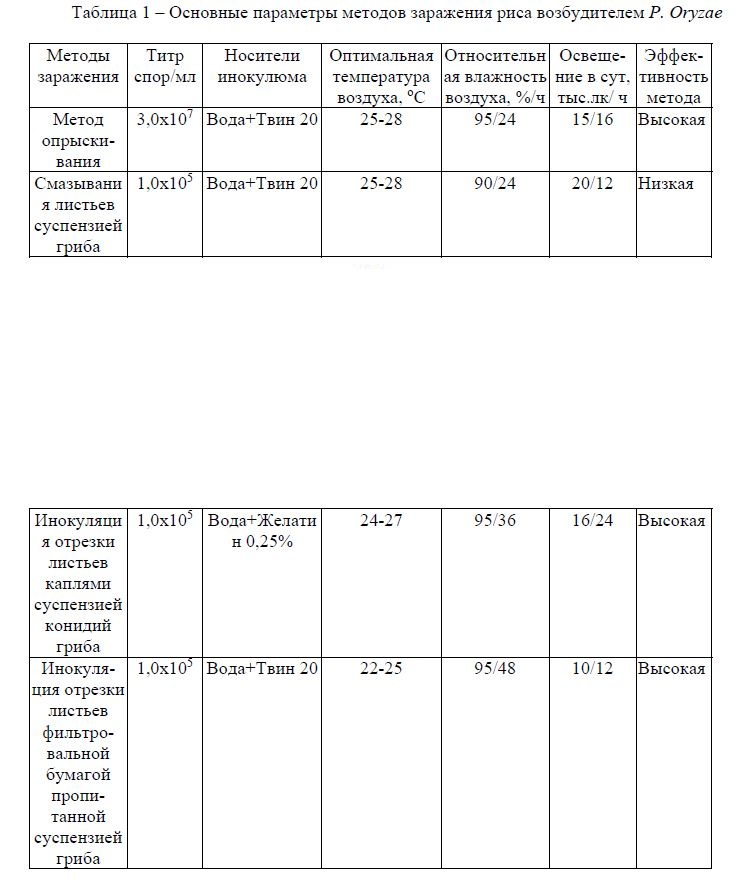
Как видно из данных таблицы 1, что почти все применяемых методов можно использовать с водным носителем. Чтобы сохранить конидии в суспензии, необходимо добавит нефитотоксичный смачивающий агент, такой как Tвин 20 и желатин, а так же для заражения может быть использован опрыскиватель, щетка, фильтровальная бумага, шприц или микропипетка. Установлено, что процесс инфицирования проростков риса возбудителем P. oryzae происходит в интервале температур 22-28 оС с удлинением влажного периода до 48 ч. По литературным данным [12] наиболее благоприятной можно считать температуру, близкую к 26 оС, при которой первые признаки заражения проявляются уже после 4 сут заражения. Чем больше температура воздуха отклоняется от оптимальной (26 оС) в ту или иную сторону, тем требуется больший период увлажнения для инфицирования и проявления признаков пирикуляриоза на растениях.
Следует отметить, что для освещения растений мы использовали световую установку, состоящую из ртутно-дуговых люминесцентных ламп высокого давления (ДРЛ-2000), следовательно, в опытах освещенность была в пределах 10-20 тыс. люкс. При использовании отдельных методов затраты времени и труда значительны, но риск контаминации минимален и в научном плане высокоэффективен. В любом случае выбранный метод зависит от цели инокуляции, количества инокулируемых растений, количества пригодного инокулюма и материально-технической возможности экспериментатора.
Таким образом, на основе анализа проведенных исследований установлено, что наиболее эффективными лабораторными методами создания инфекционного фона пирикуляриоза риса является инокуляция отрезки листьев растений фильтровальной бумагой, пропитанной конидиальной суспензией гриба и инокуляция отрезки листьев растений каплями конидиальной суспензии патогена. Кроме этого, «Метод опрыскивания» остается один из эффективных методов инокуляции растений возбудителем P. oryzae. Методика «смазывания листьев суспензией гриба» неэффективен для определения ювенильной устойчивости сортов риса к пирикуляриозу.
Работа выполнена в рамках программы грантового финансирования Республики Казахстан на 2013-2015 гг. (грант №2495/ГФЗ).
Литература
- Мухина Ж.М., Волкова С.А., Дубина Е.В. Изучение биоразнообразия фитопатогенного гриба Magnoporthe grisea (Herbert) Barr с использованием методов молекулярного маркирования (Методические рекомендации). – Краснодар: ВНИИ риса. – 19 с.
- Пересыпкин В.Ф. Сельскохозяйственная фитопатология. – Москва: Агропромиздат, 1989. – 479 с.
- Дьяков Ю.Т., Озерецковская О.Л., Джавахия В.Г. Общая и молекулярная фитопатология: Учеб. пособие. – Москва: Общество фитопатологов. – 2001. – 302 с.
- Jena K., Moon H.P., Mackill D.J. Marker assisted selection- a new paradigm in plant breeding // Korean J. Breed. 2003. – Vol.35. – P. 133-140.
- Dean , Van Kan J.A., Pretorius Z.A., Hammond-Kosack K.E., Di Pietro A., Spanu P.D., Rudd J.J., Dickman M., Kahmann R., Ellis J., Foster G.D. The Top 10 fungal pathogens in molecular plant pathology. // Mol. Plant Pathol. 2012. – Vol. 13. – P.804-804.
- Мусаев Ф.А., Захарова О.А., Морозова Н.И. Класс несовершенные грибы (Учебное пособие). – Рязань: Издательство РГАТУ. 2014. – 135 с.
- Гешеле Э.Э. Методические руководство по фитопатологической оценке зерновых культур. – Одесса. – 178 с.
- Санин С.С., Неклеса Н.П., Санина А.А., Пахолкова Е.В. Методические рекомендации по созданию инфекционных фонов для иммоногенетических исследования пшеницы. – Москва, 2008. – С.5-7.
- Чекалин Н.М. Генетические основы селекции зернобобовых культур на устойчивость к патогенам. – Полтава: «Iнтерграфiка», 2003. – 186 с.
- Bonman M., Vergel De Dios T.I., Khin M.M. Physiologic Specialization of Pyricularia oryzae in the Philippines // Plant Disease. – 1986. – Vol. 70 – 767-769.
- Marta Cristina Filippi, Anne Sitarama Prabhu. Phenotypic virulence analysis of Pyricularia grisea isolates from Brazilian upland rice cultivars // Pesq. agropec. bras., Brasília. – 2001. – Vol. 36. – No.1. – P. 27-35.
- Кирай З., Клемент З., Шоймоши Ф., Вереш И. Методы фитопатологии. – Москва: Колос, 1974. – С.292-295.
- Jia Y., Valent B., Lee F.N. Determination of Host Responses to Magnaporthe grisea on Detached Rice Leaves Using a Spot Inoculation Method // Plant Dis. – 2003. – Vol.87. – No.2. – P.129-133
- Takahashi W., Miura Y., Sasaki T. A novel inoculation method for evaluation of grey leaf spot resistance in Italian ryegrass // Journal of Plant Pathology. – 2009. – Vol.91. – No.1. – P.171-176.
- Рсалиев А.С., Рсалиев Ш.С., Агабаева А.Ч. Устойчивость сортов риса к пирикуляриозу в Казахстане. // Материалы международной научно-практической конференции «Современные научные достижения». – Чехия: Прага, Education and Science. – С.96-99.
- Wang Jiao-yu, Wang Xiao-yan, Li Ling, Zhang Xin, Wang Yan-li, Chai Rong-yao, Sun Guo-chang. Pathogenicity of Rice Blast Fungus Magnaporthe oryzae on Brachypodium distachyon China // Rice Science. – 2012. – Vol.19. – No.3. – 252−258.