В последнее время непрерывное развитие различных биогазовых технологий привело к необходимости усовершенствования конструкций биореакторов для увеличения выхода метана из расширяющихся ассортиментов сырья. Очевидным способом повышения производительности реакторов и снижения ВГУ является увеличение плотности, т.е. иммобилизация микроорганизмов.
Введение
Проведение исследований по оптимизации получения биогаза путем анаэробного сбраживания отходов производства поможет решить проблемы управления бытовыми и промышленными отходами в свете приоритетных направлений в Концепции экологической безопасности Республики Казахстан [1, 2]. Это позволит обеспечить экологическую безопасность и устойчивое развитие страны, и то, что по привычке на- зывается отходами, при разумном использовании способно дать значительную прибыль и освободить занимаемые свалками земли. Приоритет утилизации отходов над их ликвидацией очевиден, и исследования в области повторного использования отходов перспективны и актуальны.
Материалы и методы
Известно, что применение анаэробного метода при переработке отходов животноводства имеет существенный эффект по сравнению со многими другими методами, что выражается в значительном снижении загрязнения почвы, воды, воздуха химическими веществами и патогенной микрофлорой. Эффективность анаэробного процесса в существенной мере зависит от правильной подготовки сырья к переработке и от конструкции биореактора.
Большое значение для повышения эффективности работы биореакторов имеет использование методов иммобилизации микроорганизмов с тем, чтобы повысить выход биогаза при анаэробной переработке отходов. Основная задача таких биореакторов - интенсификация теплообмена и гомогенизация ферментационной среды, что способствует ускорению метаногенеза за счет закрепления метаногенной микрофлоры в аппарате. Поэтому в данной работе проводились исследования по изучению условий культивирования метанобразующих бактерий, а также различных полимерных композиций для обоснования их применения в качестве носителей для иммобилизации микроорганизмов, кроме того возможность использования отходов производства биогаза в виде биоудобрений.
Метанобразующие бактерии — строгие анаэробы и имеют температурный оптимум для роста в области 30–40°, поэтому в данной научной работе используется температурный предел 30-500С, оптимальный pH в области 6,5–7,5 [3, 4].
В настоящей работе для получения микробной суспензии использовали около 10 г предварительно измельченного образца. Навеску образца переносили в колбу емкостью 250 мл с 90 мл стерильной водопроводной воды, взбалтывали в течение 10 минут на механической качалке и давали отстояться грубым частицам. Затем методом разведения готовили суспензии, содержащие разные количества отходов. Одновременно из пробы отбирали 20 г отходов для определения влажности, и проводили пересчет на 1 г абсолютно сухих отходов. Из полученных разведений проводили посевы микроорганизмов на плотные питательные элективные среды [3].
Питательная среда для метанобразующих бактерий включала основные растворы солей калия гидрофосфата, хлоридов калия, магния, кальция, натрия ацетата, дрожжи, витамины В1, В2, В6, В12 , С, РР, агар-агар. На питательную среду было помещёно небольшое количество разведённого дистиллированной водой навоза, в составе которого находились метаногенные бактерии. Колбу с питательной средой плотно закрыть пробкой, создав анаэробные условия и поместить в термостат при температуре 30°С на 2 недели. По истечению срока на питательной среде можно обнаружить колонии бактерий, природу которых проверяют окраской по Грамму [5].
Так как состав перерабатываемых отходов определяет течение метанового брожения, в настоящей работе анализу были подвергнуты различные смеси отходов, такие как птичий помет, коровий навоз, свиной навоз, а также соломы и травы, с целью выбора оптимальных вариантов прохождения процесса сбраживания, при этом были проведены расчет выхода биогаза с предварительным определением влажности сырья [4].

Таким образом, по результатам исследований наибольший выход биогаза наблюдался при использовании птичьего помета с влажностью 80% в качестве субстрата для экспериментов.
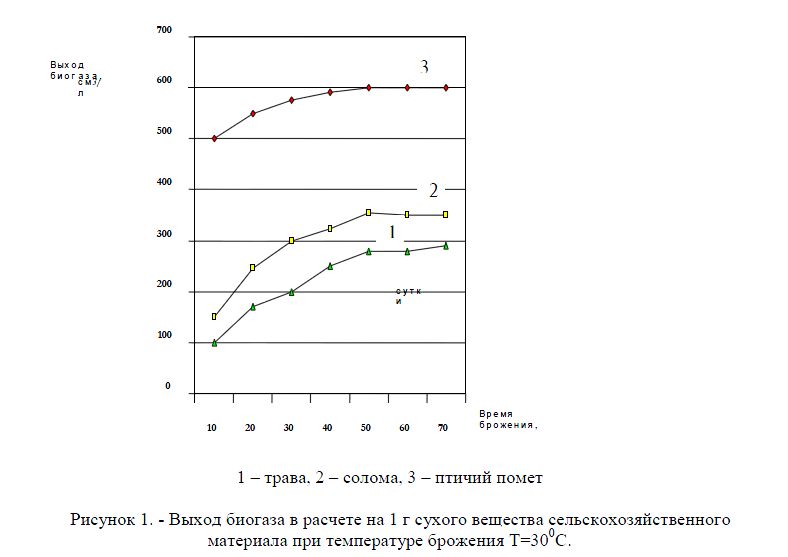
Рисунок 1. - Выход биогаза в расчете на 1 г сухого вещества сельскохозяйственного материала при температуре брожения T=300C.
С целью выделения из окружающей природной среды биоценоза метанобразующих бактерий были взяты навоз в количестве 50 г, которые были загружены в конические колбы емкостью 200 мл. Контролировали объем выделившегося газа. Газ - метан свидетельствовал об интенсивности процесса метанового брожения и, следовательно, о накоплении смешанной культуры метанобразующих бактерий. Полученные данные приведены на рисунках 2 и 3, из них видно, что выход газа увеличивается при использовании иммобилизованной культуры метанобразующих бактерий.
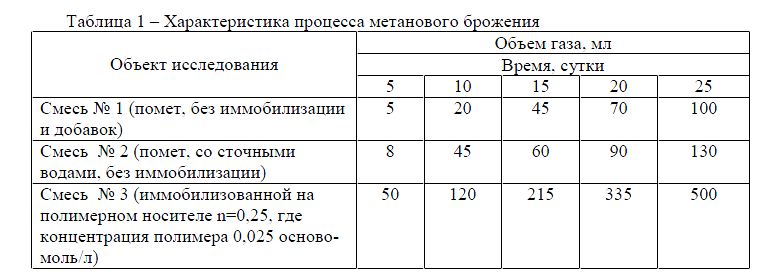
Таким образом, был проконтролирован объем выделившегося газа, которые свидетельствуют об интенсификации процесса метанового брожения и соответственно, о накоплении смешанной культуры метанобразующих бактерий. Результаты представлены в таблице 1.
Таблица 1 – Характеристика процесса метанового брожения
На рисунке 2 показана кинетика микробиологических процессов при созревании метанового биоценоза, происходящих в реакционной смеси без иммобилизации. Из полученных данных видно, что газ – метан, свидетельствующий о начале третьей, метанобразующей фазы начинает интенсивно образовываться на 14 – 16 сутки от начала процесса, а на 22 – 24 сутки наступает торможение процесса.
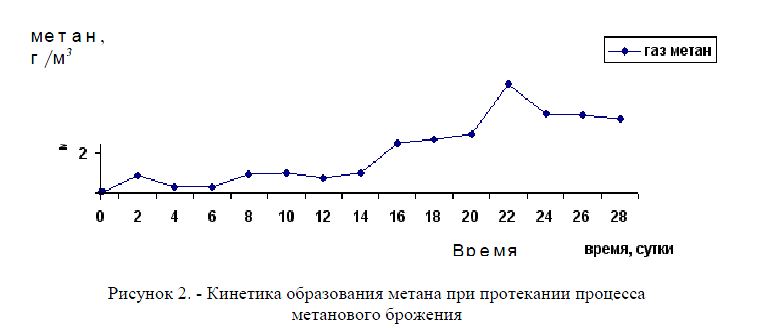
Рисунок 2. - Кинетика образования метана при протекании процесса метанового брожения
В процессе анаэробного сбраживания снижается количество метанобразующих бактерий. Как показано в работе [6], причиной, тормозящей процесс, является образование кислых продуктов бактериального гидролиза. Экспериментальные данные по измерению рН среды подтверждают это предположение. В ходе созревания метанового биоценоза рН изменилось от 7,5 в начале процесса до 5,7 в конце (Рисунок 3). Таким образом, рН среды в ферментере является чувствительным параметром, используемым для определения стабильности брожения.
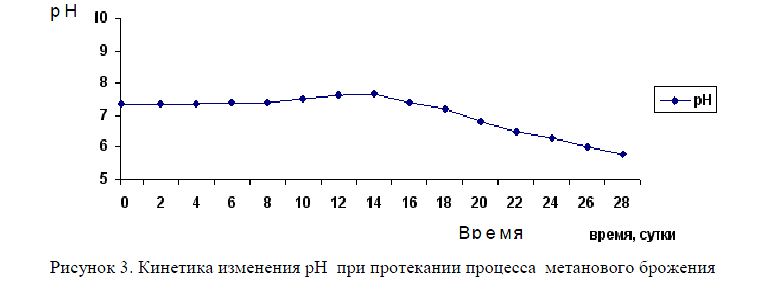
Рисунок 3. Кинетика изменения рН при протекании процесса метанового брожения
Адсорбционные методы иммобилизации относятся к числу наиболее простых и "естественных". В природе почти всегда микроорганизмы и их ассоциаты существуют не в изолированной (свободной) форме, а в адсорбированном состоянии. Примером этому являются микробные популяции почвы, кишечника, рубца, некоторые азотфиксирующие микроорганизмы растений и т.д.В случае адсорбционной иммобилизации используется естественная способность многих микроорганизмов закрепляться на разнообразных твердых или гелеобразных носителях и продолжать свою жизнедеятельность в таком обездвиженном состоянии. [7].
Разнообразие свойств поверхности клеток и адсорбентов обусловливает различные механизмы адсорбционного взаимодействия и различные виды сил адгезии. Адгезия клеток на адсорбенте определяется следующими причинами:
- Образование химических связей между поверхностями клетки и адсорбента (хемосорбция);
- Ион - ионные взаимодействия, образование ионных пар и триплетов, например, NH3+.. .~ —ООС— и —СОО—~... Са2+ ... ~ —ООС—;
- Электростатические (неионные) взаимодействия заряженных поверхностей клеток и адсорбента;
- Силы Ван-дер-Ваальса (взаимодействие диполь—диполь, диполь—наведенный диполь, ион — диполь);
- Влияние электролитов, гидратационных эффектов, капиллярных свойств;
- Флокуляция и коагуляция;
- Гидрофобное взаимодействие;
При адсорбционной иммобилизации клеток, которая обусловлена электростатическими силами, одновременно реализуется несколько типов адгезионного взаимодействия, поэтому трудно выделить роль каждого из них по отдельности. Наибольшее влияние на связывание микроорганизма с носителем оказывают ковалентные и ионные взаимодействия [7].
Выводы
Полимерные композиции на основе производных полакрилонитрила вызывают интерес тем, что поверхность полимера является заряженной, что предполагает взаимодействие между поверхностью полимерного носителя и поверхностью микроорганизмов
Литература
- Новый Казахстан в новом мире//Казахстанская Правда от 2 марта 2007 г. – С. 2-3
- Концепция экологической безопасности республики Казахстан на 2004-2005 годы // Казахстанская правда от 10.12.2003. – С. 7-8.
- Michael J. Franklin, William J. Wiebe, and William B. Whitman. 1988. Populations of Methanogenic Bacteria in Georgia Salt Marsh. Appl. Environ. Microbiol. 54:1151-1157.
- Deublein D. Steinhauser A. Biogas from Waste and Renewable Resources. - Wiley, 2008, isbn: 3527318410, 472 р.
- Bergey David H. Bergey's Manual of Determinative Bacteriology. — 9th ed.. — Lippincott Williams & Wilkins,
- Панцхава Е.С., Давиденко Е.В. Метангенерация твердых органических отходов городов // Биотехнология, 1990, № 4. - С. 49 -52.
- Alatriste-Mondragon, F., Samar, P., Cox, H.H.J., Ahring, B.K., Iranpour, R., Anaerobic codigestion of municipal, farm, and industrial organic wastes: A survey of recent literature. Water Environment Research, 78, 607-636.