Анализ статистических данных за последние годы свидетельствует о нарастании заболеваемости населения различными формами онкопатологии. Среди причин смертности онкологические заболевания вышли на второе место после сердечно-сосудистой патологии. Снижение заболеваемости и смертности от злокачественных новообразований онкологи связывают с широким внедрением профилактических мер и ранней диагностикой.
Рак молочной железы (РМЖ) является одним из центральных вопросов современной клинической онкологии. Из диагностических методов при РМЖ наиболее широкое применение, помимо клинического обследования, нашли маммография, ультразвуковое исследование, цитологическое исследование пунктатов. Как показывает практика, применяемые на сегодня скрининговые программы (осмотр, самообследование, маммография и т.п.) не полностью отвечают поставленным задачам в связи с тем, что чувствительность этих методов не превышает 65 % [1–3].
Клиническая цитология — иммуноцитохимия (ИЦХ) — изучает клеточный состав патологических процессов. Объектом цитологического исследования служат пунктаты опухолевидных образований, пунктаты регионарных лимфатических узлов, выделения из соска, соскобы с эрозированных и язвенных поверхностей соска и кожи, содержимое кистозных полостей, отпечатки и соскобы опухоли и лимфатических узлов при интраоперационной диагностике. Критерии цитологической диагностики злокачественных новообразований основываются прежде всего на морфологии клетки, особенно ядра, изменениях клеточного состава в норме и при патологии, оценке не одной отдельно взятой клетки, а совокупности клеток. Пункционная биопсия более простая, малотравматичная процедура, практически не сопровождающаяся осложнениями, позволяющая получить достаточное количество клеточного материала для цитологического исследования. Иммуноцитохимия не требует больших временных затрат, выполняется быстро, в течение 2–3-х ч. Замечено, что мембранные и цитоплазматические маркеры чаще положительно окрашиваются в цитологических, чем в гистологических препаратах. Возможно, это связано с более щадящей обработкой цитопрепаратов, отсутствием потери и маскировки антигенов при проводке и депарафинизации материала с использованием агрессивных химических реагентов, что негативно сказывается на мембранных и цитоплазматических рецепторах. Однако возможности ИЦХ-метода ограничиваются плохим качеством мазков или малым количеством клеток в цитопрепаратах [3–5].
Существенный вклад в решение вышеупомянутых проблем может внести внедрение иммунологических методов исследования в лабораторную практику. Целью иммунологической онкодиагностики является разработка надежных тестов ин витро, позволяющих обнаружить опухоль до развития клинических симптомов и определить ее локализацию. Такие тесты необходимы при ранней и дифференциальной клинической диагностике. Именно с помощью стандартных унифицированных иммунологических методов можно проводить массовый скрининг и выявить группы повышенного риска. За последние годы в мире достигнут значительный прогресс в клиническом использовании различных биологических маркеров. В их числе онкогены, рецепторы эстрогенов (РЭ) и прогестерона (РП), маркеры апоптоза, рецепторы факторов роста и т.д. Все эти показатели позволяют более детально изучить молекулярно-биологические особенности злокачественных опухолей, ассоциируются со степенью дифференцировки, способностью к инвазии и метастазированию, чувствительностью к химиотерапии, а следовательно, с особенностями течения и прогнозом заболевания в каждом конкретном случае. В настоящее время описано много различных монои поликлональных антител, выявляющих экспрессию тех или иных белков, связанных со структурными компонентами клетки, продуктами клеточного синтеза (гормонов, ферментов, иммуноглобулинов), рецепторами и т.д. [4–9].
В последнее десятилетие благодаря успехам иммунохимии в лабораторную практику медицинских учреждений прочно вошли методы иммуноанализа, позволяющие определять специфические белки, синтезируемые опухолями различного типа, так называемые опухолевые маркёры. Согласно определению Я.В.Бохмана, «опухолевый маркёр» — это любая белковая субстанция, которая появляется у онкологического больного и коррелирует с наличием опухоли, степенью ее распространенности и регрессией в результате лечения. Опухолевые маркёры применяются для раннего выявления рецидивов и метастазов злокачественных новообразований. Как правило, начало повышения концентрации опухолевого маркёра в крови на несколько месяцев опережает клиническое проявление рецидива и метастазов опухоли. Мониторинг опухолевых маркёров используется также для контроля за эффективностью радиои химиотерапии опухолей. Злокачественная опухоль должна вырасти до определенного минимального размера (так называемой критической массы), чтобы «наработать» количество опухолевого маркёра, достаточное для определения современными методами анализа. Установлено, что опухолевая клетка способна выделять 1 пикограмм (10-12 г) опухолевого маркёра в кровь. Таким образом, опухоль размером 1 см3 может выделить в кровь 1 мг антигена, что в пересчете на концентрацию составляет около 200 нг/мл. Даже допустив, что в силу разных причин реальная концентрация опухолевого маркёра будет в 10 раз ниже, чувствительность современных радиоиммунных и иммуноферментных тест-систем вполне достаточна для выявления превышения установленного порогового уровня маркёра [6–12].
Иммуноферментный анализ является одним из современных иммунологических методов, широко применяемых в иммунодиагностике вирусных и бактериальных инфекций в медицине и ветеринарии. В отличие от классических методов диагностики иммуноферментный анализ — это эффективный подход, совмещающий в себе специфичность иммунологической реакции и чувствительность химической реакции, высокую стабильность применяемых реагентов и простоту детекции ферментной метки. В патентной и научной литературе появляется все больше сведений о рекордных пределах обнаружения веществ данным методом (вплоть до 10-21 молей в образце). Широкое применение твердофазного ИФА, основанного на использовании планшетов из непористых полимерных материалов — полистирола, поливинилхлорида и т.д., обусловлено его простотой и возможностью автоматизации за счет того, что каждая лунка планшета является отдельным реактором, в котором происходят все стадии анализа, начиная с иммобилизации и заканчивая измерением физико-химического параметра ферментативной реакции [13,14].
При разработке иммуноферментных тест-систем актуальным является правильный подбор параметров применения компонентов набора, от которых в большей степени зависит качество получаемых результатов. Все варианты ИФА являются многокомпонентными системами и несоответствие одного параметра может приводить к неадекватным результатам. Целью исследований являлось определение оптимальных параметров адсорбции и фиксации клеточной суспензии опухолевых клеток для проведения иммуноферментного анализа.
Материалы и методы
Культивируемые линии аденокарциномы молочной железы MCF-7 и карциномы молочной железы ZR-75 получены из Российской коллекции клеточных культур (Институт Цитологии, г.СанктПетербург). Клетки культивировали при температуре 37 °С в атмосфере 5 % СО2 на питательной среде ДМЕМ («HiMedia», Индия) с добавлением 50 мкг/мл гентамицина и 10 % фетальной сыворотки крупного рогатого скота. Для снятия монослоя клеток использовали 0,25 %-й раствор трипсина и 0,02 %-й раствор версена («HiMedia», Индия). Подсчет клеток и морфологический анализ культур проводили при помощи инвертированного микроскопа. Концентрацию клеток в суспензии, а также число жизнеспособных клеток подсчитывали в камере Горяева с применением 0,4 %-го раствора трипановой сини.
Для постановки иммуноферментного анализа иммунологические полистироловые планшеты иммобилизовывали интактными клетками опухолевых клеток в испытуемых концентрациях в питательной среде DMEM (HiMedia, Индия) при продолжительности инкубации 24 часа в СО2инкубаторе при температуре 37 °С.После инкубации планшеты отмывали три раза ЗФР рН 7,2 с 0,05 %-м твин-20 и три раза — ЗФР без твина. Блокировку свободной поверхности лунок проводили 0,5 %-м раствором бычьего сывороточного альбумина при 37°С в течение 1 часа. После отмывки вносили испытуемые сыворотки иммунных мышей, начиная с разведения 1:100, в объеме 0,1 мл и инкубировали при 37 0С в течение 60 минут. Отрицательным контролем в данном случае служили образцы сыворотки крови здоровых мышей (негативная сыворотка). После инкубирования планшет отмывали для удаления неспецифически связавшихся антител. Затем в лунки планшет вносили кроличьи антитела к иммуноглобулинам мыши, меченые пероксидазой хрена (антивидовой конъюгат — Sigma, Германия) в объеме 0,1 мл и инкубировали в течение 1 часа. Для проявления реакции в лунки вносили по 0,1 мл раствора субстрата фермента, который готовили путем растворения 0,01 г ортофенилендиамина (Sigma, США) в 10 мл 1 %-го раствора лимонной кислоты с рН 4,5 и добавления 0,005 мл 30 %-й перекиси водорода. Реакцию останавливали добавлением в лунки планшет раствора 2М серной кислоты. Результаты ИФА учитывали с помощью спектрофотометра с вертикальным потоком света при длине волны 492 нм.
Для получения позитивных сывороток 2 группы мышей (по 3 мыши в каждой) были иммунизированы интактными клетками аденокарциномы молочной железы MCF-7 и карциномы молочной железы ZR-75 по следующей схеме: в первый день иммунизации вводили внутрибрюшинно 10 млн. клеток в 0,1 мл полного адъюванта Фрейнда (ПАФ). На 7,11,12,13 дни иммунизации мышам повторно вводили внутрибрюшинно аналогичное количество опухолевых клеток в забуференном физиологическом растворе (ЗФР).
Результаты исследований
Эффективность проведения микроанализа методом ИФА существенно зависит от формирования слоя иммобилизованного антигена путем адсорбции на поверхности пластика. Многие макромолекулярные антигены — белки, ферменты, липополисахариды, целые вирусные частицы, компоненты клеток и целые клетки — могут быть связаны с поверхностью полимерных носителей путем адсорбции. Длительность процесса адсорбции и максимальное количество связанного с поверхностью антигена являются характеристиками, индивидуальными для каждого процесса и зависящими от гидрофобности, заряда и молекулярной массы молекулы антигена. Степень адсорбции также зависит от физико-химических свойств молекул, от концентрации молекул в растворе, от отношения площади связывания к объему внесенного образца, а также от температуры и времени инкубации [13,14].
На начальном этапе исследований нами предусматривалась отработка оптимальных условий рассева клеточной суспензии опухолевых клеток для постановки непрямого варианта иммуноферментного анализа (ИФА). Для сенсибилизации твердой фазы использовали опухолевые клетки культивируемых линии аденокарциномы молочной железы MCF-7 и карциномы молочной железы ZR-75. Культура клеток аденокарциномы молочной железы MCF-7 представлена эпителиоподобными клетками полигональной формы с четкими, хорошо выраженными границами и округлыми ядрами, которые растут колониями, равномерно распределяясь по всей культуральной поверхности матрасов. В последующих пассажах пролиферативная активность опухолевых клеток возрастает, культура становится морфологически однородной. Пересев культур проводили по мере формирования монослоя. Монослой при пассажах формировался на 3–5-е сутки. Из матрасов с выросшим монослоем (90–95 % поверхности) удаляли питательную среду, вносили в них подогретую до 37 °С смесь раствора версена (0,02 %) и трипсина (0,25 %) в соотношении 1:1 в количестве, необходимом чтобы покрыть весь клеточный монослой. Матрасы помещали в термостат на 3–5 минут для отделения клеток от поверхности. Клеточную взвесь тщательно пипетировали до образования однородной массы и добавляли свежую ростовую среду. Коэффициент пересева составлял 1:2 – 1:3, т.е. клетки, снятые с одного матраса, рассеивали на 2–3 аналогичных матраса. Оптимальная плотность пересева составляла 2,0–4,0х104 клеток/см2.
В качестве позитивных сывороток использовали сыворотки мышей, иммунизированных интактными клетками линии MCF-7 и ZR-75–1 по 15-дневной схеме иммунизации (в дозе 10 млн. клеток на одну инъекцию). Отрицательным контролем (негативная сыворотка) служили сыворотки здоровых мышей.
Выбор оптимальной плотности насыщения поверхности носителя клеточной суспензией опухолевых клеток проводили в диапазоне от 10 до 100 тыс. клеток/мл при продолжительности инкубации 24 часа в СО2-инкубаторе при температуре 37 °С (табл.1).
Т а б л и ц а 1
Выбор оптимальной плотности насыщения опухолевыми клетками поверхности твердого носителя
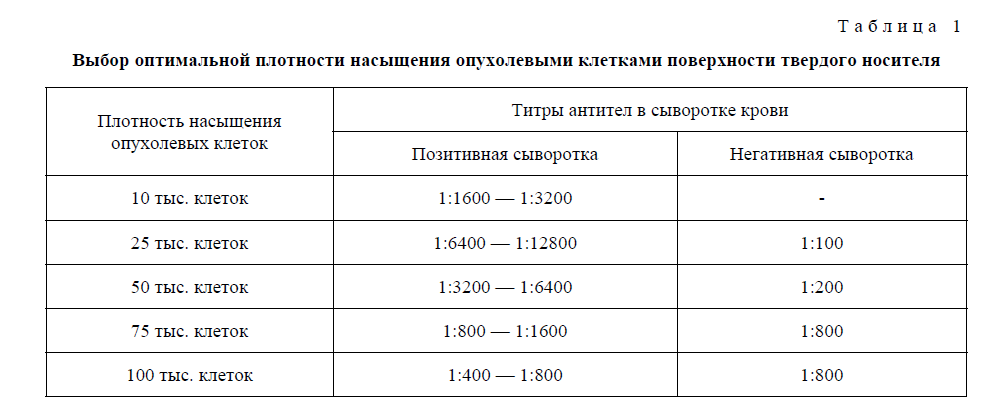
Анализ полученных результатов свидетельствует, что при всех использованных концентрациях опухолевые клетки по-разному сорбируются на носителях. Установлено, что оптимальной концентрацией клеточной суспензии опухолевых клеток, обеспечивающих достаточную чувствительность непрямого ИФА является 20–25 тыс.клеток/мл, при которой максимальные титры специфических антител в позитивных сыворотках достигали значении 1:6400 — 1:12800. При использовании растворов с более высоким содержанием интактных клеток на единицу поверхности носителя эффективность адсорбции снижается, что выражается в ослаблении титров позитивных сывороток и превышении «фонового сигнала» негативной сывороткой, обусловленного артефактным обнаружением иммуноглобулинов, не обладающих специфичностью к данному антигену. Наблюдаемое при этом ослабление прочности связывания, объясняется, вероятно, своего рода «наслаиванием» избыточного количества интактных клеток на поверхность носителя, при котором в дальнейшем происходит существенное вымывание антигена [10, 12–14].
Таким образом, при оптимальной концентрации 20–25 тыс.клеток/мл происходит равномерное распределение антигена по поверхности и почти полное предотвращение его вымывания с поверхности носителя.
Одним из существенных факторов, оказывающих влияние на адсорбцию клеточной суспензии опухолевых клеток к поверхности твердой фазы, является эффективность растворов для фиксации клеток, в качестве которых нами были использованы 1 %-й формалин, 70 %-й этанол и 100 %-й ацетон (табл. 2).
Сенсибилизацию твердой фазы цельными бактериальными клетками осуществляют обычной адсорбцией, однако эукариотическим клеткам с целью укрепления ковалентной связи с носителем необходима дополнительная фиксация. Выбор метода фиксации определяется спецификой конкретной реакции антиген-антитело и предполагаемой локализацией антигена, но при этом антигенные детерминанты их молекул должны более или менее сохранять свою пространственную структуру и быть доступными антителам. При использовании клеточного слоя как нерастворимого антигена целью фиксации является сохранение клетки, прекращение активности внутриклеточных ферментов, предотвращение распада клеточных компонентов. Формалин хорошо связывается с белками, сшивая их с помощью метильных мостиков и тем самым вызывая денатурацию. Ацетон обезвоживает коллоиды цитоплазмы и приводит к осаждению белков, что не дает глубоких изменений в структуре белка. Однако ацетон, так же как и формалин, приводит к необратимой потере активности мембранных и цитоплазматических рецепторов клеток. Фиксирующее действие спиртов связано с осаждением белков. Спирты могут нарушать сольватные оболочки входящих в белки групп, «уплотнять молекулы» и вызывать появление новых конфигураций функциональных групп в белковой молекуле. Фиксация белков спиртами в ряде случаев обратима [3–5, 13, 14].
Эффективность растворов для фиксации опухолевых клеток
Т а б л и ц а 2
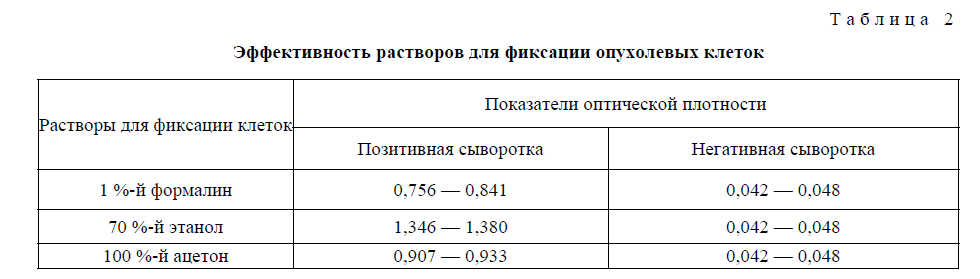
Результаты опытов показали, что фиксация опухолевых клеток была минимальной при использовании 1 %-го формалина и 100 %-го ацетона. Применение 70 %-го этанола приводило к существенному увеличению адсорбции опухолевых клеток поверхностью твердой фазы. При этом значения экстинкции достигали соответственно 0,756–0,841, 0,907–0,933 и 1,346–1,387 о.е. Данный показатель при использовании негативной контрольной сыворотки был в пределах 0,042–0,048.
Используемые в ИФА носители должны соответствовать ряду требований, обусловленных спецификой метода: 1) быть нерастворимыми при условиях, в которых проводится анализ, 2) обладать достаточной для аналитических целей емкостью (т.е. количеством иммобилизованного белка на единицу массы или площади поверхности носителя), 3) обеспечивать прочное необратимое связывание белка с носителем и стабильность препарата при хранении, 4) обладать минимальной способностью к неспецифическому связыванию компонентов, находящихся в анализируемых биологических жидкостях, 5) быть удобным для анализа в методическом плане, т.е. легко и точно дозироваться, быстро осаждаться, без потерь подвергаться процедурам промывки и т.д. [3–6].
Сравнительная оценка интенсивности связывания опухолевых клеток в лунках полистироловых планшетов разных фирм
Т а б л и ц а 3
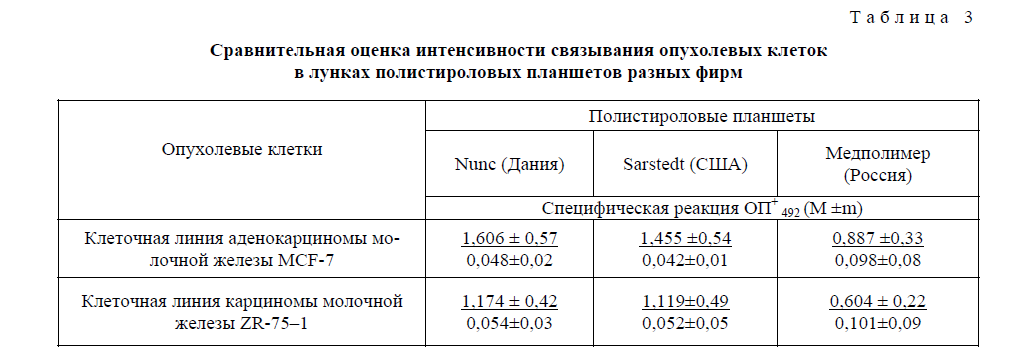
Примечание. В числителе — средние значения оптической плотности (492 нм) позитивной сыворотки при разведении 1:100; в знаменателе — средние значения оптической плотности (492 нм) негативной сыворотки при разведении 1:100.
При изучении сорбционных свойств твердой фазы для постановки непрямого ИФА были испытаны 96-луночные полистироловые планшеты для культивирования фирм «Nunc» (Дания),«Sarstedt» (США) и «Медполимер» (Россия), которые отличаются составом и сорбционными свойствами полимера. Средние значения оптической плотности (ОП+ 492) реакционной жидкости лунок с адсорбированными опухолевыми клетками, в которых вносились образцы позитивной и негативной сывороток, представлены в таблице 3.
В результате установлено, что наиболее высокими сорбционными свойствами для сенсибилизации клеточной суспензией опухолевых клеток обладали полистироловые носители фирм «Nunc» (Дания) и «Sarstedt» (США), что сопровождалось их высокой аналитической емкостью (2000–2500 опухолевых клеток на лунку) и минимальной способностью к неспецифическому связыванию (наибольшая оптическая плотность была выше фоновой примерно в 10–15 раз).
Таким образом, проведенные нами исследования по изучению сорбционных свойств полистироловых планшетов для сенсибилизации клеточной суспензией опухолевых клеток в ИФА, а также определение оптимальной плотности насыщения поверхности носителя и эффективности растворов для фиксации опухолевых клеток позволили оптимизировать условия рассева и фиксации клеточной суспензии опухолевых клеток для постановки непрямого варианта иммуноферментного анализа (ИФА).
Список литературы
- Цешковский М.С. Раннее выявление рака молочной железы // Вопросы онкологии. — — Т. 29. — № 1. — С. 68–79.
- Канцерогенез / Под ред. Д.Г.Заридзе. — М.: Медицина, 2004. — 576 с.
- Ермилова В.Д. Роль современной патоморфологии в характеристике рака молочной железы // Практ. онкология. — 2002. — Т. 3. — № 1. — С. 15–20.
- Иммунологические методы / Под ред. Г.Фримеля. — М.: Медицина, 1987. — 420 с.
- Лефковитс И., Пернис Б. Иммунология: методы исследовании. — М.: Мир, 1983. — 349 с.
- Петров Р.В. Иммунология / Под ред. И.А.Кондратьевой, В.Д.Самуилова. — М.: Изд-во МГУ, 2001. — 350 с.
- Хаитов Р.М., Игнатьева Г.А., Сидорович И.Г. Иммунология. — М.: Медицина, 2000. — 275с.
- Klug L., Bast R.C., Niloff Y.M. Monoclonal antibody: immunonassay for an antigenic determinant. — Cancer Rec. — 1984. — V. 44. — Р. 1048–1053.
- Lioyd O. Human tumor antigens: Detection and characterization with monoclonal antibodies. In: Basis and clinical Tumor immunology. R.B.Herberman{ed}. Boston. — 1983. — Р.159–214.
- Таранов А.Г. Лабораторная диагностика опухолевых заболеваний (радиоиммунный и иммуноферментный методы анализа) // Новосибирск: Наука. — 1995. — С.
- Абелев Г.И. Принципы иммунодиагностики опухолей // Иммунология. — 1982. — № 4. — С. 5–12.
- Зорин Н.А. Новые подходы к диагностике онкозаболеваний // Новости «Вектор-Бест». — 1997. — № 2. — С. 43–49.
- Иммуноферментный анализ / Под ред. Т.Нго, Г.Ленхоффа. — М.: Мир. — 1988. — 286 с.
- Егоров А.М., Осипов А.П., Дзантиев Б.Б. Теория и практика иммуноферментного анализа. — М.: Высш. шк. — 1991. — 288 с.