Экогенетика — относительно новая область генетики человека, исследующая генетические признаки, ответственные за адаптационные [1–5] и патологические реакции организма при определенных воздействиях факторов окружающей среды [6,7], в том числе промышленных. В этой связи актуальными являются проблемы отбора на уровне генных комплексов и целостного организма мутационных изменений. При анализе доступной литературы нами не обнаружено сведений о мутагенном действии промышленных факторов, в частности, вибрации и пыли. Поэтому в данной статье впервые поставлена цель оценки мутагенной опасности при сочетанном воздействии производственных факторов физической природы [8–11].
Анализ распределения аберраций по клеткам: известно, что исследование распределения цитогенетических повреждений по клеткам выявляет природу взаимодействия повреждающего агента с компонентами клетки. Исходя из характеристики спектра нарушений, более целесообразно рассматривать не число аберраций, а число разрывов хромосом при анализе типа распределения, ввиду того, что именно разрывы являются основными повреждениями, позволяющими выявить механизм мутационного процесса (табл. 1–3) в условиях сочетанного воздействия промышленных факторов.
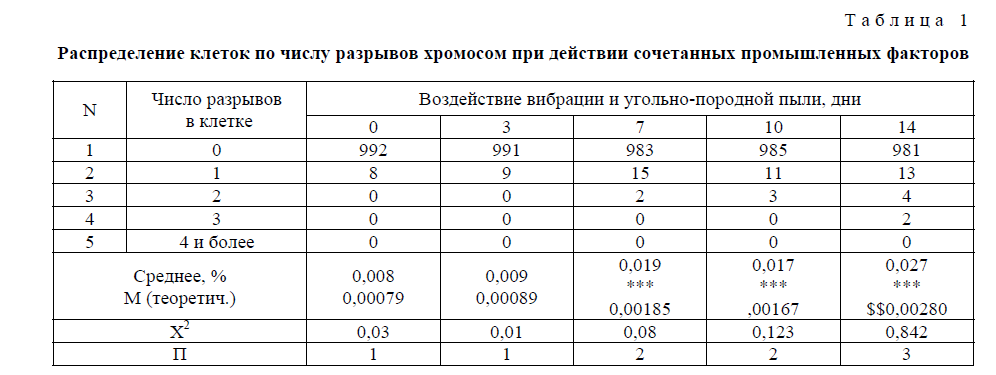
На 7-й день воздействия наблюдали достоверное увеличение частоты клеток с одним хромосомным разрывом, на фоне появления перестроенных метафаз в клетках костного мозга (табл. 1).
Т а б л и ц а 1
Распределение клеток по числу разрывов хромосом при действии сочетанных промышленных факторов
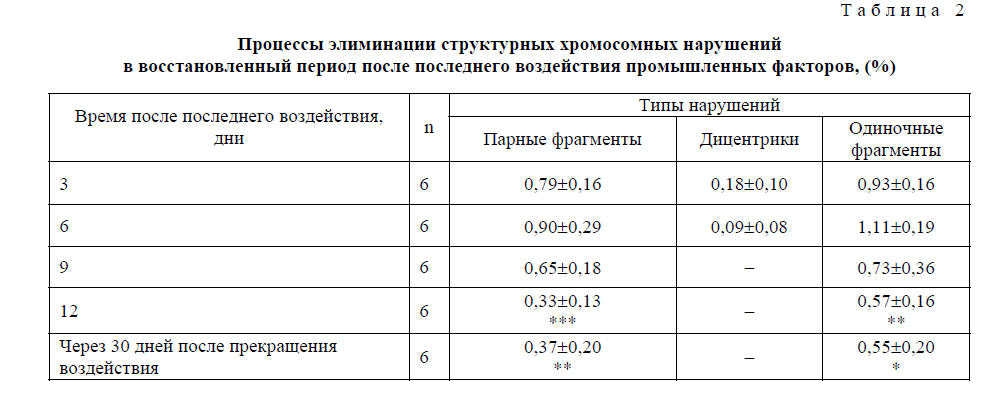
Элиминация структурных нарушений хромосом в клетках костного мозга — анализ элиминации хромосомных аберраций в клетках костного мозга крыс, находящихся под влиянием тех же факторов, выявил, что при 3-дневном эксперименте частота нарушений незначительно снижалась до уровня 1,91±0,26 % (табл. 2). При этом изменения в основном происходят в спектре мутаций. Отношение частоты хромосомных разрывов к уровню хроматидных нарушений продолжало оставаться равным 1. Наблюдали достоверное увеличение встречаемости парных хромосомных фрагментов в среднем до 0,79±0,16 %, Р<0,01 по сравнению с контролем. Отмечали снижение числа дицентрических хромосом в 1,7 раза до 0,18±0,10 %.
На третий день после последующего воздействия уровень одиночных фрагментов возрастал в среднем до 0,93±0,16 по сравнению с данными 14-дневной экспозиции — 0,82±0,19 % (Р<0,01).
На 6-й день после того же воздействия статистически достоверные изменения в частоте клеток со структурными нарушениями хромосом не наблюдали. Практически неизменным оставалось общее число хромосомных разрывов. Однако при более точном анализе спектра нарушений обнаружили снижение количества дицентриков в 2 раза по сравнению со значением данного параметра через 3 дня после воздействия до 0,09±0,08 %. Продолжало расти число парных ацентрических фрагментов до 0,90±0,29 и одиночных хроматидных разрывов до 1,11±0,19 %.
Процессы элиминации структурных хромосомных нарушений в восстановленный период после последнего воздействия промышленных факторов, (%)
Т а б л и ц а 2
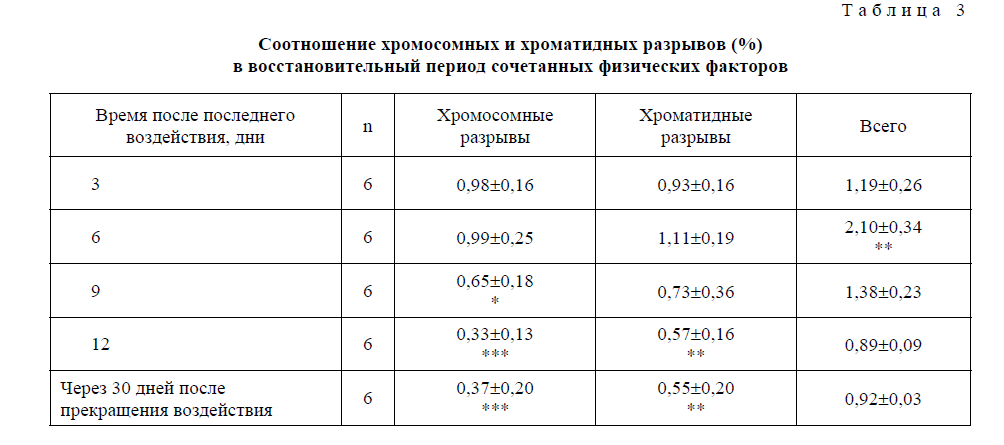
Установлено некоторое повышение частоты хромосомных разрывов по сравнению с хроматидными (табл. 3). Относительный коэффициент был равен 8,9.
Соотношение хромосомных и хроматидных разрывов (%) в восстановительный период сочетанных физических факторов
Т а б л и ц а 3
Через 9 дней уровень нарушений хромосом начинал снижаться, достигая значения 1,38±0,23 %, что является статистически достоверным при сравнении с данными трех предыдущих экспериментов, Р<0,01. Продолжало сохраняться преобладание хроматидных нарушений — 0,73±0,36 над хромосомными разрывами — 0,65±0,18 %. В спектре аберраций отсутствовали дицентрики. Имело место заметное снижение числа парных фрагментов в среднем до 0,65+0,18 и одиночных фрагментов до 0,73+0,36 %.
На 12-е сутки после комбинированного воздействия промышленных продолжалось снижение числа хромосомных аберраций до 0,89±0,09 ‰. Уровень хроматидных разрывов практически достигал контрольных значений — 0,57±0,16 %. Незначительны отклонения от контроля в числе разрывов хромосом — 0,33±0,13 %. Данные показатели практически полностью складывались из количества парных и одиночных фрагментов.
Интересно отметить, что через 1 месяц после 14-дневного воздействия продолжали встречаться клетки с хромосомными и хроматидными разрывами с частотой 0,37±0,20 и 0,55±0,20 % соответственно, за счет сохранения мутагенных факторов в организме после прекращения их воздействия. Общий уровень хромосомных аберраций несколько превышал контроль — 0,92±+0,03 %, что, скорее всего, объясняется небольшим объемом выборки.
Таким образом, анализ процессов элиминации хромосомных аберраций показал, что на первой неделе после вибрационного и пылевого воздействия частота «нестабильных» аберраций значительно выше, чем сразу после воздействия. На наш взгляд, такое явление объясняется наличием в костном мозге популяций клеток с разной скоростью деления.
В ходе митоза «нестабильные» аберрации элиминировали довольно интенсивно — число ацентрических фрагментов и дицентрических хромосом снижалось экспоненциально со временем
Дицентрическая хромосома может распределяться по одной дицентрической хроматиде в дочерние клетки без нарушения ее целостности. Вместе с тем не исключена возможность образования «моста» на стадии анафазы, что приводило к разрыву дицентрика и гибели клетки. Исходя из этих особенностей трансформации полицентрических хромосом можно признать скорость элиминации дицентриков очень высокой, что и было подтверждено в эксперименте.
Ацентрические фрагменты могут случайно оказываться рядом с хромосомами и таким образом вовлекаться в реконструирующееся ядро. Если фрагменты остаются вне ядра, то они должны быть резорбированы в цитоплазме либо образовывать микроядра. Следовательно, ацентрические фрагменты, являясь нестабильными нарушениями, элиминируются согласно экспоненциальному закону, что согласуется с представленными данными.
Наличие ацентрических фрагментов через месяц после воздействия свидетельствует, повидимому, о более длительном состоянии покоя некоторых стволовых клеток.
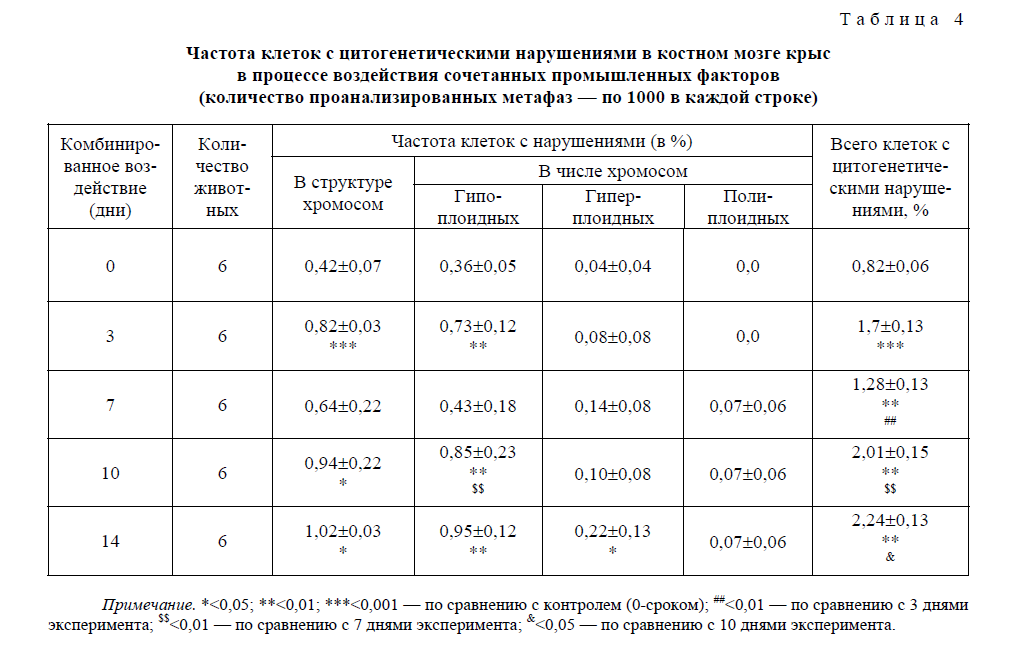
Геномные нарушения при воздействии вибрации на фоне ингаляции угольно-породной пыли: экспериментально показано, что хроническое сочетанное воздействие промышленных факторов может приводить к образованию анеуплоидных клеток в клетках костного мозга. Известно, что при этом в клетке отсутствуют одна или несколько хромосом из обычного набора, или представлены дополнительными копиями. В нашем эксперименте (табл. 4, рис. 1), уже на 3-и сутки наблюдали статистически значимое увеличение частоты клеток с измененным числом хромосом на 95 % в среднем до 0,82±0,03 %, P<0,001. Среди нарушений преобладали гипоплоидные — 0,73±0,12 %. Появлялись клетки с гиперплоидными хромосомными наборами, но в значительно меньшем количестве — 0,08+0,08 %. Причиной расхождения в частотах, вероятно, является природа данных типов анеуплодии. По-видимому, если гиперплоидия возникает за счет нерасхождения хромосом (хроматид), то причиной ее образования является не только следствие нерасхождения, но и отставание хромосом в ходе самого деления или может быть результатом аномального распределения в дочерних клетках аберрантных хромосом. Следовательно, уже на 3-й день воздействия после прохождения большинством клеток 1-го митоза наблюдали изменения на геномном уровне из-за нарушений веретена клеточного деления. Через 7 дней комбинированного воздействия происходило некоторое снижение частоты геномных мутаций по сравнению с данными 3-дневной экспозиции до 0,64±0,22 %. Однако эти изменения не были статистически достоверными. Уменьшение числа нарушений в хромосомах наблюдали за счет снижения частоты гипоплоидных клеток до 0,43±0,18, в то время как уровень гиперплоидии продолжал расти, достигая значения до 0,14±0,08 %. Появлялись тетраплоидные клетки с частотой 0,07±0,06 %. Вероятно на 7-й день воздействий вибрации и пыли не происходило значительных
Частота клеток с цитогенетическими нарушениями в костном мозге крыс в процессе воздействия сочетанных промышленных факторов (количество проанализированных метафаз — по 1000 в каждой строке)
Т а б л и ц а 4
количественных изменений в частоте геномных мутаций, так как все обнаруженные изменения статистически недостоверны по сравнению с данными 3-х дней эксперимента. Однако обращает на себя внимание факт качественных сдвигов в спектре геномных нарушений. Появление клеток с тетраплоидным хромосомным набором свидетельствует, скорее всего, не о нарушении аппарата деления, а о разрушении клеточной мембраны. Это положение согласуется с данными об активизации свободнорадикальных процессов, по уровню которых можно судить о деструкции клеточных мембран.
Через 7 дней комбинированного воздействия происходило некоторое снижение частоты геномных мутаций по сравнению с данными 3-х дневной экспозиции до 0,64±0,22 %. Однако эти изменения не были статистически достоверными. Уменьшение числа нарушений в хромосомах наблюдали за счет снижения частоты гипоплоидных клеток до 0,43±0,18, в то время как уровень гиперплоидии продолжал расти, достигая значения до 0,14±0,08 %. Появлялись тетраплоидные клетки с частотой 0,07±0,06 %. Вероятно, на 7-й день воздействия вибрации и пыли не происходило значительных изменений.
На 10-й день экспозиции не обнаружено существенных изменений в частоте гиперплоидных клеток. Значительно возрастал уровень гипоплоидных клеток, в среднем до 0,85±0,23 % по сравнению с данными 7-го дня эксперимента. Статистически достоверный рост этих параметров, однако, не повлиял на изменения интегрального показателя — нарушения в числе хромосом. Частота геномных мутаций к 10-и дням эксперимента достигала 0,94±0,12 %. По-видимому, через 10 дней воздействия вибрации и пыли продолжалась относительная стабилизация частоты геномных нарушений, что, скорее всего, свидетельствовало не только об изменениях клеточного деления, но и отражало состояние клеточной мембраны.
После 14 дней комбинированного воздействия наблюдали увеличение числа клеток с геномными нарушениями до 1,02±0,03, в основном за счёт увеличения частоты гипоплоидных клеток — 0,95±0,32 %. Уровень гиперплоидии с высокой степенью достоверности возрастал в 2,2 раза по сравнению с результатами 10-дневной экспозиции до 0,22±0,13 ‰. Частота полиплоидных клеток составляла 0,07±0,06 %.
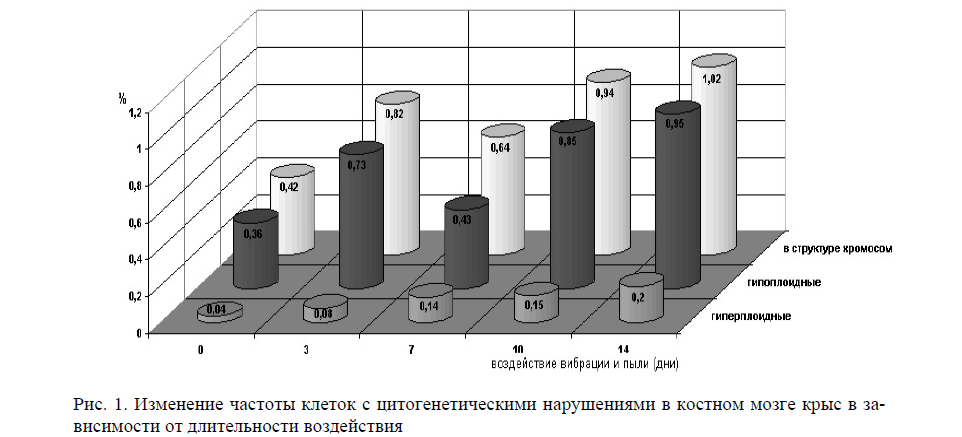
Рис. 1. Изменение частоты клеток с цитогенетическими нарушениями в костном мозге крыс в зависимости от длительности воздействия
Таким образом, частота геномных нарушений увеличивается в ранние сроки эксперимента через 3 дня воздействия и далее остается неизменной в другие сроки. Некоторые отклонения в численном выражении данного параметра объясняются, скорее всего, колебаниями, причиной которых являлись флуктуации уровней гипоплоидии. Последние данные свидетельствуют о том, что причиной анеуплоидии могут быть изменения в клеточной мембране, в результате которых хромосомы изолируются после деления с формированием микроядер и их дальнейшей резорбцией, что, в конечном счете, приводило к гипоплоидии. По-видимому, именно этот механизм имеет место в случае хронического воздействия вибрации на фоне угольно-породной пыли.
Появление полиплоидных клеток на 7-й и 14-й дни эксперимента также можно объяснить активизацией деструктивных процессов в клеточных мембранах.
Не следует, однако, исключать вклад процесса отставания хромосом в возникновении гипоплоидии. Величина эта складывается из удвоенного количества клеток с отставанием хромосом (в этом случае обе клетки будут гипоплоидными) и числа клеток с отставанием хроматид. О вкладе в величину гипоплоидии нерасхождения хромосом можно судить по величине гиперплоидии, уровень которой на всех сроках эксперимента не превышал 0,21 частоты гипоплоидии, что является вполне достаточным для того, чтобы принять во внимание этот путь формирования анеуплоидных клеток.
Таким образом, комбинированное воздействие способно индуцировать нарушения в числе хромосом как за счет разрушения веретена клеточного деления (что приводит к отставанию хромосом), так и за счет деструктивных процессов в клеточной мембране (приводящих к снижению ее резистентности при обработках гипотоническим раствором и приготовлении препаратов).
Изменения митотической активности: исследование митотической активности в клетках костного мозга белых крыс (рис. 2) показало, что митотический индекс после 3-х дней воздействия имел тенденцию к возрастанию до 31,08±2,02 по сравнению с контролем 26,3±2,05 %, Р<0,05. Через 7 дней данный показатель по сравнению с 3-х дневным сроком незначительно увеличивался, в среднем до уровня 32,13±2,03 %, Р<0,01. К 10-и дням воздействия митотическая активность клеток костного мозга росла более интенсивно, достигая статистически значимых различий по сравнению с данными 3-дневного эксперимента до 41,15±3,03 %, Р<0,001. На 14-й день экспозиции митотическая активность клеток костного мозга падала практически до уровня контрольных значений — 26,05±0,08 %. Последнее, по-видимому, связано со снижением продвижения клеток по митотическому циклу.
По-видимому, повышение активности деления клеток костного мозга на 3, 7 и 10-й дни эксперимента связано с развитием компенсаторно-адаптивных реакций организма.
Снижение числа метафаз на 14-й день вибрационного и пылевого воздействия объясняется как декомпенсацией организма, так и неизбежным последствием увеличения частоты геномных мутаций и структурных нарушений хромосом.
Результаты исследования митотической активности хорошо согласуются с данными определения ДНК, РНК в клетках печени и активности кислой ДНК-азы крови.
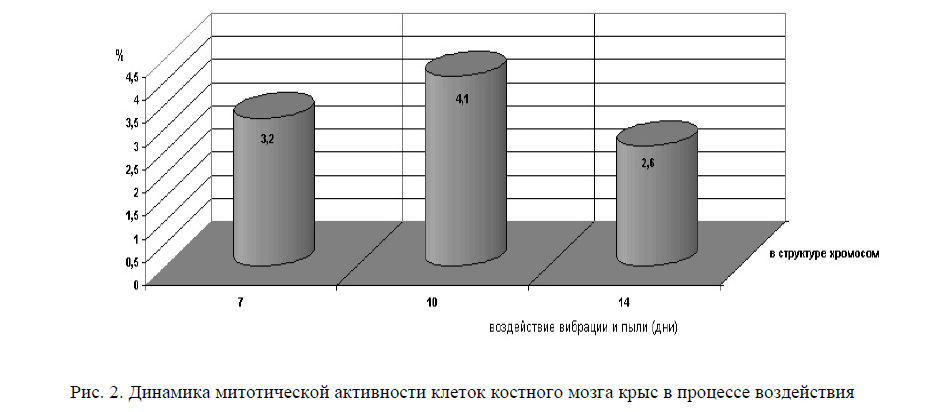
Рис. 2. Динамика митотической активности клеток костного мозга крыс в процессе воздействия
Индивидуальные колебания хромосомных аберраций: известно, что на частоту хромосомных аберраций, прежде всего, оказывают влияние 2 фактора: доза мутагена и стадия клеточного цикла. Второй фактор может привести к различиям в индивидуальном эффекте мутагенного воздействия изза неодинаковой длительности клеточного цикла. При этом имеет значение температура, при которой происходило воздействие, а также генетические особенности животных, от которых получены клетки. Доказано, что цитогенетический эффект при действии физических мутагенов может быть обусловлен двумя типами факторов: случайными (ошибки эксперимента) и неслучайными (генотипические различия доноров).
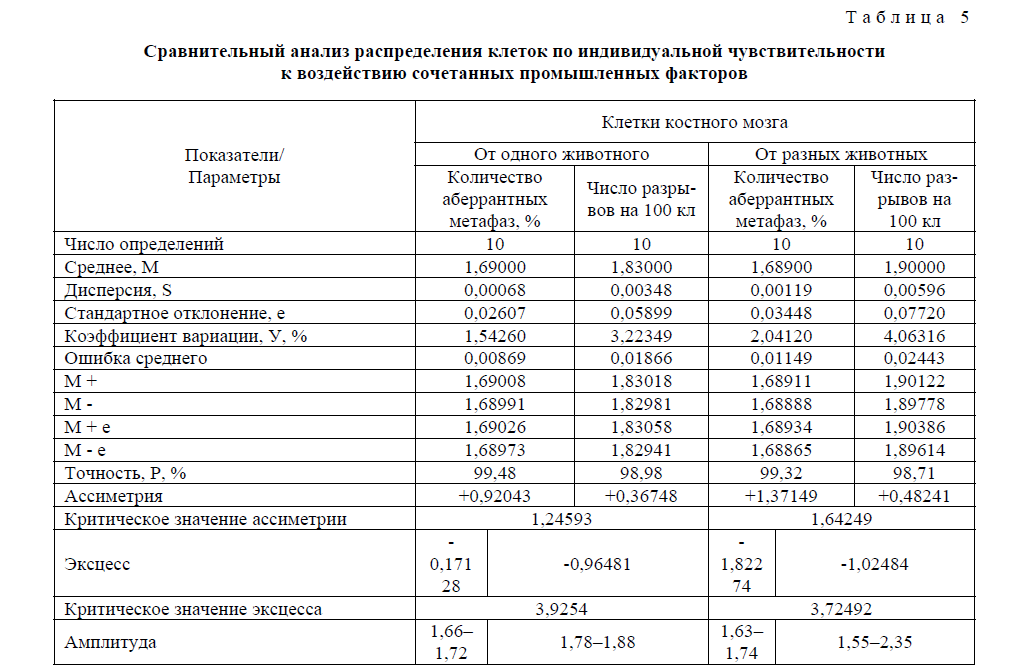
Данные по проценту аберрантных метафаз и числу разрывов на 100 клеток распределялись в соответствии со статистическим законом нормального распределения. Об этом свидетельствовала незначительность отклонения от нуля ассиметрии и эксцесса, а также тот факт, что практически все отдельные изменения укладывались в 99 %-й доверительный интервал. Исключение составляли данные от разных животных, где уровень доверия был равен 98,71 %.
Проведенный анализ таблицы 5 показал, что в обоих случаях данные по проценту аберрантных метафаз и числу разрывов на 100 клеток распределялись в соответствии со статистическим законом нормального распределения. Об этом свидетельствовала незначительность отклонения от нуля ассиметрии и эксцесса, а также тот факт, что практически все отдельные изменения укладывались в 99 %-й доверительный интервал. Исключение составляли данные от разных животных, где уровень доверия был равен 98,71 %.
Величина коэффициента вариации менее 5 % позволяет считать, что исследованные клетки от одного животного и разных животных представляли собой статистически однородные совокупности. Однако следует отметить, что уровень дисперсии для одного животного на 75 % и на 71 % больше, чем для разных животных в случае аберрантных метафаз и числа разрывов на 100 клеток соответственно. Коэффициент вариации для клеток от разных животных в обоих случаях на 33 % выше, чем для одного животного, что естественно, ввиду того, что разброс по данным показателям для одного животного был значительно меньшим, чем для клеток, полученных от разных животных.
Можно полагать, что в первом случае вся величина дисперсии обусловлена ошибками эксперимента и схоластическими ошибками при оценке эффекта. Во втором случае значительное увеличение дисперсии, в 2 раза по сравнению с предыдущим случаем, объясняется величиной добавочной дисперсии, обусловленной повышенной чувствительностью разных животных, что приводит, в конечном счете, к увеличению коэффициента вариации.
Таким образом, доказано объективно существующее различие в чувствительности клеток разных животных к мутагенному воздействию сочетанных промышленных факторов.
Мутагенное воздействие промышленных факторов определяется по тесту, выявляющему аномальные головки спермиев у экспериментальных животных. В настоящее время изучение морфологии спермиев включает в себя выявление аномалий головки, акросомы и хвоста, хотя считается, что для анализа мутагенного воздействия достаточная оценка только формы головки, поскольку вариабельность этого признака менее всего зависит от внешних факторов.
Т а б л и ц а 5
Сравнительный анализ распределения клеток по индивидуальной чувствительности к воздействию сочетанных промышленных факторов
Через 3 дня вибрационного и пылевого воздействия достоверно увеличивалось на 31 % число спермиев с аномальной головкой в среднем до 0,51±0,08 % по сравнению с контролем — 0,39±0,04 %, Р<0,001 (рис. 3). Причем большую часть аномалий составляли клетки с аморфными головками — 0,24±0,06 %. Уровни клеток с микрои макроголовкой увеличивались незначительно.
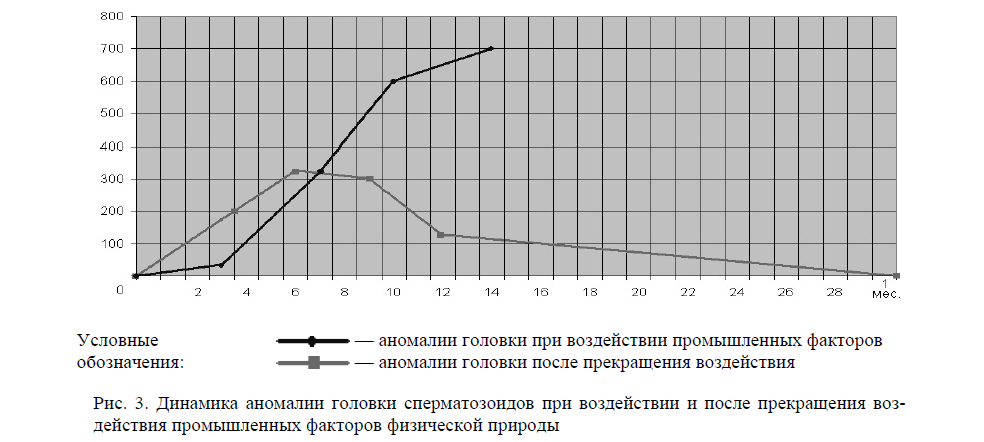
Рис. 3. Динамика аномалии головки сперматозоидов при воздействии и после прекращения воздействия промышленных факторов физической природы
На 7-й день комбинированного воздействия количество аномальных сперматозоидов с высокой степенью достоверности возрастало в 4,5 раз — до 1,77±0,06 %. Число клеток с аморфной головкой повышалось в среднем до 0,94±0,07 %, и данная аномалия продолжала оставаться преобладающей. Обнаружено статистически достоверное увеличение частоты спермиев с аномальными головками 2-х патологических размеров — большого и малого. Таким образом, на 7-й день экспозиции наблюдали значительный рост частоты всех видов аномальных головок репродуктивных клеток.
Через 10 дней эксперимента число аномальных спермиев продолжало увеличиваться в среднем до 2,21±0,06 % по сравнению с данными 7-дневного эксперимента, Р<0,001. Количество клеток с аморфной головкой практически не изменялось, но данный вид аномалии продолжал оставаться преобладающим. Достоверно возрастало число клеток с микроголовкой — в среднем до 0,63±0,05 %, Р<0,001 и макроголовкой — до 0,57±0,04, Р<0,01 по сравнению с теми же показателями через 7 дней эксперимента. Обнаружено появление раздвоения хвостовой части спермиев — 0,03±0,02 %.
На 14-й день воздействия наблюдали незначительное увеличение числа спермиев с аномальной головкой в среднем до 2,57±0,12 %, но существенных изменений в спектре аномалий не обнаружено. Продолжался рост частоты микросомии до 0,87±0,16 %, макросомии — до 0,63±0,01 %, клеток с аморфной головкой — до 1,09±0,15 %, двухвостовой аномалии — до 0,06±0,03 %. Однако эти изменения оставались на уровне показателей 10-дневного эксперимента.
Известно, что форма головки спермиев находится под строгим генетическим контролем и даже незначительные изменения морфологических характеристик репродуктивных клеток могут свидетельствовать о нарушении на генном уровне.
Таким образом, хроническое воздействие сочетанных промышленных факторов вызывает количественные и качественные нарушения в мужских репродуктивных клетках и оказывает негативное влияние на более глубоком субтильном уровне регуляции. При этом преобладающим видом аномалии следует признать аморфную головку. Обращает на себя внимание также факт появления на 10-й и 14-й дни весьма редких аномалий в виде двухвостых клеток.
Установлена коррекция между показателями метафазного цитогенетического анализа и данными теста на аномальные головки спермиев (r³0,7). По данным регрессионого анализа кривая зависимости частоты аномальных спермией от длительности вибрационного воздействия имеет S-образный характер, повторяя аналогичную кривую для уровня хромосомных аберраций.
Процессы элиминация репродуктивных клеток с аномальными головками в восстановительный период (после прекращения воздействия) сравнивали с таковыми для клеток костного мозга. Существенное отличие этих двух процессов объясняется физиологическими особенностями половых клеток, выведение которых из организма происходит в основном за счет их одновременного массового выброса. Установлено, что через 3 дня после прекращения 14-дневного эксперимента уровень спермиев с аномальной головкой заметно снижался в среднем до 0,70±0,01 %. При этом число спермиев с аморфной головкой уменьшалось до 0,30±0,03 %, а частота микросомии составляла 0,22±0,02 %, макросомии — 0,18±0,02 %. На 6-й день после вибрационного на фоне пылевого воздействия наблюдали достоверное повышение уровня клеток с аномалиями головок, достигавшее 1,25±0,06 %, Р<0,01. Частота микросомии спермиев соответствовала данным 3-х дневного эксперимента. Частота макросомии спермиев увеличивалась почти в 2 раза, составляя 0,32±0,03 %. Через 9 дней после прекращения комбинированного воздействия частота выявления аномальных клеток статистически не изменялась. Уровень микросомии составлял 0,25±0,02 %, макросомии — 0,38±0,04 %, вероятность появления клеток с аморфной головкой была равна 0,60±0,05 %. На 12-е сутки после прекращения воздействия вибрации и угольно-породной пыли отмечено снижение уровня спермиев с аномальными головками в среднем до 0,46±0,05 %. При этом частота встречаемости клеток с аморфной головкой составила 0,18±0,04 %. Уровни макрои микросомии понижались до 0,12±0,01 % и 0,16±0,02 % соответственно. Через 1 месяц после прекращения воздействия число спермиев с аномальной головкой уменьшилось до уровня контрольных значений. Частота аморфных головок и микросомии статистически достоверно по сравнению с показателями 12-и дней после прекращения воздействия вибрации. Уровень макросомии достоверно уменьшился в 2 раза и соответствовал контрольному значению. Таким образом, через 1 месяц после прекращения 14-дневного вибрационного воздействия на фоне угольно-породной пыли происходил возврат к контрольному уровню.
Снижение морфологических изменений головки на 3-й день восстановительного периода объясняется, скорее всего, периодическими непроизвольными выбросами спермиев. Затем этот показатель несколько увеличивался, но статистически недостоверно, сохраняя данную тенденцию к 9-ти дням. Вероятно, это небольшое колебание объясняется устанавливающимся равновесием между процессами созревания и выброса спермиев.
В заключение необходимо отметить, что анализ распределения аберрации по клеткам выявил природу взаимодействия повреждающих факторов с компонентами клетки, т.е. механизм мутационного процесса. Достоверно установлено увеличение клеток с одним хромосомным разрывом на фоне появления перестроечных метафаз в клетках костного мозга на 7-й день эксперимента и лишь на 14-й день — появление метафазных пластинок с тремя разрывами. Анализ процессов элиминации хромосомных аберраций показал увеличение частоты «нестабильных» аберраций на первой неделе после воздействия вибрации и угольно-породной пыли, что, по-видимому, объясняется наличием в костном мозге популяции клеток с разной скоростью деления. В ходе митоза «нестабильные» аберрации элиминировали довольно интенсивно — число ацентрических фрагментов и дицентрических хромосом снижалось экспоненциально со временем. Наличие ацентрических фрагментов через месяц после воздействия промышленных факторов свидетельствует, по-видимому, о более длительном состоянии покоя стволовых клеток. Анализ геномных нарушений позволяет считать, что воздействие вибрации на фоне угольно-породной пыли способно индуцировать нарушения в числе хромосом как за счет разрушения веретена клеточного деления, что приводит к отставанию хромосом, так и за счет деструктивных изменений в клеточной мембране, приводящих к изменению ее резистентности. Анализ митотической активности клеток костного мозга белых крыс позволил установить повышение активности деления клеток на 3, 7-й и 10-й дни эксперимента, по-видимому, компенсаторно-адаптивного характера. Снижение числа метафаз на 14-й день эксперимента объясняются декомпенсацией организма и неизбежным последствием увеличения частоты геномных мутаций и структурных нарушений хромосом. Эти данные коррелируют с содержанием ДНК, РНК и активностью кислой РНК-азы в клетках крови. Доказано объективно существующее различие в чувствительности клеток разных животных к мутагенному воздействию вибрации и угольно-породной пыли.
Хроническое воздействие промышленных факторов производственной среды вызывает количественные и качественные нарушения в мужских репродуктивных клетках, при этом преобладающим видом аномалии является аморфная форма головки сперматозоидов, на 7-й день — макрои микроголовки, а на более поздних стадиях эксперимента (10-й и 14-й дни) — редкие аномалии в виде раздвоения хвостовой части клеток. Однако все выявленные изменения в восстановительный период через 1 месяц после прекращения эксперимента восстанавливаются и возвращаются к контрольному уровню.
Список литературы
- Салганик Р.И. Молекулярные механизмы стресс-индуцируемой наследственной изменчивости // Генетика. — 1987. — Т. 23. — N 6. — С. 1050–1063.
- Novorodovski A.G. Экогенетический подход к исследованию адаптации и здоровья человека // Генетика. — Т. 28. — N 4. — С. 176–185.
- Батырханов М.С., Святова Г.С. Роль генетических наследственных факторов нарушения сперматогенеза мужчин в РК // Новые лечебно-диагностические технологии в акушерстве, гинекологии и педиатрии: Материалы науч.-практ. конф. — Караганда, 2004. — С. 97–99.
- Титенко Н.В. Гигиена окружающей среды и экогенетика // Методология фундаментальных исследований в гигиене окружающей среды. — М., 1989. — С. 216–222.
- Чеботарев А.Н. Закономерности хромосомной изменчивости соматических клеток человека // Вестник РАМН. —— N 10. — С. 61–69.
- Владимирцев Т.М., Успенская Ю.А., Нефедова В.В., Егорова А.Б. Окислительный стресс и нарушение морфологии гамет, индуцируемых хлоридом цинка // Гигиена и санитария. — 2003. — N — С. 58–59.
- Pastor S., Greus A., Parron T. et al. // Mutagenesis. — 2003. — V. 18. — N 3. — P. 243–258.
- Джангозина Д.М. Цитогенетические и клеточно-молекулярные изменения при воздействии некоторых производственных факторов // Медицина труда и промышленная экология. — 2002. — N — С. 20–24.
- Дюсенбаева Н.К. Гигиеническое значение оценки мутагенных эффектов химических факторов окружающей и производственной среды // Гигиена труда и промышленная экология. — 2006. — N — С. 24–31.
- Юрченко В.В., Подольная М.А., Ингель Ф.И. и др. Полиорганный микроядерный тест в эколого-гигиенических исследованиях. — М., 2007. — С. 220–267.
- Юрченко В.В., Кривцова Н.И., Беляева Ф.Н. и др. Применение микроядерного теста для оценки питьевой воды // Гигиена и санитария. — 2008. — N — С. 49–53.