Гидразин и несколько тысяч его производных, гидразиды, гидразоны и родственные им соединения, нашли широкое применение в различных отраслях промышленности, сельском хозяйстве, медицине. Они используются в нефтяной промышленности в качестве антиоксидантов. В аэрокосмической промышленности гидразин, 1,1 ДМГ и их смеси применяются как горючие компоненты в ракетном топливе [1], в металлургии, в химии — при производстве красителей и пластмасс [2]. В сельском хозяйстве производные гидразина используются в качестве регуляторов роста растений и гербицидов. Около 30 наименований пестицидов — производных гидразина ежегодно патентуется в мире. Продолжается использование водного гидразина в качестве ингибитора коррозии в системах горячего отопления. В последние годы ряд представителей этого класса находит применение в медицине [3] в качестве противотуберкулезных препаратов, ингибиторов моноаминооксидазы.
При хронических интоксикациях гидразинами преобладают признаки поражения печени и, в меньшей степени, других систем (центральной нервной, сердечно-сосудистой, выделительной, кроветворной) [4]. Патогенез поражений производными гидразина очень сложный и реализуется путем повреждения биохимических реакций почти всех изученных видов обмена. Однако среди множества биохимических процессов, повреждаемых гидразинами, можно выделить круг реакций, имеющих непосредственную связь с возникновением и развитием ведущих патогенетических эффектов отравления. К ним в первую очередь следует отнести энзимы, катализирующие процессы окисления, переаминирования, дезаминирования и фосфорилирования. Блокирование ферментов опосредовано взаимодействием гидразинов с кофакторами по типу образования гидрозонов, хелатов и восстановления активных функциональных групп [5]. Кроме перечисленных выше механизмов, реализация токсического эффекта производных гидразина также осуществляется благодаря промежуточным соединениям радикальной природы. Главными из них являются супероксидные радикалы, которые образуются при биотрансформации гидразинов в микросомах печени. Эти радикалы могут давать различные токсические эффекты, в том числе и усиливать процессы ПОЛ [6].
Несмотря на распространенность в природе, широкое применение гидразинов и изученность острых и хронических отравлений производными гидразина, их влияние на морфологическую структуру печени недостаточно изучено.
Цель и задачи исследования. Исследовать воздействие некоторых производных гидразина (нитрозодиметиламина, серного гидразина, гидразида изоникотиновой кислоты, 2,4-фенилгидразина) на структуру печени.
Материалы исследования. Эксперименты проводились на 260 белых беспородных крысах массой 250–300 гр. Было изучено действие хронических доз производных гидразина — гидразида изоникотиновой кислоты, нитрозодиметиламина, гидразин сульфата и 2,4-динитрофенилгидразина и на фоне коррекции препаратом «Салсоколлин». Микроскопическое исследование препаратов было проведено общепринятыми методами.
Результаты исследования и их обсуждение. Результаты, полученные в ходе исследования морфологических изменений печени экспериментальных животных, даны в таблице.
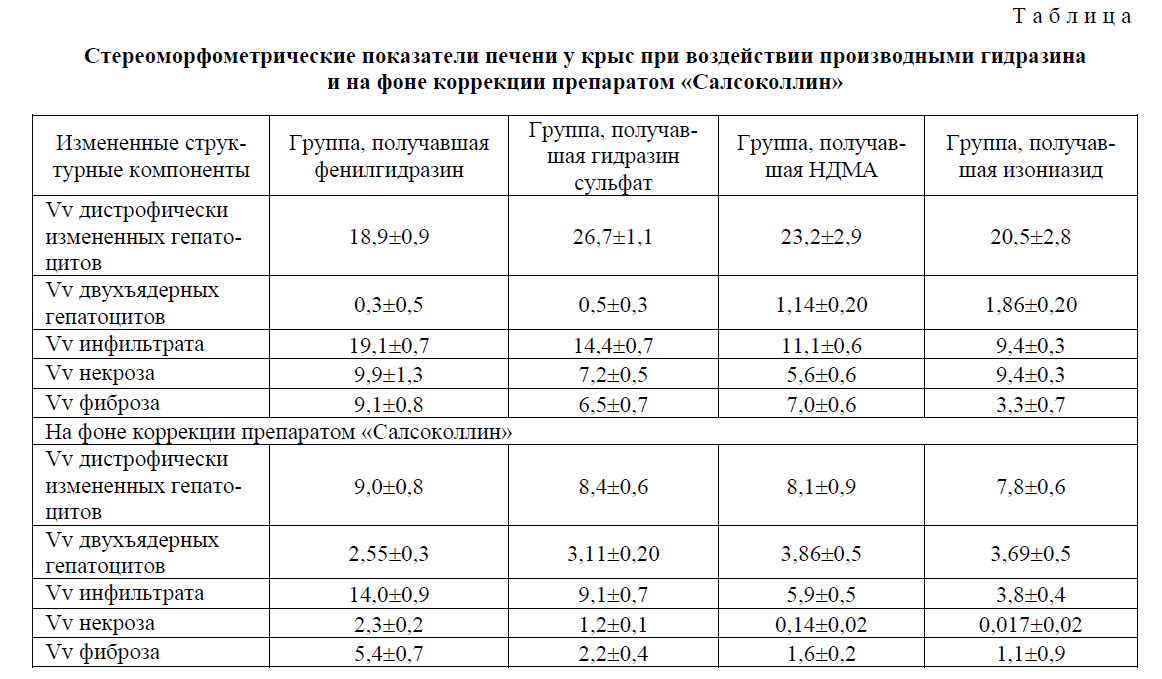
Т а б л и ц а
Стереоморфометрические показатели печени у крыс при воздействии производными гидразина и на фоне коррекции препаратом «Салсоколлин»
При микроскопическом исследовании печени экспериментальных животных, получавших в течение 3 месяцев различные химические соединения гидразина, выявлялись стереотипные патоморфологические изменения, которые варьировали только по степени выраженности тяжести патологического процесса и зависели от вида использованного химического вещества. В целом они характеризовались гемолимфоциркуляторными нарушениями, воспалительной инфильтрацией как портальных трактов, так и внутри долек мононуклеарными клетками, дистрофическими и деструктивными изменениями в клетках функциональной паренхимы, что в конечном итоге проявлялось нарушением гистоархитектоники органа, а также развитием различной степени выраженности фибропластических процессов. Так, микроскопический и морфометрический анализ гистологических препаратов показал, что в случае использования в опыте фенилгидразина на первый план выступали гемомикроциркуляторные нарушения, особенно в системе оттока крови из паренхимы органа.
Центральные вены и прилежащие к ним синусоидные капилляры были расширены, заполнены эритроцитами, нередкими были очаги диапедезных кровоизлияний (рис. 1).
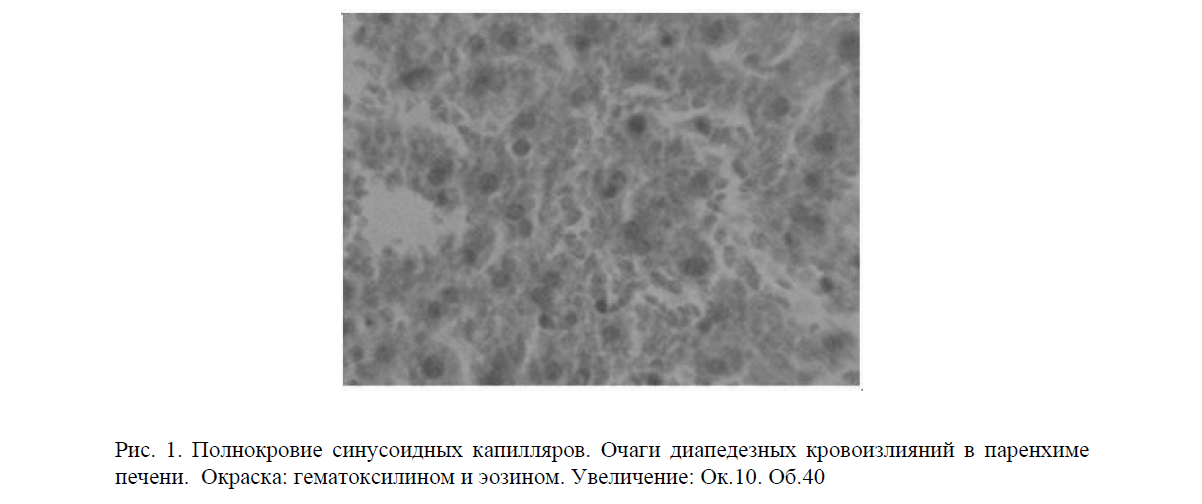
Рис. 1. Полнокровие синусоидных капилляров. Очаги диапедезных кровоизлияний в паренхиме печени. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
В паренхиме печени преобладали деструктивные изменения, особенно в центральных отделах дольки, что выражалось мелко-среднекапельной жировой дистрофией и гидропической (рис. 2).

Рис. 2. Жировая и гидропическая дистрофия гепатоцитов печени. Очаги колликвационного некроза. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
Очаги некроза гепатоцитов носили мозаичный характер. Альтернативные изменения гепатоцитов соответственно сопровождались развитием как портального, так и перипортального, а в дольке перинекротических воспалительных инфильтратов, которые в основном носили лимфоцитарный характер с примесью полиморфноядерных лейкоцитов и плазматических клеток. Портальные тракты были расширены, лимфацитарный инфильтрат проникал в окружающую печеночную паренхиму, где были видны ступенчатые некрозы (рис. 3).
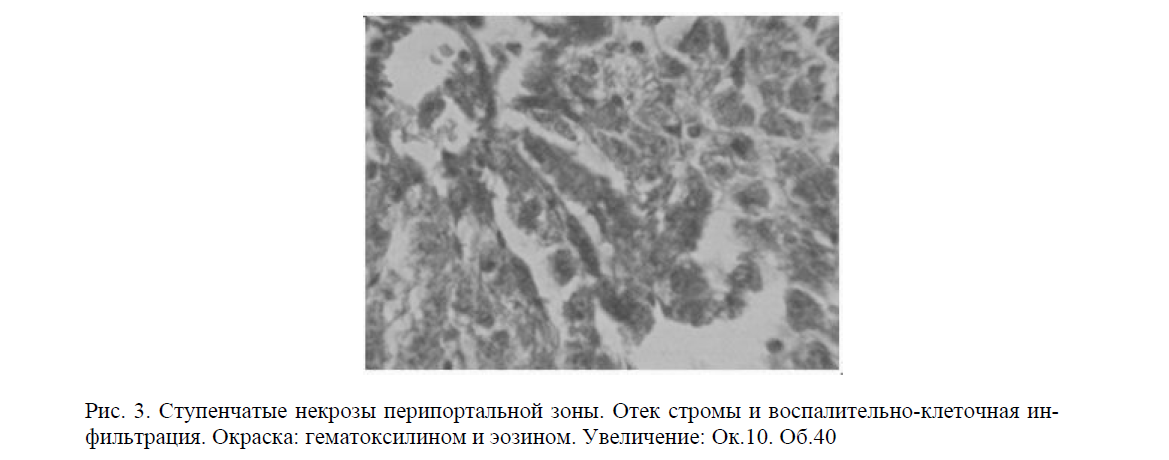
Рис. 3. Ступенчатые некрозы перипортальной зоны. Отек стромы и воспалительно-клеточная инфильтрация. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
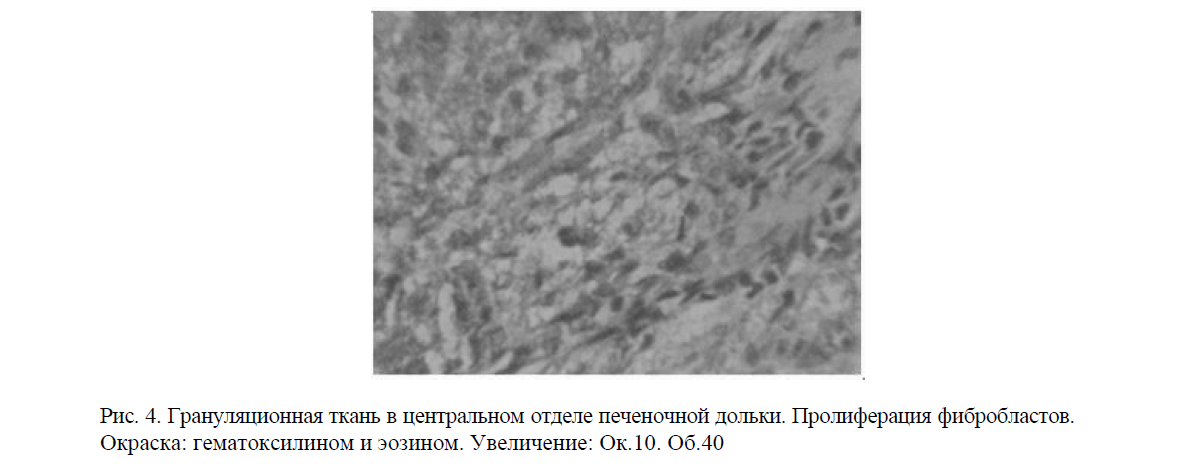
Рис. 4. Грануляционная ткань в центральном отделе печеночной дольки. Пролиферация фибробластов. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
Наряду с морфологическими признаками повреждения органа отмечались разрастания грануляционной ткани на месте некротизированных гепатоцитов с выраженной фибробластической реакцией (рис. 4).
Как показала PAS-реакция на гликоген, уровень его содержания в гепатоцитах значительно снижался (рис. 5).

Рис. 5. Слабовыраженная PAS-реакция в гепатоцитах печени. Окраска: PAS-реакция на гликоген. Увеличение: Ок.10. Об.40
По результатам сравнительного морфометрического и микроскопического анализа гистологических препаратов, в случае использования в опыте гидразин сульфата, хронический гепатит, который развивался у опытных животных, носил слабовыраженную степень активности.
Некротизированные гепатоциты выявлялись преимущественно в перипортальных и центральных зонах, Vv которых была достоверно ниже в сравнении с группой, получавшей фенилгидразин (9,9±1,3 и 7,2±0,5). Очаги некроза были окружены лимфоидными клетками и макрофагами (рис. 6).
Иногда единичные некрозы печеночных клеток встречались в других отделах долек, хотя Vv доля дистрофически измененных гепатоцитов существенно не отличалась от группы, получавшей фенилгидразин. Преобладала зернистая и вакуольная дистрофия печеночных клеток (рис. 7).
Vv доля клеточной инфильтрации была также несколько ниже в сравнении с группой, получавшей фенилгидразин. Объемная доля постнекротического фиброза также была несколько ниже.
При микроскопическом исследовании ткани печени животных, получавших нитрозодиметиламин, морфологические изменения характеризовались, прежде всего, сосудистой реакцией, что проявлялось умеренным полнокровием синусоидных капилляров и сосудов (рис. 8).
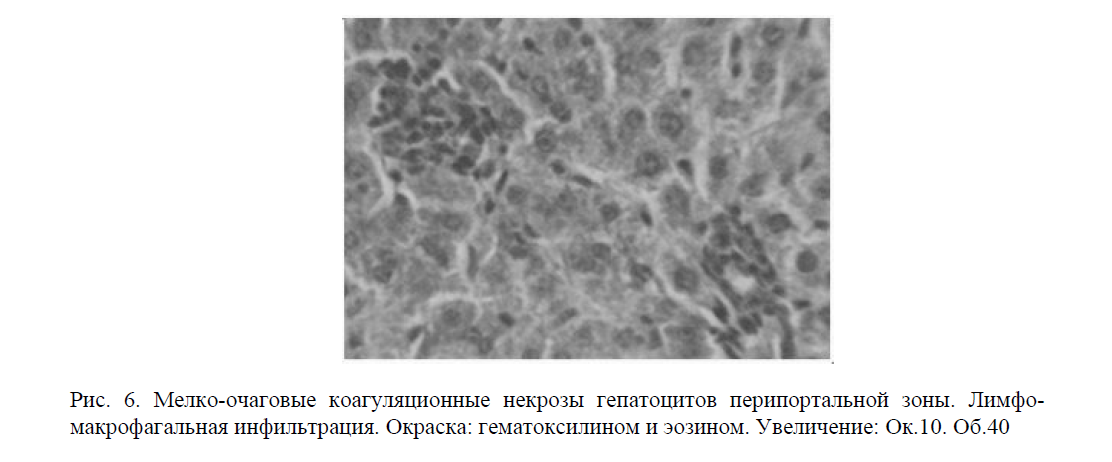
Рис. 6. Мелко-очаговые коагуляционные некрозы гепатоцитов перипортальной зоны. Лимфомакрофагальная инфильтрация. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40

Рис. 7. Умеренно-выраженное полнокровие синусоидных капилляров, зернистая и вакуольная дистрофия печеночных клеток. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
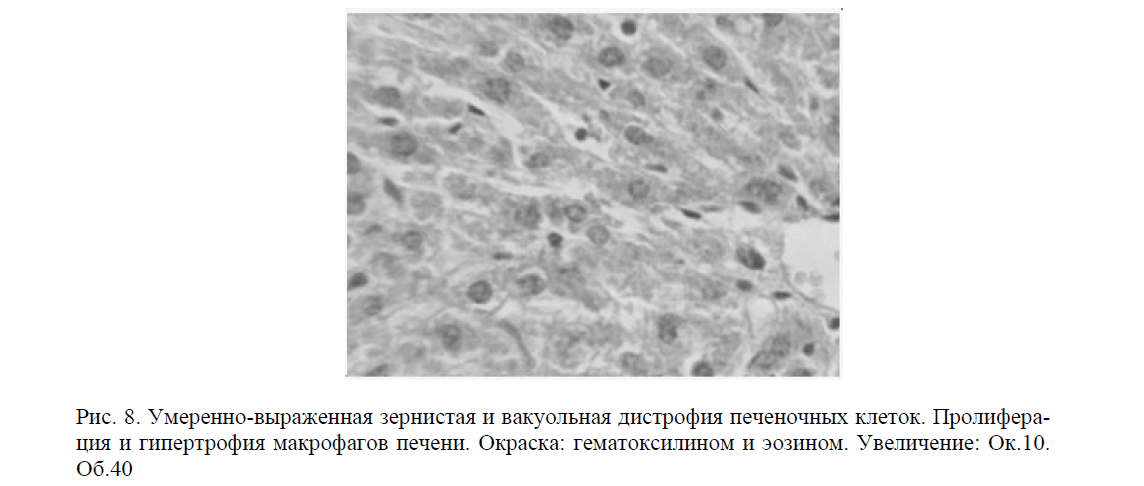
Рис. 8. Умеренно-выраженная зернистая и вакуольная дистрофия печеночных клеток. Пролиферация и гипертрофия макрофагов печени. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
Печеночные макрофаги умеренно пролиферировали. Как показал морфометрический анализ, сохранялась и нарастала тенденция к снижению количественно-качественных показателей деструктивных изменений в паренхиме органа. В гепатоцитах преобладала зернистая дистрофия, которая проявлялась накоплением белковых гранул в цитоплазме печеночных клеток. Отмечались единичные клетки с гидропической дистрофией (рис. 9).
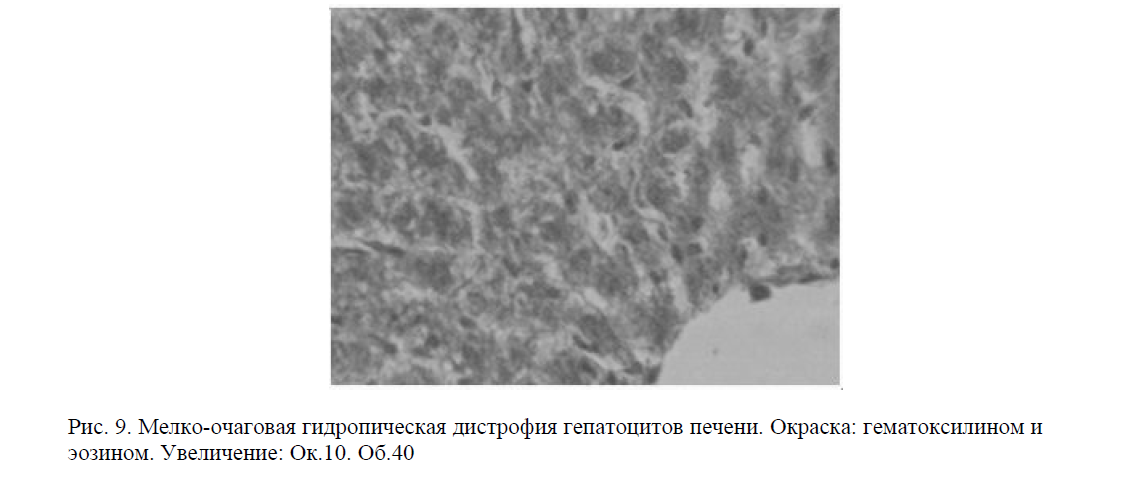
Рис. 9. Мелко-очаговая гидропическая дистрофия гепатоцитов печени. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
В различных отделах печеночных долек встречаются мелкие очаги некроза паренхимы с разрушением аргирофильной стромы и скоплением в этих участках макрофагов и лимфоцитов сегментоядерных лейкоцитов. Выражена пролиферация и гипертрофия звездчатых ретикулоэндотелиоцитов (рис. 10).
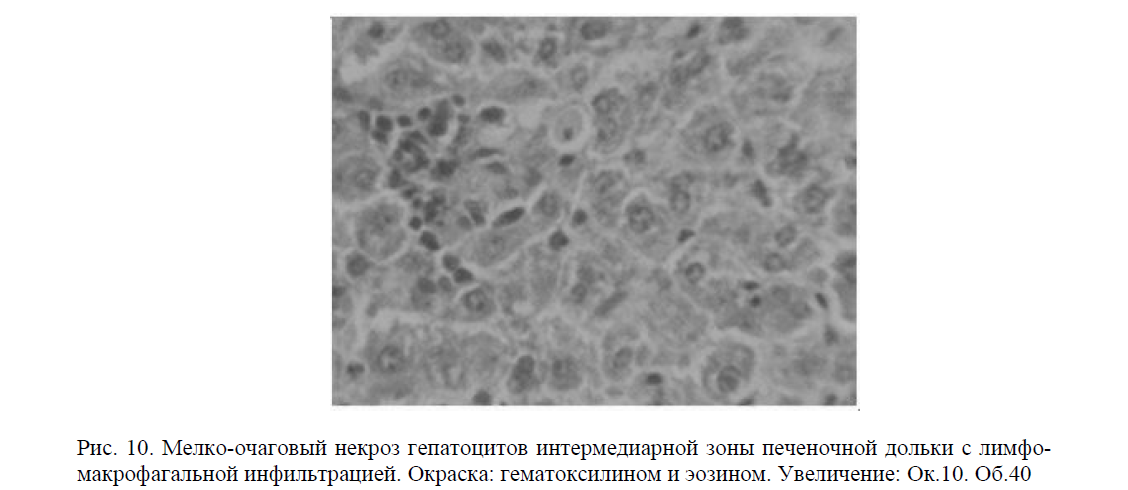
Рис. 10. Мелко-очаговый некроз гепатоцитов интермедиарной зоны печеночной дольки с лимфомакрофагальной инфильтрацией. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
PAS-реакция на гликоген отражала снижение его насыщенности в центральных отделах, что создавало неравномерность его распределения в дольке. В периферических отделах дольки его насыщенность была высокой и снижалась в интермедиарном и центральном отделах (рис. 11).
Гистоархитектоника печени значительных изменений не претерпевала. Vv доля постнекротического фиброза достоверно снижалась в сравнении с группами, получавшими фенилгидразин и гидразин сульфата.

Рис. 11. Хорошо выраженная PAS-реакция в цитоплазме гепатоцитов печени. Окраска: PAS-реакция на гликоген. Увеличение: Ок.10. Об.40
В группе животных, получавших изониазид, гистологическое и морфометрическое исследование показало картину портального гепатита. Клеточный инфильтрат составлял 9,4±0,3 (рис. 12).
Явления интоксикации носили различную степень выраженности, в основном зернистой дистрофии. Гидропическая дистрофия выявлялась в отдельных клетках печеночной ткани. Все указанные виды дистрофии были локализованы преимущественно в перипортальной и промежуточных зонах. Некрозы гепатоцитов были единичны, преимущественно колликвационного характера и встречались в промежуточной зоне.
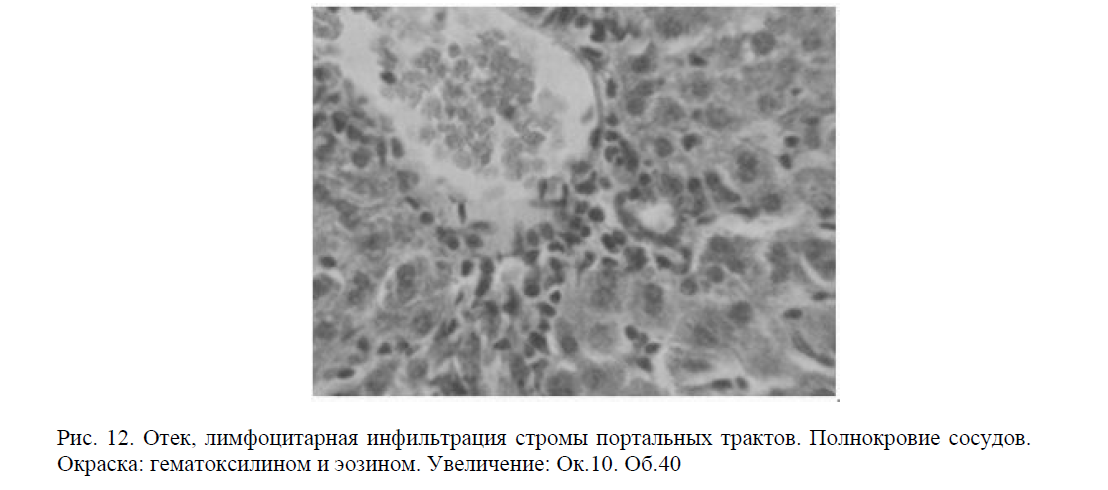
Рис. 12. Отек, лимфоцитарная инфильтрация стромы портальных трактов. Полнокровие сосудов. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
Пролиферативная активность звездчатых ретикулоэндотелиоцитов носила очаговый характер и имела различную степень выраженности. Гликогенизация гепатоцитов выглядела относительно равномерной и была несколько снижена в центральных отделах дольки. Гистоархитектоника печени изменений не претерпевала, Vv фиброза составляла 3,3±0,7.
К концу эксперимента с введением лечебной дозы «Салсоколлина» результаты нашего комплексного исследования гистологических препаратов, как видно из приведенной выше таблицы, подтвердили достоверное снижение объемных показателей, отражающих деструктивные изменения в паренхиме органа, и возрастание показателей, отражающих репаративные процессы в ткани печени.
Так, существенным образом возрастало количество двухъядерных гепатоцитов. Появлялось большое количество гипертрофированных печеночных клеток, что свидетельствовало о внутриклеточных репаративных процессах (рис. 13).
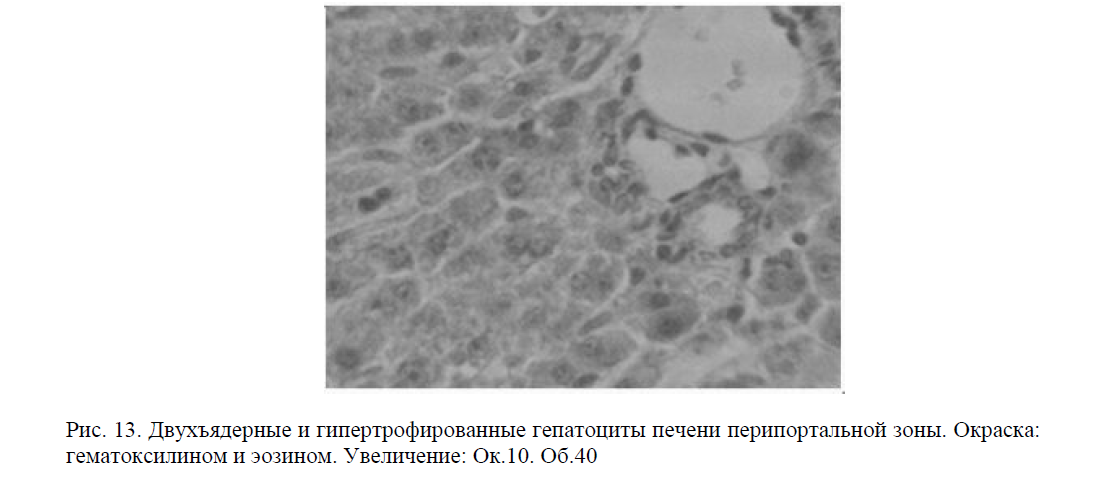
Рис. 13. Двухъядерные и гипертрофированные гепатоциты печени перипортальной зоны. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
При микроскопическом исследовании ткани печени по сравнению с нелеченной группой патоморфологические изменения были менее выражены. Некрозы паренхимы в группе, получавшей фенилгидразин, носили мелкоочаговый или фокальный характер, объемная доля которых была значительно меньше чем в группах сравнения, а в группах, получавших нитрозодиметиламин и изониазид, не выявлялись.
Портальные тракты выглядели несколько расширенными, умеренно или скудно инфильтрированными. В инфильтрате преимущественно определялись клетки лимфацитарного ряда. Инфильтраты, как правило, не выходили за пределы портальной стромы, которая была в этой группе очаговосклерозирована. Существенно снижались объемные показатели воспалительно-клеточной инфильтрации как в портальных трактах, так и внутри долек (рис. 14).
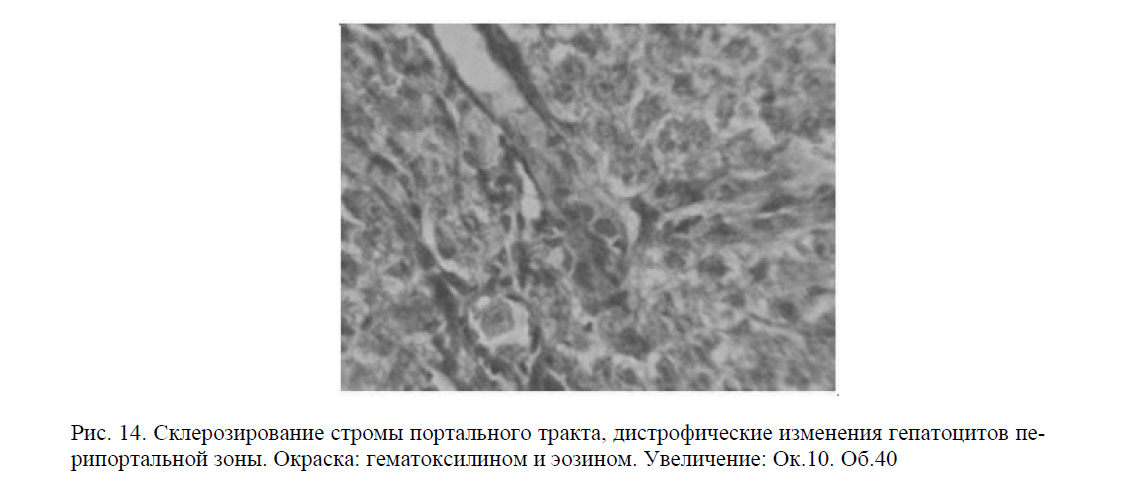
Рис. 14. Склерозирование стромы портального тракта, дистрофические изменения гепатоцитов перипортальной зоны. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
Объемная доля дистрофически измененных гепатоцитов также существенно снижалась и носила белковый зернистый характер. Признаки жировой или вакуольной дистрофии не обнаруживались.
При постановке PAS-реакции на гликоген обнаруживалось его равномерное распределение в цитоплазме. Чаще встречались частицы гликогена средних размеров (рис. 15).

Рис. 15. Гликоген печени с мелко-зернистой диффузной реакцией в гепатоцитах печени. Окраска: гематоксилином и эозином. Увеличение: Ок.10. Об.40
Таким образом, при длительном введении различных химических соединений гидразина наблюдались патоморфологические изменения, которые начинались с гемомикроциркуляторных нарушений в виде полнокровия вен, нарушения проницаемости стенки сосудов, кровоизлияний в окружающие ткани с дальнейшим развитием деструктивных изменений функциональной паренхимы. Глубина и степень выраженности морфологических изменений находились в прямой зависимости от вида использованного химического соединения гидразина.
Наиболее выраженные деструктивные изменения печени, сопровождающиеся интенсивной инфильтрацией портальных трактов и внутри дольки мононуклеарными клетками, а также развитием постнекротического фиброза, обнаруживались при интоксикации фенилгидразином и гидразинсульфатом и в меньшей степени — НДМА и изониазидом.
При введении препарата «Салсоколлин» степень выраженности морфологических изменений печени была значительно меньше, чем при интоксикации гидразинами, что свидетельствует о благоприятном влиянии данного препарата на печень.
Список литературы
- Химический энциклопедический словарь. — М.: Наука, 1988. — Т. 1. — С. 547–550.
- Juchan M.R. et. al. // Drug metabol. Rev. — 1972. — V. 1. — P. 71–100.
- Toth B. // J.Cancer Rez. — 1980. — V. 97. — P. 97–108.
- Богданов Н.А. Патология, клиника и терапия поражений жидкими ракетными топливами. — Л.: ВМОЛА, —С. 36–38.
- Портянная Н.И., Осипенко Б.Г., Москадынова Г.А., Новохатский Н.К. и др. К биохимическому механизму токсического действия гидразинов / 1-й Съезд токсикологов России: Тезисы докл. — М., 1998. — С.
- Авакян А.Х. Новые молекулярные критерии оценки токсического действия производных гидразина. Активные формы кислорода как ключевые агенты в механизме токсичности // Фармакология и токсикология. — 1990. — Т. 53. — N — С. 70–73.