С каждым годом в металлургическое производство вовлекается все большее количество мышьяксодержащего сырья, при переработке которого по традиционным схемам образуются токсичные отходы, которые ухудшают экологическую обстановку в прилегающих районах, а также требуют организации дорогостоящих спецзахоронений.
При пирометаллургической переработке полиметаллического никель-, мышьяксодержащего сырья основное количество мышьяка распределяется между всеми продуктами, из которых наиболее концентрированным по мышьяку является шпейза. В [1] отмечается, что с целью извлечения мышьяка из никелевых шпейз, они подвергаются обжигу намертво, в результате чего арсениды никеля окисляются с образованием оксидов и арсенатов. При переработке других промпродуктов никель извлекается рядом пиро-, гидрометаллургических или комбинированных схем [2-6].
Одним из перспективных методов деарсенации промпродуктов является вакуумтермическая возгонка мышьяка в процессе сульфидирования [7].
В работе выполнен термодинамический анализ данного процесса путем расчета изменения энергии Гиббса ряда предполагаемых реакций взаимодействия диарсенида никеля с элементной серой в зависимости от температуры и давления.
Расчет изменения энергии Гиббса предполагаемых реакций взаимодействия диарсенида никеля (NiAs2) с элементной серой при атмосферном давлении с выделением в газовую фазу сульфидной или элементной форм мышьяка выполнен по программе HSC-5 фирмы Outоkumpu [8]. Уравнения реакций составлены для 1 моля NiAs2.
Анализ 230 предполагаемых реакций сульфидирования диарсенида никеля парами элементной серы показал, что при расходе серы, не превышающем 2,5 моля/моль, наибольшую вероятность имеет реакция с максимальным количеством серы, в ходе которой образуется дисульфид никеля (NiS2), а мышьяк возгоняется в виде трисульфида (As2S3). Чуть меньшую вероятность имеет реакция сульфидирования NiAs2 с образованием NiS2 и As4S4, что связано с различными теплотами образования сульфидов мышьяка.
В интервале температур, близких к температурам деарсенации NiAs2 без сульфидирования (800-900 К), значения изменения энергии Гиббса всех рассмотренных реакций изменяются в интервале от +57,549 (образуются Ni3S2, Ni5As2, As2) до -137,231 (образуются NiS2, As2S3) кДж/моль.
При расположении полученных реакций в группы по возрастанию количества реагируемой серы, приходящейся на 1 моль NiAs2, отмечено, что при расходе серы до 0,5 моля/моль мышьяк возгоняется в виде элементного. Наиболее вероятной является реакция с образованием NiS2, Ni11As8, NiAsS и возгонкой мышьяка в виде As4. Расход серы составляет 0,32 моля/моль. В результате наименее вероятной реакции образуются Ni3S2, Ni5As2 и As2 (расход серы – 0,32 моля/моль).
При увеличении расхода сульфидизатора от 0,5 до 0,67 моля/моль, наряду с элементным мышьяком, в газовую фазу выделяются и его сульфиды. В данной группе наиболее вероятна реакция (расход серы 0,64 моля/моль), в течение которой образуется Ni11As8, а мышьяк возгоняется в виде тетрасульфида. Также в этой группе довольно вероятны реакции при расходе серы 0,6 и 0,65 моль с получением, кроме Ni11As8 и As4S4, NiAs (обе) и Ni5As2 (расход серы 0,65 моля/моль). Менее вероятна реакция с образованием NiS и As2 (расход серы 0,5 моля/моль), а также реакция с образованием NiAsS, NiS и As2 (расход серы 0,5 моля/моль).
При дальнейшем увеличении расхода серы свыше 0,67 моля мышьяк возгоняется в основном в виде сульфидов, исключение составляют реакции при расходе серы в 1 моль/моль, в результате которых образуется дисульфид никеля (NiS2), а мышьяк возгоняется в виде As2 или As4. Причем реакция с возгонкой мышьяка в димерном составе менее вероятна, чем реакция с возгонкой As4, что связано с разницей теплот образования As4 и As2. Наибольшую вероятность имеют реакции, протекающие при расходе серы 2 и 2,5 моля/моль, в результате которых образуется NiS2, а мышьяк удаляется в виде As2S3 или As4S4. Менее вероятна реакция с получением дисульфида никеля и возгонкой мышьяка в димерной форме (расход серы 1 моль/моль, ΔG = 3,763 кДж/моль).
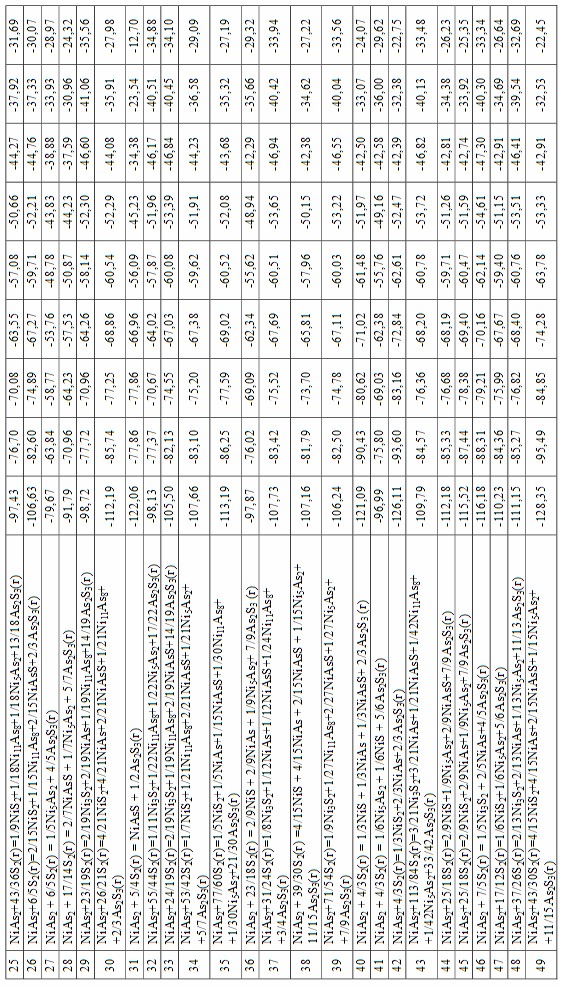
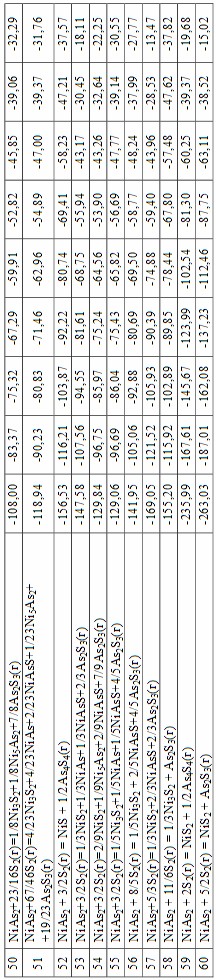
Более детальный термодинамический анализ проведен с наиболее вероятными реакциями, выбранными из 230 реакций, сформированных в группы в зависимости от формы возгоняемого мышьяка (As2, As4, As2S3, As4S4). Результаты представлены в табл. 1. Как видно, наиболее вероятны реакции с удалением в газовую фазу трисульфида мышьяка. Исключение составляют реакции 8, 20, 52, 59, в которых образуется тетрасульфид мышьяка.
При расходе серы до 1 моля/моль наиболее вероятна реакция 3 с образованием Ni11As8, менее вероятна реакция 1 с образованием NiAs. При расходе сульфидизатора в 1 моль/моль наибольшую вероятность имеет реакция 8, в ходе которой образуются Ni5As2, NiS, As4S4, менее вероятна реакция 6 с образованием NiAsS, NiAs, As2S3. При дальнейшем увеличении количества серы (реакции 9-13) наиболее вероятно образование NiS2, Ni11As8 (реакция 13), менее – совместное образование NiAsS, Ni11As8, Ni5As2, NiAs (реакция 10). При расходе серы 1,12-1,13 моля/моль (реакции 14-16) более вероятна реакция 14, реакции 15 и 16 имеют почти одинаковую термодинамическую вероятность. При увеличении расхода серы до 1,14 моля/моль (реакции 17-21) более вероятным является образование NiS2 и Ni5As2 (реакция 20), менее вероятно образование NiAsS, Ni5As2, NiAs (реакция 17).
При расходе серы 1,17-1,21 моля/моль (реакции 22-29) наибольшую вероятность имеют реакции с образованием NiS2, Ni11As8, NiAsS (реакция 26) и Ni3S2, NiAs, Ni11As8 (реакция 29). Менее вероятна реакция 27, в ходе которой образуется Ni5As2.
При расходе серы 1,24-1,29 моля/моль (реакции 30-37) наиболее вероятна реакция 30 с образованием NiS2, NiAs, NiAsS, Ni11As8, менее вероятна реакция 36 с образованием NiS, NiAs, Ni5As2.
При дальнейшем увеличении расхода серы до 2,5 моля/моль наиболее термодинамически вероятно протекание сульфидирования NiAs2 элементной серой с образованием NiS2, менее – NiS2, Ni5As2, NiAsS.
 -30
-30
-40 54 1
6
GP900, кДж/моль
-40 8
 -50 3
-50 3
13
-60
-70 14 20
GP900, кДж/моль
-50
-60
-70
17
10 27
36,41
15
47
-80
-90
-100
-110
-120
-130
-140
26
30
49 42
60
0,1 1 10
Р, кПа 100
0,1 1 10
Р, кПа 100
а) б)
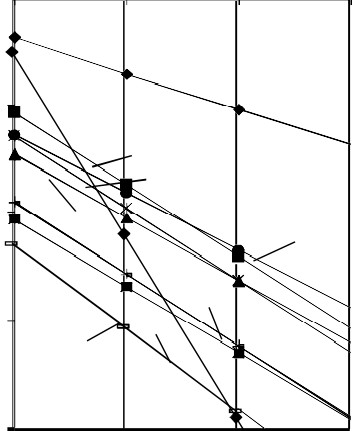
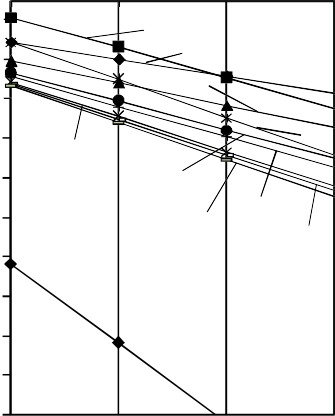
Зависимость изменения энергии Гиббса реакций взаимодействия NiAs2 с парами элементной серы от давления при 700 К: а – менее вероятные реакции; б – более вероятные реакции

Как известно [9], в реакциях с участием газовой фазы понижение давления сдвигает равновесие в сторону увеличения количества образовавшейся газовой фазы. Расчет изменения энергии Гиббса при пониженном давлении проводили по выражению:

ΔGP = ΔGT+ ΔnRTlnP,
Т
где ΔGP и ΔGТ, кДж - изменение энергии Гиббса при пониженном и атмоcферном давлении
Т
соответственно, Δn – изменение количества молей газообразной фазы в ходе реакции, R – универсальная газовая постоянная, кДж/моль*К, Т – температура, К, Р – остаточное давление, атм.
Результаты расчета изменения энергии Гиббса при пониженном давлении для 700 К (рисунок 1) показали, что с понижением давления вероятность протекания большинства рассмотренных реакций понижается, а также изменяется предпочтительность некоторых реакций, что объясняется различным количеством и свойством образующейся газовой фазы в реакциях и, соответственно, разным влиянием на изменение ΔGP .
Т
Таким образом, термодинамическим анализом реакций взаимодействия NiAs2 с элементной серой показано, что вероятность протекания и состав конденсированных фаз определяется расходом сульфидизатора, температурой и давлением, причем при пониженном давлении наиболее вероятна реакция взаимодействия NiAs2 с парами элементной серы с образованием дисульфида никеля и As2S3 в конденсированной фазе (реакция 60).
ЛИТЕРАТУРА
- Чижиков Д.М. Металлургия тяжелых цветных металлов. М., Л.: Изд-во АН СССР, 1948. – 1057 с.
- Позняков В.Я., Четвертков М.С. Поведение свинца, цинка и мышьяка в производстве никеля из сульфидных руд // Цветные металлы. – 1971. – № 4. – С. 18-23.
- Цветная металлургия Восточной Германии под ред. Фролова В.А., Металлургиздат, 1947.
- Худяков И.Ф., Тихонов А.О., Деев В.И., Набойченко С. Металлургия меди, никеля и кобальта. М.: Металлургия, 1977. – 262 с.
- Лисицына Т.И. Переработка мышьяково-никелевой шпейзы методом хлорирования // Бюллетень Минцветмет ССР, ЦИИН 1957. – № 6. – С. 17-20.
- Исабаев С.М., Мильке Э.Г., Кузгибекова Х.М. и др. Способ переработки шпейзы // А.С. 1028733 СССР. Опубл Б.И. 1983, № 20.
- Нестеров В.Н., Исакова Р.А. Переработка шпейзы методом возгонки под вакуумом // Известия АН КазССР. – 1958. – Вып. 3. – С. 54-60.
- HSC Chemistry 5.11. Программа фирмы Outokumpu. 2002 г.
- Крестовников А.Н., Владимиров Л.П., Гуляницкий Б.С. Фишер А.Я. Справочник по расчетам равновесий металлургических реакций. М. 1963. 416 с.