Лимфома ХоДжкина (ЛГ) является оДной из наиболее распространенных злокачественных лимфоиДных опухолей. ЛГ составляет не более 0,5% от общей распространенности рака; оДнако его необычная биология, эпиДемиология и реакция на лечение привлекают пристальное внимание. ЭпиДемиология злокачественных лимфом варьируется в преДелах и межДу географическими регионами.
Лимфома Ходжкина (ЛХ) представляет собой злокачественное новообразование из лимфоидной ткани, В-клеточного происхождения, , морфологическим субстратом являются гигантские многоядерные клетки БерезовскогоРидШтернберга и одноядерные клетки Ходжкина, располагающиеся в своеобразном клеточном скоплении «гранулеме», образованной смесью опухолевых и неопухолевых реактивных клеток: лимфоцитов, нейтрофилов, плазмоцитов, иногда окруженных волокнами коллагена. Клетки БерезовскогоРидШтернберга являются производными В-клеток зародышевых центров лимфатической ткани. Они составляют лишь около 1 % от массы всей опухолевой ткани.
ЛХ является редким новообразованием, частота которого значительно варьируется в зависимости от возраста, пола, этнической принадлежности, географического положения и социально-экономического статуса.
Показатели заболеваемости выше в более развитых регионах мира и иниже в Азии, причем чаще болеют мужчины. В Соединенных Штатах, по оценкам 2013 года было зарегистрировано около 9 300 новых случаев ЛХ, заболеваемость составила 2,8 на 100 000 человек в год [2].
Хотя в структуре общей онкологической заболеваемости на долю ЛХ приходится примерно 0,67%, ЛХ составляют около 30% случаев от общего числа лимфом. Важно отметить, что в возрасте от 15 до 24 лет каждый шестой онкологический диагноз это ЛХ[1].
Отличительной чертой эпидемиологии ЛХ является ее вариабельность по возрасту при постановке диагноза. Это представлено в промышленно развитых странах хорошо известной бимодальной кривой, показывающей два пика: самый значительный для молодых людей (15-34 лет) и второй, наблюдаемый в более позднем возрасте (старше 50 лет). Эти пики состоят в основном из разных подтипов заболевания, вариант нодулярного склероза преимущественно представлена в более раннем пиковом возрасте, а смешанноклеточный вариант преобладает в более позднем пиковом возрасте[3].
Несмотря на относительно низкую заболеваемость и низкий риск на протяжении жизни, ЛХ составляет 15% всех случаев рака у молодых людей, что оказывает большое влияние на качество жизни.
В настоящее время проводятся различные эпидемиологические исследования ЛХ, которые позволят более полно изучить природу этого заболевания, выявить географические, этнические, социально-демографические и экономические факторы, влияющие на развитие этой патологии.
Целью нашей работы былоотразить особенности эпидемиологии ЛХ в Казахстане,
Материалы и методы.
Для того, чтобы осветить вопросы эпидемиологии ЛХ мы ознакомились с данными Международного агентства по исследованию рака (IARC), GLOBOCAN 2012 [4], в котором отражены данные по заболеваемости онкопроцессами и смертность от них во всем мире, опубликованы в 2013г. Интересные данные были представлены европейской исследовательской группой в статье «Эпидемиологический обзор лимфомы Ходжкина в бассейне Средиземного моря», опубликованной в журнале Mediterranean Journal of Hematology and Infectious Disease в июле 2014г. Данные о смертности от ЛХ и временных тенденциях для указанных средиземноморских стран были получены из онлайновой базы данных о смертности Всемирной организации здравоохранения (ВОЗ) [5].
Были изучены статистические данные онкологической службы Республики Казахстан за последние годы , что позволило проанализировать показатели заболеваемости, смертности, запущенности, распределение по регионам Казахстана, динамику заболеваемости ЛХ.
Здесь и далее мы ссылаемся на классический вариант ЛХ . Эпидемиология ЛХ.
Эпидемиология Лимфомы Ходжкина, мировые данные.
Классификация лимфоидных новообразований Всемирной организации здравоохранения (ВОЗ) продолжает развиваться, признавая различные варианты лимфопролиферативных заболеваний, которые включают в себя не только ЛХ, Неходжкинскую лимфомы (НХЛ), но также новообразования из плазматических клеток и лимфоидные лейкозы[6]. Согласно оценкам 2012 года, было зарегистрировано почти 566 000 новых случаев лимфомы во всем мире и около 305 000 смертей от этого заболевания[7]. Каждый отдельный вариант лимфопролиферативного заболевания в принципе не имеет большого значения в общей картине заболеваемости злокачественными новообразованиями, но в совокупности лимфомы занимают седьмое место по частоте выявляемости среди онкопатологии в мире [7].
По подсчетам GLOBOCAN, в 2012 году было зафиксировано более 385 000 случаев НХЛ и почти 66 000 случаев ЛХ, а в
2012 году около 200 000 смертей от НХЛ и более 25 000 смертей от ЛХ[8] . Для НХЛ новые случаи чаще выявлялись в регионах с высоким , средним и низким уровнем дохода; однако смертность чаще происходила в странах со средним и низким доходом (62%). В том же году для ЛХ подавляющее большинство новых случаев и смертей (56% и 75%, соответственно) произошло в регионах с низким уровнем дохода в мире. Регионы с высоким уровнем включают все регионы Европы, Северной Америки, Австралии / Новой Зеландии и Японии. В регионы со средним и низким уровнем дохода входят все регионы Африки, Азии (кроме Японии), Латинской Америки и Карибского бассейна, Меланезии, Микронезии и Полинезии. Прогнозы показывают, что как частота заболеваемости, так и смертность для НХЛ и ЛХ увеличится к 2035 году, возможно, из-за улучшения методов диагностики, индустриализации, старения населения и роста ВИЧ-инфекции в некоторых регионах [8-9].
ЛХ составляла в 2012 году не более 0,5% от общей нагрузки на рак во всем мире; однако его необычная биология, эпидемиология и положительный ответ на лечение привлекают пристальное внимание[8]. Общая частота ЛХ значительно варьируется по всему миру Патогенез данного географического несоответствия не известен; однако факторы окружающей среды и образа жизни были теоретизированы как потенциальные факторы.
В отличие от НХЛ, которая показывает экспоненциальное увеличение возрастной заболеваемости, возрастные показатели заболеваемости ЛХ являются бимодальными, причем первый пик наблюдается в возрасте от 15 до 34 лет, а второй после 60 лет в европейской, американской, латиноамериканской и австралийской популяциях. В странах со средним уровнем дохода заболеваемость ЛХ высока в раннем детстве и среди самых старых возрастных групп. Высокая заболеваемость в детском возрасте связана с повышенным риском молодого взрослого варианта ЛХ, что свидетельствует о задержке контакта с обычным инфекционным агентом. Тогда как для детей, живущих в менее благоприятных условиях жизни характерен высокий уровень заболеваемости лимфомами.
Прогресс в лечении, улучшение диагностических возможностей, и доступ к медицинской помощи сделали ЛХ в значительной степени излечимой во многих районах мира. Сообщается о снижении смертности более чем на 75% в Северной Америке, Западной Европе и Японии[11]. . Заметное снижение смертности ЛХ наблюдалось также в большинстве стран Латинской Америки, за исключением Кубы, Коста-Рики, Мексики и Венесуэлы.
В 1971 году международный опрос ЛХ показал, что распределение бимодального возраста в западном мире коррелировали с уровнем социально-экономического развития населения . В развивающихся странах заболеваемость ЛХ была бы относительно высокой у мальчиков, но у молодых взрослых мужчин была невысока, в отличие от развитых регионов, где заболеваемость ЛХ была низкой у детей, но высокая у молодых людей. Другие данные свидетельствуют о том, что ЛХ в развивающихся регионах преобладает подтипами смешанной клеточности или лимфоцитов, а в развитых регионах преобладает подтип нодулярного склероза [ 12 ]. Экологическая корреляция между социально-экономическим уровнем и показателями заболеваемости ЛХ показала противоположную роль детской среды в отношении риска ЛХ у детей и молодых людей. Одна из моделей предполагала, что ЛХ является редким последствием общей инфекции, риск которой будет увеличиваться, когда возраст заражения задерживается, например, путем улучшения условий жизни .
Доказательства, подтверждающие, что социальноэкономическая среда детства влияет на риск ЛХ в молодом возрасте, были предоставлены из нескольких исследований. Например, в исследовании учитывались такие критерии как уровень социально-экономической обеспеченности в детстве, тип жилья, образование матери и социальный класс по отцовской линии, результаты ассоциировались с повышенным риском ЛХ у молодых взрослых, чем в детском возрасте[ 12].
Таким образом, эти результаты подтверждают многофакторную модель заболевания для патогенеза ЛХ с участием как генетических факторов, так и факторов риска окружающей среды[ 13].
Эпидемиологическая ситуация по лимфомам в Республике Казахстан (РК).
В настоящее время в РК работает онкологический регистр (cancer-регистр), благодаря которому появилась возможность получать информацию по основным эпидемиологическим показателям связанным с лимфопролиферативными заболеваниями. К сожалению пока нет возможности получить полную информацию по отдельно взятому варианту лимфомы. Но зная, что около 30% лимфом это ЛХ, можно получить представление по эпидемиологической ситуации с ЛХ в РК.
Абсолютное число пациентов с диагнозом злокачественная лимфома, состоящих на диспансерном учете, в 2016г. составило 4104, заболеваемость лимфомой в абсолютных цифрах 776 случая(4,40 /00), темп прироста заболеваемости 9,0% за год ( в сравнении с 2015г.).
Рисунок 1

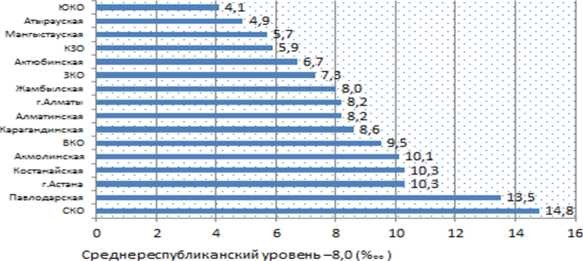
Наиболее высокий уровень заболеваемости, выше среднего республиканского ( 8 на 100 000 населения), в таких регионах как: Акмолинская , Восточно-Казахстанская , Карагандинская, Костанайская, Павлодарская, Северо-Казахстанская области и г.Астана. Отчасти это связано с этническим составом населения, возможно есть связь с доступностью диагностики. Большое значение имеет возможности морфологической верификации. В последнее десятилетие в стандарты диагностики лимфопролиферативных заболеваний прочновошли гистологические и иммунологический методы исследования. Согласно Протоколам диагностики и лечения в РК эти методы верификации лимфом являются обязательными.
Давайте посмотрим какова ситуация по морфологической диагностике лимфом в РК.
О 20 40 60 80 1О0 120
Среднереспубликанский уровень морфологической верификации -86,4%
Морфологическая верификация лимфом, распределение по областям
Рисунок 2

Морфологическая верификация диагноза лимфомы в среднем по Казахстану составляет 88,6%, наиболее высокие показатели в Северо-Казахстанской, Восточно-Казахстанской, Павлодарской областях и г. Астана.
Огромное значение в плане прогноза имеет стадия заболевания. Каков процент ранних стадий в РК?
Удельный вес Іи 2 стадии по регионам
Атъ pay:-ля
А-.«лолиос-ля Паглодарс-дя
•_Аг-«-а Жамбвлс -ля юко А<тэо6мос«ля ско •-Azs'j-в Костаоаос-ля ВКО
ЗКО
Алѵятмкіая
КЗО


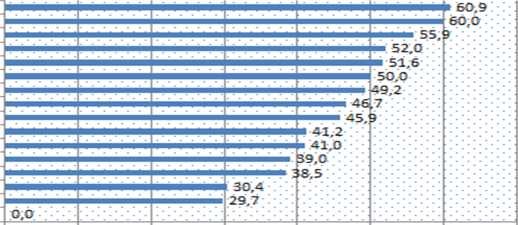
Среднереспубликанский уровень —44,5%
Рисунок 3
В среднем по РК процент выявления ранних стадий лимфом составляет 44,5%. Самый большой процент I и II стадии заболевания выявлен в Карагандинской (60,9%), Атырауской (60,0%) и Акмолинской(55,9%) областях. Самый низкий в Мангыстауской (38,5%), Западно-Казахстанской (30,4%) и Алматинской (29,7%) областях. Что касается поздних (запущенных или распространенных) стадий заболевания.

Среднереспубликанский уровень выявления IV стадии лимфом составил 8,3%, причем наиболее высокий процент выявления в Атырауской (30%), Жамбылской областях (20,6%), наименьший в г.Алматы (2,4%) и СевероКазахстанской (5,4%) области.
Основным методом терапии лимфопролиферативных заболеваний в настоящее время является химиотерапевтическое лечение, 85-88% больных с впервые установленным диагнозом лимфома получают специализированное лечение, причем в 65% случаев это лекарственная терапия (химиотерапия).
Одногодичная летальность у пациентов с лимфомой достаточно высокая 26,9%, что говорит о высокой агрессивности опухолевого процесса. Для наглядности годичная летальность при раке молочной железы -6,6%, рак тела матки-10,6%, рак предстательной железы 11,5%. Пятилетняя выживаемость больных с диагнозом лимфома составила в 2016г. 53,9%.
В структуре заболеваемости отмечается некоторое преобладание мужчин над женщинами, приблизительно 2,3 на 100 000 населения мужчины к 2, 1 на 100 000 населения женщины.
Смертность от лимфомы в 2016г. в абсолютных числах 332 случая (1,8 на 100тыс. населения), в динамике наблюдается тенденция к снижению смертности , например, в 2013г. этот показатель был равен 2,1 на 100 тыс. населения.
В общей структуре онкопатологии заболевания лимфоидной и кроветворной системы, в том числе лимфомы, занимают 8 ранговую позицию, около 4% от общего количества, в структуре смертности гемобластозы тоже занимают 8 место[14].
Среднереспубликанский уровень смертности составляет 1,8 на 100 000 населения. Наибольший показатель смертности от злокачественных лимфом в Карагандинской (2,8 на 100 000 населения ), Павлодарской (3,3 на 100 000 населения), СевероКазахстанской ( 3,1 на 100 000 населения) областях.
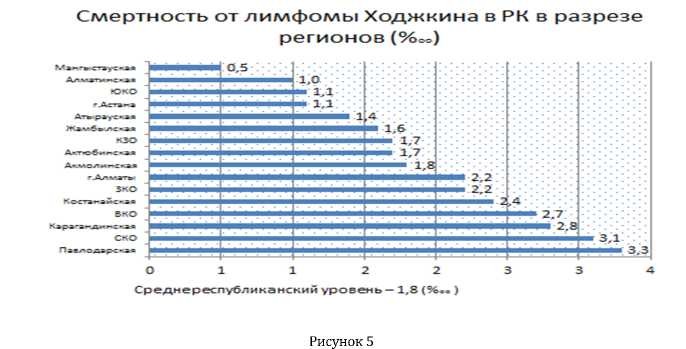
Среднереспубликанский уровень смертности составляет 1,8 на 100 000 населения. Наибольший показатель смертности от злокачественных лимфом в Карагандинской (2,8 на 100 000 населения ), Павлодарской (3,3 на 100 000 населения), СевероКазахстанской ( 3,1 на 100 000 населения) областях.
Выводы: Эпидемиология злокачественных лимфом варьируется внутри и между географическими регионами. Ряд исследований показывает, что характеристики, показатели заболеваемости и выживаемость различных подтипов лимфомы для некоторых расовых групп отличаются от других. Лучшее понимание этих факторов будет иметь важное значение для выявления изменяющихся барьеров в лечении и облегчения шагов по улучшению результатов для всех пациентов. Имеет бимодальное распределение с увеличением заболеваемости у молодых людей, а также у пациентов 55 лет и старше.
В общей структуре онкопатологии заболевания лимфоидной и кроветворной системы, в том числе лимфомы, входят в первую десятку онкопатологий, в Казахстане занимают 8 ранговую позицию, около 4% от общего количества, в структуре смертности гемобластозы тоже занимают 8 место.Наиболее высокий уровень заболеваемости лимфомой в таких регионах как: Акмолинская , Восточно-Казахстанская , Карагандинская, Костанайская, Павлодарская, СевероКазахстанская области и г.Астана. Отчасти это связано с этническим составом населения, возможно есть связь с доступностью диагностики. . Наибольший показатель смертности от злокачественных лимфом в Карагандинской , Павлодарской , Северо-Казахстанской областях.
СПИСОК ЛИТЕРАТУРЫ
- Howlader N, Noone AM, Krapcho M, Garshell J, Neyman N, Altekruse SF, Kosary CL, Yu M, Ruhl J, Tatalovich Z, Cho H, Mariotto A, Lewis DR, Chen HS, Feuer EJ, Cronin KA, editors. SEER. Рак, статистический обзор, 1975-2010. Bethesda: National Cancer Institute, 2011. 248 р.
- Каверзнева М.М., Кременецкая А.М., Моисеева Т.Н., Воробьев А.И. Лимфогранулематоз. Руководство по гематологии. М.: 2007. С. 389-308.
- Cozen W, Katz J, Mack TM. Зависимость риска возникновения болезни Ходжкина в Лос Анжелесе от клеточного типа // Cancer Epidemiol Biomark Prev. 1992. №1(4). Р. 261-268.
- Ferlay J, Soerjomataram I, Ervik M, Dikshit R, Eser S, Mathers C, Rebelo M, Parkin DM, Forman D, Bray F. GLOBOCAN 2012 v10. Заболеваемость раком и смертность в мире.: IARC Cancer Base No. 11. Lyon, France: International Agency for Research on Cancer, 2013. 394 р.
- ВОЗ. Информационная система. WHO Mortality Database. 2007.
- Swerdlow SH, Campo E, Pileri SA и др. Пересмотр классификации лимфоидных новообразований Всемирной организации здравоохранения в 2016 году // Кровь. 2016. №127. С. 2375-2390.
- Jaffe E, Swerdlow S, Вардиман J. Гематопоэтические и лимфоидные злокачественные опухоли // Всемирный отчет о раке 2014 года. Лион, Франция: Международное агентство по изучению рака, Всемирная организация здравоохранения, 2014. С. 482494.
- Muller A.M, Igorst H, Mertelsman R. и др. Эпидемиология неходжкинской лимфомы (НХЛ): тенденции, географическое распределение и этиология // Энн Гематол. 2005. №84. Р. 1-12.
- Baris D, Zahm SH. Эпидемиология лимфом // Curr Opin Oncol. 2000. №12. С. 383-394.
- Health Disparities and the Global Landscape of Lymphoma Care Today // Annals of Oncology. 2013. №24(9). Р. 2245-2255.
- Macmacon B. Эпидемиологические данные о характере болезни Ходжкина // Рак. 1957. №10. С. 1045-1054.
- Macmacon B. Эпидемиология болезни Ходжкина // Рак. 1966. №26. С. 1189-2011.
- Massimiliano Salati,1 Marina Cesaretti,1 Matteo Macchia,1 Mufid El Mistiri,2 and Massimo Federico. Эпидемиологический обзор Лимфомы Ходжкина в Средиземноморском бассейне // Mediterr J Hematol Infect Dis. 2014. №6(1). Р. 45-52.
- «Показатели онкологической службы Республики Казахстан за 2014-2016гг», статистические материалы.