Внедрение современных программных протоколов полихимиотерапии гемабластозов позволили достичь эффективных результатов в лечении острого лимфобластного лейкоза у детей. В статье представлено состояние углеводного обмена у детей с острым лимфобластным лейкозом на фоне глюкокортикостероидной терапии.
Введение. Острый лимфобластный лейкоз (ОЛЛ) наиболее частое заболевание среди гемабластозов у детей [1, 2]. Эффективные результаты в лечении ОЛЛ достигнуты благодаря качественно разработанным протоколам и внедрением современных, сложных и интенсивных программ полихимиотерапии (ПХТ) с использованием четко определенных доз и комбинаций химиопрепаратов в жестко установленные сроки [3, 4]. В программе лечения ОЛЛ базисными препаратами являются глюкокортикостероиды (ГКС) [5]. Общеизвестно, что при КГС-терапии ОЛЛ у детей нередко возникают нарушения углеводного обмена вплоть до развития стероидного сахарного диабета (ССД). По отдельным литературным данным развитие осложнений углеводного обмена, таких как стероидный сахарный диабет (ССД) у детей с ОЛЛ за последние десятилетия составила от 2,8% до 8,7%. у детей, больных ОЛЛ, находившихся на ПХТ [5, 6]. Надо отметить, что ССД в 69% случаев манифестировал на противорецидивном лечении и в 92% развивался на терапии дексаметазоном, чем на преднизолоне [5].
Цель исследования. Изучить состояние углеводного обмена у детей с острым лимфобластным лейкозом на фоне глюкокортикостероидной терапии.
Материалы и методы исследования. Ретроспективно изучены 526 медицинских карт стационарных больных детей ОЛЛ, находившихся на лечении в онкогематологических отделениях НЦ ПиДХ МЗ РК за последние 18 месяцев (с января 2017 года по июнь 2018 года). В соответствие с поставленной целью исследования, отобрано 70 карт 70 больных с ОЛЛ и нарушенным углеводным обменом (НУО), получавшие ГКС-терапию по протоколу AIEOP BFM-ALL 2009 (протокол I, протокол II) [2,3].
У всех обследованных больных анализировались жалобы, клинические признаки сахарного диабета (полидипсия, полиурия, похудание, сухость кожных покровов), оценка параметров массы тела на день поступления и на момент выявленного НУО. Углеводный обмен оценивался согласно диагностическим критериям сахарного диабета и других нарушений углеводного обмена, рекомендованным Комитетом экспертов ВОЗ (1999г.). Протокол лабораторноинструментальных методов исследования включал в себяопределение уровней гликемии, амилазы в биохимическом анализе крови, оценка показателей ОАМ (удельная плотность мочи, наличие кетоновых тел и глюкозурии), результатов УЗИ параметров поджелудочной железы и печени.
Статистическая обработка: офисная система Microsoft Excel XP (арифметическое среднее (М), стандартная ошибка средней (m), оценка достоверности (t-критерий Стьюдента), коэффициент корреляции (r)).
Результаты исследования. Среди отобранных 70 больных с ОЛЛ по гендерному признаку мальчиков преобладало в 2,04 раза (мальчиков 67,14%, девочек 32,86%), что также согласуется с литературными данными [5].
Оценить характерные жалобы и клинические проявления НУО у больных с ООЛ сложно, так как симптомы сходны и с основным заболеванием у детей. Среди анализированных медицинских карт 39 (55,7%) детей предъявляли жалобы на слабость, 29 (41,4%) на вялость, 23 (32,9%) на снижение массы тела. На момент выявленного НУО в клинике преобладала слабость (68,6%), похудание (15,7%), гепатомегалия (8,6%), боли в животе (5,7%), тошнота (4,3%). При анализе массы тела больных с ОЛЛ на момент диагностированного НУО, отмечено достоверное снижение у 11 (15,7%) детей (< 0,002), как проявления «похудание» при углеводном нарушении. Классические признаки СД, как жажда и полиурия у детей не выявлены, что предполагает патогенетическое течение с развитием инсулинорезистентности периферических тканей.
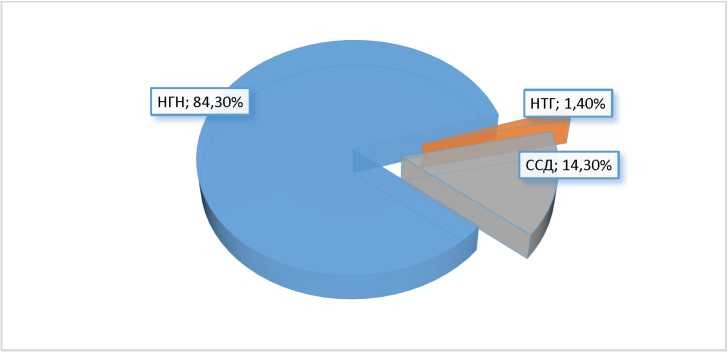
Среди всех больных, подвергшихся ретроспективному анализу нарушения углеводного обмена (ВОЗ, 1999г.) выявлены в 13,3% случаев. В структуре НУО (рисунок 1) отмечено преобладание нарушенной гипергликемии натощак в 5,9 раз относительно выявленного ССД и нарушенной толерантности к глюкозе. Преимущественное влияние на развитие ССД на фоне ГКС-терапии отмечено на фоне приема дексаметазона (у 70,0%), относительно преднизолона (у 30,0%), что связано с выраженным диабетогенным действием первого препарата. Следует отметить, согласно проводимой ПХТ-терапии у 3-х больных (4,3%) в последующем протоколе на фоне лечением ГКС (дексаметазон) отмечалась повторная гипергликемия с показателями характерными для ССД.
Рисунок 1 Структура НУО у больных детей с ОЛЛ на фоне КГС-терапии
При оценке экскреторной функции поджелудочной железы у детей с НУО выявлено достоверное повышение уровня амилазы референсных значений у 3 (4,3%) детей и средний повышенный уровень составил 112,66±5,11 Ед/л (р<0,001), что свидетельствует о развитии панкреатопатии на фоне ГКС терапии или патологических процессов у больных ОЛЛ. При анализе показателей общих анализов мочи специфических изменений, характерных ССД не выявлено.
При ультразвуковом исследовании печени визуализировалось увеличенные размеры правой доли у 82,5% детей, левой доли у 67,5% больных ОЛЛ с диагностированным НУО, среднее значение повышенных показателей долей печени соответственно составили 111,30±16,03 см и 55,07±9,67 см. По результатам УЗИ поджелудочной железы увеличение её головки визуализировалось у 16,2%, тела 13,5%, хвоста 2,7% детей. Сочетание НУО с повышенным уровнем амилазы и увеличенными ультразвуковыми размерами печени и поджелудочной железы выявлены у 8,6% детей (рисунок 2). Анализируя взаимосвязь с повышенными значениями гликемии и увеличенными размерами поджелудочной железы, выявлена сильная прямая взаимосвязь (r=0,88).
0 0,5 1 1,5 2 2,5 3 3,5 4 4,5
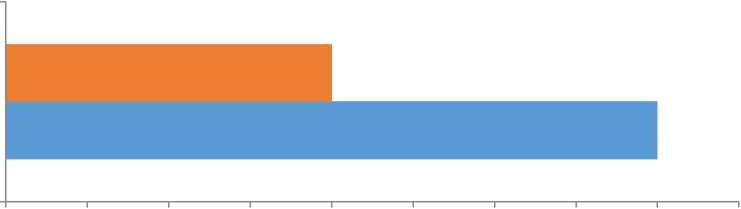
■ увеличение размеров печени, поджелудочной железы, повышение уровня амилазы
■ увеличение печени, поджелудочной железы
Рисунок 2 Сочетание гипергликемии с увеличенными размерами печени, поджелудочной железы и уровня амилазы
Выводы:
У детей с ОЛЛ на фоне проводимой КГС-терапии нарушения углеводного обмена наблюдаются в 13,3 % случаев;
На фоне программного лечения острого лимфобластного лейкоза в 4,3% случаях наблюдаются повторные патологические повышения гликемии на фоне глюкокортикостероидной терапии;
Дексаметазон обладает выраженным диабетогенным действием в 70%, приводящий к развитию сахарного диабета;
Нарушения углеводного обмена у детей с острым лейкозом имеют прямую корреляционную связь с вовлечением патологических изменений в поджелудочной железе (r=0,88);
В группе риска детей с развитием нарушением углеводного обмена необходимо комплексное обследование: контроль гликемии натощак, определение постпрандиальной гликемии, по показаниям проведение стандартного глюкозо-толерантного теста, исследование уровня инсулина;
Детям на фоне ГКС-терапии рекомендуется исследование экскреторной функции поджелудочной железы (определение уровней амилазы в крови) и ее структуры (проведение УЗИ диагностики поджелудочной железы) для исключения панкреатопатии и/или патологических изменениях.
СПИСОК ЛИТЕРАТУРЫ
- Hunger S.P., Mullighan C.G. Acute lymphoblastic leukemia in children // N Engl J Med. 2015. №373(16). Р. 1541-1552
- Клинический протокол диагностики и лечения «Острый лимфобластный лейкоз у детей (первичный)», Одобрен Объединенной комиссией по качеству медицинских услуг МЗ и СР РК от «29» ноября 2016 года Протокол № 16
- Протокол лечения AIEOP-BFM -ALL 2009. Международный общий протокол лечения детей и подростков с острым лимфобластным лейкозом. Редакция 1.2 протокола лечения от 15 апреля 2011 года с включенными несущественными Поправками от 15 апреля 2011 года.
- Румянцева Ю.В., Карачунский А.И., Румянцев А.Г. Оптимизация терапии острого лимфобластного лейкоза у детей России // Педиатрия. 2009. №4(87). С. 19-27.
- Спивак И.И., Богачева М.В., Билялутдинова Д.И., Волкова К.Б., Башарова Е.В. Частота стероидного диабета на программной полихимиотерапии у детей с лимфобластным лейкозом // Педиатрический вестник Южного Урала. 2014. №1-2. С. 30-33.
- Степанова Т.В., Поздняков А.М., Ширяева Л.И., Трубникова Г.В., Осипова Е.В. Осложнение глюкокортикоидной терапии у больных острым лимфобластным лейкозом при применении программы BFM-90 Минск // Труды участников конференции по противоопухолевой терапии. М.: 1996. С.97-103.