В статье проведен обзор всех актуальных на сегодня возможностей повышения эффективности применения программ вспомогательных репродуктивных технологий у пациенток старшего репродуктивного возраста, в том числеметод ПГС: флуоресцентная гибридизация insitu (FISH); а также, методы полногеномного хромосомного скрининга:количественная ПЦР (qPCR), сравнительная геномная гибридизация на микрочипах (aCGH), анализ одиночных нуклеотидов SNP-array, секвенирование нового поколения (New generation sequencing NGS).
Бесплодие является актуальной проблемой во всем мире, частота его в мире не имеет тенденции к снижению и начинает конкурировать с невынашиванием как причина снижения рождаемости в популяции [1,2].
По данным литературы, в том числе ВОЗ, в мире 8-14% супружеских пар репродуктивного возраста страдают бесплодием [1]. По данны ВОЗ в 2010 г. 48,5 мдн пар страдали бесплодием [2,6], причем количество это увеличится в 2,5 раза в связи с сокращением сроков диагностики бесплодия с 5 до 2 лет. В настоящее время в мире от 72,4 до 80 млн человек бесплодны [1,2].
С целью улучшения качества преодоления бесплодия и повышения эффективности во всех возрастных группах женщин ежегодно разрабатываются новые подходы и методы [1,2].
Успешное завершение процедур ВРТ зависит от множества факторов: типа бесплодия, возраста супругов, качества и количества эмбрионов, состояния полости матки, соматического здоровья женщины [3,4].
С увеличением возраста женщины вместе со снижением количества и качетсва ооцитов уменьшается и количество эмбрионов высокого качества, особенно это заметно становится после 37 лет. Так же снижается частота нормального оплодотворения ооцитов [5]. Что, повидимому, связано с нарушением регуляторных механизмов мейоза и клеточного цикла в ооцитах женщин старшего репродуктивного возраста [6].
В литературе имеются противоречивые данные касательно морфологического качества эмбрионов и частоты наступления беременности.
На рисунке 1 представлено исследование AntonioCapalbo и соавторов, которые провели анализ 956 бластоцист женщин старшего репродуктивного возраста.
Частота имплантации
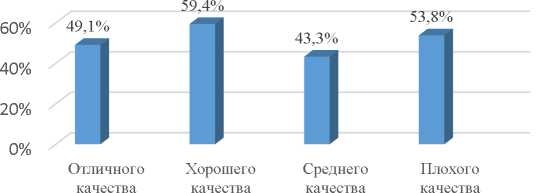
Рисунок 1 Частота имплантации в зависимости от морфологического качества бластоцист,HumanReproduction, Vol.29, No.6 pp. 1173-1181, 2014
Авторы разделили полученные бластоцисты на 4 группы по их морфологической характеристики: отличные >3АА, хорошие 3,4,5,6 АВ и ВА; средние 3,4,5,6 ВВ, АС и ССА; плохие <3ВВ. При переносе в полость матки бластоцисты отличного качества беременность наступила в 49,1% случаев; при переносе бластоцисты хорошего качества 59,4% пациенток забеременели; при переносе бластоцисты среднего качества беременность наступила в 43,3% случаев; при переносе бластоцисты плохого качества 53,8% женщин забеременели. На основании чего авторы пришли к выводу, что морфологическая характеристика эмбрионов не являлась предиктором потенциала развития этих эмбрионов при переносе в полость матки, Рисунок 1[7].
Другие авторы [8] отмечают, что бластоцисты более высокого качества имеют больший потенциал имплантации, что бластоцисты низкого качества.
Выбор эмбриона, наиболее компетентного для переноса в полость матки на основе только его морфологических характеристик, в настоящее время считается недостаточным [3,9]. Даже после переноса эмбриона отличного или хорошего качетсва достичь имплантации удается не всегда [7]. Одной из предполагаемых причин неудач имплантации является наличие хромосомных аномалий (анеуплоидий) у морфологически нормальных эмбрионов [8,10]. Анеуплоидии являются основным фактором, снижающим частоту имплантации, наступления беременности, а также они ассоциированы с высоким уровнем ранних потерь беременности [8,10]. В большом количестве эмбрионов, получаемых при ВРТ, обнаруживаются хромосомные аномалии, особенно в эмбрионах, полученных от женщин старшего репродуктивного возраста [11,12,13]. Значительная часть анеуплоидных эмбрионов способна достичь самых высоких баллов по морфологической шкале, а некоторые эуплоидные эмбрионы часто характеризуются плохой морфологией [13].
Таким образо, слабая зависимость морфологического качества эмбрионов и хромосомного набора привела к введению предимплантационного генетического скрининга ( далее ПГС) в клиническую практику, и широкому распространению метода. ПГС направлен на отбор эмбрионов и перенос в полость матки только эмбрионов с нормальным набором хромосом, что позволяет повысить шансы на имплантацию и наступление беременности [3,7].
ПГС, впервые предложенный Верлинским и Кулиевым в 1996 году [14], основывался на пяти предположениях: 1) большинство циклов оплодотворения invitro имеют отрицательный результат из-за анеуплоидных эмбрионов; 2) устранение аномальных эмбрионов до их переноса, следовательно, улучшит результаты ЭКО; 3) только биопсия трофэктодермы на стадии бластоцисты является репрезентативной для всей трофэктодермы; 4) плоидность трофэктодермы надежно представляет внутреннюю клеточную массу; 5) плоидия не изменяется (то есть, самовосстанавливается) в дальнейшем развитии от стадии бластоцисты [14].
Существует несколько современных подходов для проведения процедуры ПГС [3,10,15,16]: флуоресцентная гибридизация insitu (FISH); а также, методы полногеномного хромосомного скрининга: количественная ПЦР (qPCR), сравнительная геномная гибридизация на микрочипах (aCGH), анализ одиночных нуклеотидов SNP-array, секвенирование нового поколения (Newgenerationsequencing NGS).
Первоначально был предложен PGS полярного тела для диагностики моногенных заболеваний, сцепленных с полом [17], но, в связи с технически более простой процедурой, в практике быстро перешли на более инвазивные биопсии эмбрионов (3-й день) [16].
Этот метод PGS, именуемый так же PGS 1.0, получил широкую популярность, хотя ряд клинических испытаний в Бельгии не смогли продемонстрировать преимущества в результатах [18].
В литературе имеются разноречивые данные касательно результативности ПГС: часть авторов считают, что ПГС улучшает результативность ВРТ, вторая часть что не меняет показатели ЧНБ и родов, третьи считают, что ПГС снижает результативность ВРТ Mastenbroek и др. опубликовали в 2007 году их «печально известное» клиническое исследование, которое показало отсутствие эффективности в улучшении результатов ЭКО с применением ПГС, но, фактически, у женщин старшего репродуктивного возраста (то есть пациентов с плохим прогнозом) продемонстрировало вред в виде более низких показателей беременности [19]. Стало очевидно, что процедура PGS требует улучшений. Основное внимание уделялось техническим аспектам процедуры. Появление новых диагностических технологий с явно улучшенной точностью хромосомных оценок дало широкие возможности для технических усовершенствований. Они не только были более точными, чем PGS 1.0, но также позволили проводить полные исследования хромосом вместо ограниченных хромосомных панелей [16].
У каждого из методов ПГС имеются свои преимущества и недостатки. До недавнего времени наиболее распространенной методикой была флуоресцентная гибридизация insitu (FISH) [1,4,9]. Метод FISH достаточно ограничен и неточен: анализу подвергается ограниченное количество хромосом, вероятность ошибок 7-10%, что может быть связано с высоким уровнем мозаицизма в исследуемом материале [4,10,13]. Данные нескольких исследований показывают, что даже хорошо отработанные техники FISH не способны определить около 20% анеуплоидий [15]. Методика Ғ^^ключает в себя ряд технически сложных этапов фиксация клеток на слайде для микроскопии, что может привести к потери исследуемого материала. Комплексный скрининг всех 24 хромосом с использованием более автоматизированных подходов направлен на преодоление ограничений FISH [1,4,9]. Поэтому в современных условия, метод FISH теряет свою актуальность для ПГС. Но он может быть использован для верификации заключения aCGH или для ПГД некоторых аномалий, таких как сбалансированные робертсоновские транслокации, определенные случаи несбалансированных перестроек [10]. По данным достаточно большого количества рандомизированных клинических исследований -11, ПГС методом FISH не улучшает результативность программ ВРТ [14,15,10].
Сравнительная геномная гибридизация на микрочипах (aCGH) является относительно новым молекулярногенетическим методом и уже широко используется в большинстве клиник ВРТ. В нашей Республике впервые метод внедрен в 2016 г. [4,11,16,10,21,22]. Высокая точность, чувствительность и воспроизводимость метода подтверждены множеством исследований. aCGH позволяет определять в масштабе всего генома увеличение или уменьшение копийности хромосомных локусов [9,16,21,22]. Основным инструментом является микрочип, на котором расположены тысячи локус-специфичных ДНК-фрагментов. Анализируемая ДНК гибридизируется с подобным микрочипом; каждый сигнал соответствует определенному локусу генома, а изменение интенсивности сигнала свидетельствует об изменении того или иного участка хромосом [16,23]. У «классического» кариотипирования предел чувствительности составляет 5-10 миллионов пар оснований, aCGH способна достигать разрешения менее 100 тысяч нуклеотидов [24]. Метод предполагает конкурентную гибридизацию меченых образцов ДНК и нормальных метафазных хромосом (тестируемая ДНК зеленый, контрольная ДНК красный). Соотношение зеленого/красного сигналов флуоресценции по длине каждой хромосомы указывает на то, есть ли любая потеря или увеличение хромосомного материала в тестируемом образце [9,23]. Таким образом в сочетании с методикой полногеномной амплификации (WGA) можно тестировать любой клеточный материал: полярные тела, бластомеры или клетки трофэктодермы [11]. Результат анализа представляет собой средний результат от всех биопсированных клеток, минимизируя влияние мозаицизма. Некоторые исследования демонстрируют крайне высокие показатели частоты имплантации и рекомендуют использование ПГС методом aCGH совместно с переносом одного эмбриона (SET) как наилучший подход к достижению высоких результатов программ ВРТ [25,26]. Рекомендовано не переносить более одного эмбриона в программах после скрининга методом aCGH, так как это ассоциировано с высоким уровнем многоплодной беременности 57% при высоких уровнях имплантации, количество переносимых эмбрионов должно быть снижено [12, 13].
Преимущества aCGH по сравнению с FISH [3,16,10]: высокая разрешающая способность, скрининг всех хромосом (полногеномный скрининг), возможность количественной детекции участков хромосом и однородительскихдисомий, простота интерпретации и объективность результатов, автоматизация исследования, сроки получения результата 1-3 суток [4,11]
Как и любой другой метод aCGH имеет некоторые особенности, как правило не влияющие на его успешное применение в клинической практике ВРТ [12]. Невозможность определения следующих аномалий: сбалансированные перестройки (реципрокные транслокации, инверсии, робертсоновкиетранслокации, реципрокные инверсии), несбалансированные перестройки за границей разрешения метода (точечные мутации, тринуклеотидные экспансии, делеции/дупликации ниже границы чувствительности метода) [11]. Чтобы успешно применять aCGH, необходим индивидуальный подход к лечению супружеской пары, а также применение дополнительных исследования FISH, qPCR и других. Результаты оцениваются совместно с цитогенетическими методами [11].
ПСГ методом сравнительной геномной гибридизации на микрочипах позволяет значительно расширить возможности современной предимплантационной генетической диагностики и добиться высоких показателей имплатации, частоты наступления беременности, снизить частоту ранних выкидышей и увеличить количество рожденных живых детей после процедур ВРТ [1,21,22].
Таким образом, наличие анеуплоидий непросредственно влияет на исход имплантации, и является частой причиной неудачных попыток ЭКО, особенно у пациентов старшего репродуктивного возраста [1,21,22]. Метод aCGH позволяет выявить геномный дисбаланс и является незаменимым инструментом в ПГС для селективного переноса диплоидных эмбрионов, что способствует увеличению частоты успешной имплантации, увеличивает частоту наступления беременности и приводит к снижению числа спонтанных абортов [4,9,21,23]. И особенно актуален у пациенток старшего репродуктивного возраста, имеющих часто плохой прогноз для программ ВРТ.
В научной литературе до сих пор активно обсуждается вопрос о необходимости проведения ПГС пациентам при проведении ВРТ. Учитывая низкую результативность ВРТ в старшей возрастной группе вопрос о проведении ПГС методом aCGH является достаточно актуальным и не решен окончательно. До настоящего времени нет четких показаний к проведению ПГС, критериев отбора пар для проведения скрининга [2,22,26].
Таким образом, проблема особенностей программ вспомогательных репродуктивных технологий у женщин старшего репродуктивного возрастаявляется исключительно актуальной, в ней много нерешенных вопросов как научного, так и практического плана, требующих на более высоком технологическом и методологическом уровнях исследовать эту проблему с уточнением механизмов снижения фертильности в зависимости от возраста женщины, разработкой методов снижения влияния возраста на частоту наступления беременности и родов в результате применения вспомогательных репродуктивных технологий.
СПИСОК ЛИТЕРАТУРЫ
- В.Н.Локшин,Н.В.Кондакова, Ш.К.Карибаева. Перспективы использования метода сравнительной геномной гибридизации на микрочипах (aCGH) для процедуры предимплантационного генетического скрининга (ПГС) // Репродуктивная медицина. 2016. №2-3(27-28). С. 68-74.
- В.Н. Локшин, С.Ш. Исенова, А.Н. Рыбина, А. Малик, Ф. Акимжан Современные возможности повышения эффективности программ ВРТ у женщин старшего репродуктивного возраста // Репродуктивная медицина. 2017. №3(32). С. 67-73
- Fragouli, E., Katz-Jaffe, M., Alfarawati, S., Stevens, J., Colls, P., Goodall, N., Tormasi, S., Gutierrez-Mateo, C., Prates, R., Schoolcraft, W., Munne, S. and Wells, D. Comprehensive chromosome screening of polar bodies and blastocysts from couples experiencing repeated implantation failure // Fertility and Sterility. 2010. №94(3). Р. 875-887.
- Lee, E., Illingworth, P., Wilton, L. and Chambers, G. The clinical effectiveness of preimplantation genetic diagnosis for aneuploidy in all 24 chromosomes (PGD-A): systematic review // Human Reproduction. 2014. №30(2). Р. 473-483.
- Yajie Chang, JingjieLi Xiaolan Li Hong'e Liu Xiaoyan Liang. Egg Quality and Pregnancy Outcome in Young Infertile Women with Diminished Ovarian Reserve // Medical Science Monitor. 2018. №24. Р. 7279-7284.
- Gr0ndahl ML, Christiansen SL, Kesmodel US, Agerholm IE, Lemmen JG, Lundstr0mP, et al. Effect of women's age on embryomorphology, cleavage rate and competenceBA multicenter cohort study // PLoSONE. 2017. №12(4). Р. 172-186.
- Antonio Capalbo, Laura Rienzi, Danilo Cimadomo, Roberta Maggiulli, Thomas Elliott, GrahamWright, Zsolt Peter Nagy, and Filippo Maria Ubaldi. Correlation between standard blastocyst morphology, euploidy and implantation: an observational study in two centers involving 956 screened blastocysts // Human Reproduction. 2014. Vol.29, №6. Р. 1173-1181.
- Irani M, O'nell C, Palermo GD, Xu K, Zhang C, Qin X, Zhang Q, Clarke RN, Ye Z, Zaninovic N, Posenwaks Z. Blastocyst development rate influences implantation and live birth rates of similarly graded euploid blastocysts // Fertikity Sterility. 2018. №110(1). Р. 95-102.
- Harper, J., Coonen, E., De Rycke, M., Fiorentino, F., Geraedts, J., Goossens, V., Harton, G., Moutou, C., PehlivanBudak, T., Renwick, P., SenGupta, S., Traeger-Synodinos, J. and Vesela, K. What next for preimplantation genetic screening (PGS)? A position statement from the ESHRE PGD Consortium steering committee // Human Reproduction. 2010. №25(4). Р. 821-823.
- Ajuk, A, Zernicka-Goetz, Advances embrio selection methods. M.: 2012. 367 р.
- Yang, Z., Liu, J., Collins, G., Salem, S., Liu, X., Lyle, S., Peck, A., Sills, E. and Salem, R. Selection of single blastocysts for fresh transfer via standard morphology assessment alone and with array CGH for good prognosis IVF patients: results from a randomized pilot study // Mol Cytogenet. 2012. №5(1). Р. 24-29.
- Forman, E., Hong, K., Ferry, K., Tao, X., Taylor, D., Levy, B., Treff, N. and Scott, R. In vitro fertilization with single euploid blastocyst transfer: a randomized controlled trial // Fertility and Sterility. 2013. №100(1). Р.100-107.
- Forman, E., Upham, K., Cheng, M., Zhao, T., Hong, K., Treff, N. and Scott, R. Comprehensive chromosome screening alters traditional morphology-based embryo selection: a prospective study of 100 consecutive cycles of planned fresh euploid blastocyst transfer // Fertility and Sterility. 2013. №100(3) Р. 718-724.
- Verlinsky Y, Kuliev A. Preimplantation diagnosis of common aneuploidies in infertile couples of advanced maternal age // Hum Reprod. 1996. №11. Р. 2076-2077
- Norbert Gleicher, Raoul Orvieto. Is the hypothesis of preimplantation genetic screening (PGS) still supportable? A review // J Ovarian Res. 2017. №10. Р. 21-28.
- Ata, B., Kaplan, B., Danzer, H., Glassner, M., Opsahl, M., Tan, S. and Munne, S. Array CGH analysis shows that aneuploidy is not related to the number of embryos generated // Reproductive BioMedicine Online. 2006. №24(6). Р. 614-620.
- Verlinsky Y, Cieslak J, Ivakhnenko V, Evsikov S, Wof G, White M, Lifchez A, Kaplan B, Moise J, Valle J, Ginsberg N, Strom C, Kuliev A. Preimplantation diagnosis of common aneuploidies by the firstand second-polar body FISG analysis // J Assist reprod genet. -1998. №15. Р. 285-289.
- Platteau P, Staessen C, Michiels A, Van Steirteghem A, Liebaers I, Devroey P. Preimplantation genetic diagnosis for eneuploidy screening in women older than 37 years // Fertil Steril. 2005. №84. Р. 319-324
- Mastenbroek S, Twisk M, van Echten-Arends J, SikkemaRaddatz B, Kovaar JC, Verhoeve HR, Vogel NE, Arts EG, de Vries JW, Bossuyt PM, Buys CH, Heineman M, Repping S, van der Veen F. In vitro fertilization with preimplantation genetic screening // N Engl J Med. 2007. №8. Р. 357-359.
- Карибаева Ш.К., Малик А., Локшин В.Н. Первые программы преимплантационного генетического скрининга в Казахстане // Репродуктивная медицина. 2017. №1(30). С. 54-57.
- Р.К. Валиев, В.Н. Локшин, Ш.К. Карибаева, А. Малик, А.Н.Рыбина, К.Т. Нигметова, К.А.Уразымбетова Возможности PGS в преодолении влияния возрастного фактора на результаты ВРТ // Репродуктивная медицина. 2017. №4(33). С. 20-23.
- Mastenbroek, S., Twisk, M., van der Veen, F. and Repping, S. Preimplantation genetic screening: a systematic review and meta-analysis of RCTs // Human Reproduction Update. 2008. №19(2). Р. 206-206.
- Микитенко Д.А. Сравнительная геномная гибридизация в клинической практике URL: http://www.ivf.com.ua/web/uploadfiles/Webinar_20120120_Mykytenko.pdf
- Forman, E., Upham, K., Cheng, M., Zhao, T., Hong, K., Treff, N. and Scott, R. Comprehensive chromosome screening alters traditional morphology-based embryo selection: a prospective study of 100 consecutive cycles of planned fresh euploid blastocyst transfer // Fertility and Sterility. 2013. №100(3). Р. 718-724.
- Debrock, S., Melotte, C., Spiessens, C., Peeraer, K., Vanneste, E., Meeuwis, L., Meuleman, C., Frijns, J., Vermeesch, J. and D'Hooghe, T. Preimplantation genetic screening for aneuploidy of embryos after in vitro fertilization in women aged at least 35 years: a prospective randomized trial // Fertility and Sterility. 2010. №93(2). Р. 364-373.