В рамках научно-исследовательских работ по теме магистерской диссертации «Фармацевтическая разработка фитосубстанции на основе лекарственного растительного сырья исландского мха (Cetrariaislandica (L.)Ach.)»6bLA использован спектрофотометрический метоД определения биологически активных веществ (БАВ) в слоевище исландского мха (C. islandica). Данный спектрофотометрический метод предлагается для количественного определения полисахаридов и фенольных соединений (усниновая кислота) в слоевище C. islandica.
Слоевища C. islandica собраны и заготовлены, согласно требованиям Надлежащей практики культивирования и сбора лекарственных растений (GACP), проведена стандартизация в соответствии с требованиями Государственной Фармакопеи Республики Казахстан.
Актуальность. В составе C. islandica обнаружено больше 10 полезных микроэлементов: активный компонент лихенин, изолихенин, сахара, воск, камедь, марганец, железо, йод, медь, титан, пигменты, лишайниковые кислоты (усниновая, лихестериновая, протолихестериновая, фумарпротоцентраровая и другие). Наличие кислот придают растению горечи, а также обуславливают его антисептические и тонизирующие свойства. Богатый состав микроэлементов, наличие полисахаридов способствуют укреплению защитных сил организма человека [1].
Слизистое вещество устраняет раздражение, обволакивает воспаленные слизистые желудка, ротовой полости, гортани, кишечника.
Натриевая соль усниновой кислоты, которая обладает антибактериальным свойством, успешно используется в составе препаратов цетрарии. Лихестериновая, а также протолихестериновая кислоты особо активны в отношении стрептококков, стафилококков и прочих устойчивых микробов. Уснинат натрия употребляется наружно при терапии трофических язв, инфицированных ран, ожогов.
Благодаря уникальному составу, исландский мох считается природным антибиотиком, сила которого нередко преобладает над обычными антибиотиками. На болезнетворные бактерии, вирусы и грибки эффективно воздействуют кислоты лишайника, в частности усниновая [2]. Целью исследования является количественного определения полисахаридов и фенольных соединений (усниновая кислота) спектрофотометрическим методом.
Материалы и методы исследования.
Слоевища исландского мха собраны в мае-июне 2018 г. в х.Заилийского Алатау,ущелье ТургеньТалгарского района, Алматинской области.
Нами проведен спектрофотометрический метод анализа БАВ в слоевище C. islandicaс помощьюспектрофотометраSPEKOL 1300, также в работе были использованы центрифуга ОПн-8УХЛ4.2, водяная баня, весы технические OHAUS, обратный холодильник, вытяжной шкаф LAMSYSTEMS, термометр ртутный ТТЖ- М, сушильный шкаф ШС-80.
Результаты и обсуждения.
Для выделения отдельных групп углеводов из образцов слоевища C. islandica использовали стандартную методику, схема которой приведена на рисунке 2 [10]. Полученные фракции полисахаридов подвергали очистке и гидролизу для исследования их мономерного компонентного состава [6, 7, 8, 9]. Количественное определение суммы свободных моносахаридов и водорастворимых полисахаридов, проводили по известным методикам [6, 10].
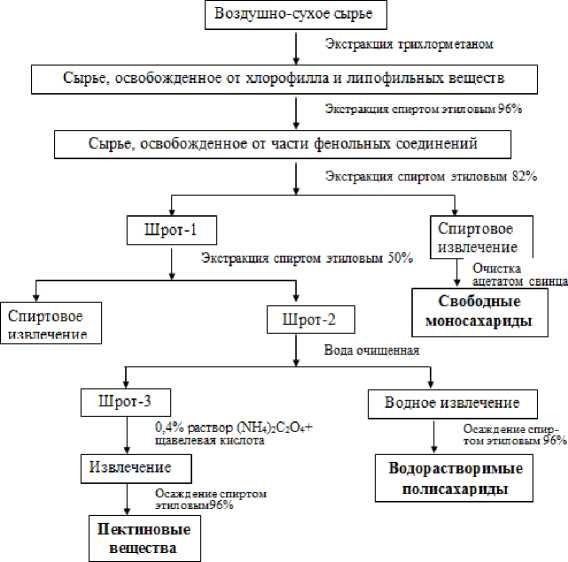
Рисунок 1 - Схема выделения углеводов из слоевища C. islandica
Минусы этого метода в том, что оно требует большее количество времени, и поэтому мы предлагаем более короткий путь количественного определения суммы полисахаридов в сырье.
Для построения калибровочного графика взяли0,1400 г (точная навеска) глюкозы высушенной до постоянной массы при 100-105 °С, которую растворяют в воде очищенной в
мерной колбе вместимостью 100 мл и доводят объем водой очищенной до метки (раствор А). 1 мл полученного раствора переносят в мерную колбу вместимостью 25 мл и доводят объем раствора водой до метки (раствор Б). 1 мл раствора Б содержит 0,000056 г глюкозы.
В 5 пробирок вносят раствор Б и воду очищенную в количествах,указанных ниже
Таблица 1
|
Объем раствораБ,мл |
0 ,2 |
,4 |
,6 |
,8 |
|
|---|---|---|---|---|---|
|
Объем воды очищенной,мл |
0 ,8 |
,6 |
,4 |
,2 |
|
|
Содержание глюкозы,мкг |
1 1,2 |
2,4 |
3,6 |
4,8 |
6 |
Далее осторожно прибавляют в каждую пробирку к 1 мл полученного раствора 0,25 мл 5% раствора фенола и 2,5 мл кислоты серной концентрированной. Затем пробирки помещают в водяную баню с температурой 10-15°С на 5 минут, при этом смесь осторожно встряхивают. Пробирки ставят на кипящую водяную баню на 16 минут, охлаждают на водяной бане при температуре 10-15 °C и определяют оптическую плотность полученного раствора на спектрофотометре. Измерение оптической плотности растворов проводят при длине волны 490 нм относительно извлечения в
кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют смесь: 0,25 мл воды очищенной и 0,25 мл 5 % раствора фенола и 2,5 мл кислоты серной концентрированной, выдержанную в тех же условиях, что и опытная смесь.
Расчет содержания полисахаридов (в %) проводят на абсолютно-сухое сырье в пересчете на глюкозу с использованием калибровочного графика,в координатах зависимости оптической плотности полученного раствора от содержания глюкозы (мкг/мл), по формуле:
С°*12500х
Мх(100-ш)
где С0 -концентрация глюкозы по калибровочному графику; М-масса навески сырья,г; «-потеря в массе при высушивании сырья,%.
Определения выполняют для каждого образца в трехкратной повторности.
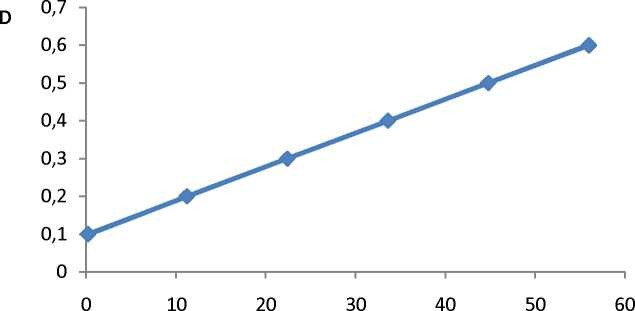
C (мкг/мл)
Рисунок 2 - Калибровочный график
По оси абцисс - концентрация глюкозы, мкг/мл; по оси ординат - оптическая плотность.
Методика определения суммы полисахаридов. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм.
Около 1 г (точная навеска) измельченного сырья помещают в колбу вместимостью 100 мл со шлифом, прибавляют 50 мл воды очищенной. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 2 ч. Извлечение фильтруют через бумажный фильтр в плоскодонную колбу вместимостью 50 мл доводят объем раствора водой очищенной до метки.
10 мл полученного извлечения с помощью пипетки переносят в мерную колбу вместимостью 25 мл и доводят объем раствора водой очищенной до метки (раствор А).
1 мл раствора А переносят в центрифужную пробирку, добавляют 2 мл 95%-ного этанола, перемешивают и нагревают на водяной бане в течение 5 минут. Через 1 ч содержимое пробирки центрифугируют в течение 10 минут в центрифуге со скоростью вращения 3000 об/мин. Осадок промывают 5 мл раствора спирта этилового 50 %-ного и количественно
переносят 10 мл воды очищенной при нагревании на водяной бане в мерную колбу вместимостью 100 мл доводят объем водой очищенной до метки (раствор Б). К 1 мл раствора Б 0,25 мл 5 % раствора фенола и 2,5 мл кислоты серной концентрированной. Затем пробирки помещают в водяную баню с температурой 10-15 °C на 5 минут, при этом смесь осторожно встряхивают. Пробирки ставят на кипящую водяную баню на 16 минут, охлаждают на водяной бане при температуре 10-15 C и определяют оптическую плотность полученного раствора на спектрофотометре. Измерение оптической плотности растворов проводят при длине волны 490 нм относительно извлечения в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют смесь: 0,25 мл воды очищенной и 0,25 мл 5 % раствора фенола и 2,5 мл кислоты серной концентрированной, выдержанную в тех же условиях, что и опытная смесь.
Расчет содержания полисахаридов (в %) проводят на абсолютно-сухое сырье в пересчете на глюкозу с использованием калибровочного графика, в координатах зависимости оптической плотности полученного раствора от содержания глюкозы (мкг/мл), по формуле:
С0 *125000 *100
* 100%,
М*1*10*106*(100-ш)
где С0 -концентрация глюкозы по калибровочному графику; М-масса навески сырья ,г; «-потеря в массе при высушивании сырья,%.
Результаты определения полисахаридов по описанной выше методике представлены в таблице.
Согласно полученным данным, содержание полисахаридов в слоевище цетрарииисландской должно составлять не менее 49,21%.
Количественное определение усниновой кислоты в слоевище исландского мха.
Около 10 г (точная навеска) измельченного сырья помещают в круглодонную колбу вместимостью 250 мл, прибавляют 100 мл спирта этилового 96% (хлороформ, ацетон, этилацетат) и экстрагируют на кипящей водяной бане в течении 2 часов. Охлаждают, фильтруют в коническую колбу, прибавляют 30 мл 10% раствора кальция карбоната и 10% раствор кислоты хлороводородной до прекращения образования мути. Водный слой отделяют в делительный воронке, прибавляют 10% раствор кислоты хлороводородной до образования осадка. Осадок отфильтровывают, промывают на фильтре водой очищенной, высушивают.
Сухой осадок растворяют в ацетоне, хлороформе и этилацетате: раствор пропускают через слой (2-3 см) силикагеля Л 51/40 М. колонку промывают тем же растворителем. Элюат концентрируют, остаток высушивают до постоянной массы.
Сухой остаток растворяют в любом указанном растворителе в мерной колбе вместимостью 50 мл, доводят объем раствора до метки и замеряют оптическую плотность полученного раствора при длине волны 290 ни в кювете с толщиной слоя 10 мм.
Содержание лишайниковых кислот в абсолютно сухом сырье в процентах(Х), в пересчете на кислоту усниновую, рассчитывают по формуле:
D* 50 * 100 * 100 P * m(100 W)
где, Dоптическая плотность испытуемого раствора при длине волны 290 нм; mмасса навески сырья( препарата), в граммах;
Wпотери в массе при высушивании сырья, в процентах;
P=85,7удельный показатель поглощения раствора кислоты усниновой при длине волны 290 нм. * Возможно определение кислот лишайниковых весовым методом [5].
D=0,3.
Х =1,87% усниновой кислоты в перерасчете на абсолютно сухое сырье.
Выводы. Для количественного определения БАВ (полисахаридов и фенольных кислот) используют разные методы, которые могут быть не достаточно точными и воспроизводимыми. Предлагаемый метод является более доступным и менее затратным в отношении времени.Полученные результаты позволят внести соответствующее дополнение в аналитический нормативный документ на сырье.
СПИСОК ЛИТЕРАТУРЫ
- Криштанова Н.А. Разработка стандартного образца полисахаридного состава для оценки качества липы сердцевидной листьев, цетрарии исландской слоевищ и лекарственных средств на их основе: дисс. ... канд.фарм.наук СПб., 2007. 220 с.
- А.Л. Тахтаджян Жизнь растений. М.: Просвещение, 1981. 267 с.
- Лекарственные растения и их применение. М., Наука и техника, 1974. 197 с.
- nhamiGulfinMunirOktay,O.irfanKufrevioglu,AliAslanDetermination of antioxidant activity of lichen Cetrariaislandica(L) Ach // Journal of Ethnopharmacology. 2002. №79. Р. 325-329.
- ВФС РК 42-332-2000 «Слоевища пармелииVegans»
- Березина В. С. и др. Содержание и состав суммарных водораство-римых полисахаридных комплексов в надземной части LamiumalbumL. и GaleobdolonluteumHuds // Раст. ресурсы. 2003. Т. 39, Вып. 1. - С. 69 76.
- Дудкин М. С., Денисюк Н. А.Углеводы Symphytumasperum // Химия природ. соедин. 1984. №1. С. 15-20.
- Оленников Д. Н., Танхаева Л. М. Методика количественного определения группового состава углеводного комплекса растительных объектов // Химия растительного сырья. 2006. №4. С. 29 33.
- Остроженкова Е.Г. и др. Выделение и анализ полисахаридной фракции из биомасс штаммов Panaxginseng C.A.Mey и P. quinquefoliusL. с герматраном «LX-5» // Раст. ресурсы. 2002. Т.38, Вып. 2. С. 120-125.
- Тулайкин А.И., Березина В.С., Гончаров М.Ю. Углеводы из надземной части: выделение и анализ // Раст. ресурсы. 2004. Т. 40, Вып. 4. С . 73-79.