Хроническая болезнь почек является важной медицинской и социальной проблемой современной медицины. В статье представлены современные сведение оРААС системе, антигенов HLA, внутриклеточных механизмах участвующих в возникновении и развитии ХПН.
Введение.
Хроническая почечная недостаточность (ХПН) — симптомокомплекс, развивающийся при хронических двусторонних заболеваниях почек вследствие постепенной необратимой гибели нефронов и характеризующийся нарушением гомеостатической функции почек, при котором почки не могут удалить конечные продукты метаболизма из крови и регулировать баланс жидкости, электролитов и рН внеклеточных жидкостей. Терминальная ХПН (ТХПН) — исход заболеваний почек с хроническим прогрессирующим течением — соответствует понятию «почечной смерти». Морфологической основой ТХПН является нефросклероз, а функциональной — утрата почечных функций, приводящая к нарушению гомеостаза и смерти пациента. Заболевание становится необратимым задолго до ТХПН, практически с момента установления ХПН [1].
Хроническая почечная недостаточность в основном является следствием ряда условий, которые вызывают постоянную потерю нефронов, включая диабет, гипертонию, гломерулонефрит и поликистозную болезнь почек.
Согласно статистики по данным МИАЦ ЮКО за 01.01.200931.08.2009 год. наблюдались 15017 больных с заболеванием различных этиологий почек в Южно-Казахстанской области. По данным Департамента по контролю и социальной защите по ЮКО за 2009 год всего инвалидов с ХПН- 1230 человек, из них: инвалиды 1 группы- 206, инвалиды 2 группы- 776, ребенок-инвалид 1 группы- 4, ребенок-инвалид- 244. В том числе из них: получающие программный гемодиализ - 155 человек, перенесшие операции по трансплантации почек - 20 человек. С каждом годом эти показатели растут [15]. Неблагоприятные показатели эпидемиологии ХПН связаны с увеличением не только числа больных с патологией почек, но и сахарным диабетом, ожирением, постарением населения, увеличением числа пациентов с повреждениями почек сосудистой природы, в частности ишемии почек [16]. Важность проблемы хронической почечной недостаточности с медицинской, социальной и организационной точек зрения обусловлена высокой летальностью, инвалидизацией и сложностью технического обеспечения современных методов лечения этой патологии. Диагностика ХПН, ранняя диагностика ХПН нередко вызывает трудности. С одной стороны, нередко наблюдается многолетнее бессимптомное течение ХПН, особенно характерное для хронического пиелонефрита, латентного нефрита, поликистозной болезни. С другой стороны, в связи с полиморфизмом поражений внутренних органов при далеко зашедшей ХПН на первый план могут выходить ее неспецифические "маски": анемическая, гипертоническая, астеническая, подагрическая, остеопатическая. Наличие у больного стойкой нормохромной анемии в сочетании с полиурией и артериальной гипертонией должно настораживать в отношении ХПН [2].
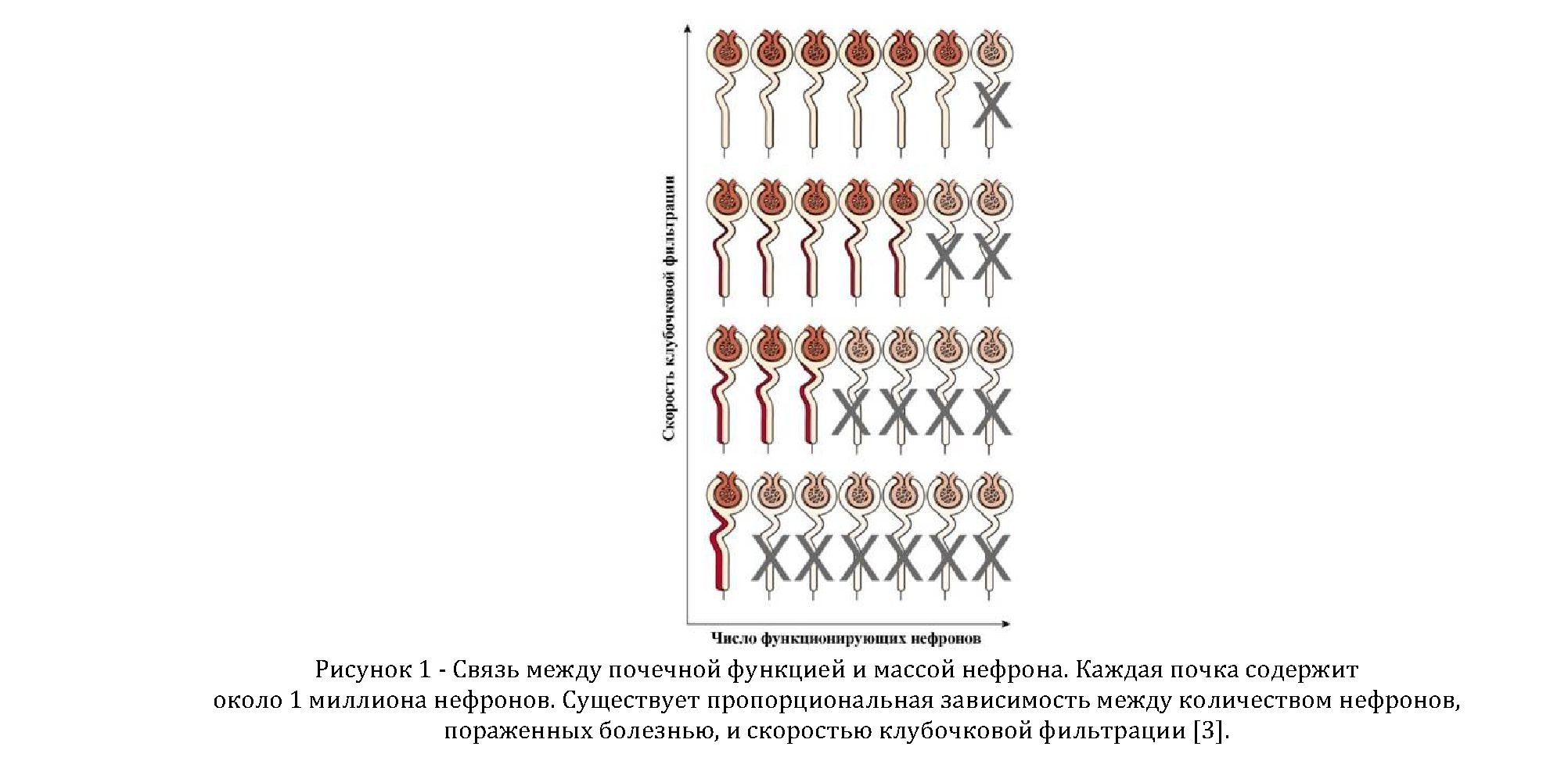
Механизм развития ХПН носит многосторонний характер и может включать в себя поражения разных систем и внутренних органов больного. Нарастает задержка в крови азотистых шлаков, пигментов, в ряде случаев электролитов (калия), нарушается эндокринная функция органа. Несмотря на сохранение почками водовыделения или даже его усиление, в крови накапливаются белковые шлаки, кислотные радикалы (мочевина, мочевая кислота, аминокислоты, креатинин, гуанидин, фосфаты, сульфаты); как правило, возникает и нарастает артериальная гипертензия, что в конце концов приводит к хронической уремии. [2] Как правило, признаки и симптомы почечной недостаточности развиваются постепенно и становятся очевидными тогда, когда болезнь будет на поздних стадиях развитая. Это связано с удивительной компенсаторной способностью почек. По мере разрушения структур почек оставшиеся нефроны подвергаются структурной и функциональной гипертрофии, каждый из которых увеличивает свою функцию как средство компенсации потерянных (рисунок 1). Только когда несколько оставшихся нефронов разрушаются, становится заметно проявления почечной недостаточности [3].
Хроническая болезнь почек является важной медицинской и социальной проблемой современной медицины. Количество больных с терминальной хронической почечной недостаточностью увеличивается быстрыми темпами. Так, в мире популяция больных, получающих заместительной почечной терапии (ЗПТ), увеличилась с 500 000 в 1990 г. до почти 2 млн человек к 2010 г., а количество больных с консервативно курабельной стадией ХПН превышает популяцию ТХПН более чем в 50 раз [4]. Развитие технологий заместительной почечной терапии привело к значительному повышению качества гемодиализа и увеличению продолжительности жизни больных с терминальной почечной недостаточностью.
Система РAAС.
РAAС (Ренин-ангиотензин-альдостероновая система) была в центре внимания исследования прогрессирования ХПН из-за эффективности ингибирования его компонентов при ХПН.В ответ на снижение давления перфузии в почках ренин (протеаза)продуцируется юкстагломерными клетками почки.Этот фермент действует на неактивный пептид, называемый ангиотензиноген, продуцируемый печенью, превращая его в ангиотензин-I который является начальным компонентом действия РAAС. Ангиотензин-I катализируется в октапептиды с помощью ангиотензинпревращающего фермента (АСЕ- дипептидилкарбоксипептидаза), продуцируемого в легких и лимфоцитах [5], с образованием ангиотензина II, который является активным пептидом [6]. Ангиотензин II также продуцируется химазой и катепсином G, которые не зависят от активности ACE. Эффекты ангиотензина II опосредуются рецепторами, связанными с G-белком, то есть ангиотензином типа 1 (AT1), рецепторами ангиотензина типа 2 (AT2) [7] или рецептором MAS [5].
 Активация рецепторов АТ1 ангиотензином II в почках сужает эфферентную артериолу, что приводит к уменьшению кровотока, влияющего на клубочковую фильтрацию, путем повышения давления в клубочковом капилляре.Это, в свою очередь, приводит к повреждению клубочков и увеличению продуцирования нефротоксичных реакционноспособных видов кислорода, профибротических цитокинов и факторов роста. Производство этих компонентов стимулирует митогенез фибробластов, которые приводят к почечному фиброзу и ХПН [8, 9].Альдостерон образуется в клубочковой зоне коры надпочечников и является единственным поступающим в кровь минералокортикоидом человека. Регуляция синтеза и секреции альдостерона осуществляется преимущественно ангиотензином-II, что дало основание считать альдостерон частью ренин-ангиотензин-альдостероновой системы (РААС), обеспечивающей регуляцию водно-солевого обмена и гемодинамики.Альдостерон связывается с минералокортикоидным рецептором, который регулирует натриево-калиевые насосы [10], и поскольку он обладает клеточными пролиферативными и профибротическими свойствами, он непосредственно увеличивает экспрессию и продуцирование профибротического цитокина «трансформирующий фактор роста ß» (TGF-ß).В моделях заболевания почек синтез альдостерона увеличивается и замешан в пролиферации фибробластных клеток, почечного фиброза и индукции гипертонии из-за перегрузки натрия [11]. Все эти эффекты синергически провоцируют почечные болезни.
Активация рецепторов АТ1 ангиотензином II в почках сужает эфферентную артериолу, что приводит к уменьшению кровотока, влияющего на клубочковую фильтрацию, путем повышения давления в клубочковом капилляре.Это, в свою очередь, приводит к повреждению клубочков и увеличению продуцирования нефротоксичных реакционноспособных видов кислорода, профибротических цитокинов и факторов роста. Производство этих компонентов стимулирует митогенез фибробластов, которые приводят к почечному фиброзу и ХПН [8, 9].Альдостерон образуется в клубочковой зоне коры надпочечников и является единственным поступающим в кровь минералокортикоидом человека. Регуляция синтеза и секреции альдостерона осуществляется преимущественно ангиотензином-II, что дало основание считать альдостерон частью ренин-ангиотензин-альдостероновой системы (РААС), обеспечивающей регуляцию водно-солевого обмена и гемодинамики.Альдостерон связывается с минералокортикоидным рецептором, который регулирует натриево-калиевые насосы [10], и поскольку он обладает клеточными пролиферативными и профибротическими свойствами, он непосредственно увеличивает экспрессию и продуцирование профибротического цитокина «трансформирующий фактор роста ß» (TGF-ß).В моделях заболевания почек синтез альдостерона увеличивается и замешан в пролиферации фибробластных клеток, почечного фиброза и индукции гипертонии из-за перегрузки натрия [11]. Все эти эффекты синергически провоцируют почечные болезни.
Сигнальный путь Wnt / β-catenin играет существенную роль в органогенезе и гомеостазе тканей, который после активации транслоцирует ß-катенин в ядро, где последний связывается с фактором Т-клеток (TCF) или лимфоидным усиливающим фактором (LEF) вместе с другими coфакторами, такими как CREB-связывающий белок (CBP).У здоровых людей в почках этот путь неактивен, но при ХПН он активируется [12].В ходе биоинформатических исследованийZhouetal. [13] былообнаружено, что все гены RAS имеют предполагаемые сайты связывания факторов TCF / LEF в своих промоторныхобластях. Это вероятная связь между активацией RAS Wnt / β-catenin сигнального пути с развитием ХПН [14].
HLA комплекс.
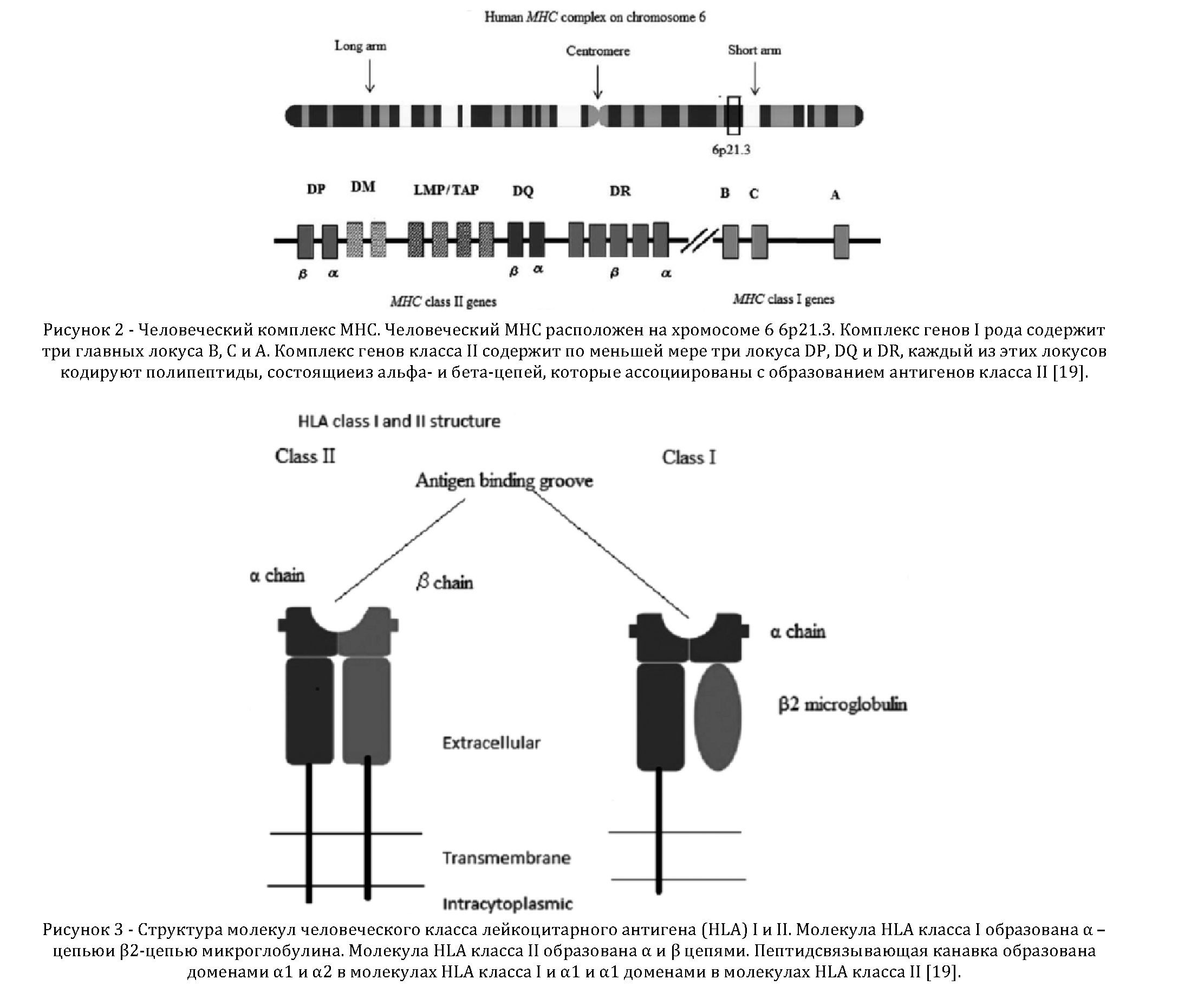
Как известно, ранняя диагностика ХПН основана преимущественно на лабораторных и биохимических методах, когда уже болезнь находится на поздних стадиях развития. Сейчас существуют современные молекулярногенетические методы исследования по выявлению и предотвращению возникновения патологий на основе генетических маркеров. Данными маркерами выступают следующие гены: Class I HLA-A, B, and C; Class II HLA- DRB1/3/4/5, HLA-DQA1, HLA-DQB1, HLA-DPA1, and HLA-DPB1. Семейство генов HLA кодирует группу родственных белков, известных как человеческий комплекс лейкоцитарного антигена (HLA). Комплекс HLA помогает иммунной системе отличать собственные белки организма от белков, полученных от чужеродных организмов, таких как вирусы и бактерии.HLA является человеческой версией основного комплекса гистосовместимости (MHC), семейства генов, которое встречается у многих видов. Основные гены гистосовместимости (МНС) являются наиболее полиморфными локусами в геноме человека и широко изучены в различных популяциях и этнических группах. У людей комплекс MHC состоит из более чем 200 генов, расположенных близко друг к другу на хромосоме 6 (рисунок 2) [17]. У людей есть три основных гена I класса MHC, известные как HLA-A, HLA-B и HLA-C. Они состоят из одной транс-мембранной тяжелой цепи с тремя внеклеточными доменами (a1-3) и b2-микроглобулином (b2m) легкой цепи. Белки, полученные из этих генов, присутствуют на поверхности почти всех клеток. На поверхности клеток эти белки связаны с белковыми фрагментами (пептидами), которые были экспортированы из клетки. Белки MHC класса I представляют эти пептиды в иммунную систему. Если иммунная система распознает пептиды как чужеродные (такие как вирусные или бактериальные пептиды), она реагирует путём запуска заражённой клеткиксаморазрушению. Существует шесть основных генов MHC класса II у людей: HLA-DPA1, HLA-DPB1 , HLA-DQA1 , HLA-DQB1 , HLA-DRA и HLA-DRB1 . Каждый белок класса II HLA содержит альфа- и бета-цепь, оба из которых кодируются в MHC (например, HLA-DRA с HLA- DRB1). Гены MHC класса II кодируют белки, которые присутствуют почти исключительно на поверхности определенных клеток иммунной системы. Подобно белкам MHC класса I, эти белки, интегрированные в мембрану клеток, отображают короткие пептиды на поверхности клеток[17, 18, 19]( рисунок 3).
Известно, что специфические типы HLA связаны с патогенезом многих аутоиммунных заболеваний, аллергий и воспалительных заболеваний кишечника [20, 21].
Определение специфических типов HLA оказалось ценным инструментом для диагностики некоторых важных заболеваний, таких как как анкилозирующий спондилоартрит, воспалительное заболевание кишечника и рассеянный склероз [22, 23]. Несколько новых исследований описали значительные корреляции между HLA и некоторыми почечными заболеваниями, такими как диабетическая нефропатия, нефропатия IgA и гломерулонефрит [24, 25]. Однако конкретные типы HLA связанные с ТХПН, не были хорошо документированы.
На базе РГП на ПХВ «Научно-производственный центр трансфузиологии» была изучена частота встречаемости HLA-антигенов I-класса (HLA-A, B) и II-класса (HLA-DRB1*) у 388 пациентов с тХПН и 565 здоровых доноров добровольцев, проживающих в Казахстане. Типирование пациентов (HLA-A, B, DRB1) и доноров крови НLА ІІ-класса (HLA-DRB1*) определяли молекулярно-генетическим методом (Рrotrans, Германия)[26]. Исследования показали, что существует связь между наличием в фенотипе пациентов HLA-A*01; B*15, *60, *61 и развитием почечной патологии. В ходе исследования также установлена предположительно защитная роль в отношении почечной патологии ряда антигенов HLA-A*11, *23, *28, *33; B*46, *62; DRB1*03, *08, *14.
В связи с этим, мы планируем совместно с сотрудниками Института Трансфузиологии провести исследованиеследующих генов, являющихся маркерами хронической почечной недостаточности в европейской
популяции:ClassIHLA-A, B, andC; ClassIIHLA-DRB1/3/4/5, HLA- DQA1, HLA-DQB1, HLA-DPA1,HLA-DPB1.
СПИСОК ЛИТЕРАТУРЫ
- О.Н.Сигитова. Вестник современной клинической медицины // Научно-практический журнал. – 2008. – Т.1, №1. – С. 96-108.
- Папиш Т.Г, Ротаренко И.В., Ушакова Е.С. Хроническая+ почечная недостаточность и современные методы ее лечения // ГБОУ СПО ККБМК министерства здравоохранения Краснодарского края. – Краснодар: 2014. – С. 52-59.
- C.Porth Essentials of pathophysiology : concepts of altered health states. - Philadelphia :LippincottWilliams&Wilkins ©. - 2004. – 445 с.
- Е.В.Захарова. Проблемы диагностики и консервативной терапии хронической почечной недостаточности // Медицинский совет. – 2010. - №11. – С. 25-36.
- Jankowski V, Vanholder R, van der Giet M, Henning L, Tölle M, Schönfelder G, et al. Detection of angiotensin II in supernatants of stimulated mononuclear leukocytes by matrix-assisted laser desorption ionization time-of-flight/time-of-flight mass analysis // Hypertension. – 2005. - №46(3). – Р. 591–597.
- Skeggs LT, Jr, Kahn JR, Lentz K, Shumway NP. The preparation, purification, and amino acid sequence of a polypeptide renin substrate // J Exp Med. – 1957. - №106(3). – Р. 439–453.
- Lavoie JL, Sigmund CD. Minireview: overview of the renin-angiotensin system – an endocrine and paracrine system // Endocrinology. – 2003. - №144(6). – Р. 2179–2183.
- Dzau VJ, Re R. Tissue angiotensin system in cardiovascular medicine. A paradigm shift? // Circulation. – 1994. - №89(1). – Р. 493–498.
- Wolf G. Angiotensin II as a mediator of tubulointerstitial injury // Nephrol Dial Transplant. – 2000. - №15, Suppl 6. – Р. 61–63.
- Schweda F. Salt feedback on the renin-angiotensin-aldosterone system // Pflugers Arch. – 2015. - №467(3). – Р. 565–576.
- Wenzel U. Aldosterone and progression of renal disease // Curr Opin Nephrol Hypertens. – 2008. - №17(1). – Р. 44–50.
- He W, Kang YS, Dai C, Liu Y. Blockade of Wnt/beta-catenin signaling by paricalcitol ameliorates proteinuria and kidney injury // J Am SocNephrol. – 2011. - №22(1). – Р. 90–103.
- Zhou L, Li Y, Hao S, Zhou D, Tan RJ, Nie J, et al. Multiple genes of the renin-angiotensin system are novel targets of Wnt/beta-catenin signaling // J Am SocNephrol. – 2015. - №26(1). – Р. 107–120.
- Prathibha Reddy Gajjala,1 Maryam Sanati,1 and Joachim Jankowski1. Cellular and molecular mechanisms of chronic kidney disease with diabetes mellitus and cardiovascular diseases as its comorbidities // Front. Immunol. – 2015. - №8. – Р. 41-47.
- Ускенбаев М.К. Всемирный День Почки // Доклады. http://www.dark-diabet.kz/doklady/647.html
- Лавиль М. Роль артериальной гипертонии в прогрессировании почечной недостаточности, эффективность антигипертензивной терапии // Нефрология. – 2000. - Т.4, №1. - С.119-121.
- Khan MA, Mathieu A, Sorrentino R, Akkoc N. The pathogenetic role of HLA-B27 and its subtypes // Autoimmun Rev. – 2007. - №6(3). – Р. 183-189.
- Marsh SG, Albert ED, Bodmer WF, Bontrop RE, Dupont B, Erlich HA, Geraghty DE, Hansen JA, Hurley CK, Mach B, Mayr WR, Parham P, Petersdorf EW, Sasazuki T, Schreuder GM, Strominger JL, Svejgaard A, Terasaki PI, Trowsdale J. Nomenclature for Factors of the HLA System, 2004 // Hum Immunol. – 2005. - №66(5). – Р. 571-636.
- Y.M. Mosaad. Clinical Role of Human Leukocyte Antigen in Healthand Disease (review) // Scandinavian Journal of Immunology. – 2015. – P. 283-291.
- Kaimen-Maciel DR, Reiche EM, Borelli SD, Morimoto HK, Melo FC, Lopes J, et al. HLA-DRB1* allele-associated genetic susceptibility and protection against multiple sclerosis in Brazilian patients // Mol Med Rep. – 2009. - №2. – Р. 993–998.
- Giarola LB, Dos Santos RR, Bedendo J, da Silva Júnior WV, Borelli SD. HLA molecules and nasal carriage of Staphylococcus aureus isolated from dialysis and kidney transplant patients at a hospital in Southern Brazil // BMC Res Notes. – 2012. - №5. – Р. 90-99.
- Ahmad T, Marshall SE, Jewell D. Genetics of inflammatory bowel disease: the role of the HLA complex // World J Gastroenterol. – 2006. - №12. – Р. 3628–3635.
- Kallaur AP, Kaimen-Maciel DR, Morimoto HK, Watanabe MA, Georgeto SM, Reiche EM. Genetic polymorphisms associated with the development and clinical course of multiple sclerosis (review) // Int J Mol Med. – 2011. - №28. – Р. 467–479.
- Vuong MT, Lundberg S, Gunnarsson I, Wramner L, Lundström E, Fernström A, et al. Genetic evidence for involvement of EJMI 5 adaptive immunity in the development of IgA nephropathy: MHC class II alleles are protective in a Caucasian population // Hum Immunol. – 2013. - №74. – Р. 957–960.
- Dai CS, Chu CC, Chen SF, Sun CY, Lin M, Lee CC. Association between human leucocyte antigen subtypes and risk of end stage renal disease in Taiwanese: a retrospective study // BMC Nephrol. – 2015. - №16. – Р. 177-186.
- Protrans medizinische diagnostische Produkte GmbH Ketschau 2, D-68766 Hockenheim, Germany