В данной статье описаны особенности поражения почек при АНЦА-ассоцированных васкулитах на основе клинического случая. К васкулитам, при диагностике которых AНЦА имеют решающее значение, относятся Гранулематоз с полиангиитом (ГПА), микроскопический полиангиит (МПА) и синдром Чарга–Стросс (ЧСС), все они являются васкулитами мелких сосудов. Их характеризует тяжелое течение, высокая вероятность летальных исходов, частое вовлечение легких, верхних дыхательных путей и почек. Дифференциальная диагностика с другими васкулитами и заболеваниями неваскулитной природы (в первую очередь инфекциями) нередко представляет значительные трудности.
Актуальность. В последнее время отмечено значительное увеличение частоты заболеваемости системных васкулитов, что свидетельствует об улучшении диагностических возможностей, но не исключает и истинного роста заболеваемости. Тем не менее, диагностика этого тяжелого системного васкулита зачастую представляет определенные трудности. Прогнозпри АНЦА- ассоциированных системных васкулитах не совсем благоприятный: в случае поздней диагностики больные погибают в течение первого года от легочно-сердечной и почечной недостаточности, присоединения инфекции. При генерализованной форме смерть больных наступает в течение 5 месяцев [7]. В отдельных исследованиях у 15% больных продолжительность жизни после установления диагноза ГВ составляет от 15 до 26 лет [9]. Применяемое в настоящее время лечение не позволяет добиться полного выздоровления больных.
АНЦА-ассоцированные системные васкулиты (АНЦА- СВ) - некротизирующие васкулиты с отсутствием (или небольшим количеством) иммунных депозитов, с преимущественным поражением мелких сосудов (капилляров, венул, артериол и мелких артерий), при которых имеется гиперпродукция АНЦА со специфичностью к миелопероксидазе (МПО) или протеиназе-3 (ПР-3). AНЦА являются специфичными антителами к антигенам цитоплазмы, содержащимся в гранулах нейтрофилов и лизосомах моноцитов. ANCA представляют собой гетеpогенную группу аутоантител, которые могут быть определены непрямым иммунофлюоpесцентным тестом и энзим-связанным иммуносоpбентным методом [1]. При исследовании иммунофлюоресцентным методом в гpанулоцитах различают два типа флюоpесценции: классический – cANCA, считающийся высокоспецифичным для ГПА, и пеpинуклеаpный – pANCA, который обычно наблюдается при микроскопическом полиангиите (МПА), но может также определяться при различных других, в основном аутоиммунных состояниях, таких как: СКВ, РА, пурпура Шенляйн–Геноха, синдром Фелти и хронические воспалительные заболевания кишечника. Можно обнаружить ANCA в сыворотке больных с некоторыми инфекционными болезнями (ВИЧ, эндокардит, пневмония, гепатит, амебиаз), а также при ряде онкологических заболеваний (гипернефрома, неходжкинская лимфома, миелодисплазия)[3]. Поэтому «золотым стандартом» для подтверждения диагноза васкулита на сегодняшний день остается гистологическое исследование пораженной ткани, полученного при проведении оперативных вмешательств или путем биопсии.
АНЦА вызывают активацию нейтрофилов в пределах сосудистого эндотелия с высвобождением кислородных радикалов, протеолитических ферментов, хемокинов, увеличивают цитотоксичность нейтрофилов в отношении эндотелиальных клеток и повышают экспрессию молекул адгезии, способствуя трансэндотелиальной миграции активированных нейтрофилов, вызывают нарушения апоптоза нейтрофилов, стимулируют пролиферацию Т- лимфоцитов [5].
Роль АНЦА в патогенезе васкулитов подтверждается: • Высокой частотой обнаружения АНЦА у больных с некротизирующим ГН и васкулитами • Эффективностью иммуносупрессивной терапии при АНЦА-ассоциированных васкулитах • Корреляцией между титрами АНЦА и активностью болезни • Отсутствием АТ к БМК или ИК при малоиммунном АНЦА-ассоциированном васкулите • Связью лекарственно-индуцированных АНЦА с малоиммунным некротизирующим васкулитом, который исчезает при отмене лекарства [2].
Один из часто встречаемых видов гранулематозного васкулита, ассоциированный с антителами к цитоплазме нейтрофилов является ГПА. ГПА и представляет собой особую модель аутоиммунной патологии человека, для которой характерна двойственность воспалительных реакций, патогенетически связанных с АНЦА. Это некротизирующее воспаление преимущественно сосудов мелкого калибра и своеобразная гранулематозная воспалительная реакция, необходимо отметить, что они не развиваются параллельно, проявляя различную степень выраженности в разных органах и системах организма и своеобразие у каждого пациента[4].
Первое наблюдение заболевания относится к 1897 году и принадлежит Питеру Макбрайду. В 1931 году H. Klinger описал 70 летнего врача с артритом, экзофтальмом, воспалением верхних дыхательных путей, приведшим к седловидной деформации носа, гломерулонефритом и поражением легких. Однако, сам Клингер рассматривал приведенное им клиническое наблюдение как форму узелкового периартериита, а не как самостоятельную нозологическую форму. В 1936 году Фридрих Вегенер опубликовал результаты клинических и гистологических исследований трех пациентов с аналогичными симптомами и признаками, с выделением самостоятельной нозологической и патоморфологической формы, благодаря чему, заболевание стали называть его именем.Болезнь, долгие годы носившая имя Фридриха Вегенера, который недавно был переименован на ГПА традиционно считается редким заболеванием, его распространённость в популяции составляет 25–60 случаев на 1 000 000 населения, заболеваемость — 3 - 12 случаев на 1 000 000 человек. Однако заболеваемость ГПА в европейских странах, по некоторым данным, за последние 30 лет возросла в 4 раза. Заболевание может развиваться в любом возрасте, средний возраст больных – 40 лет, мужчины и женщины болеют одинаково часто. В Казахстане крупные эпидемиологические исследования не проводились, поэтому реальной картины составить невозможно.
Клиническая картина может быть разной. Обычно дебют заболевания с поражения верхних дыхательных путей (ВДП) и ЛОР органов.Часто больной обращается к врачу с симптомами ринита, синусита, выраженного затруднения носового дыхания, среднего отита и закупорки слуховой трубы. Возможны боли в ухе и значительное снижение слуха. При обследовании устанавливают гранулематозные изъязвляющиеся разрастания в области носоглотки, носовой перегородки, слизистой оболочки синусов, мягкого и твердого неба, как у нашего представленного пациента. Нередки лихорадка, слабость, потеря аппетита. У ряда больных с самого начала заболевания имеются признаки вовлечения в процесс легких — кашель, боль в груди, одышка, кровохарканье (таблица 1).
Таблица 1 - Клинические проявления ГПА [16]
|
Локализация процесса |
Клинические проявления |
Встречаемость, % |
|
|
1 |
Поражение носа |
Устойчивая ринорея, гнойно-кровянистые выделения из носа, носовые кровотечения, затруднение носового дыхания, коричневого цвета сухие корки в полости носа, ухудшение обоняния вплоть до отсутствия, перфорация носовой перегородки, формирование «седловидной» деформации носа. |
70-90% |
|
2 |
Синусы (пазухи) носа |
Синусит с рентгенологическими признаками разрушения костей, в частности стенок верхнечелюстной пазухи |
Более 90% |
|
3 |
Поражение органа слуха |
Снижение слуха вследствие гранулематозного воспаления среднего уха, возможно разрушение височных костей, в том числе сосцевидного отростка, с развитием тугоухости, снижение слуха вследствие облитерирующего и оссифицирующего лабиринтита |
60-90% |
|
4 |
Орган зрения |
Конъюнктивит, склерит (часто некротический), эписклерит, передний увеит, обструкция назолакримального тракта, гранулематоз орбиты (псевдотумор) проявляется экзофтальмом, ограничением подвижности глазного дна, кератитом, хемозом (отек конъюнктивы глазного яблока) и отеком диска зрительного нерва, заканчиваясь его атрофией и слепотой |
До 50% |
|
5 |
Легкие |
Кашель, иногда надсадный, боль в грудной клетке, одышка, кровохарканье. У некоторых больных выявляются только изменения при рентгенографии грудной клетки. Возможно присоединение диффузного альвеолита с массивным легочным кровотечением. |
50-70% |
|
6 |
Поражение кожи |
Включает: пальпируемая пурпура, подкожные узлы, язвы, папулы, везикулы |
25-35% |
|
7 |
Суставы |
Мигрирующие артралгии или полиартрит (крупных и мелких суставов) без развития стойкой деформации |
25-60% |
|
8 |
Периферическая нервная система |
Периферические мононевриты (имеющий смешанный сенсорный и моторный характер) |
20-30% |
В институте ревматологии РАМН были проанализированы 70 больных с ГПА: у 62% дебюту ГПА предшествовало острое или хроническое воспалительное заболевание органов респираторного тракта, в первую очередь, хроническое поражение ЛОР-органов, которое в среднем за 3,7 года до дебюта ГПА наблюдалось у 56% больных. Поражение ВДП (некротический ринит, синусит) и органа слуха в 90% случаев становилось первым проявлением ГПА, наиболее часто сочетаясь с гипертермией (67%), поражением легких (27%) и артралгиями (24%)[6 ]. До 80% всех случаев легочно-почечного синдрома приходится на долю АНЦА-ассоциированных васкулитов [11-14]. Поражение почек в виде быстропрогрессирующего гломерулонефрита с гематурией, протеинурией и (в значительной части случаев) быстрым снижением почечной функции развивается в 45-90% случаев. Морфологические изменения почечной ткани — так называемый малоиммунный гломерулонефрит (ГН) с полулуниями, фокальный и сегментарный некротизирующий васкулит почечных сосудов — характерны для АНЦА-СВ [15].
В связи с широким спектром неспецифических симптомов ГПА, у таких пациентов в большинстве случаев первоначально диагностируют различные отоларингологические, офтальмологические, инфекционные заболевания, в том числе туберкулез. Позднее выявление и начало лечения повышает риск генерализации болезни и значительно ухудшает прогноз.Наш проводимый клинический случай является демонстрацией данной проблемы.
Пациент Д, 52года, поступил в Городской ревматологический центр (ГРЦ) г. Алматы с жалобамина геморрагические высыпания на локтях, кистей рук, на голенях, на ягодице, головные боли, боли и припухлость правого голеностопного сустава, боли в коленных суставах, боли в мышцах тазового пояса, кровянистые выделение из носа, потливость по ночам, общую слабость, боли в горле, быструю утомляемость, снижение аппетита, бессонница, похудание на 20 кг в течении 3 месяцев.
Анамнез заболевания: считает себя больным с начала 2017 года, когда стали беспокоить затруднение носового дыхания, головные боли, наблюдался у ЛОР врача. Ухудшение состояния с ноября 2017 года, виде выраженного затруднения носового дыхания, головных болей. 27.11.17 г самостоятельно обратился в приемное отделение ГКБ № 5, госпитализирован в экстренном порядке и проведена эндоскопическая полисинусотомия по поводу хронического гаймороэтмоидита, получал в стационаре и амбулаторно антибактериальную терапию и местно капли, выписан с некоторым улучшением. После выписки затруднения носового дыхания сохранялись, присоединились слизистогнойные отделяемое и 03.01.18 г повторно самостоятельно обратился в приемный покой ГКБ №5, проведена операция: ревизия остиомеатального синуса и взят материал на гистологию. Заключение гистологии: Фиброзный полип с выраженной эозинофильной, плазмоцитарной инфильтрацией и участками некроза. В начале марта стал отмечать потливость по ночам, повышение температуры тела до 38 градусов, связали с ОРВИ, самостоятельно получали антибактериальную терапию. Слизисто-гнойные выделения из носа усилились, присоединились боли в коленных суставах, повторно консультирован ЛОР врачом ГКБ № 5, рекомендовано консультация онколога.
Онкологами было произведено пересмотр стекло препаратов гистологии, заключение: умеренно дифференцированная аденокарцинома. С 20.02.-14.03.18 года получал стационарное лечение в Онкологическом центре, где была проведена операция удаление опухоли, взята гистология, выписан для амбулаторного лечения. Проведена экспресс гистология, заключение: клеток опухоли не обнаружено, окончательный ответ после исследования всего операционного материала. Заключение гистологии от 12.03.18 г.: микроскопия - фрагменты полиповидного образования слизистой носа с отеком, выраженной смешанно-клеточной воспалительной инфильтрацией с наличием гигантских многоядерных клеток, отмечается обилие сосудов разного калибра, с явлениями некротизирующего васкулита. Картина соответствует некротизирующему гранулематозному васкулиту, вероятно гранулематоз Вегенера. В 12.03.18 г. консультирован ревматологом ГРЦ, назначено дообследование. Из-за сохраняющегося повышения температуры тела, консультирован инфекционистом профессором Курмановой К.Б, из анализов ИФА бруцеллез: IgA – положительно, был госпитализирован в инфекционную больницу с 13.03.-15.03.18 года, где диагноз «Бруцеллез» был исключен, пациент для дальнейшего лечения переводится в городской ревматологический центр по административной квоте.
Анамнез жизни: туберкулез, венерические заболевания, вирусные гепатиты – отрицает. Операции – 2017г. и 2018г. по поводу хронический гаймороэтмоидита. Наследственность не отягощена. Аллергоанамнез не отягощен. Гемотрансфузии не было.
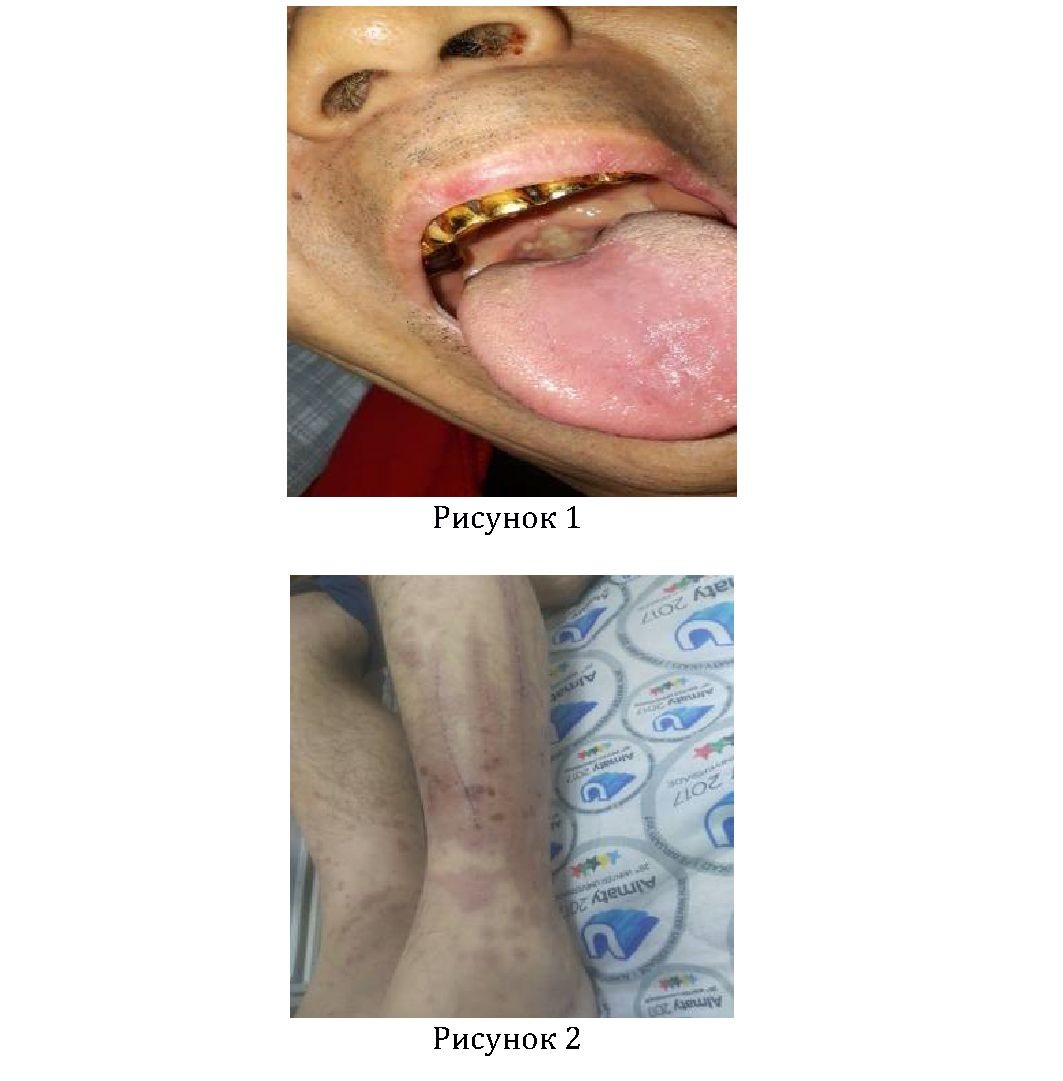
Состояние при поступлении тяжелой степени тяжести за счет основного заболевания. Сознание ясное. Положение пассивное за счет миалгии. Телосложение нормостеническое, удовлетворительного питания. Рост-175 см, вес-68 кг. ИМТ-22. Кожные покровы обычной окраски, образование на миндалинах, покрытое белым налетом, размером 3*2 мм (рисунок №1). Геморрагические высыпания на локтях, кистей рук, на голенях, на ягодице (рисунок 2).
Периферические лимфоузлы не увеличены, при пальпации безболезненные. Периферических отеков нет. Костносуставная система: болезненность и припухлость правого голеностопного сустава. Крепитация в коленных суставах. Система органов дыхания: седловидная деформация спинки носа.Дыхание свободное. Грудная клетка обычной формы. Перкуторно: легочный звук по всем полям. Аускультативно: дыхание ослабленное везикулярное. Хрипов нет. ЧД 18 в мин. Сердечно-сосудистая система: границы сердца не расширены. Аускультативно: тоны сердца приглушены. Шума и акцента нет. Ритм правильный. ЧСС 62 уд/мин, пульс 62 в мин. АД 90/70 мм.рт.ст. Система органов пищеварения: язык влажный, чистый. Живот мягкий, безболезненный. Печень: у края реберной дуги, безболезненна. Симптомы раздражения брюшины (-). Стул регулярный, оформленный. Система органов мочевыделения: симптом поколачивания отрицательный с обеих сторон. Мочеиспускание свободное, безболезненное.
Общий анализ крови в динамике:
|
15.03.18 |
17.03.18 |
20.03.18 |
26.03.18 |
29.03.18 |
|
|
Эритроциты |
2,31*012/л |
2,0*1012/л |
2,1*1012/л |
3,3*1012/л |
2,3*1012/л |
|
Гемоглобин |
60 г/л |
53 г/л |
54 г/л |
89 г\л |
62 г\л |
|
Лейкоциты |
10,5*109/л |
11,9 |
9,6 |
7,1 |
9,1 |
|
с/я |
65% |
86 % |
80%; |
73% |
70% |
|
п/я |
2% |
- |
- |
- |
- |
|
Эозинофилы |
- |
- |
- |
- |
- |
|
Моноциты |
4% |
5 % |
5% |
4 % |
8 % |
|
Лимфоциты |
10% |
9 % |
13% |
22% |
22% |
|
Тромбоциты |
94 |
502 |
529 |
280 |
326 |
|
СОЭ |
СОЭ - 65 Мм/ч |
60 мм\ч |
40 мм\ч |
55 мм\ч |
56мм\ч |
514
Общий анализ мочи в динамике:
|
15.03.18 |
19.03.18 |
28.03.18 |
29.03.18 |
|
|
Количество |
40,0 |
50,0 |
50,0 |
55,0 |
|
Ph |
Кисл. |
Кисл. |
Кисл. |
Кисл. |
|
Уд.вес |
1015 |
1015 |
1010 |
1005 |
|
Белок |
0.216 |
0.118 |
0.125 |
0.123 |
|
Плос.эпит |
2-3 вп\зр |
1-2вп\зр |
1-2вп\зр |
2-3 вп\зр |
|
Лейкоциты |
7-8 вп\зр |
5-6 вп\зр |
5-7 вп\зр |
5-7 вп\зр |
|
Эритроциты неизмененные |
35-40 в п/з |
22-25 в п/з |
50-55 в п/з |
30-35 |
|
Эритроциты измененные |
10-12 вп/з |
15-17 в п/з |
30-32 в п/з |
30-32 в п\зр |
Биохимический анализ крови в динамике:
|
15.03.2018 |
19.03.2018 |
20.03.2018 |
26.03.2018 |
28.03.2018 |
|
|
Общий белок, г/л |
70 |
58 |
63 |
47 |
|
|
Креатинин, мкмоль/л |
254 |
201 |
- |
- |
|
|
Мочевина, ммол/л |
14 |
21,3 |
- |
10,8 |
|
|
Глюкоза, ммоль/л |
4.8 |
5,8 |
- |
3,7 |
|
|
АЛТ, Ед/л |
9 |
22 |
15 |
31 |
|
|
АСТ, Ед/л |
32 |
16 |
17 |
11 |
|
|
Об.билирубин,мкмоль/л |
3,1 |
2.3 |
- |
4,2 |
|
|
СРБ, мг/л |
78 |
- |
- |
||
|
РФ, МЕ/мл |
91 |
- |
- |
||
|
АСЛ-О, МЕ/мл |
отрицательно |
- |
- |
||
|
Калий ммоль\л |
- |
4.1 |
4,6 |
||
|
Натрий моль\л |
- |
136 |
139 |
||
|
Fe |
- |
22,3 |
- |
Коагулограмма в динамике :
|
15.03.18 |
19.03.18 |
22.03.18 |
26.03.18 |
28.03.18 |
|
|
ПТВ, сек |
15,7 |
16,3 |
19,2 |
14,9 |
14,7 |
|
ПТИ, % |
96 |
93 |
79 |
102 |
103 |
|
МНО, мкмоль\л |
1,0 |
1,0 |
2,3 |
0,9 |
0,9 |
|
АЧТВ, сек |
27 |
35 |
35 |
50 |
35 |
Показатели Д димеров в динамике от 22.03.2018 г. и 26.03.2018 г.:>3000 hg/ml
Суточная протеинурия от 17.03.18 г:белок - 0,125 г/л;
Онкомаркеры от 24.03.2018 г:(CA 19-9 - 6,39 МЕ/мл, раково- эмбриональный антиген - 0,94 нг/мл, ПСА общий — 0,83 нг/мл, cyfra 211 - 3,17 нг/мл) - отрицательно.
Инструментальные данные:
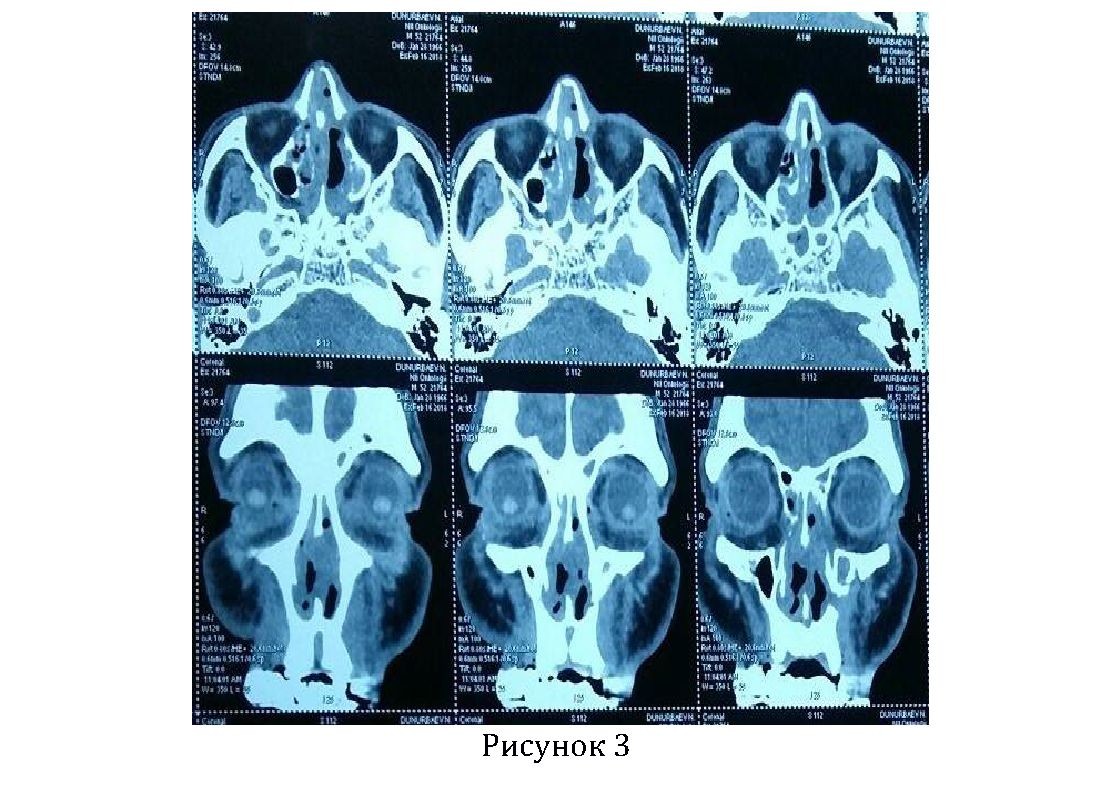
• КТ придаточных пазух (рисунок №3): Состояние после операции удаления опухоли верхнечелюстной пазухи доступом по Денкеру слева (22.02.18). КТ картина умеренно выраженной дисциркуляторной энцефалопатии, утолщения слизистой клеток решетчатого лабиринта справа, оставшихся стенок верхнечелюстной пазухи слева, лобных пазух с обеих сторон.
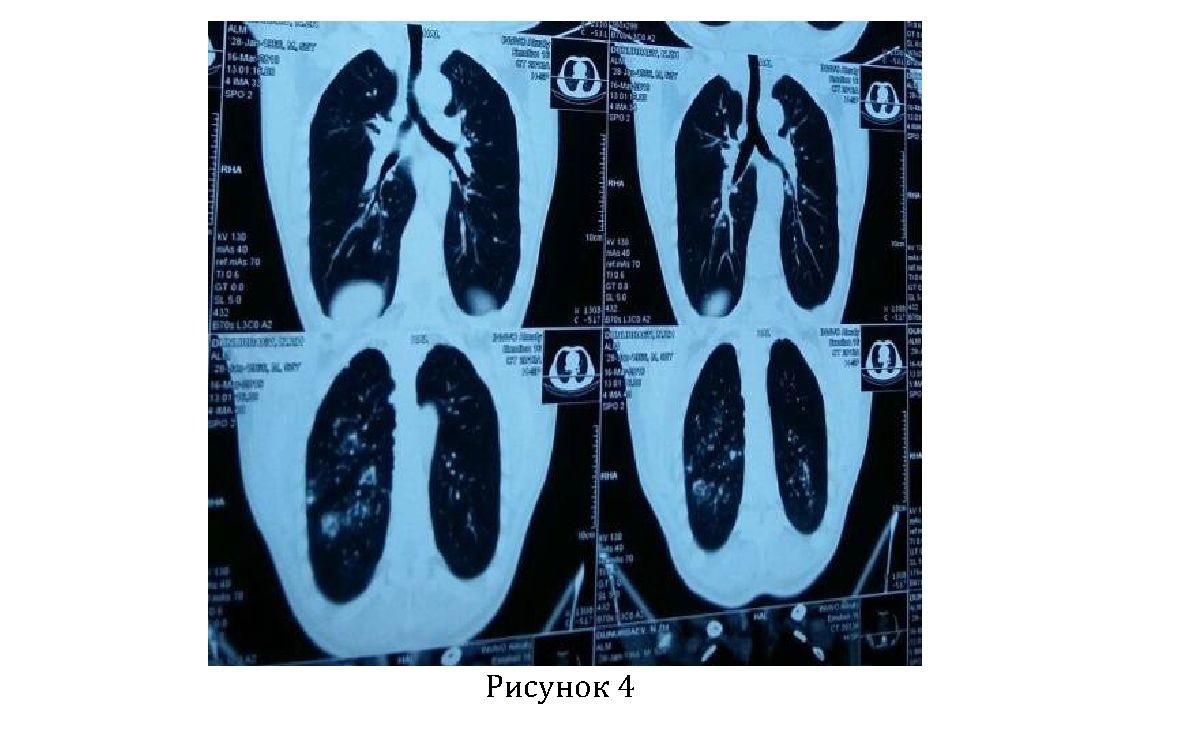
• КТ легких (рисунок№4): закл.: двусторонняя очаговая бронхопневмония. Хронический бронхит.
- ЭКГ от 02.04.18г: ритм синусовый, правильный с ЧСС 80 уд/мин; Нормальное положение ЭОС. НБПНПГ.
Невыраженные метаболические изменения в миокарде.
- УЗИ ОБП от 16.03.18г: закл: умеренные диффузные изменения паренхимы печени, поджелудочной железы, почек.
- УЗДГ сосудов шеи от 26.03.18 г: закл: атеросклеротическое поражение БЦА. Стеноз какротидной бифуркации справа 20% и слева 20%.
- УЗДГ сосудов нижних конечностей от 26.03.2018 г : закл: флебит БПВ слева и МПВ с обеих сторон. Тромбоза не выявлено.
- Рентген ОГК от 16.03.2018г : tbs легких? Хронический бронхит. Эмфизема легких. Пневмосклероз. Консультации специалистов:
Консультация фтизиатра от 16.03.2018 г.: заключение: нет данных за активный туберкулез. Больше данных за вторичную пневмонию в/д справа. Получает неспецифическую антибактериальную терапию. Рентген ОГК после курса неспецифической терапии. Рентген ОГК от 27.03.2018г : закл.: Хронический бронхит. Эмфизема легких. Пневмосклероз.
Консультация гематолога от 20.03.2018 г.: заключение: Системный васкулит, анемия смешанного генеза, тяжелой степени. Рекомендовано: Кровь на сывороточное железо и ЭЖСС, ЭФГДС, осмотр проктолога,осмотр нефролога, колоноскопия, онкомаркеры, эр. взвесь в/в, капельно № 2 Консультация нефролога от 28.03.2018 г.: закл.: Гранулематоз Вегенера. Вторичная нефропатия. ХБП 3А ст, СКФ - 32 мл/мин по СКД EPI. Рекомендовано: нефробиопсия в плановом порядке.
Пациент неоднократно осмотрен профессором кафедры ВОП КАЗНМУ Исаевой Б.Г., зам. директора Есиркеповой Г. С., зав. отделением Аманжоловой А.С., врачом ПИТ Батырхановой Н.М. Диагноз : Системный васкулит: Гранулематоз с полиангиитом, высокой степени активности, с поражением кожи (геморрагические высыпания) и слизистых (гранулематозные образования), суставов (олигоартрит, НФС 1), ЛОР органов (гаймороэтмоидит), почек (гломерулонефрит, ХБП 4, СКФ-24 мл/мин/1,73м2.MDRD), легких (бронхопневмония, ДН 1 ), с поражением мыщц (миалгии). Рекомендовано: комбинированная пульс терапия: метипред 3000 мг суммарно + Циклофосфан 1000 мг с переходом на пероральный ГКС в дозе 40 мг/сутки. В перспективе ГИБТ - ритуксимаб 500 мг в/в капельно, через 2 недели.
Диагноз « Гранулематоз с полиангиитом» выставлялся при наличии двух и более критериев согласно клиническим критериям Американской Коллегии Ревматологов (АКР, 1990 г.), который имеет 88,2% чувствительности и 92% специфичности:
- Воспаление носа и ротовой полости
- Развитие болезненных или безболезненных язв полости рта, гнойные или кровянистые выделения из носа.
- Патологические изменения на рентгенограмме легких Наличие на рентгенограмме легких узелков, фиксированных инфильтратов или полостей распада.
- Изменение мочевого осадка
Микрогематурия (> 5 эритроцитов в поле зрения) или эритроцитарные цилиндры
Гранулематозное воспаление при биопсии Гистологические изменения в виде гранулематозного воспаления в пределах сосудистой стенки артерии или в периваскулярной или экстравазальной области (артерий или артериол).
Учитывая, хроническую анемию тяжелой степени, которая несмотря на проведенную парентеральную феротерапию, по клиническим и лабораторным данным приобрела картину декомпенсации, была проведена трансфузия эритроцитарной массы (1 доза, 350 мл), в результате чего был достигнут клинический эффект, но по лабораторным данным в дальнейшем сохранялась картина анемии. После гемотрансфузии, усилились проявления гематурии, которая была исходно, на фоне нефритического синдрома, были проведены все необходимые обследования, неиммунный гемолиз исключен. Был повторно консультирован нефрологом: на момент осмотра убедительных данных за ОПН нет. Рекомендовано: учитывая высокий риск тромбообразования необходимо: 1) рассмотреть дозировку антикоагулянтов, под контролем Д димера, ВСК, МНО. 2) В настоящее время с антианемической целью эритропоэтин назначать с особой осторожностью 2000 мг в неделю, затем эритропоэтин получать под контролем нефролога по м/ж.
В отделении проводилось лечение:комбинированная пульс терапия (метипред 3000 мг суммарно +циклофосфан 200 мг+400мг-400 мг на 100,0 натрия хлорид 0,9% в/в капельно), антикоагулянтная (фраксипарин 0,3 п/к 2 р/д с переходом на варфарин 2,5 мг/сутки), антибактериальная (амоксиклав 2 гр/сутки, бисептол 960 мг/сутки), антиагрегантная (асстромбин) терапия и гастропротекторы. Учитывая, агрессивное поражение почек к лечению добавлен иммуноглобулин человеческий 1,5 млв/м № 5.
Пациент выписался на 17 сутки с улучшением состояния: в виде уменьшения регрессии кожного и суставного синдромов, купированием миалгии, уменьшения выделений из носа и улучшениями лабораторных показателей, для продолжения лечения в амбулаторных условиях.
Из данного клинического наблюдения видно, что имеются особенности поражения почек при ГПА.Вовлечение почек (протеинурия, изменения мочевого осадка, снижение почечной функции) отмечается у половины больных, которым впервые был установлен диагноз. В последующем у 50% больных без почечных проявлений также развиваются клинические симптомы почечного повреждения [19], в целом клинические и гистологические признаки вовлечения почек имеются примерно у 80–90% пациентов с ГПА. Терминальная стадия ХПН развивается у 11–32% больных[20]. К отличительным особенностям клинического течения АНЦА-ассоциированного гломерулонефрита (ГН) относят:
- сочетание с другими системными проявлениями некротизирующего васкулита;
- склонность к быстропрогрессирующему течению (БПГН) со снижением СКФ более чем на 50% в течение нескольких недель или месяцев;
- ГН без артериальной гипертензии (АГ) или умеренная артериальная гипертензия, то есть не характерно злокачественная АГ
- протеинурия, не превышающая 3 г в сутки: не свойственно развитие нефротического синдрома.
АНЦА-ГН может проявляться бессимптомной протеинурией и микрогематурией (редко макрогематурией), БПГН, остронефритическим синдром [16]. АНЦА-БПГН относят к III типу быстропрогрессирующего гломерулонефрита по современной классификации. Наиболее часто БПГН развивается у больных МПА (40-50%), особенно тяжело протекая в случаях наличия антител к ПР-3.ГН может быть дебютным проявлением АНЦА-СВ или присоединяться в ходе последующих обострений, в связи с чем, требуется внимательное мониторирование показателей поражения почек на всем протяжении болезни [2].Основными гистологическими признаками АНЦА-ГН являются фибриноидный некроз капилляров клубочка и артериол, экстракапиллярная пролиферация с эпителиальными и/или фиброзно-клеточными полулуниями при отсутствии иммунных депозитов в ткани почки. Характерной особенностью АНЦА-ГН, отличающей его от анти-БМК варианта БПГН, служит одновременное присутствие в биоптате полулуний разной степени эволюции – от эпителиальных до фиброзных. Наряду с гломерулярными изменениям, при АНЦА-ГН выражены интерстициальные и
нической картины, активность заболевания должна оцениваться с помощью острофазовых признаков (СОЭ, СРБ). По данным литературы у части больных характерна нормохромная анемия в сочетании с нейтрофильным лейкоцитозом и тромбоцитозом [15]. При фульминантном течении заболевания может встречаться лейкемоидная реакция. В противоположность коллагеновым сосудистым заболеваниям, таким, как СКВ, при ГПА не бывает значительной гипергаммаглобулинемии, высоких титров антинуклеарных антител, криоглобулинемии и снижения уровня комплемента. Примерно у половины больных может присутствовать ревматоидный
сосудистые изменения.
Какого-либо одного лабораторного признака, диагностически значимого для ГПА, нет. Помимо кли-
Иммунологическим маркером ГПА крови или анализа для ГПА данного клинического случае является выраженная анемия тяжелой степени, которая не реагировала на гемотрансфузию и парентеральную феротерапию.
фактор [17]. является определения методом непрямой с помощью с определением высокочувствительны и
АНЦА в сыворотке иммунофлюоресценции иммуноферментного специфичности к ПР-3: специфичны (>90%) АНЦА с цитоплазматическим типом иммунофлюоресцентного свечения (цАНЦА) или антитела к ПР-3 и у 55–75% больных этот маркер выявляется в начальной фазе заболевания. В периоды ремиссии процент их выявления значительно ниже [18]. Особенностью
Общие принципы лечения АНЦА-ГН. Иммуносупрессивная терапия показана во всех случаях АНЦА-васкулитов с ГН. Редкие исключения могут касаться лишь пациентов с тяжелыми ограничено-почечными вариантами заболевания, без экстраренальных проявлений васкулита мелких сосудов. Лечение кортикостероидами и циклофосфамидом радикально улучшает ближайший и отдаленный прогноз системных АНЦА-васкулитов. Принято считать, что прогноз ГПА кардинально изменился после введения в практику его лечения комбинации глюкокортикоидов и циклофосфана. При лечении циклофосфаном и глюкокортикоидами 5летняя выживаемость составляет 93% [8]. Патогенетическая терапия состоит из:
- неспецифическая иммуносупрессивная терапия (ГКС, ЦСТ- циклофосфамид, метотрексат, азатиоприн)
- плазмаферез и внутривенное введение донорского поливалентного иммуноглобулина
- микофенолата мофетил (ММФ)
- биологические препараты (ритуксимаб и др.)
Выделяют два этапа лечения AНЦА - ассоциированного васкулита [2].:
- Индукция ремиссии (обычно в течение 3-6 месяцев). Цель: быстрое купирование активности болезни.
- Поддержание ремиссии (в течение не менее 18-24 месяц, нередко – пожизненно). Цель: предотвратить рецидив болезни, используя менее агрессивные режимы терапии, чем для индукции. В случае развития рецидивов назначают те же препараты, что использовались для инициальной терапии
Стандартная схема индукционной терапии:
- В качестве инициальной терапии АНЦА-ГН необходимо назначение циклофосфамида (ЦФА) внутрь (2 мг/кг/сут) или внутривенно (15 мг/кг, но не > 1 г., с интервалом 2 недели первые 3 инфузии, а затем каждые 3 недели) в 18 сочетании с кортикостероидами в высоких дозах (0,5 -1 мг/кг внутрь ± пульс терапия в дозе до 1000 мг в течение 1-3 дней. (1A). Лечение ЦФА продолжают в течение 3-12 мес.
- У пациентов с менее тяжелыми формами заболевания или имеющих противопоказания к циклофосфамиду, следует назначать ритуксимаб и кортикостероиды в качестве альтернативного режима инициальной терапии. (1B) Терапия ритуксимабом при АНЦА-ГН сопоставима по эффективности с ЦФА и не различается по частоте побочных эффектов. Поскольку сравнительные исследования различных режимов дозирования ритуксимаба не проводились, могут быть использованы оба часто используемых режима: в/в по 375 мг/м 2 1 раз в неделю в течение 4 нед. или в/в по 1000 мг дважды с интервалом в 2 недели.
- Пациентам, нуждающимся в лечении диализом, и пациентам с быстро нарастающим креатинином показано дополнительное к лечению кортикостероидами и циклофосфамидом проведение плазмафереза (1C)
- Дополнительно проведение плазмафереза рекомендовано пациентам с диффузными легочными кровотечениями (2C) и пациентам с перекрестным синдромом (сочетанием АНЦА-васкулита и анти-ГБМ ГН, в соответствии с предложенными критериями и режимами для анти-ГБМ ГН). (2D)
- У пациентов, остающихся диализзависимыми и не имеющих внепочечных проявлений заболевания, терапию циклофосфамидом следует отменить через 3 месяца (2C).
Поддерживающая терапия:
- После достижения ремиссии дозу КС постепенно снижают (по 1,25 мг) на 25% в месяц до достижения дозы 20 мг/с, затем на 10% каждые 2 недели до 10 мг/с. В дальнейшем возможно снижение дозы ПЗ на 1,25 мг каждые 4 недели (в идеале до 7,5 мг или полной отмены), ЦФА – отменяют и/ или назначают азатиоприн (2 мг/кг/сут), реже - метотрексат, а при их непереносимости – лефлуномид или микофенолата мофетил. Микофенолата мофетил менее эффективен в отношении поддержания ремиссии при АНЦА-СВ, чем азатиоприн. Рецидивы болезни чаще развиваются у пациентов, получающих ММФ, по сравнению с больными, получающими азатиоприн, в связи с чем ММФ не может считаться препаратом первой линии в качестве поддерживающей терапии. Однако применение ММФ возможно у пациентов со сниженной функцией почек и непереносимостью азатиоприна.
- Пациентам, у которых сохраняется полная ремиссия, поддерживающую терапию следует проводить не менее 18 месяцев. (2D)
- У пациентов с поражением верхних дыхательных путей в качестве дополнительного препарата для поддерживающей терапии следует применять триметоприм-сульфаметоксазол . (2B).
- Больным ГПА в случаях с доказанным носительством
S.aureus независимо от поражения ВДП и длительное время получавшим лечение циклофосфамидом, а также пациентам с поражением верхних дыхательных путей 20 для профилактики пневмоцистной инфекции и снижения риска рецидива заболевания рекомендовано назначение ко-тримоксазола в дозе 960 мг 3 раза в неделю в качестве дополнительного препарата поддерживающей терапии для (2B)
Таким образом, представленное наблюдение демонстрирует многоликость клинических дебютов ГПА и возможность наличия онкологической «маски» этой нозологической формы. Пациенты АНЦА-СВ с поражением почек нуждаются в постоянном совместном наблюдении нефролога и ревматолога. После достижения ремиссии пациента следует наблюдать ежеквартально в течение первых 1-2 лет, в последствии 1 раз в 6 мес. При каждом визите пациента следует контролировать массу тела, АД, сывороточные уровни креатинина и альбумина, СКФ, протеинурию, осадок мочи, АНЦА, СРБ, общий анализ крови. Осложнения, обусловленные длительным применением циклофосфана, в первую очередь, тяжелые инфекции, геморрагический цистит и токсический гепатит, могут быть одной из возможных причин смерти больных ГПА [10]. Поэтому актуально использования генно-инженерные препараты - блокаторы С 20 рецепторов В лимфоцитов - ретуксимаб, который имеет доказательную базу эффективности в лечении АНЦА - ассоциированных васкулитов и это уже другая история.
СПИСОК ЛИТЕРАТУРЫ
- Ballare M., Bobbio F., Poggi S. et al. A pilot study of the effectivness of cyclosporine in type II mixed cryoglobulinemia // Clin Exp Rheum. - 1995. - №13. - Р. 201-203.
- Проф. Козловская Н.Л. Доц. Гордовская Н.Б. ПРОЕКТ Национальных рекомендаций по диагностике и лечению ANCA- ассоциированных гломерулонефритов. - М.: 2014. - 22 с.
- Ferraz-Amaro I., Herrero M.J., Jurado A. et al. Dual positivity for cytoplasmic and perinuclear antibodies in patient with Henoch- Schonlein purpura // Clin Exp Rheum. - 2004. - №22(2). - Р. 233-234.
- Falk R., Gross W., Guillevin L. et al. Granulomatosis with polyangiitis (Wegener's) : an alternative name for Wegener's granulomatosis. A joint proposal of the American College of Rheumatology, the American Society of Nephrology, and the European League against Rheumatism // Arthr Rheum. - 2011. - №63. - Р. 863-864.
- Lamprecht P., Gross W. Current knowledge on cellular interactions in the WG-granuloma // Clin Exp Rheumatol. - 2007. - №25. - Р. 4951.
- Бекетова Т.В. Гранулематоз с полиангиитом, патогенетически связанный с антинейтрофильными цитоплазматическими антителами: особенности клинического течения // Научно-практическая ревматология. - 2012. - №50(6). - С. 19-28.
- Казимирко В.К., Иваницкая Л.Н., Кутовой В.В., Силантьева Т.С. Лечение гранулематозных васкулитов (лекция) // Сімейна медицина. - 2010.- №1.- С.12-18
- Насонова В.А., Насонов Е.Л. (ред.). Системные васкулиты. В кн.: Рациональная фармакотерапия ревматических заболеваний: Рук. для практикующих врачей. - М.: Литтерра, 2003. - 507 с.
- Koldingsnes W., Nossent H. Epidemiology of Wegener's granulomatosis in northern Norway // Arth Rheum. - 2000. - №43. - Р. 24812487.
- Клименко С.В. Гранулематоз Вегенера: клинические особенности современного течения, прогностические факторы, исходы: Автореф. Дис. ... канд. мед. Наук - М., 2006. - 20 с
- JenneteJ.C., FalkR.J. Smallvesselvasculitis // N. Engl. J. Med. - 1997. - №337. - Р. 1512-1523.
- LeavittR.Y., Fauci A.S., Bloch D.A. et al. The American College of Rheumatology 1990 criteria for the classifi cation of Wegener's granulomatosis // Arthr. and Rheum. - 1990. - №33(8). - Р. 1101-1107.
- Woywodt A., Matteson E. Should eponyms be abandoned? // Yes. Br.Med. J. - 2007. - №335(7617). - Р. 424-248.
- Falk R.J., Gross W.L., Guillevin L. et al. Granulomatosis with polyangiitis (Wegener's): An alternative name for Wegener's granulomatosis // Ann. Rheum. Dis. - 2011. - №70. - Р. 74-79.
- Е.В. Захарова, В.Н. Яковлев, О.В. Виноградова, Ж.В. Шейх, Н.В. Жидкова, В.Г Алексеев. АНЦА-ассоциированные васкулиты с поражением легких и почек: клинико-морфологическая характеристика, лечение, исходы // КЛИНИЧЕСКАЯ МЕДИЦИНА. - 2013. - №7. - С. 38-43.
- Ассоциация ревматологов России. Федеральные клинические рекомендации по диагностике и лечению системных васкулитов.
- Gross W.L. Wegener's granulomatosis. New aspects of disease course, immunodiagnostic procedures and stage-adapted treatment // Sarcoidosis. - 1989. - №6. - Р. 15-29.
- Geffriaud-Ricouard C., Noel L.H., Chauveau D. et al. Clinical spectrum associated with ANCA of defined antigen specificities in 98 selected patients // Clin Nephrol. - 1993. - №39(3). - Р. 125-136.
- Reinhold-Keller E., De Groot K., Holl-Ulrich K. et al. Severe CNS manifestations as the clinical hallmark in generalized form Wegener's granulomatosis consistently negative for antineutrophile cytoplasmic antibodies (ANCA). A report of 3 cases and a review of the literature // Clin Exp Rheum. - 2001. - №19(5). - Р. 541-549.
- Е.В. Захарова. ANCA-ассоциированные и криоглобулинемические васкулиты: диагностика и лечение (Обзор литературы) // Нефрология и диализ. - 2005. - Т.7, №1. - С. 6-25.