Пластика посттравматических дефектовостается актуальной темой для обсуждения из-заанатомических особенностей. Несмотря на то, что существуют многочисленные методы реконструктивных вмешателств, выбор идеального варианта пластики представляет оперделенные трудности. Хорошим решением может стать пересадка тканевых комплексов, которая позволяет в короткие сроки ликвидировать дефекты мягких и костных тканей, восстанавливая нормальное послойное строение пораженной области, с полной функциональной и косметической реабилитацией.
Введение.
Проблема лечения посттравматического дефекта пяточной области до настоящего времени остается актуальной. За последний год возросло количество пострадавших с травмами стопы, приводящих впоследствии к дефектам и деформациям, лечение которых зачастую затягивается на месяцы и годы. В итоге более 60% пациентов остаются нетрудоспособными [1,2,3].
Длительность лечения и высокий процент инвалидности пострадавших обусловлен не только характером полученных повреждений, но и качеством оказания им медицинской помощи. Ввиду особенностей анатомического строения тканей стопы, испытывающей постоянную нагрузку импульсного характера, применение аутодермопластики на гранулирующие раны стопы (очень распространенная методика в разнопрофильных стационарах) мало оправдано.
Внедрение микрохирургического метода в восстановлении, реконструкции и пластике поврежденных конечностей с применением лоскутной хирургии остается методом выбора. Уже более 10 лет пересадка тканевых комплексов позволяет в короткие сроки ликвидировать дефекты мягких и костных тканей, восстанавливая нормальное послойное строение пораженной области, с полной функциональной и косметической реабилитацией [4].
Цель. Ознакомить медицинскую общественность с некоторыми возможностями пластической микрохирургии в лечении дефекта мягких тканей.
Клинический случай.
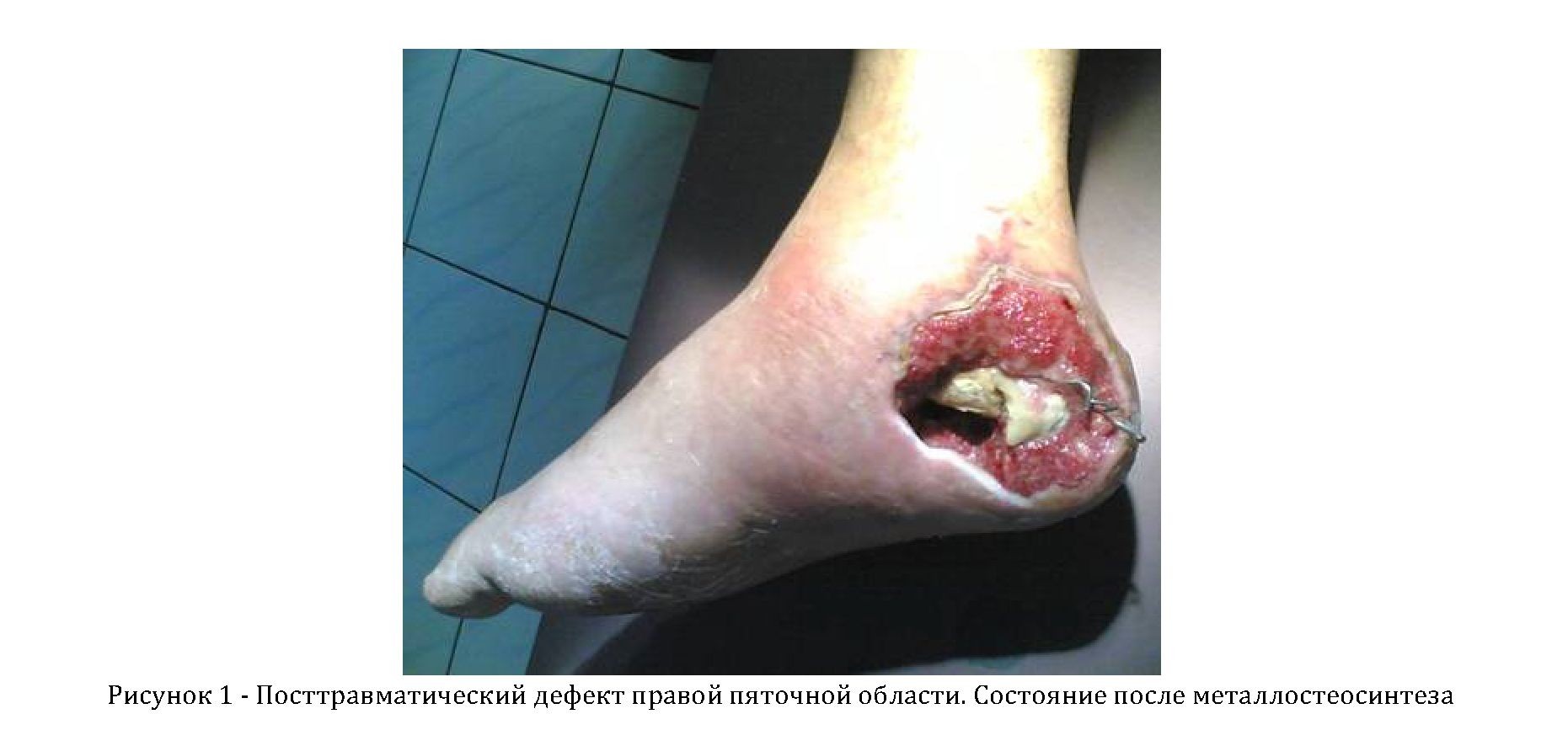
Пациент, 41 год,госпитализирован в отделении микрохирургии акционерного общества «Национальный Научный центр хирургии имени Александра Николаевича Сызганова» с диагнозом: «Инфицированная рана правой стопы. Посттравматический дефект мягких тканей пяточной области. Многооскольчатый перелом пяточной кости с дефектом костной ткани. Хронический остеомиелит. Состояние после спицевогометаллоостеосинтеза». За три месяца до обращения у пациента был закрытый многооскольчатый перелом пяточной кости правой стопы. На третьи сутки в условиях травматологического стационара выполнена открытая репозиция отломков пяточной кости с фиксацией последних тремя спицами Киршнера. На 10 сутки имело место нагноение раны, некроз мягких тканей. Выполнена некрэктомия, санация и дренирование раны. Назначена антибактериальная терапия. Эффекта от проведенного лечения не отмечено. Сохранялись боли, вынужденное возвышенное положение конечности, рана не заживала. В течение 2 месяцев образовался дефект тканей, развился остеомиелит. В течение всего периода времени пострадавший не работал. Направлен в отделение микрохирургиидля дальнейшего хирургического лечения.
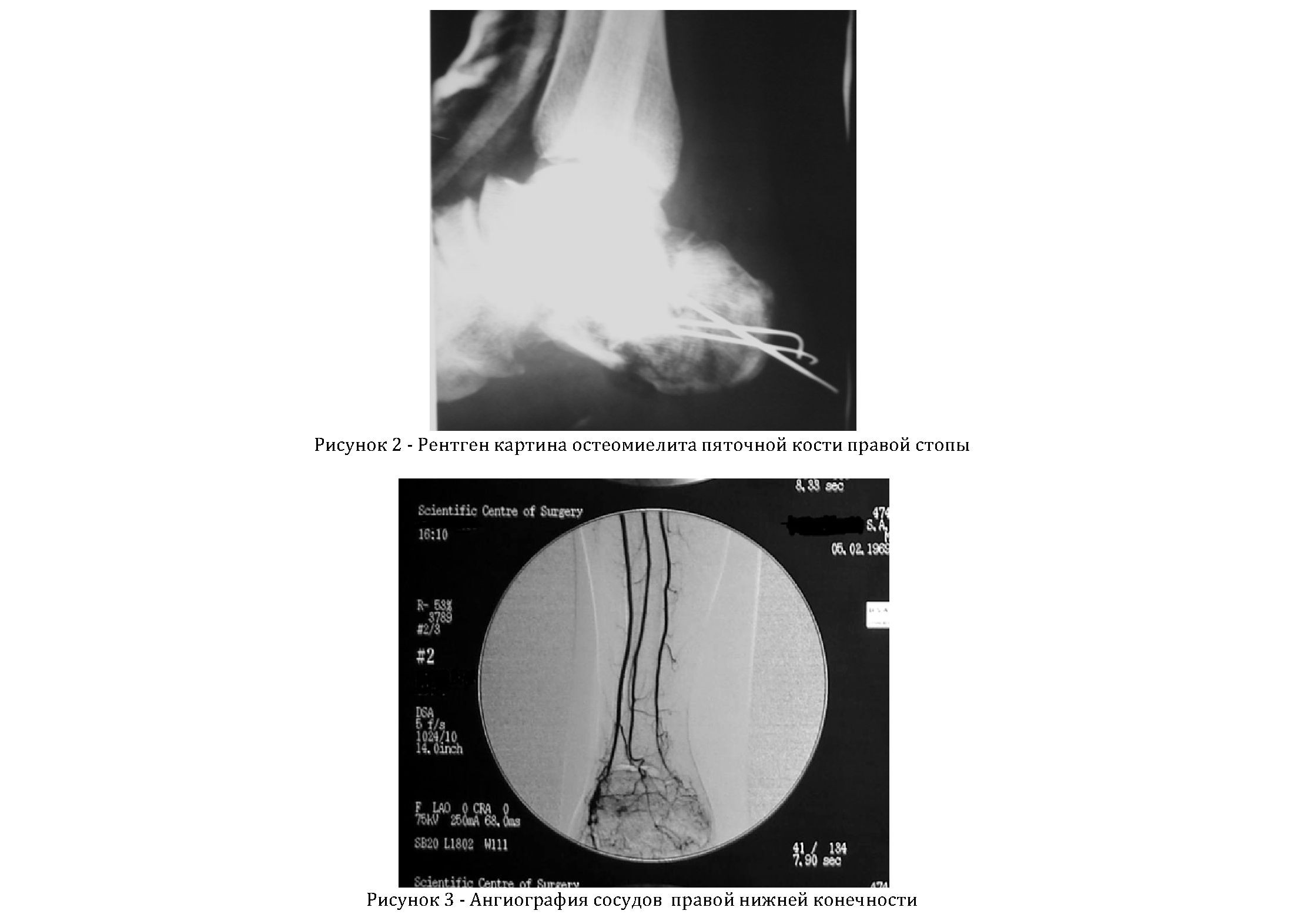
При поступлении (рисунок 1) локально: правая стопа и голень отечны, ткани пастозны. На внутренней поверхности стопы имеется рана, распространяющаяся от уровня внутренней лодыжки с переходом на пяточную область, область бугристости пяточной кости, подошвенную поверхность (1/3) пятки до предплюсны. Отделяемое гнойное, серо-желтого цвета, сливкообразной консистенции. Из раны - гнилостный запах. Края раны каллезные, с вялыми грануляциями, местами с гнойным и фибриновым налетом. Дно раны: отломки пяточной кости желто-серого цвета, "сахарной" плотности, фиксированные тремя спицами. Спицы и отломки подвижны. Движения стопой болезненны, в пределах качательных. Гипестезия в зоне иннервации большеберцового нерва. Пульсация передней большеберцовой артерии отчетливая. Посев из раны - синегнойная палочка. На рентгенограмме - многооскольчатый перелом пяточной кости. Состояние после спицевого остеосинтеза. Остеомиелит (рисунок 2). Проведено ангиографическое исследование. Сосуды правой нижней конечности проходимы (рисунок 3).
Ввиду обширности тканевого дефекта, гнойновоспалительного процесса использование различных лоскутов стопы (подошвенный, тыльный и т.п.) не представлялось возможным. Таким образом, относительно простой способа лечения этой патологии - транспозиция комплекса тканей, остаетсяметодом выбора [5].
Пациенту в один этап выполнены секвестрэктомия и пересадка островкового кожно-фасциально-мышечного лоскута,кровоснабжающегосяперфорантными сосудами задней большеберцовой артерии на периферической сосудистой ножке. Операция выполнялась под 5-кратным увеличением лупы с применением микрохирургической техники.
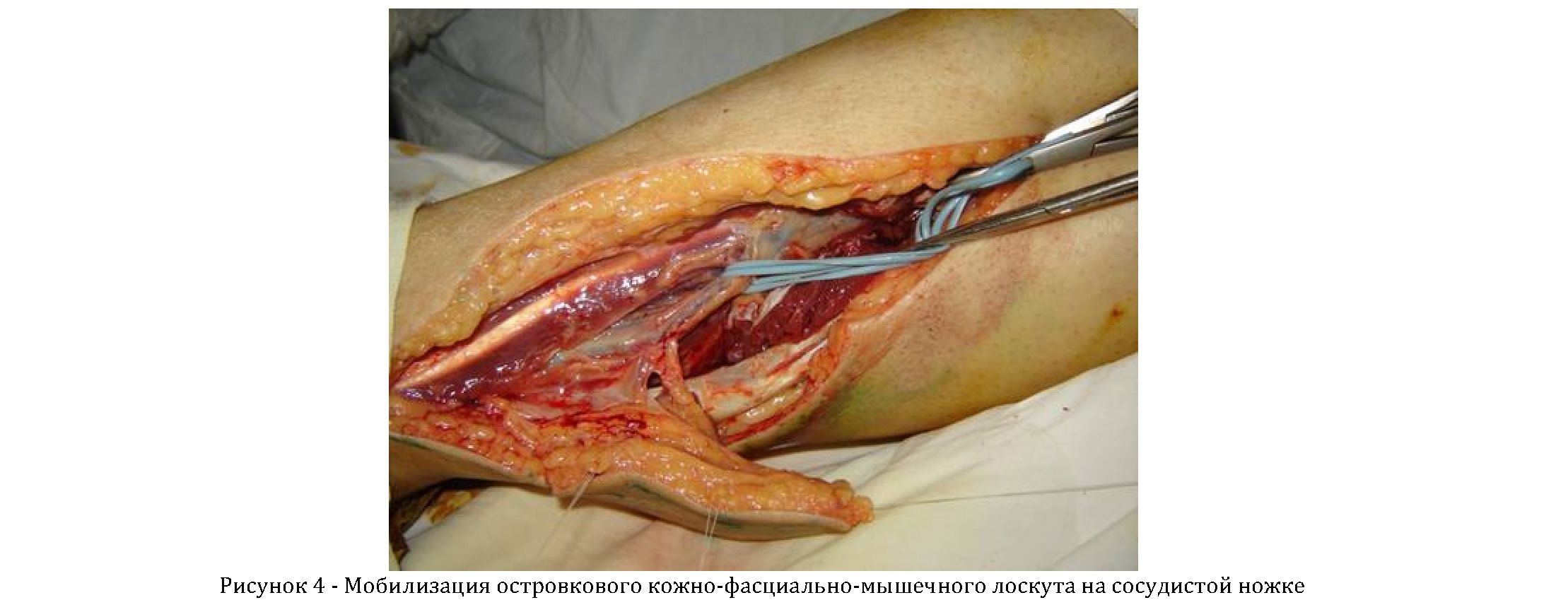
Основные этапы операции. После удаления костных фрагментов, подвергшихся деструктивным изменениям,произведены замеры образовавшегося дефекта и границ забираемого лоскута, соответственно размерам дефекта. Определена необходимая для ротации длина сосудистого пучка и места отхождения двух дистальных перфорантных сосудов (под контролем допплероскопии). Лоскут размерами 12х6см выкраивали субфасциально от центра к периферии (рисунок 4).
На границе верхней и средней трети голени выделяли задний большеберцовый сосудисто-нервный пучок. Сосудистый пучок вместе с перфорантными сосудами, находящимися в межмышечной перегородке, отделяли от большеберцового нерва. После выкраивания лоскута вместе с фрагментом камбаловидной мышцы мобилизовали артерию и вены на протяжении 8 см. Диаметр артерии составил 3,2мм. Проксимальнееперфорантного сосуда сосудистый пучок был пересечен (рисунок 5). Пересечение сосудов выполнено для увеличения дуги ротации лоскута. Так как длина перфорантных сосудов не позволяла выполнить транспозицию лоскута на необходимое расстояние.
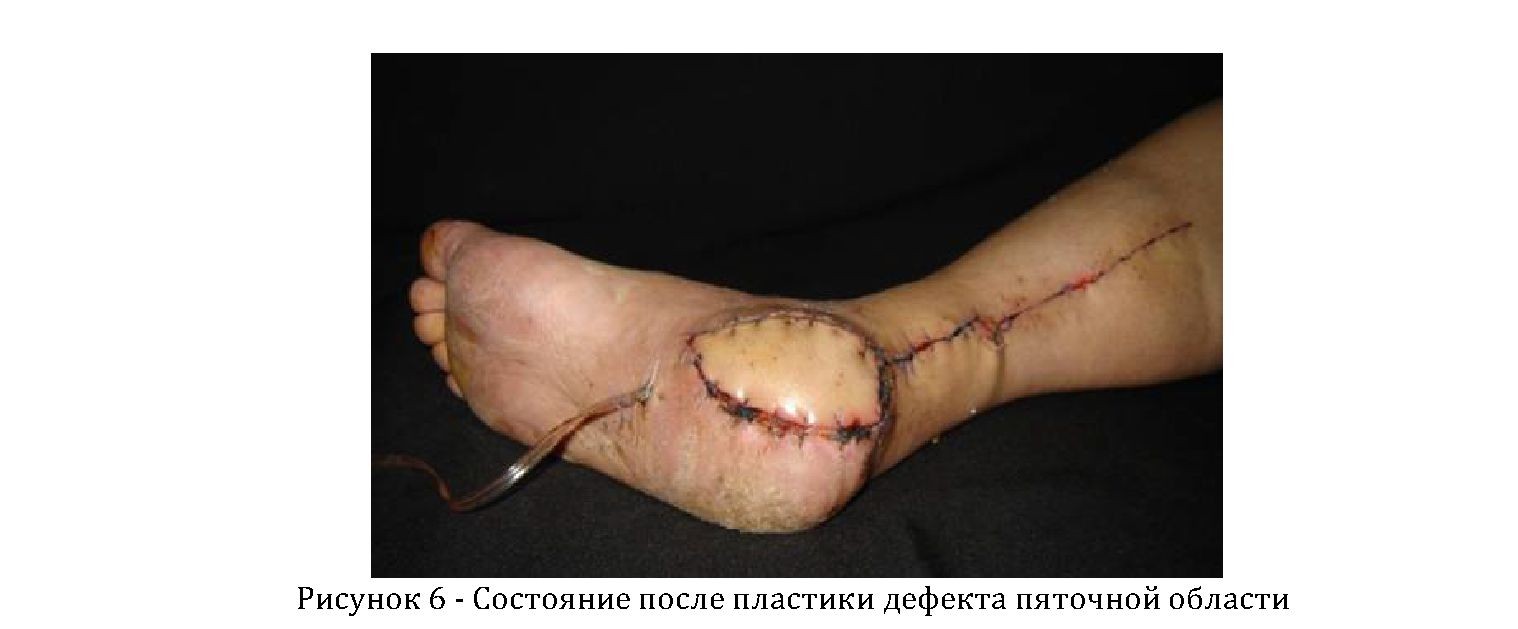
Точка ротации лоскута была расположена на 3 см проксимальнее внутренней лодыжки. Дефект донорской области был устранен пластикой местными тканями, рана ушита внутрикожным рассасывающим швом. Лоскут был уложен на дефект. Подлоскутное пространство дренировали активным дренажем в течение 28 суток (рисунок 6).

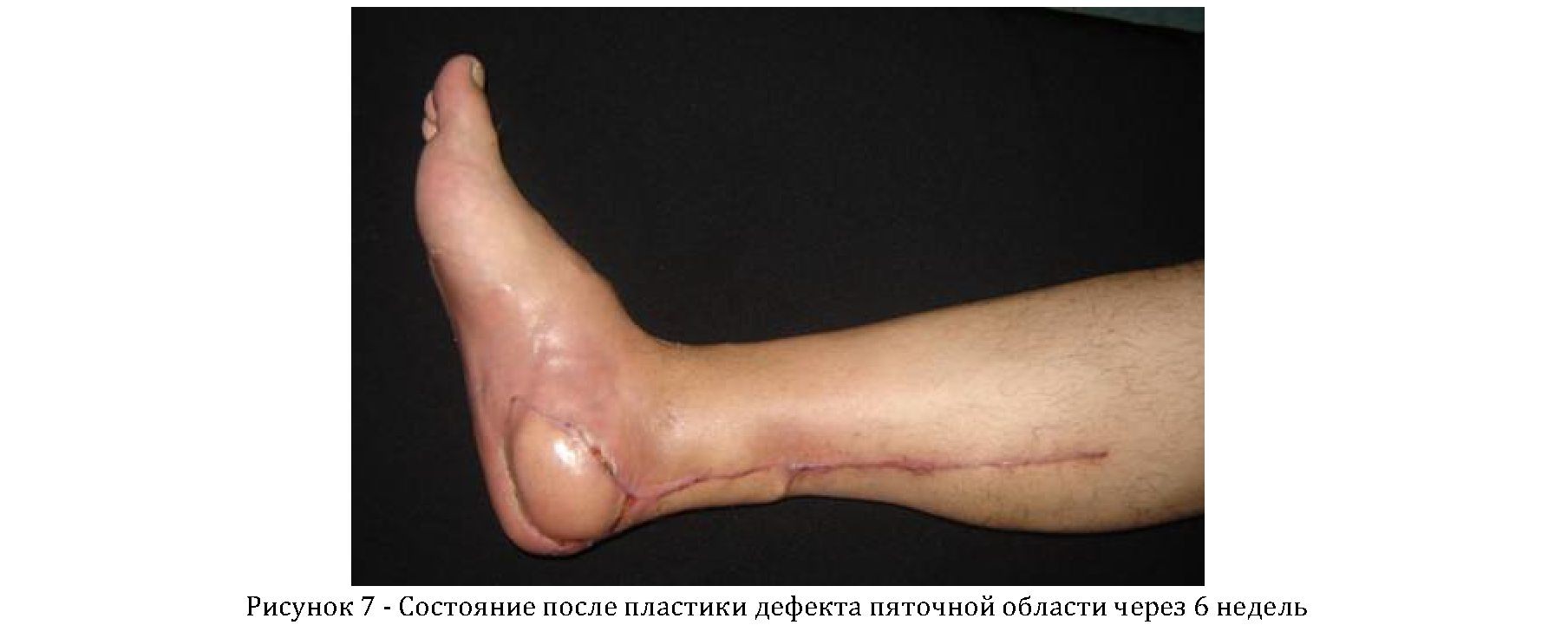
При этом отделяемое каждые 5 суток подвергалось бактериологическому исследованию для оценки эффективности антибактериальной терапии. Раны зажили первичным натяжением, кровообращение лоскута компенсировано. Проводилась антибактериальная, противовоспалительная терапия, ежедневные перевязки. Швы с лоскута сняты на 14 сутки. В течение 5 дней сохранялась отечность голени и стопы. На 17 сутки, после активизации конечности, отмечено повторное нарастание отека стопы и лоскута. Дополнительных мероприятий по купированию отека не проводилось (сохранялась возможность наличия инфекции в пяточной кости). Через 6 недель (рисунок 7) пациент начал обходиться без помощи костылей, выписан.
Полная регрессия отека наступила через 8 недель со дня операции. На контрольной рентгенограмме, произведенной через 3 месяца, признаков остеомиелита пяточной кости не выявлено, локально границы перемещенного лоскута сгладились. Повторные вмешательства по коррекции формы пяточной области не выполнялись.
Демонстрация клинического случая выполнена после письменного согласия пациента и одобрения этического комитета акционерного общества «Национальный научный центр хирургии имени Александра Николаевича Сызганова».
Подобные операции были выполнены и двум другим пациентам. Разница была только в размерах перемещенных лоскутов. Послеоперационный период был аналогичным. Обсуждение.
Традиционные методы лечения посттравматических дефектов стопы не всегда позволяют достичь требуемых анатомо-функциональных результатов [6,7].На
сегодняшний день благодаря усовершенствованию медицинских технологий, представляется возможным разрешения ее с помощью микрохирургической аутотрансплантации комплексов тканей. Применение микрохирургических методик лечения, являющихся самыми сложными, но, в то же время,наиболее эффективными, показано при пластике обширных дефектов нижних конечностей, сопровождающихся обнажением костей и суставов, нервов и сосудов, длительно незаживающих инфицированных дефектов мягких тканей, трофических язвах, дефектах мягких тканей, сочетающихся с остеомиелитом [8, 9].
Васкуляризированная пластика несвободным лоскутом - на постоянной сосудистой ножке, исключает образование рубцов между лоскутом и подлежащими тканями. Хорошее
кровоснабжение тканей обеспечивает невосприимчивость к инфекции, что определяет возможность применения данного метода у пациентов с инфицированными ранами [10,11,12]. Данный вид пластики обладает хорошей выносливостью к механической нагрузке и их применение целесообразно там, где традиционные методы пластической хирургии малоэффективны. Исходя из этого, показаниями к проведению данных процедур, являются дефекты мягких тканей дистальных отделов нижних конечностей [3,13, 14]. Оценка результатов васкуляризированной кожной пластики при пластике дефектов нижних конечностей представляет собой трудную задачу. Мнения многих авторов по данному вопросу расходятся, поэтому выбор критериев оценки требует индивидуального подхода. Оценку результатов лечения проводили по жизнеспособности лоскута и степени его приживления, количеству этапов кожной пластики, цвету и толщине пересаженного лоскута, степени восстановления чувствительности [15].
Заключение.
Таким образом, применение микрохирургической несвободой пересадки лоскутов содномоментной секвестрэктомией и тампонированием полости, с закрытием костной ткани мышцами голени в лечении посттравматических дефектов тканей стопы, осложненных остеомиелитом пяточной кости, позволяет не только сохранить конечность, одномоментно восполнить объем тканей, сократить сроки послеоперационной реабилитации, но и получить хороший функциональный и эстетический результат как в раннем, так и в позднем послеоперационном периоде. Хирургическое лечение пациентов данной группы должно быть индивидуальным, так как на сегодняшний день количество представленных случаев и доказательных данных, которые сравнивали бы различные варианты
методик лечения, недостаточно.
СПИСОК ЛИТЕРАТУРЫ
- Donski P.K, Fogdestram I. Distally based fasciocutaneous flap from the sural region. A preliminary report // Scand J PlastReconstr Surg. - 1983. - №3(17). - Р.191-196.
- БелоусовА.Е. Пластическая, реконструктивная и эстетическая хирургия. - СПб.: Гиппократ, 1998. - 744 с.
- Миланов Н.О., Адамян Р.Т., Трофимов Е.И., Зелянин А.С. Устранение дефектов опорной поверхности стопы с применением микрохирургических аутотрнсплантатов // Материалы V международного конгресса по пластической реконструктивной и эстетической хирургии. - Ереван: 2006. - С. 55-61.
- Атаев А.Р., Ахмедов Б.А., Скугина А. Лечение обширных дефектов мягких тканей и костей стопы // Травматология и ортопедия России. - 2006. - №2. - С. 25-26.
- Родомонова Л.А., Кочиш А.Ю. Реконструктивные микрохирургические операции при травмах конечностей. - СПб.: РНИИТО, 2012. - 115 с.
- Yogesh C. Bhatt, Sumer Singh,* PiyushDoshi, and Sanjay G. Vaghani. Reverse Peroneal Artery Flap for Large Heel and Sole Defects: A Reliable Coverage // WorldJPlastSurg. - 2017. - №6(2). - Р. 212-219.
- Ciofu R.N.,Zamfirescu D.G.,PopescuS.A and Lascar I. Reverse sural flap for ankle and heel soft tissues reconstruction // J Med Life. - 2017. - №10(1). - Р. 94-98.
- Follmar K.E., Erdmann D. Reversed sural artery flap. Pu LLQ, Levine JP, Wei FC. Reconstructive surgery of the lower extremity // Quality Medical Publishing. - 2013. - Р. 665-679.
- ShaheenAkhtar, Hameed A. Versatility of the suralfasciocutaneous flap in the coverage of lower third leg and hind foot defects // Journal of Plastic, Reconstructive & Aesthetic Surgery.August. - 2006. - Vol. 59, Issue 8. - P. 839-845.
- Jia-xiangGu, MD, PhD.,An-shiHuan, MD., Nai-chen Zhang, MD., Hong-jun Liu, MD., Shi-cong Xia, MD., SubhashRegmi, MD., Lin Yang, MD.Reconstruction of Heel Soft Tissue Defects Using Medial Plantar Artery Island Pedicle Flap: Clinical Experience and Outcomes Analysis // Journal of Foot and Ankle Surgery. - 2017. - Vol.56, Issue 2. - P. 226-229.
- Godina M. Early microsurgical reconstruction of complex trauma of the extremities // Plast Reconstr Surg. - 1986. - №78(3). - Р. 285292.
- Gravem P.E. Heel ulcer in leprosy theated with fascio-cutaneous island flap from the instep of the sole // Scand. J. Plast. Reconstr.Surg. - 1991. - Vol. 25. - № 2. - P. 155-160.
- Jian-Wei Wei, MD, Jiang-Dong Ni, MD, Zhong-Gen Dong, MD,Li-Hong Liu, MD, Ying Yang, MD. A Modified Technique to Improve Reliability of Distally Based SuralFasciocutaneous Flap for Reconstruction of Soft Tissue Defects Longitudinal in Distal Pretibial Region or Transverse in Heel and Ankle // Journal of Foot and Ankle Surgery.. - 2016. - Vol.55, Issue 4. - P. 753-758.
- Yildirim S, Gideroğlu K, Aköz T. Anterolateral thigh flap: ideal free flap choice for lower extremity soft-tissue reconstruction // J ReconstrMicrosurg. - 2003. - №19(4). - Р. 225-233.
- Mohamed El-Shazly, MD, Osama Yassin, MSc, Ahmed Kamal, MSc, Mohamed Makboul, MSc, GiulioGherardini, MD, PhD. Soft Tissue Defects of the Heel: A Surgical Reconstruction Algorithm Based on a Retrospective Cohort Study // Journal of Foot and Ankle Surgery. . -
- - Vol.47, Issue 2. - P. 145-152.