Моделирование нейродистрофического процесса позвоночника у животных на фоне создания второстепенной чувствительной доминанты в головном мозге уменьшает воспалительно-отечные процессы в тканях и ускоряет репарацию хрящевых тканей.
Болевые синдромы - наиболее часто встречающееся состояние в практике врачей многих специальностей. До последнего времени считалось, что основную часть болевых синдромов составляет ноцицептивная боль и лишь приблизительно 1 - 1,5% в популяции страдает хронической нейропатической болью любой этиологии [1]. Однако последние исследования, проведенные в этой области, вынуждают более тщательно дифференцировать эти представления [2].
В частности, при нейродистрофических изменениях пояснично-крестцового отдела позвоночника совокупным результатом механических, воспалительных, дисметаболических нарушений и ишемии являются ирритация нервных волокон, изменение нейрофизиологических характеристик корешка, блок проведения импульсов по нему, аксональная дегенерация и повреждение шванновских клеток. Кроме того, возникающие болевые раздражения, как острые, так и хронические, являясь для организма стрессом, изменяют функциональное состояние неспецифических структур головного мозга, в результате чего могут измениться соотношения ноцицептивных и антиноцицептивных систем, что будет поддерживать патологический процесс в мышцах и интенсивность болевого синдрома [3, 4, 5].
Далеко не все пациенты могут описать свои симптомы, пользуясь дескрипторами, характерными именно для этого патологического состояния, что приводит к постановке ошибочного диагноза и выбору неправильной терапии.
Поэтому серьезным подспорьем для разработки механизмов боли являются морфофункциональные исследования тканей у животных на модели дегенеративно-дистрофического повреждения позвоночника.
Материал и методы исследования.
Были использованы 60 подопытных животных (белые лабораторные крысы, массой 180-220 гр.). Все подопытные животные были разделены на следующие группы:
- группа - интактные животные (n = 15).
- группа - крысы с экспериментальным остеохондрозом позвоночника (n = 20).
- группа - крысы с экспериментальным остеохондрозом позвоночника, которым дополнительно был создан очаг раздражения на хвосте (n = 25).
Для моделирования остеохондроза в остистый отросток исследуемого позвонка под общим наркозом вводили иглу со шприцем с 0,5 мл раствора, состоящего из 40% раствора глюкозы и 96% этилового спирта 1:1 [6].
группе крыс травмировали кожу хвоста, для создания дополнительного болевого раздражения и новой доминанты в головном мозге по своей интенсивности, физиологического характера. Затем проводили гистологическое исследование тканей поясничнокрестцового отдела позвоночника через 1 и 2 недели, 1, 2 и 3 месяца после эксперимента с соблюдением правил обращения с животными, соответственно с положениями IV Европейской Конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей (ETS 123, 1986).
Статистическая обработка полученных данных проводилась при помощи пакета стандартных статистических программ STATISTICA 6.0.
Собственные результаты и их обсуждение.
В контрольной группе, у животных с экспериментальным остеохондрозом, в тканях позвоночника на первой неделе наблюдался умеренный отек межуточного основного вещества, структура хрящевых клеток и волокон была сохранена, увеличено число вакуолей в хрящевых клетках (рисунок 1).
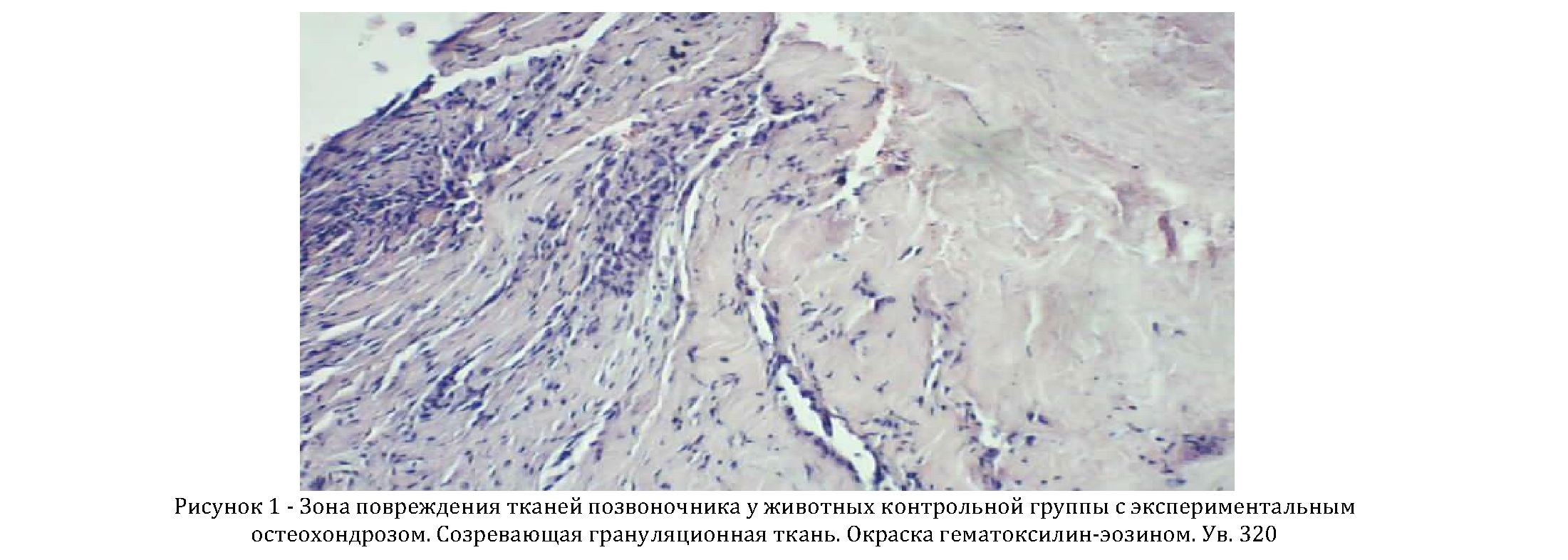
В основной группе, у животных с экспериментальным остеохондрозом позвоночника на фоне дополнительного отвлекающего болевого фактора, в течение первой недели отмечался умеренный отек межуточного основного вещества. Нормальная структура клеток хряща и волокон оставалась сохраненной (рисунок 2).
Через один месяц во второй, контрольной группе животных с экспериментальным остеохондрозом, умеренный отек стромы сохранился местами, зерна и глыбки в хрящевых клетках стали больше (признак деструкции клеток), в пространствах вокруг изогенных групп клеток содержимое сохранилось лишь местами, оставались признаки
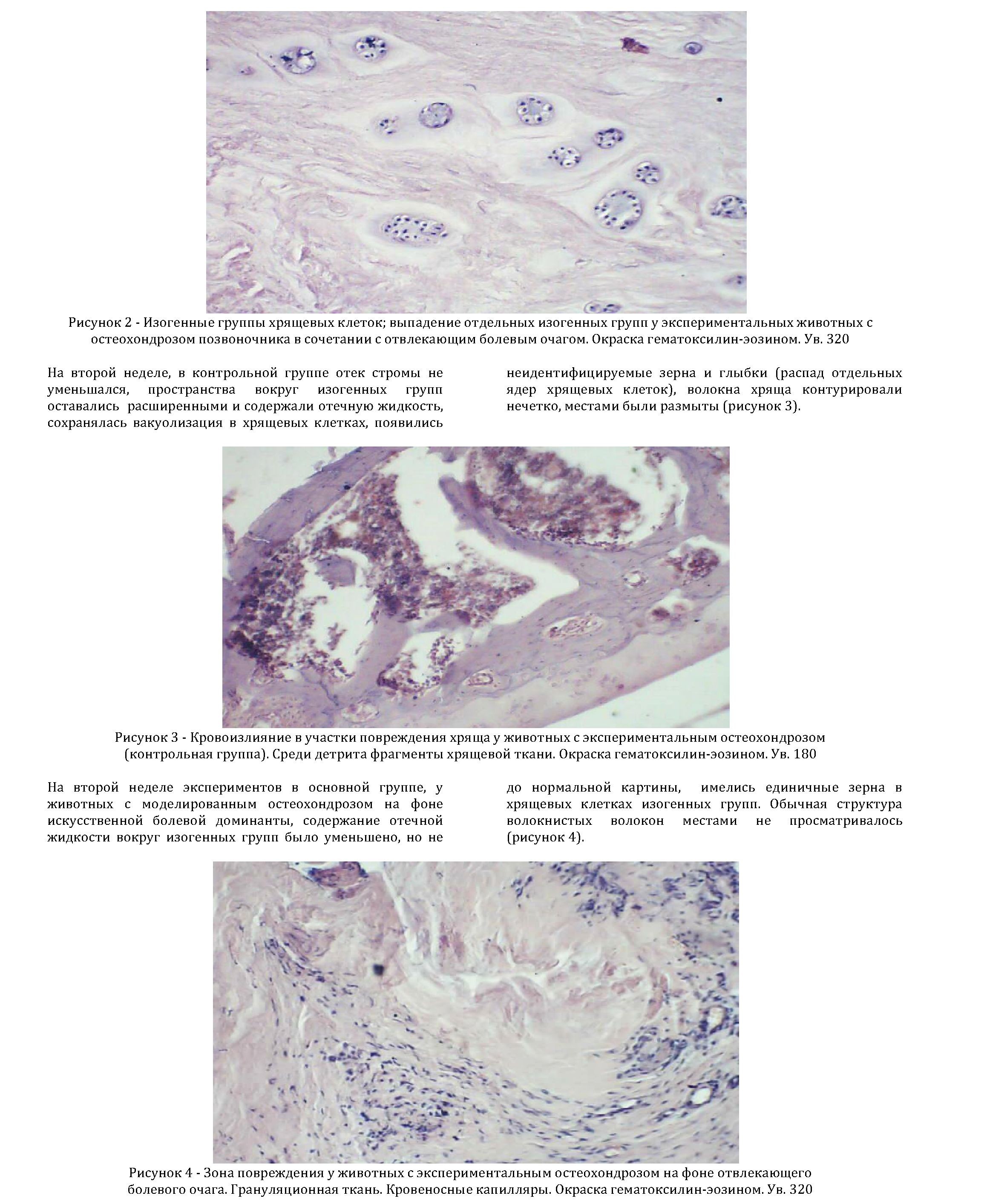
деструкции волокон. Число хондробластов было умеренно увеличено (рисунок 5).

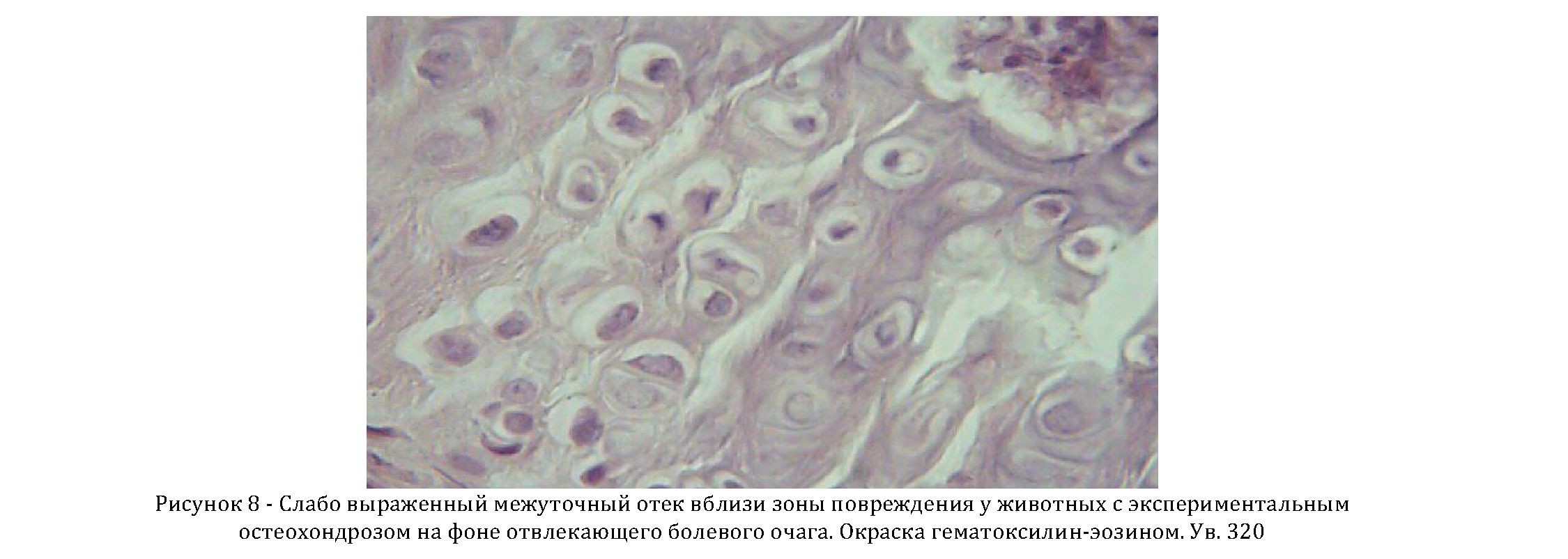
В группе животных с экспериментальным остеохондрозом позвоночника на фоне дополнительного отвлекающего болевого фактора, через два месяца отек стромы, имевший место ранее, стал менее выраженным, основное вещество окрашивалось равномерно, просматривалась четкая структура волокнистых структур, единичные зерна в хрящевых клетках сохранились, структура хрящевых клеток не отличается от нормы. Отек в изогенных группах практически уменьшился. Имелось большое количество молодых хондробластов, которые начали формировать изогенные группы, состоящие из 3-4 хрящевых клеток (рисунок 8).
Через три месяца, в контрольной группе у животных с экспериментальным остеохондрозом все еще сохраняются некоторые признаки деструкции хряща, зернистость в клетках, местами не всегда четкая структура волокнистых структур и неравномерная окрашиваемость основного вещества, много молодых хрящевых клеток хондробластов (рисунок 9, 10).
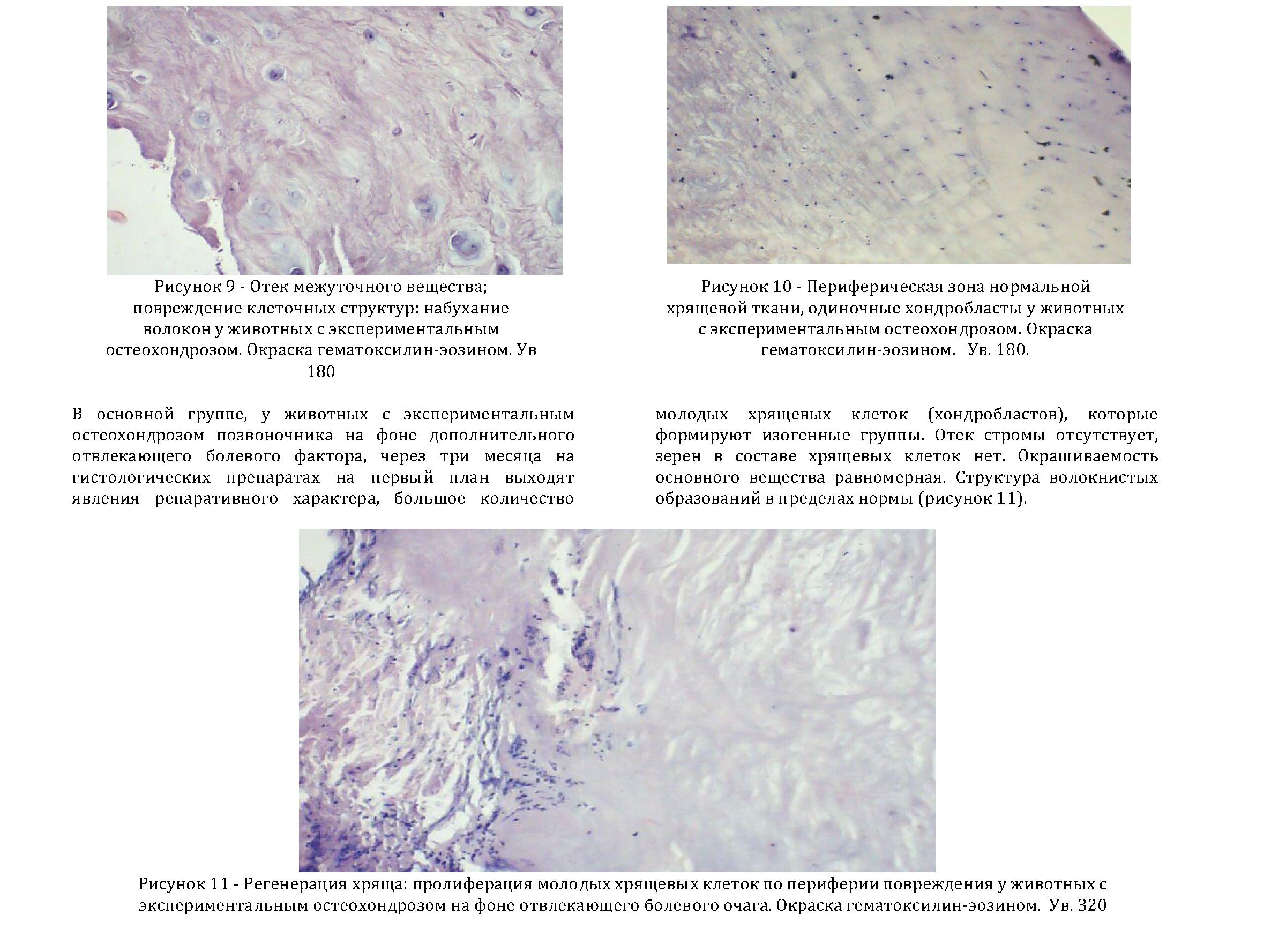
При остеохондрозе, дегенеративно-дистрофическиепроцессы, сопровождаются сдавливанием корешков спиномозговых нервов, вызывая выпадение нейротрофического влияния на окружающие ткани и нейрогенное воспаление, которое, в свою очередь, повышает возбудимость ноцицептивных нейронов задних рогов спинного мозга и соответствующих мотонейронов, формируя болевой синдром.
Дело в том, что в случае ненарушенного трофического влияния на воспалительный участок его действие, направлено на оптимальное течение воспаления и ликвидацию его последствий. С другой стороны, любое нарушение этого трофического влияния создает в ткани условия, способствующие развитию воспаления, хотя бы потому, что в дистрофических тканях могут возникать расстройства, требующие вмешательства защитных тканевых механизмов.
Таким образом, моделирование нейродистрофического процесса позвоночника у животных на фоне создания второстепенной чувствительной доминанты в головном мозге, снижает патологическую импульсацию со стороны ЦНС на фоне дополнительного выброса эндорфинов под влиянием дополнительного очага боли физиологического характера. В итоге, уменьшаются воспалительно-отечные процессы в тканях и ускоряется репарация хрящевых тканей.
СПИСОК ЛИТЕРАТУРЫ
- Myers R. How neuropathic is sciatica? The mixed pain concept // Orthopade. - 2004. - №33. - Р. 568 - 575.
- Wall P.D., Melzack R. Textbook of Pain 4th ed. - London, England: Churchill Livingstone, 1999. - 569 p.
- Данилов А.Б., Давыдов О.С. Нейропатическая боль.- М.: Боргес, 2007. - 192 с.
- Клименко А.В., Головченко Ю.И., Калищук-Слободин Т.Н. и др. Особенности ведения больных с хроническим вертеброгенным болевым синдромом пояснично-крестцовой локализации // Здоров'я Украïни. - 2007. - №2(159) . - С. 38-39
- Команденко К.П., Рыжов А.И., Жураковский И.П. Экспериментальная модель остеохондроза позвоночника // Бюлл. Экспериментальной биологии и медицины. - 1998. - №6., Т. 125. - С. 706-708.
- Попелянский Я.Ю., Штульман Д.Р. Боли в шее, спине и конечностях // Болезни нервной системы. - М.: Медицина, 2001. - С. 293 - 316.
- B. Geleskhanov