Совершенствование ранней диагностики рака является важным условием успешного лечения рака и предотвращения развития метастатической болезни. Существенный прогресс в этом направлении следует ожидать от разработки новых подходов к идентификации особого состояния организма, несущего клинически не проявляющуюся злокачественную опухоль, и характеризующегося комплексом прямых и косвенных изменений регуляции иммунного гомеостаза. Взаимоотношения злокачественной опухоли и иммунной системы представляют собой сложную иерархическую систему, динамически развивающуюся по мере развития опухоли, которые согласно современной гипотезе иммуноредактирования рака разделены на три последовательных стадии: «элиминация», «равновесие» и «ускользание». Последняя из них характеризуется присутствием в опухолевой ткани и в периферической крови различных иммунорегуляторных клеток, угнетающих противоопухолевую активность NK-клеток и цитотоксических Т-лимфоцитов. Среди таких клеток особую важность представляют миелоидные супрессорные клетки (MDSC), Т-регуляторные клетки (Treg) и регуляторные NK-клетки (NKreg). Используя проточную цитофлуориметрию, мы показали, что у онкологических больных содержание этих клеток в периферической крови статистически значимо повышено, поэтому предлагаем использовать их в качестве новых биомаркеров онкологического процесса. Для верификации такого утверждения необходимы обширные скрининговые исследования данных клеточных субпопуляций периферической крови больных с различными видами онкологических заболеваний, находящихся на различных стадиях болезни.
Рак является второй причиной смертности в мире после сердечнососудистых заболеваний, а к 2030-му году, возможно, выйдет на первое место. Лечение рецидивирующих и метастатических опухолей практически всегда гораздо менее эффективно, чем воздействие на первичный очаг новообразования. Из этого становится очевидным важность ранней диагностики рака. Среди диагностических средств, разработанных за последние несколько десятилетий, опухолевые маркеры обеспечивают комбинацию высокой точности и низкой стоимости анализа, что делает их пригодными для диагностики, мониторинга и скрининга. Однако, несмотря на огромное количество исследований, проводимых в этой области, только небольшая часть маркеров (например, AFP, CEA, Cа125, PSA) нашла широкое применение в клинике. Для большинства опухолей пока не обнаружены специфические маркеры, имеющие в перспективе потенциальную диагностическую ценность. Между тем, такие маркеры могут быть найдены в иммунной системе, контролирующей появление и рост злокачественных опухолей, клеточные компоненты которой можно оценивать в периферической крови с помощью инструментальных методов, в частности, проточной цитофлуориметрии. Взаимоотношения злокачественной опухоли и иммунной системы представляют собой сложную иерархическую систему, динамически развивающуюся по мере развития опухоли. Интерес исследователей к этим взаимоотношениям связан, прежде всего, с перспективой возможности успешного влияния на противоопухолевый иммунитет как в моно-, так и в комбинированной иммунотерапии рака. Кроме того, можно ожидать, что изменение состояния иммунной системы в ответ на рост опухоли может представлять интерес с точки зрения диагностики рака, в том числе ранней.
Согласно современной гипотезе иммуноредактирования раковой опухоли [1] развитие взаимоотношений между злокачественной опухолью и иммунной системой проходит через три различных фазы, которые получили названия: «элиминация», «равновесие» и «ускользание». Фаза элиминации представляет собой процесс реализации идеи иммунологического надзора (по Бернету), когда врожденная и адаптивная иммунные системы, работая совместно, распознают возникшую опухоль и разрушают ее без какого-либо клинического проявления. Если после этого сохраняются малочисленные клеточные варианты опухоли, фаза элиминации переходит в фазу равновесия, в которой адаптивная иммунная система предотвращает опухолевый рост, но одновременно «редактирует» опухоль, делая ее не иммуногенной [2]. Опухоль переходит в «дремлющее» состояние, которое может продолжаться годы и даже десятилетия. Во время фазы равновесия гетерогенность и генетическая нестабильность раковых клеток, которые пережили фазу элиминации, являются, вероятно, теми принципиальными силами, которые позволяют опухолевым клеткам в конечном счете противостоять иммунитету. Опухоль, на которую иммунные клетки длительно воздействуют, могут содержать раковые клетки, которые приобрели тысячи мутаций. Две взаимосвязанные причины лежат в основе этого события: потеря иммуногенности в ответ на редактирующую активность иммунной системы и изменение самой иммунной системы в ответ на иммуносупрессорную активность растущей опухоли и ее микроокружения. В фазу ускользания опухолевые клетки, которые приобрели способность обходить иммунное распознавание и деструкцию, начинают интенсивно делиться, формируя видимую опухоль.
Именно иммуносупрессорный фон, формируемый помимо самой опухоли присутствием опухолеассоциированных фибробластов [3], супрессорных эндотелиоцитов [4], опухолеассоциированных макрофагов [5, 6], толерогенных дендритных клеток [7], FoxP3+ Т- регуляторных (Treg) клеток [8, 9] и миелоидных супрессорных клеток (MDSC) [10], обеспечивает функциональную анергию цитолитических NK- клеток, CD8+ цитотоксических Т-лимфоцитов (CTL) и конверсию обычных CD4+ Т-хелперов в супрессорные Treg-клетки. В результате происходит неконтролируемый рост опухоли.
Таким образом, очевидно, именно популяция супрессорных (регуляторных) клеток, циркулирующих в кровотоке, может оказаться диагностическим критерием перехода опухолевого процесса из фазы равновесия в фазу ускользания. Поиск фенотипических маркеров таких клеток с помощью метода проточной цитофлуориметрии проводится в нашей лаборатории на протяжении последних 10 лет. Результаты, наиболее заслуживающие внимания с точки зрения перспективы разработки новых методов ранней диагностики рака, представлены в настоящем обзоре. Миелоидные супрессорные клетки (Myeloid Derived Suppressor Cells, MDSC).
Среди супрессорных клеток, участвующих в угнетении противоопухолевого иммунитета, MDSC занимают особое место ввиду их обязательного сопутствия развитию злокачественных опухолей, показанного как в эксперименте, так и в клинике. К настоящему моменту опубликовано несколько детальных обзоров, посвященных проблеме MDSC [10-17]. Кратко изложение современных представлений о свойствах MDSC и их роли в угнетении противоопухолевого иммунитета выглядит следующим образом.
MDSC представляют собой гетерогенную популяцию предшественников направления (макрофагов, дендритных клеток), у мышей по экспрессии гемопоэтических миеломоноцитарного нейтрофилов и идентифицированную
клетки в большом количестве обнаруживают в костном мозге и практически не определяются в периферической крови и селезенке. При моделировании опухолевого процесса у животных их количество значительно возрастает в селезенке и лимфоузлах, а также в строме опухоли, что совпадает с угнетением противоопухолевого иммунитета (снижение противоопухолевой активности NK-клеток CTL). При удалении опухоли или уничтожении миелоидных клеток с помощью моноклональных антител к CD11b и Gr-1 иммунная система полностью восстанавливается и приобретает утраченный опухолетоксический потенциал. Различают две субпопуляции MDSC по наличию некоторых дополнительных маркеров и форме ядра: моноцитарную (M-MDSC) и гранулоцитарную (G- MDSC).
клеточных маркеров CD11b и Gr-1. В норме эти
Фенотип MDSC человека изучен пока хуже, чем у мышей. Установлено, что эти клетки у человека не несут линейных маркеров зрелых клеток (CD3, CD19, CD56, CD14, HLA-DR), но экспрессируют миелоидные маркеры CD31, CD33, CD11b, CD15 маркер гемопоэтических стволовых клеток CD34.
Супрессорный потенциал миелоидные клетки приобретают под действием опухолевых факторов, таких как GM-CSF, M-CSF, IL-3, IL- -6,
IL-1β и SCF. Продукция этих факторов опухолью всегда связана с плохим прогнозом исхода заболевания.
Опухолеассоциированные цитокины и хемокины могут также управлять дифференциацией нейтрофилов в сторону MDSC и усиливать хоуминг MDSC в опухоль. MDSC экспрессируют ряд хемокиновых и цитокиновых рецепторов, включая CCR2, CXCR4, CXCR2, CD117 и VEGFR1. Среди них CCR2 рассматривается в качестве маркера MDSC. Показано, что MDSC мигрируют в опухоль в ответ на клеточное повреждение, инфекцию или провоспалительные медиаторы, принадлежащие к семейству S100 белков, связывающих кальций. Основное свойство MDSC, выделенных из опухолей животных, заключается в подавлении Т- и NK-клеточной активации. Механизм такого подавления различается в зависимости от субпопуляции MDSC.
Значительная часть способности MDSC супрессировать Т-клетки связана с продукцией этими клетками пероксинитрита (ONOO-), который генерируется аргиназой (ARG1) и индуцибельной NO- синтазой (iNOS). В опосредовании супрессорной трансформирующий рост фактор который непосредственно активности миелоидных клеток участвует также противоопухолевую активность CTL. Помимо своей способности иммуносупрессорному действию на антигенпрезентирующие клетки, индуцирующие активацию CD4+CD25+Foxp3+ Treg-клеток, представляющих собой другое семейство опухолеассоциированных супрессорных клеток. Опухолеассоциированные MDSC также ингибируют другие клетки, вовлеченные в противоопухолевый ответ, такие как дендритные клетки и макрофаги. Учитывая важность этих клеток в развитии злокачественных опухолей, мы провели исследование периферической крови больных раком легкого, толстого кишечника и эндометрия в сравнении со здоровыми донорами [18]. Для этого клеточную фракцию с плавучей плотностью 1,090 г/мл выделяли с помощью изопикнического центрифугирования на градиенте перкола, метили флуоресцентными моноклональными антителами и подвергали проточной цитофлуориметрии. бета (TGFЩ, угнетает к прямому эффекторные клетки, MDSC действуют как толерогенные
Оказалось, что эта фракция в гранулоцитарном гейте содержала CD34+ клетки, составляющие в среднем около 18% от общего количества клеток, причем у онкологических больных почти все клетки этого гейта имели фенотип CD34+CD33+CD15+, тогда как у здоровых людей клетки с таким фенотипом отсутствовали (рис.1). Удаление CD34+ клеток из этой фракции с помощью иммуномагнитной сепарации приводило к потере секреции во время культивирования ex vivo супрессорного цитокина TGFĒ, определяемого с помощью иммуноферментного анализа. Таким образом, высокогранулярные клетки с плавучей плотностью 1,090 г/мл с фенотипом MDSC (CD34+CD33+CD15+), здоровых доноров и поэтому могут рассматриваться как потенциальные клеточные биомаркеры рака.
обнаруженные у онкологических больных, обладали супрессорной активностью и отсутствовали у Treg-клетки составляют важное звено иммунной системы, контролирующее ответы эффекторных клеток и обеспечивающее толерантность к собственным антигенам [19]. 10% от всех CD4+ Т- лимфоцитов составляют Treg-клетки, основными маркерами которых являются CD25, FoxP3, GITR, OX40 (CD134), CTLA-4 (CD152).
Treg-клетки предотвращают возникновение аутоиммунных заболеваний, а также влияют на возникновение и течение онкологических заболеваний и инфекционный процесс [20].
Один из центральных механизмов привлечения Treg- клеток из кровяного русла в места воспаления опосредован взаимодействием между активной формой рецептора CD44 на клетках и его лигандом гиалуронаном (НА) на поверхности эндотелия [21]. Высокомолекулярный НА, основной компонент межклеточного матрикса, представляет собой полимер дисахарида, состоящего из N-ацетил глюкозамина и D-глюкуроновой кислоты, с молекулярной массой более 400 kDa. НА привлекает внимание исследователей Treg-клеток в виду его участия в механизме возникновения и регуляции воспаления, которое характеризуется его патологическим синтезом и накоплением в сайтах воспаления [22].
 Ранее было продемонстрировано, что высокомолекулярный НА приводит к увеличению экспрессии FoxP3 и продукции iL-10 Treg-клетками [23]. Более того, в исследованиях на мышах показано, что способность связывать НА дискриминировала Treg-клетки с повышенным супрессорным потенциалом [24]. Скорость синтеза и деградации НА намного выше при раке, чем в здоровой ткани [25, 26]. Было показано, что на поздних стадиях рака абберантный синтез и деградация НА трансформированными клетками в результате приводит к образованию крайне необычного микроокружения, характеризуемого аккумуляцией высокомолекулярного НА и избыточного количества его фрагментов в виде олигосахаридов, которые могут облегчать злокачественную трансформацию и выживание опухолевых клеток и повреждение функций иммунных клеток [27]. В ряде работ было показано, что опухолевая ткань при раке молочной железы содержит существенно больше НА, чем нормальная ткань или доброкачественная опухоль [28-31].
Ранее было продемонстрировано, что высокомолекулярный НА приводит к увеличению экспрессии FoxP3 и продукции iL-10 Treg-клетками [23]. Более того, в исследованиях на мышах показано, что способность связывать НА дискриминировала Treg-клетки с повышенным супрессорным потенциалом [24]. Скорость синтеза и деградации НА намного выше при раке, чем в здоровой ткани [25, 26]. Было показано, что на поздних стадиях рака абберантный синтез и деградация НА трансформированными клетками в результате приводит к образованию крайне необычного микроокружения, характеризуемого аккумуляцией высокомолекулярного НА и избыточного количества его фрагментов в виде олигосахаридов, которые могут облегчать злокачественную трансформацию и выживание опухолевых клеток и повреждение функций иммунных клеток [27]. В ряде работ было показано, что опухолевая ткань при раке молочной железы содержит существенно больше НА, чем нормальная ткань или доброкачественная опухоль [28-31].
Мы решили использовать эти факты, чтобы определить различия Treg-клеток периферической крови онкологических больных и здоровых людей по их способности связывать высокомолекулярный гиалуронан. Для этого была разработана методика иммуномагнитного разделения CD4+ Т-клеток на связывающие и не связывающие НА с последующим цитофлуориметрическим анализом маркеров Treg- клеток.
В результате проведенного анализа периферической крови больных раком молочной железы была обнаружена новая субпопуляция Treg-клеток, связывающая гиалуронан, с фенотипом CD4+CD25+CD39+, содержание которых у больных было в среднем выше (Р=0,04), чем у здоровых людей более, чем в 2 раза (рисунок 2) [32].
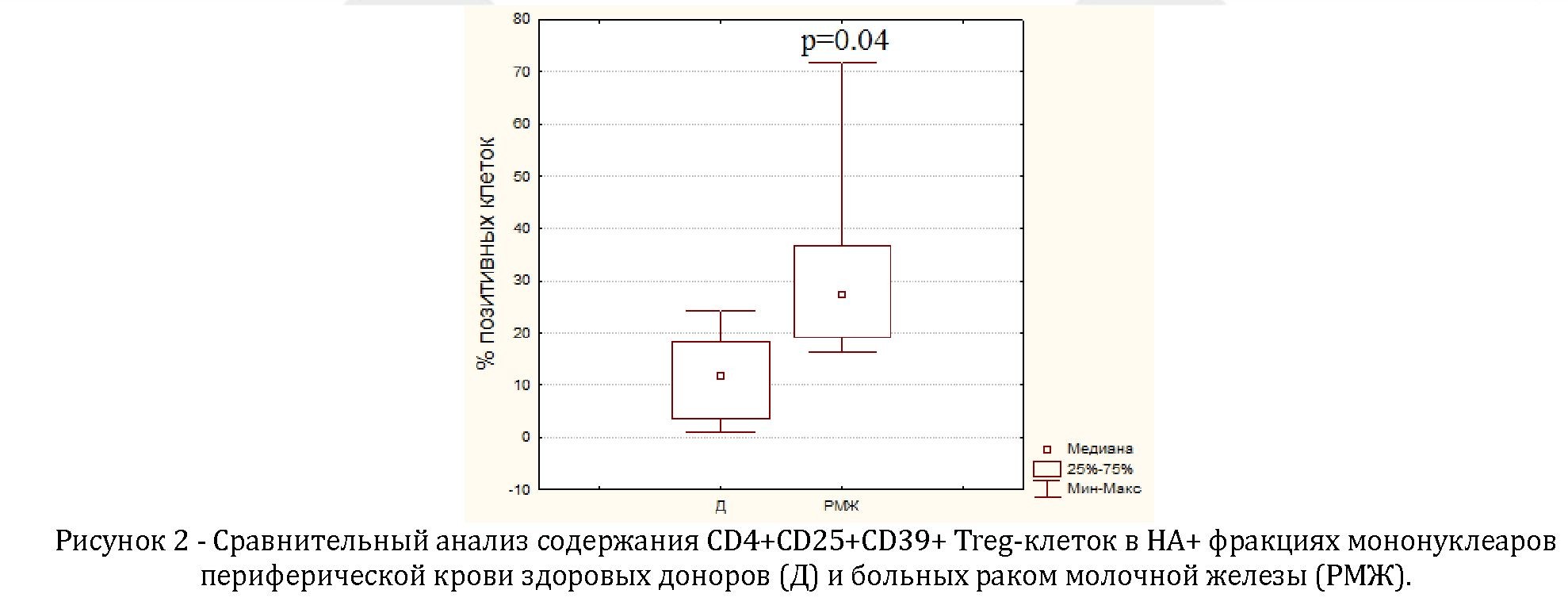 Каталитическая инактивация и конверсия внеклеточного АТФ с помощью эктонуклеотидазы CD39 является одним из ключевых противовоспалительных и иммуносупрессорных механизмов Treg-клеток. Значительное увеличение экспрессии CD39 на Treg-клетках и четкая ассоциация с опухолевой прогрессией было показано рядом авторов [33, 34].
Каталитическая инактивация и конверсия внеклеточного АТФ с помощью эктонуклеотидазы CD39 является одним из ключевых противовоспалительных и иммуносупрессорных механизмов Treg-клеток. Значительное увеличение экспрессии CD39 на Treg-клетках и четкая ассоциация с опухолевой прогрессией было показано рядом авторов [33, 34].
Мы показали, что экспрессия этого маркера при раке молочной железы ассоциирована именно с популяцией Treg-клеток, способных связывать гиалуронан, которая может выступать в качестве нового клеточного биомаркера рака.
NK-регуляторные (NKreg) клетки
Человеческие натуральные киллерные (NK) клетки рассматриваются как профессиональные цитотоксические клетки, интегрированные в эффекторную ветвь врожденного иммунитета во время противовирусного, противоопухолевого, противомикробного и противопаразитарного иммунного ответа, а также оказывающие регуляторное действие на врожденный и адаптивный иммунитет через продукцию различных цитокинов и хемокинов или межклеточных контактов [35]. Такая иммунорегуляторная функция относится, главным образом, к субпопуляции CD56bright NK-клеток, характеризующейся высокой экспрессией CD56 [36], тогда как CD56dim NK-клетки имеют более явные цитотоксические свойства [37-39].
Регуляторная субпопуляция NK-клеток (NKreg) была получена in vitro из циркулирующих в крови CD34+ гемопоэтических предшественников, экспрессирующих мембрансвязанный IL-15 [40]. Такие клетки были обнаружены in vivo среди децидуальных NK-клеток у беременных женщин, имели фенотип незрелых клеток, секретировали супрессорные молекулы (HLA-G, iL-10, iL-21) и не оказывали цитолитического действия на клетки- мишени. В другой работе NKreg-клетки супрессировали дендритные клетки и цитолитическую активность циркулирующих NK- клеток через мембраносвязанный HLA-G и секретируемый IL-10 [41]. Авторы показали, что супрессивные NK-клетки поглощали HLA-G путем трогоцитоза контактирующих клеток. NK-клетки, приобретшие HLA-G1 путем трансфекции, показывали супрессорные свойства по отношению к другим NK-клеткам. Кроме того, HLA-G- экспрессирующие CD4+ и CD8+ T-клетки человека были недавно выявлены в периферической крови и очаге воспаления. Эти клетки обладали слабым пролиферативным потенциалом и показывали супрессорные свойства, которые опосредовались через HLA-G и IL-10 [42-44].
Учитывая важность в регуляции иммунного ответа приведенных и других данных, касающихся NK- клеток, экспрессирующих IL-10, TGF-β и HLA-G, мы провели исследование периферической крови больных раком молочной железы, характеризующимся существенной недостаточностью врожденного противоопухолевого иммунитета [45-47]. В результате была обнаружена новая популяция регуляторных NK-клеток человека, содержание которых у больных раком молочной железы (РМЖ) было достоверно повышено в 1,7 раза по сравнению со здоровыми донорами (6,8±1,8; 4,0±1,1; p=0,001) [48] (рисунок 4).
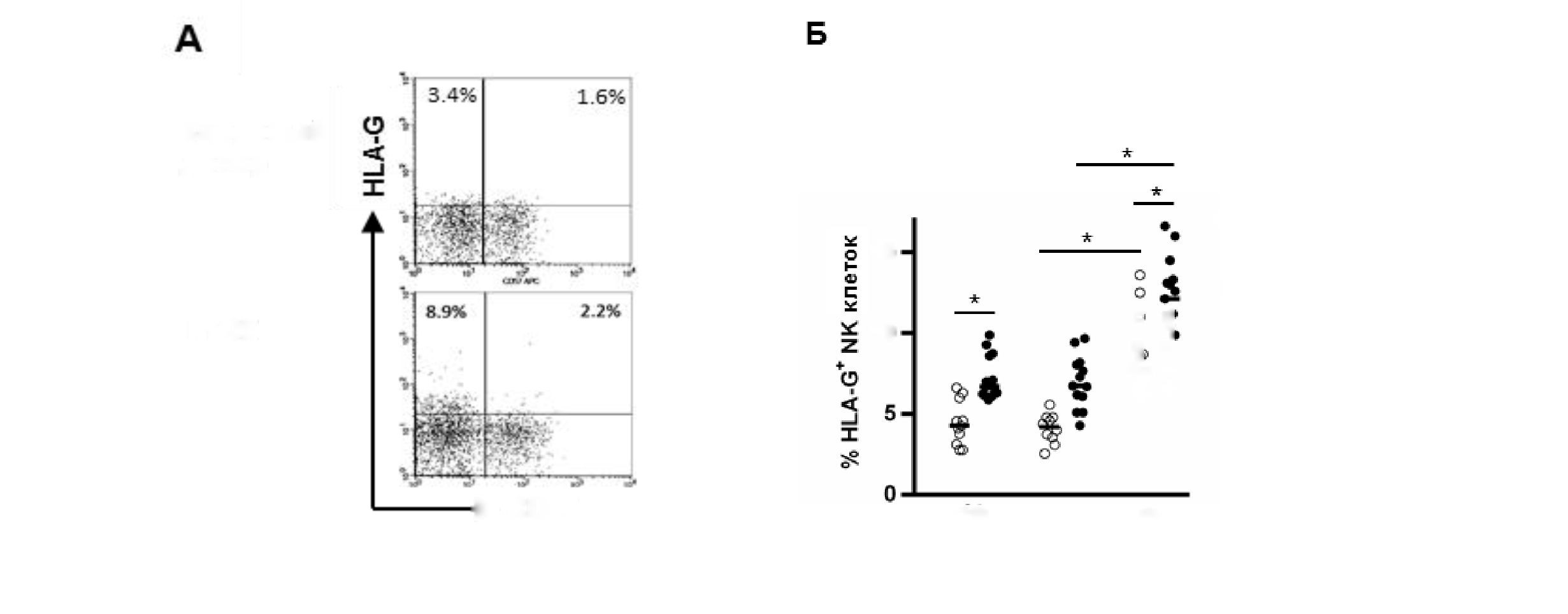 (А) Репрезентативные данные содержания HLA-G+ клеток в CD57+ и CD57- субпопуляциях NK-клеток здорового донора и больной РМЖ.
(А) Репрезентативные данные содержания HLA-G+ клеток в CD57+ и CD57- субпопуляциях NK-клеток здорового донора и больной РМЖ.
Рисунок 4 - Анализ содержания HLA-G+ NK-клеток в периферической крови здоровых доноров и больных раком молочной железы (РМЖ).
(Б) Анализ содержания HLA-G+ NK-клеток здоровых доноров и больных РМЖ (РМЖ) во фракции свежевыделенных мононуклеарных клеток (СВ), без стимуляции (БС) и после инкубации с фитогемагглютинином (ФГА). Данные представлены в виде точечного графика и медианы, достоверность отличий обозначена как: *р≤0,05 (по критерию Стьюдента).
Эти клетки экспрессировали внутриклеточные цитокины IL-10 и TGF-β и обладали супрессорной активностью в отношении Т-клеток. Таким образом, NK-клетки периферической крови с фенотипом CD3- CD56+HLA-G+ также могут быть рассмотрены как кандидаты в новые клеточные биомаркеры рака. Резюмируя наши наблюдения и литературные данные, следует отметить, что три типа исследуемых иммунорегуляторных клеток (MDSC – CD34+CD15+, Treg-клетки – CD4+CD25+CD39+HA+, NK-клетки – CD3- CD56+HLA-G+) действительно выглядят очень привлекательными с точки зрения разработки панели новых биомаркеров рака, пригодных для его ранней диагностики. Для верификации такого утверждения необходимы обширные скрининговые исследования данных клеточных субпопуляций периферической крови больных с различными видами онкологических заболеваний, находящихся на различных стадиях болезни.
СПИСОК ЛИТЕРАТУРЫ
- Schreiber R.D., Old L.J., Smyth M.J. Cancer immunoedditing: Integrating immunity's roles in cancer suppression and promotion. Science.-2011.-Vol.331.-P.1565-1570.
- DuPage M., Mazumdar C., Schmidt L.M., Cheung A.F., Jacks T. Expression of tumour-specific antigens underlies cancer immunoediting // Nature.-2012.-Vol.482(7385).-P.405–409.
- Cirri P., Chiarugi P. Cancer-associated-fibroblasts and tumour cells: a diabolic liaison driving cancer progression. Cancer Metastasis Rev.- 2012.-Vol.31.-N1-2.-P.195-208.
- Mulligan K.J., Young M.R.I. Tumors induce the formation of suppressor endothelial cells in vivo // Cancer Immunol Immunother. - 2010. - Vol.59. - P. 267–277.
- Quatromoni J.G., Eruslanov E. Tumor-associated macrophages: function, phenotype, and link to prognosis in human lung cancer // Am. J. Transl. Res. - 2012. - V.4. - N4. - P. 376-389.
- Hao N.B., Lü M.H., Fan Y.H., Cao Y.L., Zhang Zh.R., Yang Sh.M. Macrophages in tumor microenvironments and the progression of tumors // Clin. Develop. Immunol.-2012. - №11. – Р. 88-97.
- MaY., Shurin G.V., Peiyuan Zh., Shurin M.R. Dendritic cells in the cancer microenvironment // J. Cancer. - 2013. - Vol.4. -N1. - P. 36-44.
- Nishikawa H., Sakaguchi Sh. Regulatory T cells in tumor immunity // Int. J. Cancer. - 2010. - Vol.127. - P. 759–767.
- Byrne W.L., Mills K.H.G., Lederer J.A., O'Sullivan G.C. Targeting regulatory T cells in cancer // Cancer Res. - 2011. - Vol.71. - P.6915-6920.
- Gabrilovich D.I., Ostrand-Rosenberg S. Bronte V. Coordinated regulation of myeloid cells by tumours // Nature Rev. Immunol.- 2012.-Vol.12.-P.253-268.
- Youn J.I., Nagaraj S., Collazo M., Gabrilovich D.I. Subsets of myeloid-derived suppressor cells in tumor-bearing mice // J. Immunol.-2008.-Vol.181.-P.5791-5802.
- Greten T.F., Manns M.P., Korangy F. Myeloid derived suppressor cells in human diseases // International Immunopharmacology.-2011.-Vol.11.-P.802–807.
- Forghani P., Khorramizadeh M.R., Waller E.K. Natural suppressor cells; past, present and future // Frontiers in Bioscience.-2012.-E4.-P.1237-1245.
- Marigo I., Dolcetti L., Serafini P., Zanovello P., Bronte V. Tumor-induced tolerance and immune suppression by myeloid derived suppressor cells // Immunol. Rev.-2008.-Vol.222.-P.162-179.
- Gabrilovich D.I. Nagaraj S. Myeloid-derived suppressor cells as regulators of the immune system // Nature Rev. Immunol.- 2009.-Vol.9.-P.162-174.
- Ostrand-Rosenberg S., Sinha P. Myeloid-derived suppressor cells: Linking inflammation and cancer // J. Immunol.-2009.- Vol.182.-P.4499–4506.
- Peranzoni E., Zilio S., Marigo I., Dolcetti L., Zanovello P., Mandruzzato S., Bronte V. Myeloid-derived suppressor cell heterogeneity and subset definition // Curr. Opin. Immunol.-2010.-Vol.22.-P.238–244.
- Belyaev N., Perfilieva Yu., Kustova E., Zakiryanova G., Rysuly M., Aubakirova A., Baisheva S. Peripheral blood of cancer patients contents high level of CD34+ cells that can produce TGFMtZlAbstract Book. Molecular targets for cancer therapy: Fifth biennial meeting “Regulatory Myeloid suppressor cells in health and disease”, March 12-15, 2009 // Clearwater Beach. – Florida: 2009. – P. 41-48.
- Abbas A.K., Lichtman A., Pillai S. Cellular and Molecular Immunology // Saunders. - 2007. – Р. 18-24.
- Cools N., Ponsaerts P., van Tendeloo V. F. I., Berneman Z. N. Regulatory T Cells and Human Disease // Clin. Develop. Immunol. – 2007. - P. 21-29.
- DeGrendele H.C., Estess P., Picker L.J., Siegelman M.H. CD44 and its ligand hyaluronate mediate rolling under physiologic flow: a novel lymphocyte/endothelial cell primary adhesion pathway // J. Exp. Med. - 1996. - Vol.183. - P.1119-1130.
- Petrey A.C., de la Motte C.A. Hyaluronan, a crucial regulator of inflammation // Front. Immunol. - 2014. - Vol.5.-P.1-13.
- Bollyky P.L., Falk B.A., Long S.A., Preisinger A., Braun K.R., Wu R.P., Evanko S.P., Buckner J.H., Wight T.N., Nepom G.T. CD44 costimulation promotes FoxP3+ regulatory T cell persistence and function via production of IL-2, IL-10, and TGF-β // J. Immunol.-2009.-Vol.183.-P.2232-2241.
- Firan M., Dhillon S., Estess P., Siegelman M.H. Suppressor activity and potency among regulatory T cells is discriminated by functionally active CD44 // J. Blood.-2006.-Vol.107.-P.619-627.
- Iijima J., Konno K., Itano N. Inflammatory alterations of the extracellular matrix in the tumor microenvironment // Cancers. - 2011. - Vol.3. – Р. 3189-3205.
- Takeuchi J., Sobue M., Sato E., Shamoto M., Miura K., Nakagaki S. Variation in glycosaminoglycan components of breast tumors // Cancer Res.-1976.-Vol.36.-P.2133-2139.
- Bertrand P., Girard N., Delpech B., Duval C., d'Anjou J., Dauce J.P. Hyaluronan (hyaluronic acid) and hyaluronectin in the extracellular matrix of human breast carcinomas: comparison between invasive and non-invasive areas // Int. J. Cancer.- 1992.-Vol.52. - P. 1-6.
- Ponting J., Kumar S., Pye D. Co-localisation of hyaluronan and hyaluronectin in normal and neoplastic breast tissues // Int. J. Oncol.-1993.-Vol.2.-P.889-893.
- Tammia R.H., Kulttia A., Kosmab V.-M., Pirinenc R., Auvinenc P. Hyaluronan in human tumors: Pathobiological and prognostic messages from cell-associated and stromal hyaluronan. Sem // Cancer. Biol. -2008.-Vol.18.-P.288-295.
- de la Torre M., Wells A.F., Bergh J., Lindgren A. Localization of hyaluronan in normal breast tissue, radial scar, and tubular breast carcinoma // Hum. Pathol. -1993. - Vol.24. - P.1294-1297.
- Auvinen P., Parkkinen J., Johansson R., Agren U., Tammi R., Eskelinen M.J., Kosma V.M. Expression of hyaluronan in benign and malignant breast lesions // Int. J. Cancer. - 1997. - Vol.74. - P.477-481.
- Perfilyeva Yu., Ostapchuk Ye., Cetin E.A., Yilmaz A., Deniz G., Talaeva Sh., Omarbaeva N., Oskolchenko I., Belyaev N. Hyaluronan-binding T regulatory cells in peripheral blood of breast cancer patients // J. Clin. Cell Immunol. - 2015.- Vol.6(1). – Р. 286-290.
- Mandapathil M., Szczepanski M.J., Szajnik M., Ren J., Lenzner D.E. Increased ectonucleotidase expression and activity in regulatory T cells of patients with head and neck cancer // Clin. Cancer Res. - 2009. - Vol.15. - P. 6348-6357.
- Hilchey S.P., Kobie J.J., Cochran M.R., Secor-Socha S., Wang J.C., Hyrien O., Burack W.R., Mosmann T.R., Quataert S.A., Bernstein S.H. Human follicular lymphoma CD39+-infiltrating T cells contribute to adenosine-mediated T cell hyporesponsiveness // J. Immunol. - 2009. - Vol.183. - P.6157-6166.
- Zimmer J. Natural killer cells: at the forefront of modern immunology // Springer-Verlag. - Berlin, Heidelberg: 2010. – Р. 428-436.
- Poli A., Michel T., Theresine M., Andres E., Hentges F., Zimmer J. CD56bright natural killer (NK) cells: an important NK cell subset // Immunology. - 2009. - Vol.126. – Р. 458–465.
- Cooper M. A., Fehniger T. A., Caligiuri M. A. The biology of human natural killer-cell subsets // Trends in Immunol. - 2001. - Vol.22. - P. 633-640.
- Moretta L. Dissecting CD56dim human NK cells. Blood. -2010. - Vol.116. - P.3689-3691.
- Caligiuri M.A. Human natural killer cells. Blood. - 2008. - Vol.112. - P. 461-469.
- Giuliani M., Giron-Michel J., Negrini S., Vacca P., Durali D., Caignard A., Le Bousse-Kerdiles C., Chouaib S., Devocelle A., Bahri R., Durrbach A., Taoufik Y., Ferrini S., Croce M., Mingari M. C., Moretta L., Azzarone B. Generation of a novel regulatory NK cell subset from peripheral blood CD34+ progenitors promoted by membrane-bound IL-15. PLoS ONE. - 2008.-Vol.3. – 226 р.
- Caumartin J., Favier B., Daouya M., Guillard C., Moreau P., Carosella E.D., LeMaoult J. Trogocytosis-based generation of suppressive NK cells // EMBO J. - 2007. - Vol.26. - P. 1423-1433.
- Huang Y.H., Zozulya A.L., Weidenfeller C., Schwab N., Wiendl H. T cell suppression by naturally occurring HLA-G- expressing regulatory CD4+ T cells is IL-10-dependent and reversible // J. Leukoc. Biol. - 2009. - Vol.86. - P. 273-281.
- Feger U., Tolosa E., Huang Y.H., Waschbisch A., Biedermann T., Melms A., Wiendl H. HLA-G expression defines a novel regulatory T-cell subset present in human peripheral blood and sites of inflammation // Blood. - 2007. - Vol.110. - P. 568577.
- Rebmann V., Busemann A., Lindemann M., Grosse-Wilde H. Detection of HLA-G5 secreting cells. Hum // Immunol. - 2003. - Vol.64. - P. 1017-1024.
- Garner W.L., Minton J.P., James A.G., Hoffmann C.C. Human breast cancer and impaired NK cell function // J. Surg. Oncol.- 1983.-Vol.24.-P.64–66.
- Caras I., Grigorescu A., Stavaru C., Radu D. L., Mogos I., Szegli G., Salageanu A. Evidence for immune defects in breast and lung cancer patients // Cancer Immunol. Immunother. - 2004. - Vol.53. - P. 1146-1152.
- Mamessier E., Sylvain A., Thibult M.L., Houvenaeghel G., Jacquemier J., Castellano R., Gonçalves A., André P., Romagné F., Thibault G., Viens P., Birnbaum D., Bertucci F., Moretta A., Olive D. Human breast cancer cells enhance self tolerance by promoting evasion from NK cell antitumor immunity // J. Clin. Invest. - 2011. - Vol.121. - P. 3609–3622.
- Ostapchuk Y., Aktas C.E., Perfilyeva Y., Yilmaz A., Belyaev N., Deniz G. HLA-G expressing NK cell subset with suppressive properties is expanded in breast cancer. Immunology 2015. The Amirican Association of immunologists annual meeting, May 8-12, 2015 (TUM10P.1043) // J. Immunol. - 2015.-Vol.194. - 1 Suppl. – Р. 211-224.
- Ostapchuk Y.O., Cetin E.A., Perfilyeva Y.V., Yilmaz A., Skiba Y.A. d, Chirkin A.P., Omarbaeva N.A., Talaeva Sh.G., Belyaev N.N., Deniz G. Peripheral blood NK cells expressing HLA-G, IL-10 and TGF-b in healthy donors and breast cancer patients // Cell. Immunol. - 2015. - V.298. - P. 37-46.