Проведена оценка повреждающего эффекта на морфологическую структуру тиреойдных тканей крыс, получивших внутрь эквивалентную человеку радиоактивность для радиойодтерапии рака щитовидной железы и тиреотоксикоза, а также радионуклидной диагностики «Натрия йодид 131I, раствор для терапии», производства ИЯФ РК. Установены хорошая переносимость и безопасность радиофармпрепарата, степень повреждающего эффекта, соотетствующий его дозе радиоактивности. «Натрия йодид 131I, раствор для терапии» можно рекомендовать к клиническим испытаниям.
Введение. В радионуклидной терапи для внутритканевого облучения применяется тиреотропный йод-131 (131I), который избирательно включается в щитовидной железе в прямой зависимости ее функциональной активности [1]. В зрелых формах рака щитовидной железы как в папиллярной и фолликулярной, а также в их рецидивах и метастазах 131I включается также, хотя в меньшей степени, чем в нормальных тиреойдных клетках [2-4]. Для уничтожения раковых клеток применяются большие радиоактивности 3,5-7,0 ГБк (75 МБк/кг), и несколько курсов. При токсической аденоме и тиреотоксикозе накопление 131 очень высокое. При этом радиойодтерапия применятся с меньшей радиоактивностью 0,2-1,0 ГБк (8,57 МБк/кг), с целью сохранения части функционирующей ткани и доведения функции щитовидной железы с гипертиреоза до состояния эутиреоза. В настояшее время с дигностической целью широко применяется тиреотропный короткоживущий радионуклид 99mТс-пертехнетата.
Целью исследования является оценка повреждающего эффекта на тиреойдные ткани крыс, получивших эквивалентную человеку радиоактивность для радиойодтерапии рака щитовидной железы и тиреотоксикоза с «Натрия йодид 131I, раствор для терапии» (коммерческое название), производства Института ядерной физики Республики Казахстан [5].
Материал и методы. Материалом данного исследования послужили 3-х месячные лабораторные крысы весом 250300 г, которые распределялись по 5-ти группам, по 5 голов в каждой. Животным группы №1 вводилась эквивалентная радиоактивность 131I для терапи рака щитовидной железы 18,75-22,5 МБк. Крысам группы №2 вводилась радиоактивность для лечения тиреотоксикоза 2,14-2,57 МБк, животным группы №3 – диагностическая доза 7,148,57 кБк 131I.Крысам I-III групп 131I вводили внутрь через зонд. Группе крыс №4 введена эквивалентная радиоактивность 99mТс-пертехнетата для визуализации (диагностики) щитовидной железы 3,76-4,7 МБк. Группа №5 включала интанктных животных. После завершения испытания, через 8 месяцев от начала введения, всех 5 групп крысзабивали. У крыс был выделен макропрепарат гортань с щитовидной железой. Макропрепараты подвергались морфологическому изучению.
Из полученных макропрепаратов под контролем стериоскопического микроскопа МСБ-10 с помощью глазного скальпеля и пинцета осторожно выделяли щитовидную железу и для фиксации сразу же помещали в 10% раствор нейтрального формалина на 24 часа. После зафиксированные кусочки пропускали через спиртовые растворы возрастающей концентрации и заключали в парафиновые блоки, из которых затем с помощью микротома нарезали срезы толщиной 5-7 мкм. Из тканевых срезов после окрашивания гематоксилином-эозином изготовливались постоянные гистологические препараты. Морфологический анализ препаратов проводился под светооптическим микроскопом с применением объектива с десятикратным увеличением х10.
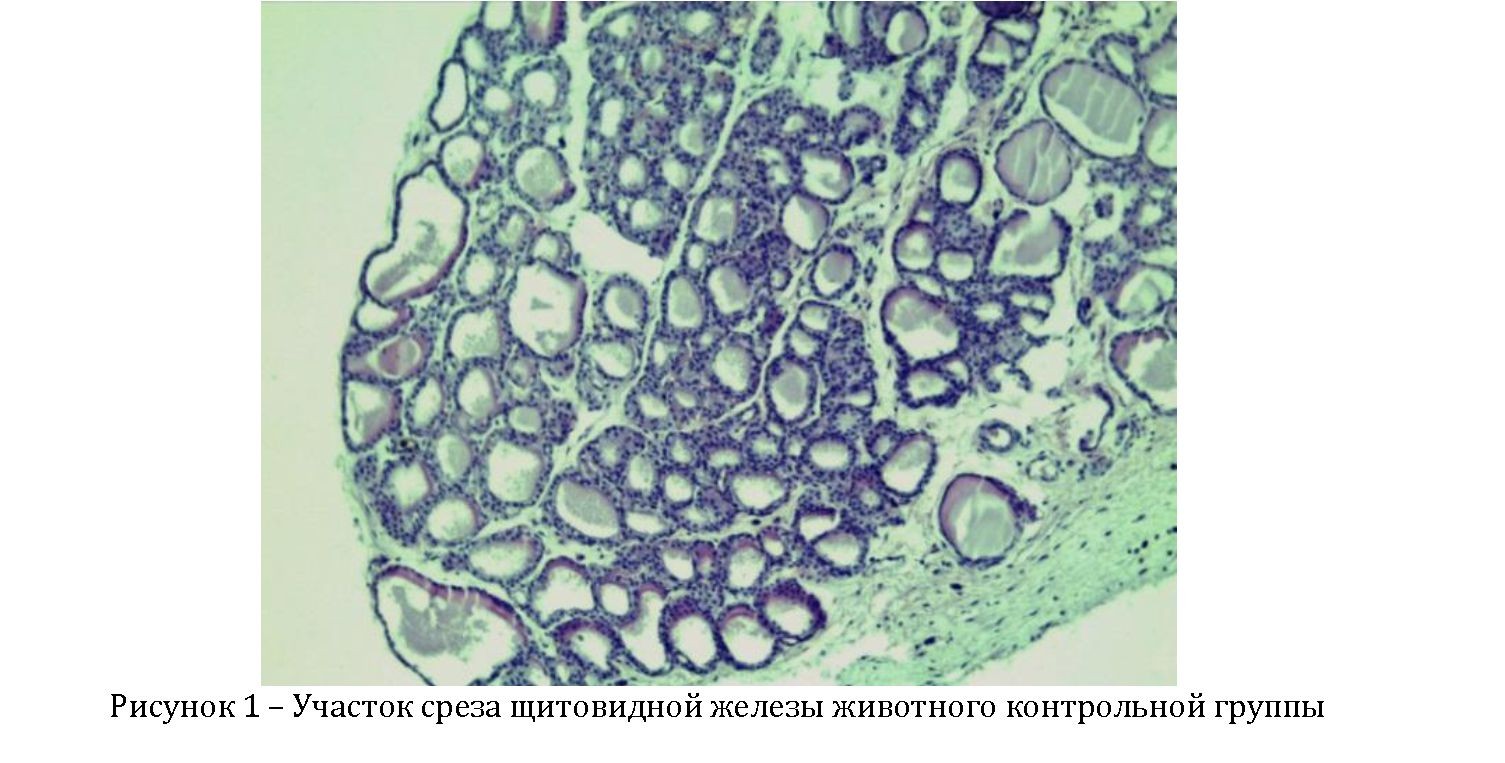
Результаты и обсуждение. Паренхима щитовидной железы крыс группы №4, которым была введена эквивалентная радиоактивность 99mТс-пертехнетата для визуализации щитовидной железы, и интактной контрольной группы №5 образована фолликулами разных размеров, отделенными друг от друга тонкими пучками соединительной ткани. При этом отсутствовала выраженная зависимость между размером фолликула и его расположением в органе. Так, например, крупные фолликулы располагались как по периферии органа, так и в центральных его участках. Диаметр самых крупных фолликулов достигает 350 мкм. Коллоид фолликулов имел либо зернистую, либо плотную консистенцию.
В мелких фолликулах эпителий кубический. В фолликулах диаметром более 70 мкм эпителий постепенно приобретал плоскую форму. Высота эпителия составляла у фолликулов с диаметром от 20 до 50 мкм - 5,92±0,19 мкм, у фолликулов диаметром от 51 до 100 мкм - 5,47±0,17 мкм, диаметром от 101 до 150 мкм - 5,42±0,15 мкм, диаметром от 151 мкм и более - 4,1±0,1 мкм.
Увеличение размера фолликулов в процессе их роста происходило за счет возрастания удельного веса их полости. Так у фолликулов диаметром 20-50 мкм диаметр полости составляет 69,6%, у фолликулов диаметром 51-100 мкм данный показатель равен 78,06%, у фолликулов диаметром 101-150 мкм - 88,2% и у фолликулов диаметром от 151 мкм и более - 91,63%.
Диаметр ядер фолликулярных клеток в процессе роста фолликула менялся незначительно. Так у фолликулов диаметром 20-50 мкм диаметр ядер составлял 4,64±0,12 мкм, у фолликулов диаметром 51-100 мкм данный показатель равен 4,16±0,1 мкм, у фолликулов диаметром 101-150 мкм - 4,21±0,1 мкм и у фолликулов диаметром 151 мкм и более - 4,04±0,14 мкм.
Щитовидная железа опытных крыс, которым была введена эквивалентная радиоактивность 131I для терапи рака щитовидной железы (группа №1) обнаруживала различную степень реакции на вводимый препарат у разных особей. У одних особей паренхима железы была образована фолликулами разных размеров. Крупные фолликулы располагались по периферии органа, а мелкие - в центре. Крупные фолликулы содержали, как зернистый коллоид, так и плотный, пронизанный трещинами. Стенка фолликулов, независимо от их размера, была высталана кубическим или слегка уплощенным эпителием с округлыми и овальными гиперхромными ядрами.
У большинства особей имело место полное отсутствие крупных фолликулов. Мелкие фолликулы содержали плотный комковатый коллоид, а их стенка имела выраженные признаки дегенерации: вакуолизированные и безъядерные фолликулярные клетки, а также клетки, содержащие пикнотические ядра. Имели место случаи полного разрушения фолликулярного эпителия.
Ткань щитовидной железы крыс 2 группы, которые получили эквивалентную радиоактивность 131I для терапи тиреотоксикоза, характеризовалась различной степенью реакции на вводимый препарат у разных особей. Крайняя степень реакции выражалась в полном отсутствии крупных фолликулов. Все исследованные нами животные имели мелкие фолликулы и обнаруживали признаки дегенерации их стенок. При этом имела место вакуолизация фолликулярных клеток, а затем их полное разрушение. Ядра эпителиоцитов в одних случаях были сморщены и гиперхромны, в других случаях они были значительно увеличены и нередко имели отчетливую кариоллему и хорошо различимые ядрышки. Коллоид в фолликулах либо отсутствовал, либо имел вид плотных бесформенных комков. Значительный удельный вес ткани железы приходится на соединительнотканные прослойки, пронизанные расширенными кровенаполненными кровеносными сосудами.
Паренхима щитовидной железы крыс 3 группы, которые получили эквивалентную диагностическую радиоактивность 131I, образована фолликулами разных размеров. Мелкие фолликулы располагаются в центре органа, крупные же фолликулы - по периферии. В крупных фолликулах коллоид чаще имел зернистый вид, хотя обнаруживался плотный коллоид, пронизанный трещинами. Имели место случаи, когда в полости крупного фолликула по периферии располагался плотный коллоид, а в центре - зернистый.
На рис. 1-4 представлены цифровые фотографии, сделанные с окрашенных гистологических срезов участков щитовидной железы животных контрольных и опытных групп.. При этом увеличение окуляра составляло х10 и объектива х10, всего х100 раз. На рисунке 1 - участок среза щитовидной железы животного контрольной группы. Такая же картина получалась у крыс, которым была введена диагностическая радиоактивность.
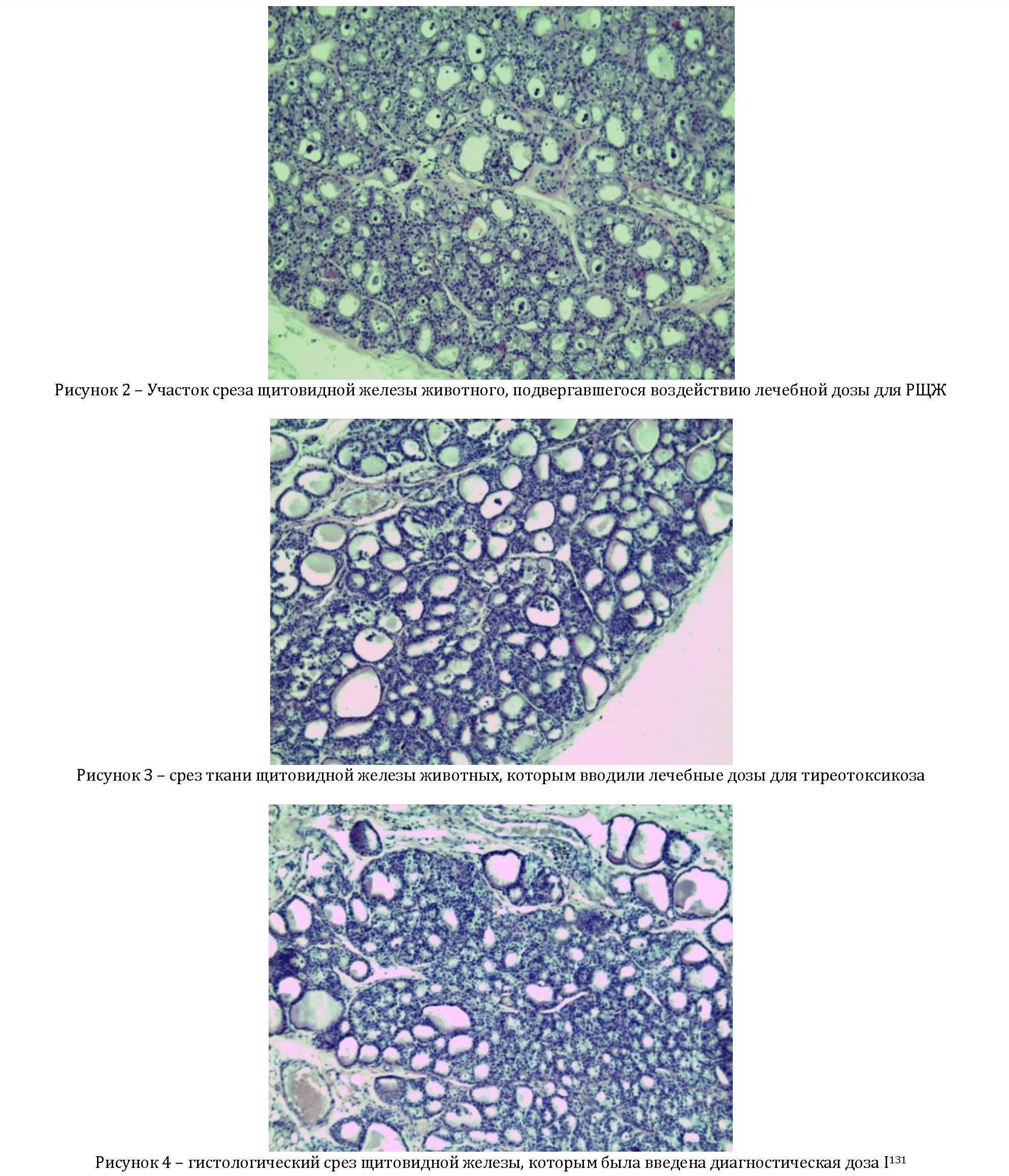
У крыс рисунок 2 – участок среза щитовидной железы животного, подвергавшегося воздействию лечебной дозы для рака щитовидной железы; рисунок 3 – срез ткани щитовидной железы животных, которым вводили лечебные дозы для тиреотоксикоза; рисунок 4 – гистологический срез щитовидной железы, которым была введена диагностическая доза I131.
Таким образом, по сравнению с контрольной группой, наибольшие морфологические изменения в щитовидных железах наблюдались в группах животных, подвергавшихся воздействию лечебной радиоактивности 131I для рака щитовидной железы и для тиреотоксикоза, причем в группах №2 и №3 доли дегенерирующих фолликулов составили приблизительно 40 и 10 процентов, соответственно. В группе №3 (диагностическая доза 131I) морфологическая картина отличалась от контрольной наличием некоторых дегенеративных изменений. Между группой №4 с диагностической радиоактивностью 99mТс- пертехнетата и контрольной (интактной) группы №5 дегенеративных изменений не выявлено. По сравнению с 99mТс-пертехнетатом повреждающий эффект 131I очень высок. При введении 100 МБк 99mТс-пертехнетата критический орган щитовидная железа получает лучевую нагрузку в (9,2 мЗв) 124 раза меньше, чем при введении 2 МБк 131I (1140 мЗв) с диагностической целью [6]. Как видно, дегенеративно-деструктивные изменения в щитовидной железе крыс прямо зависели от введенной радиоактивности «Натрия йодид 131I, раствор для терапии».
Заключение.
Изучен повреждающий эффекта на тиреойдные ткани крыс, различной радиоактивности «Натрия йодид 131I, раствор для терапии», производства Института ядерной физики Республики. Разнообразие и глубина морфологических изменений щитовидной железы крыс прямо зависели от введенной радиоактивности. Чем больше введена радиоактивность, тем разнообразнее, глубже и больще морфологические изменения в щитовидной железе крыс. Самые частые, разнообразные и глубокие морфологические изменения в щитовидной железе встречались у группы №1 крыс, которым была введена эквивалентная радиоактивность 131I для терапи рака щитовидной железы. У группы №2 крыс, которым была введена эквивалентная радиоактивность 131I для терапи тиреотоксикоза все изменения были как у группы крыс №1, проявлялись меньшей интенсивностью с признаками регенерации в виде выраженных соединительнотканных прослоек и расширенными кровенаполненными кровеносными сосудами.
В момент ߯ распада атома 131I (Тı/2=8,06 суток) испускает ß- излучение (0,25МэВ-2,8%; 0,34 МэВ-9,3%; 0,61 МэВ-87,2%; 0,81 МэВ-0,7%;), из которого слагается лечебный эффект радионуклидной терапии. Из всего широкого спектра γ- излучений, рабочей для сцинтиграфии является Eγ=364 кэВ (82,5%). Даже диагностическая радиоактивность 131I вызывает легкие структурные изменения в “органе- мишени” для тиреоидных радионуклидов - щитовидной железе у крыс. У 99mТс-пертехнетатас Т1/2=6,02 часа и моноэнергетически Eγ=140 кэВ (89,0%) повреждающий эффект меньше, чем 131I. Диагностическая радиоактивность 99mТс не вызывает морфологических изменений, и группа №4 приравнивается с контрольной №5 группой.
«Натрия йодид 131I, раствор для терапии», производства ИЯФ, обладает достаточной степенью повреждающим эффектом ткани щитовидной железы у крыс в экспериментев эквивалентной для человека интервалах радиоактиности. Установены хорошая переносимость и безопасность «Натрия йодид 131I, раствор для терапии»,введенной внутрь радиоактивности, эквивалентной для радиойодтерапии зрелых форм рака щитовидной железы и тиреотоксикоза у человека, что можно рекомендовать к клиническим испытаниям.
Выводы:
- Степень морфологических изменений ткани щитовидной железы у крыс прямо зависела от введенной эквивалентной человеку радиоактивности «Натрия йодид 131I, раствор для терапии».
- Крайне выраженные дегенеративно-деструктивные изменения наблюдались в ткани щитовидной железы у животных, после введенной радиоактивности 131I для терапии рака щитовидной железы.
- У крыс, получившие лечебную радиоактивность для тиреотоксикоза были те же изменения, но менее выраженыс признаками регенерации, чем у животных с радиоактивностью для радиойодтерапии рака щитовидной железы.
- Некоторые деструктивные изменения наблюдались у крыс, которым введена диагностическая радиоактивность 131I, незначительно отличающаяся от крыс контрольной и обследованных с 99mТс групп, но в значительно меньшей степени, чем у крыс группы №1 и №2.
- Достаточная степень повреждающего эффекта и хорошая переносимость различных радиоактивностей в эксперименте у крыс, позволяют рекомендовать «Натрия йодид 131I, раствор для терапии» к проведению клинических испытаний.
СПИСОК ЛИТЕРАТУРЫ
- Цыб А.Ф., Дроздовский Б.Я. Радионуклидная терапия. Опыт, проблемы, перспективы. Атомная стратегия XXI. - 2003. - 14 с.
- Наркевич Б.Я., Ширяев С.В. Методические основы радионуклидной терапии // Мед.радиол. рад. Безопасность. - 2003. - № 5. - С. 35-44.
- О.Е. Шлыгиной, А.Р. Борисенко Радионуклиды для терапии // Ядерная медицина. Учебное пособие. - Алматы: 2008. - С.38-39.
- О.Е. Шлыгиной, А.Р. Борисенко Терапия открытыми радиоактивными веществами // Ядерная медицина. Учебное пособие. - Алматы: 2008. - С. 273-278.
- Мясищев А.В., Тамаева К., Мустафина М.М., Тулеушева М.А. Опыт получение йода-131 в ИЯФ НЯЦ РК. Труды 5-ой Международной конференции «Ядерная и радиационная физика» 26-29 сентября 2005 г., Алматы, Казахстан (труды в печати). Том III. Радиационная экология // Ядерно-физические методы в медицине и промышленности.- Алматы: 2006. - С.424-428.
- Степаненко В.Ф., Норец Т.А., Гончарова А.Я., Яськова Е.К. Особенности определения и учета лучевых нагрузок при использовании радиофармацевтических препаратов с диагностической целью. В кн.: Стандартизированные методики радионуклидной диагностики // Методические указания. - Обнинск: 1987. - С. 63-102.