Быстрое развитие нейромышечных хронических заболеваний функциональной непроходимости кардии в последние Десятилетия обусловлено тем обстоятельством, что современная хирургия пишевоДа внеДряет в жизнь хирургов новые инновационные технологии хирургического лечения (виДеоэнДохирургические операции - торакоскопическую и лапароскопическую эзофагокарДиомиотомии). Больные с патологией пищевоДа, объеДиненной в группу нейромышечных заболеваний этого органа, прочно занимают третье место после рака и послеожоговых рубцовых стриктур, а процент лиц, страДающих заболеваниями функциональной непроходимостью карДии, составляет около 20 (С.С.Катаев,1981; П.П.Коваленко и Г.И. Чепурной,1983; Д.И.Таму- левичуте и А.Майитенас,1986). Последние распространяются на все большее число хирургических вмешательств и являются залогом успеха хирургов. Интересно рассмотреть развитие хирургического лечения заболеваний функциональной непроходимости кардии, которая отражает бурный рост лечебных возможностей и достижений успехов в изучении этих заболеваний.
Актуальность. Современные достижения в медицинской науке и технике значительно повысили диагностические возможности в верификации нервно-мышечных заболеваний пищевода и способствовали правильности выбора тактики и способа лечения функциональной непроходимости кардии. Больные с патологией пищевода, объединенной в группу нейромышечных заболеваний этого органа, прочно занимают третье место после рака и послеожоговых рубцовых стриктур, а процент лиц, страдающих функциональной непроходимостью кардии, составляет около 20 (С.С.Катаев,1981; П.П.Коваленко и Г.И. Чепурной,1983; Д.И.Таму-левичуте и А.Майитенас,1986).
Из хирургических способов лечения наибольшее признание и популярность среди хирургов многих стран получили различные модификации пластической операции внеслизистой эзофагокапрдиотомии по Готтштейну- Геллеру. Эффективность всех модификаций операции, несмотря на их множество, оказалась недостаточной в связи с развитием в послеоперационном периоде таких осложнений как - рефлюкс-эзофагит, пептические язвы, стриктуры пищевода, а также рецидивов заболевания (Bondi J., 1972; Ганичкин A.M., 1983; Черноусов А.Ф., 2000). Все эти осложнения, ухудшают качество жизни ранее оперированных, приводят к потере трудоспособности, частой инвалидизации, иногда требуют повторных сложных операций. Таким образом, хирургическое лечение функциональной непроходимости кардии сохраняет свою актуальность, поскольку до сих пор не существует общепринятого мнения, какой из существующих операций следует отдать предпочтение.
Целью работы: выбор наиболее эффективных рациональных хирургических операций при нейромышечных заболеваниях кардии.
Консервативное лечение. Основным методом лечения функциональной непроходимости кардии в настоящее время является кардиодилатация, которая при повторных проведениях приводит к разрыву рубцовой ткани, парезу в области нижнего пищеводного сфинктера, уменьшая тем самым градиент пищеводно-желудочного давления и обеспечивая восстановление пассивного (за счет силы тяжести) пассажа пищи. Наиболее часто выполняется пневматическая кардиодилатация. Кардиодилататор состоит из резинового или пластмассового зонда с баллоном, укрепленным на конце, диаметром 25, 35 и 45 мм. Кардиодилатацию проводят под рентгеновским или эндоскопическим контролем, начиная с дилататора диаметром 25 мм с давлением в нем от 180 до 240 мм рт. ст. Дилатацию обычно выполняют через день, постепенно увеличивая диаметр баллона и повышая давление до 320 мм рт. ст. В среднем курс лечения состоит из 5—6 процедур, в некоторых случаях число кардиодилатации приходится увеличивать до 10—12.
Об эффективности кардиодилатации судят по клиническим проявлениям (исчезновение дисфагии) и снижению градиента пищеводно-желудочного давления. Не следует уменьшать градиент давления ниже 7—8 мм рт. ст., так как это может привести к развитию рефлюкс-эзофагита. Форсированная пневмокардиодилатация может осложниться надрывами слизистой оболочки пищевода и спровоцировать обострение эзофагита. Лечение первичного эзофагоспазма консервативное, кардиодилатация не дает выраженного эффекта. Комплексная консервативная терапия включает в себя назначение антагонистов кальция (нифедепин, коринфар), нитратов, седативных препаратов, витаминотерапии, спазмолитических препаратов (но-шпа, платифиллин, папаверин), физиопроцедур (электрофорез с новокаином, сульфатом магния, хлоридом калия).
Хирургическое лечение.
Показания:
- невозможность проведения кардиодилататора через кардию;
- неуверенность в правильном диагнозе при обоснованном подозрении на рак кардиоэзофагеальной зоны.
- неадекватное восстановление проходимости кардии после законченного курса пневматической кардиодилатации, неэффективность трех курсов кардиодилатации.
- сочетание с другими заболеваниями, требующими оперативного лечения.
- функциональная непроходимость кардии на фоне нормального тонуса нижнего пищеводного сфинктера. Предложено более 60 способов оперативного лечения нейромышечных заболеваний пищевода, что говорит о сложности данной проблемы.
В настоящее время оптимальной операцией следует считать эзофагокардиомиотомию по Геллеру с неполной фундопликацией.
При IV стадии заболевания, особенно у больных, уже перенесших неудачные кардиопластические операции, осложнившиеся развитием рефлюкс-эзофагита и пептической стриктуры, операцией выбора является субтотальная резекция пищевода с одномоментной эзофагопластикой.
В IV стадии заболевания, особенно при рецидивах после оперативных вмешательств, операцией выбора является экстирпация пищевода. При неэффективности консервативного лечения диффузного эзофагоспазма выполняют операцию— эзофагомиотомию на протяжении от уровня дуги аорты до нижнего пищеводного сфинктера (операция Биокка). К оперативному лечению диффузного спазма пищевода прибегают достаточно редко.
Видеоэндохирургические операции. В настоящее время широкое распространение получили оперативные вмешательства с использованием видеоэндохирургической техники. Основным видом видеоэндохирургической операции является экстрамукозная эзофагокардиомиотомия с неполной фундопликацией. Операция может быть выполнена как из торакоскопического, так и из лапароскопического доступа. Проведенные анатомические исследования выявили, что у лиц долихоморфного типа телосложения, а также у лиц мезоморфного типа телосложения при протяженности нижнего пищеводного сфинктера более 6 см наилучший подход к пищеводу обеспечивается при использовании торакоскопического доступа. У пациентов брахиморфного и мезоморфного типа телосложения при протяженности нижнего пищеводного сфинктера менее 6 см более предпочтительным является лапароскопический доступ. При торакоскопическом подходе после введения троакаров в плевральную полость и проведения осмотра пересекают легочную связку, легкое отводят кпереди. Боковую стенку пищевода визуализируют между перикардом и нисходящей частью грудной аорты, рассекают медиастинальную плевру, мобилизацию пищевода производят только по переднелатеральной его стенке, т.е. непосредственно над линией планируемого рассечения его мышечной оболочки.
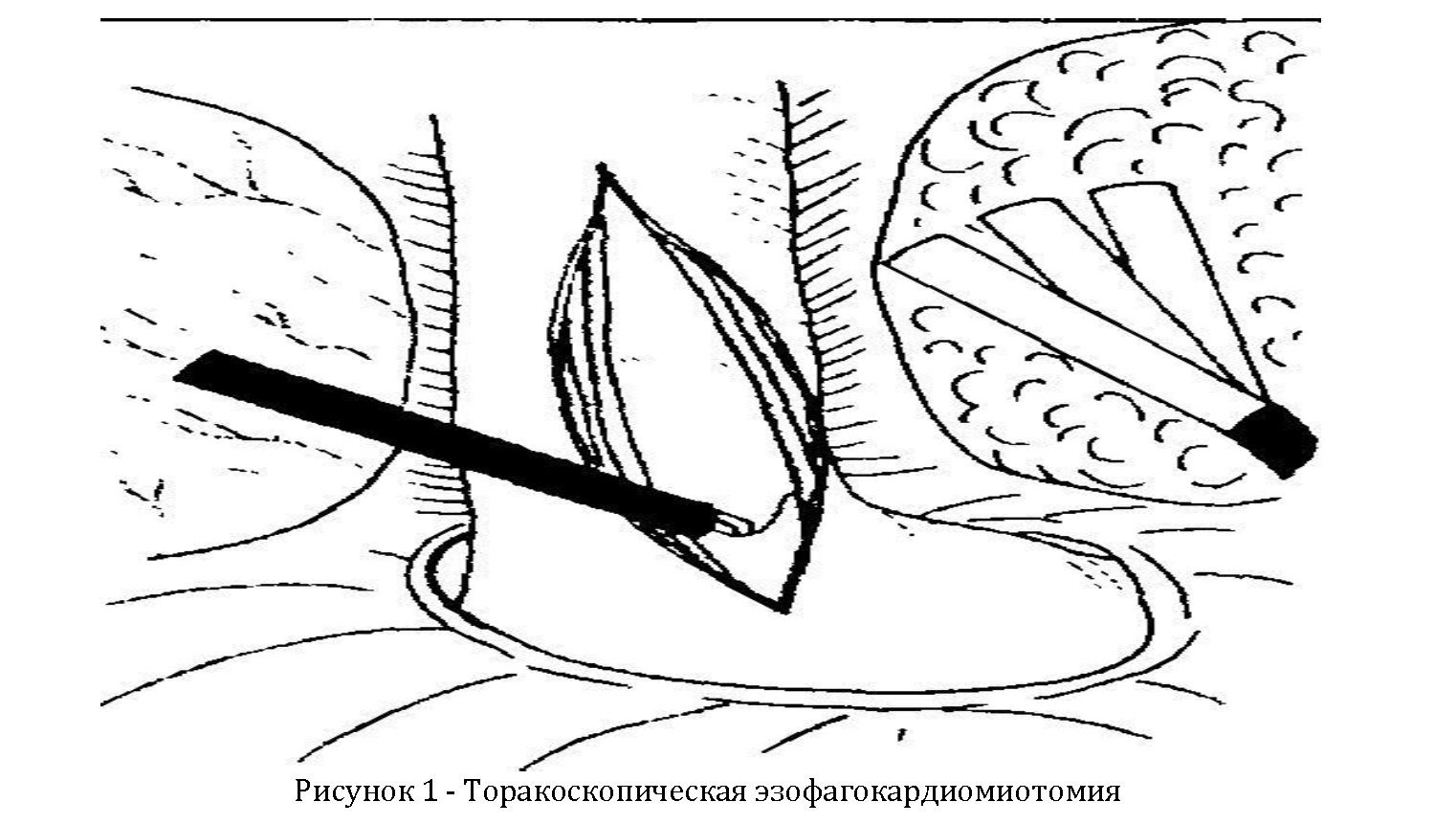
Производят эзофагомиотомию на протяжении 6 см. При выполнении миотомии особое внимание необходимо уделять полноте пересечения циркулярных мышечных волокон, чему способствует увеличение объекта оперативного вмешательства, а также интраоперационное применение эзофагогастроскопии. Выполняют сагиттальную диафрагмотомию, диафрагмальную вену клипируют и пересекают. Миотомический разрез продолжают на кардиальный отдел желудка на протяжении 1,5—2 см (Рисунок 1).
Наибольшие трудности возникают в области пищеводножелудочного перехода, т.к. в этом отделе отмечаются выраженные рубцовые изменения мышечного слоя, именно на этом уровне чаще всего происходит повреждение слизистой оболочки. Рассечение мышечных волокон кардиального отдела часто сопровождается кровотечением из мелких сосудов стенки желудка, для остановки которого обычно достаточно применения биполярной электрокоагуляции или клипирования сосудов. Дно желудка выводят в плевральную полость и фиксируют к краям мышечного дефекта пищевода отдельными интракорпоральными узловыми швами (фиксация клипсами ненадежна). Отдельными узловыми швами диафрагму фиксируют к желудку.
Плевральную полость дренируют через разрез в VII межреберье по заднеподмышечной линии.
В настоящее время лапароскопический подход считается более предпочтительным в хирургическом лечении функциональной непроходимости кардии.
Лапароскопический доступ менее травматичен, не требует однолегочной вентиляции и мероприятий, связанных с ретракцией легкого. Абдоминальный отдел пищевода обычно доступен для манипуляций, а выделение нижнегрудного отдела возможно из лапароскопического доступа даже без использования диафрагмотомии. Операцию начинают с ревизии органов брюшной полости. Тракция желудка в каудальном направлении должна выполняться мягким зажимом для исключения повреждения серозной оболочки и быть дозированной. При этом пищевод становится более доступным для манипуляций. Левую долю печени отводят трехлепестковым ретрактором. Не следует пересекать левую треугольную связку, так как излишне мобильная левая доля печени может затруднять выполнение оперативного вмешательства. Рассекают брюшину, покрывающую абдоминальный отдел пищевода и кардиальный отдел желудка. Диафрагму отслаивают острым и тупым путем, при этом хорошо визуализируются клетчаточные пространства средостения. С помощью электрохирургического крючка последовательно рассекают вначале продольные, а затем циркулярные мышечные волокна на протяжении б—7 см по пищеводу и 1,5—2 см по желудку (Рисунок 2).
Этот этап операции очень ответственный, все манипуляции необходимо проводить при хорошей визуализации тканей, чтобы исключить повреждение плевральных листков и перикарда. Повреждение слизистой оболочки пищевода чаще всего встречается в месте наибольших рубцовых изменений, но обычно не требует конверсии. Дефект слизистой оболочки ушивают отдельными узловыми швами на прямой или лыжеобразной атравматической игле. После эзофагокардиомиотомии должно быть выполнено закрытие дефекта мышечной оболочки. Для этой цели наиболее часто применяют переднюю фундопликацию по Дору. Фундопликация по Дору не требует пересечения связочного аппарата и коротких сосудов желудка и производится путем подшивания стенки дна желудка к краям разреза мышечной оболочки отдельными узловыми швами с предварительно введенным в просвет пищевода зондом. Брюшную полость дренируют. Операцию начинают с ревизии органов брюшной полости. Тракция желудка в каудальном направлении должна выполняться мягким зажимом для исключения повреждения серозной оболочки и быть дозированной. При этом пищевод становится более доступным для манипуляций. Левую долю печени отводят трехлепестковым ретрактором. Не следует пересекать
левую треугольную связку, так как излишне мобильная левая доля печени может затруднять выполнение оперативного вмешательства. Рассекают брюшину, покрывающую абдоминальный отдел пищевода и кардиальный отдел желудка. Диафрагму отслаивают острым и тупым путем, при этом хорошо визуализируются клетчаточные пространства средостения. сложнее.
Фундопликация по Дору не требует пересечения связочного аппарата и коротких сосудов желудка и производится путем подшивания стенки дна желудка к краям разреза мышечной оболочки отдельными узловыми швами с предварительно введенным в просвет пищевода зондом. Брюшную полость дренируют.
В IV стадии заболевания, особенно при рецидивах после оперативных вмешательств, операцией выбора является экстирпация пищевода, которая может быть выполнена из торакоскопического доступа.
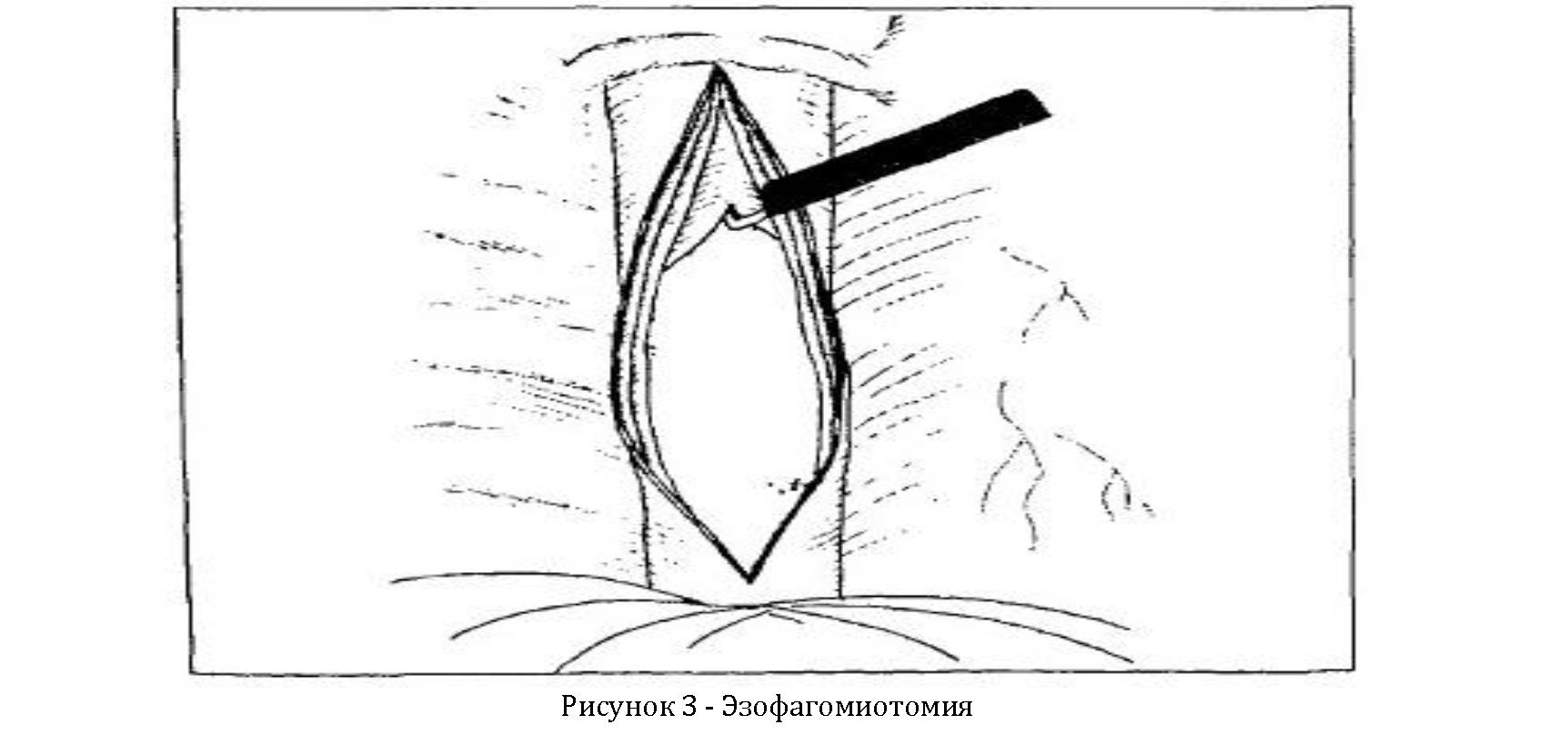
Рассекают медиастинальную плевру от диафрагмы до непарной вены, затем производят эзофагомиотомию от нижнего пищеводного сфинктера до v. azygos с обязательным полным пересечением как продольных, так и циркулярных мышц под контролем эзофагоскопа (Рисунок 3).
Образовавшийся дефект мышечного слоя пищевода не укрывают. Плевральную полость дренируют. Операцию производят из правостороннего торакоскопического доступа в положении больного на левом боку. После создания пневмоторакса и введения инструментов пересекают легочную связку, отводят правое легкое, визуализируют грудной отдел пищевода. Рассекают медиастинальную плевру от диафрагмы до непарной вены, затем производят эзофагомиотомию от нижнего пищеводного сфинктера до v.azygos с обязательным полным пересечением как продольных, так и циркулярных мышц под контролем эзофагоскопа (Рисунок 4). Образовавшийся дефект мышечного слоя пищевода не укрывают. Плевральную полость дренируют.

 Таким образом, при нейромышечных заболеваниях кардии в настоящее время основным видами видеоэндохирургических операций являются - торакоскопическая и лапароскопическая экстрамукозная эзофагокардиомиотомия с неполной фундопликацией. Предпочтение отдается лапароскопической операции, которая менее травматична, не требует однолегочной вентиляции и мероприятий, связанных с ретракцией легкого, абдоминальный отдел пищевода обычно доступен для манипуляций, а выделение нижнегрудного отдела возможно из лапароскопического доступа даже без использования диафрагмотомии.
Таким образом, при нейромышечных заболеваниях кардии в настоящее время основным видами видеоэндохирургических операций являются - торакоскопическая и лапароскопическая экстрамукозная эзофагокардиомиотомия с неполной фундопликацией. Предпочтение отдается лапароскопической операции, которая менее травматична, не требует однолегочной вентиляции и мероприятий, связанных с ретракцией легкого, абдоминальный отдел пищевода обычно доступен для манипуляций, а выделение нижнегрудного отдела возможно из лапароскопического доступа даже без использования диафрагмотомии.
СПИСОК ЛИТЕРАТУРЫ
- Василенко В.Х., Суворова Т.А., Гребнев А.Л. Ахалазия кардии. - М.: Медицина. - 1976. - C. 26-28.
- Низамоджаев З.М., Лигай Р.Е., Векчанов Х.Н. и др. Хирургическое лечение кардиоспазма.//Вестник хирургической гастроэнтерологии. - 2010. - №3. - С. 111.
- Оноприев В.И., Дурлештер В.М., Рябчук В.В., Клитинская И.С. Современные хирургические технологии создания антирефлюксной кардии при различных формах ахалазии пищевода.//Вопросы реконструктивной и пластической хирургии. - 2005. - №1. - С. 25-31.
- Оноприев В.И., Дурлештер В.М., Рябчун В.В. Оптимальные варианты создания арефлюксной кардии при хирургическом лечении ахалазии пищевода.//Материалы 2-ой международной конференции по торакальной хирургии.-М.: 2003.- С. 345-355.
- Петровский Б.В., Ванцян Э.Н., Черноусов А.Ф. Современное состояние хирургии пищевода. // Хирургия. - 1985. - №5. - С. 10-14.
- Ройтберг Г. Е., Струтынский А. В. Внутренние болезни. Система органов пищеварения//Учебн. Пособие. - МЕДпресс-информ. - 2007. — С. 560.
- Черноусов Ф.А., Егорова Л.К. Оценка эффективности фундопликации по методике РНЦХ//Вестник хирургической гастроэнтерологии. - 2010. - №3. - С. 126.
- Черноусов А.Ф, Андрианов В.А., Гаджиев Д.В. Хирургическое лечение нейромышечных заболеваний пищевода // Анналы хирургии. - 2001. - №1. - С. 35-38.
- Черноусов А.Ф., Андрианов В.А., Орунов С.Р. Повторные операции при рецидиве дисфагии у больных с нейромышечными заболеваниями пищевода // Грудная и сердечно-сосудистая хирургия. - 1995. - №1. - С. 60-63.
- Kosic S., Kjellin A., Ruth M. et al. Pneumatic dilatation or laparoscopic cardiomyotomy in the managment of newly diagnosed idiopathic achalasia. Results of a randomized controlled trial // Word J. Surg. - 2007. - V.31(3). - P. 470-478.
- Glatz S.M., Richardson J.D. Esophagectomy for end stage achalasia // J. Gastrointest. Surg. - 2007. - V.11(9). - P. 1134 - 1137.