В статье представлены современные сведения о внутриклеточных молекулярно-генетических механизмах деградации сустава. Освещена роль сигнального пути Wnt и система RANK/RANKL/OPG в ремоделировании костной ткани. Также рассмотрены вопросы, касающиеся роли DKK1 в ингибировании сигнального пути Wnt . Подробно рассмотрены молекулярно-биологические модели, объясняющие роль DKK1 и мезенхимальных стволовых клеток в развитии костей и поддержании гомеостаза костной массы, а также анаболическую и антикатаболическую функцию DKK1 в кости. Описана роль DKK1в нарушении остеогенеза и развитии остеопороза при различных процессах, вызывающих патологические изменения в суставах.
Введение.
Поражение суставов, включая остеоартрит (ОА), ревматоидный артрит (РА), разрушение поясничных дисков является одной из самых распространенных причин нетрудоспособности, вызывающей ухудшение качества жизни и значительные финансовые затраты, во всех возрастных группах по всему миру. Хотя причастность наследственных факторов в развитии каждого из этих патологий ясно установлена в многочисленных предыдущих исследованиях, основные молекулярногенетические механизмы остаются непонятными, особенно в свете многих общих патологических изменений. Эти изменения включают патологическую модификацию в субхондральной кости, воспалительные процессы в синовиальной ткани, деградацию хряща или разрушение межпозвоночных дисков. Большинство авторов признают, что чрезвычайно важную роль в ремоделировании костной ткани играют система RANK/RANKL/OPG, сигнальный путь Wnt и система костных морфогенетических белков. Кроме того, исследования патогенеза ОА показали, что Wnt-b- катениновый сигнал [1, 2, 3, 4] и другие сигнальные молекулы могут играть важную роль в развитии ОА посредством воздействия на процессы эндохондрального окостенения, включая влияние на мутации определенных генов и апоптоз хондроцитов. Также в некоторых исследованиях показано, что моделирование продукции костных морфогенетических белков является важным фактором не только в ремоделировании костной ткани, но и в индукции остеоартроза, связанного с травматическим повреждением хряща [1, 5].
Сигнальный путь Wnt.
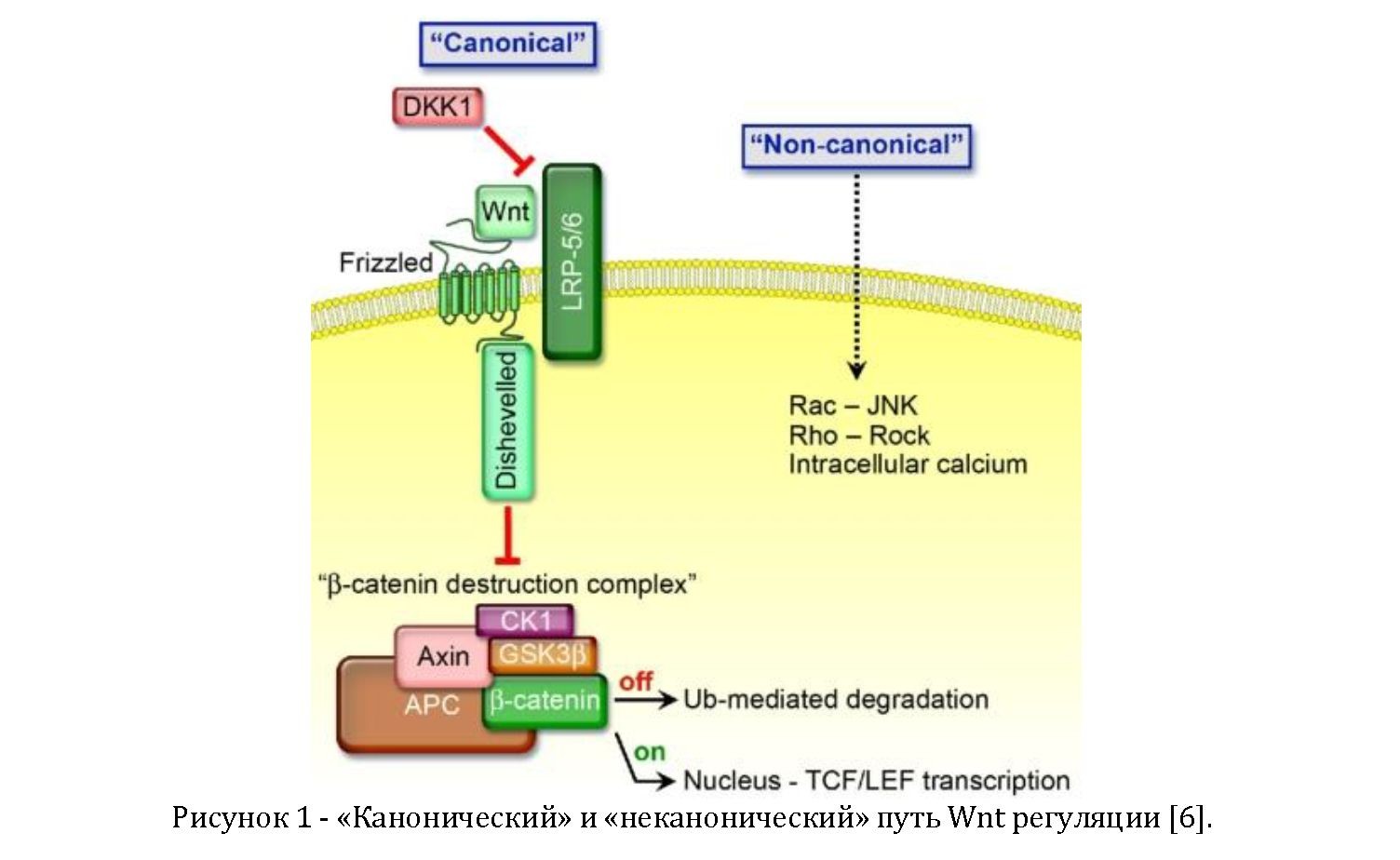
Сигнальный путь Wnt является одним из внутриклеточных регуляторных путей. Молекулы Wnt относятся к семейству гликопротеинов, это целый класс белков, регулирующих такие типы клеточной активности как гибель клетки, пролиферация, миграция, полярность и экспрессия генов. Wnt регуляция может быть «каноническая» или «неканоническая» (рисунок 1)[6]. Рассмотрим канонический путь Wnt регуляции. В отсутствие белков Wnt, молекулы гликоген-синтазы-киназы-ß (GSK3ß), Axin, adenomatouspolyposiscoli(APC) и казеин-киназы Iα (CKIα) образуют комплекс деструкции ß-катенина [7]. Фермент CKIa фосфорилирует ß-катенин в положении Ser45, а затем GSK3ß фосфорилирует ß-катенин в положении Ser33/Ser37/Thr41.
Фосфорилированный ß-катенин узнается белком ß- transducinrepeat, убиквитинируется и деградируется протеасомами.
С другой стороны, при активации канонического пути Wnt сигнализации Wnt белок связывается с одним из 10 членов frizzled (FZD) семейства рецепторов; комплекс Wnt-FZD затем связывается с липопротеином низкой плотности - lipoprotein-relatedprotein-5 (LRP5) или LRP6. Полученный комплекс активирует Dishevelled (Dvl) белок, который не дает Axin присоединиться к комплексу деструкции и противодействует способности GSK3ß фосфорилировать ß- катенин, тем самым предотвращая образования комплекса деструкции. Не деградируя, ß-катенин стабилизируется и транслоцируется в ядро, где связывается с фактором транскрипции TCF4 и повышает экспрессию гена-мишени, в том числе циклина D1, c-myc, c-jun, фактор роста эндотелия сосудов (VEGF), а также некоторых других, связанных с повышенным ростом клеток.
Канонический Wnt путь содействует кавеолин-зависимой интернализации LRP и способствует взаимодействию с белком Axin [8]. Напротив, в случае, когда белок DKK1 конкурентно связывается с LRP5/6 и привлекает белок- рецептор Kremen, это взаимодействие способствует клатрин-опосредованной интернализации, что приводит к инактивации LRP, а GSK3ß, Axin, APC, и CKIa формируют комплекс деструкции ß-катенина, препятствуя, таким
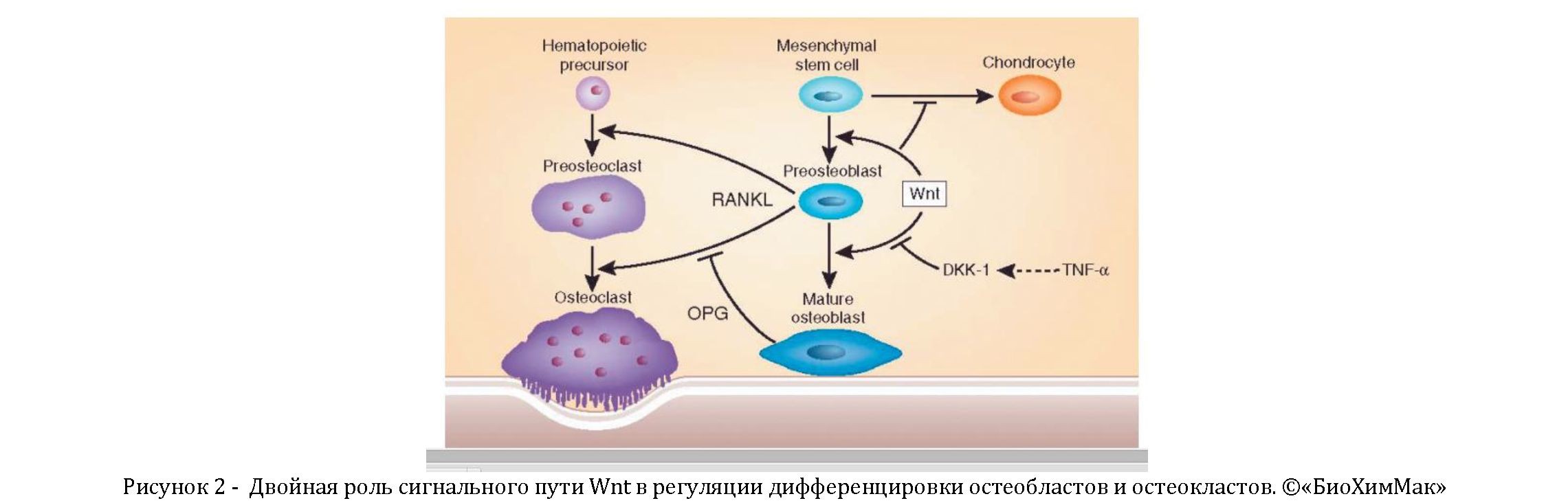
образом, Wnt-сигнализации [9, 10]. Кроме DKK1, существует целый ряд белков антагонистов, которым противостоят агонисты, усиливая или ингибируя активность канонического Wnt пути. Семейство белков DKK по современным сведениям состоит из 4 представителей, а именно DKK1, DKK2; DKK3 и DKK4. Наиболее хорошо изученный белок, Dkk-1 - это секретируемый протеин с молекулярной массой 28 кДа, растворимый ингибитор сигнального пути Wnt. Установлена важная роль Wnt- сигналинга в подавлении дифференцировки мезенхимальных клеток-предшественников в адипоциты и хондроциты (клетки хряща) и в усилении образования остеобластов. Dkk-1 участвует в регуляции костного метаболизма, т.к. останавливает дифференцировку и пролиферацию остеобластов (рисунок 2).
Участие DKK1 в регуляции развития кости и поддержании костной массы.
Рассмотрим более подробно эти процессы. Мезенхимальные стволовые клетки (MSC) костного мозга могут дифференцироваться в адипоциты, хондроциты или остеобласты. Хотя точная регуляция Wnt сигнализации во время развития костей зависит от комплекса сигналов микросреды, данные нескольких групп исследователей показывают, что белки Wnt3a, Wnt5a, Wnt7b и Wnt10b играют центральную роль в дифференцировке остеобластов (рисунок 3) [11, 12, 13, 14, 15]. Исследователями обнаружено повышение уровня ß-катенина в клетках линии остеобластов, тогда как снижение уровня ß-катенина в клетках-предшественниках остеобластов приводит к замедлению формирования костной структуры [16]. Помимо содействия остеобластной дифференцировке, канонический путь Wnt сигнализации ингибирует дифференцировку адипоцитов, в первую очередь путем стабилизации ß-катенина и последующей трансактивации TCF-отвечающих генов [17, 18]. DKK1 противодействует Wnt-опосредованному влиянию на дифференциацию кости и адипогенез. В течение 6 часов после начала адипогенеза было отмечено кратковременное повышение мРНК и белковой экспрессии DKK1 в преадипоцитах, что было связано со снижением регуляции цитоплазматического и ядерногоß-катенина.
Примечание. Wnt 3а, 5а, и 7b и Ihh совместно содействуют дифференцировке остеобластов, а DKK1 ингибирует остеобластогенез и сдвигает программу развития в сторону адипогенеза. Комплекс ß-catenin/TCF1 способствует ранней дифференцировке линии остеобластов через индукцию Runx2. Runx2 затем способствует активации транскрипции Osterix (OSX), который использует DKK1 для подавления экспрессии Runx2 для дальнейшего усиления созревания предшественников остеобластов. Также показаны фенотипические специфические маркеры для созревания остеобластов [6].
Кроме того, конститутивная экспрессия DKK1 в 3T3-L1 преадипоцитах способствует адипогенной дифференциации клеток [19]. В последнее время установлено, что трансгенная сверхэкспрессия Msx2 (гомеодоменовый фактор транскрипции, впервые выявлен в остеобластах) у мышей подавляет адипогенез при одновременном
повышении остеогенной дифференцировки, увеличении формирования объема костей, что в результате приводит к увеличению экспрессии Wnt7a и Wnt7b и снижению экспрессии DKK1. Кроме того, Msx2 ингибирует Dkk1 промоторную активность, а также снижает ассоциацию РНК- полимеразы с Dkk1 хроматином [20]. Эти данные позволяют предположить, что DKK1 ингибирует остеобластогенез и индуцирует липогенез, эффективно переключая путь дифференциации MSC (мезенхимальных стволовых клеток) (рисунок 3). Наконец, отдельные члены Wnt семейства, а именно Wnt8 и, в меньшей степени, Wnt4 способствуют дифференциации хондроцитов. Не удивительно, что белок frizzled-relatedprotein Frzb/sFRP3, антагонист Wnt1 и Wnt8 сигнализации, как было показано, ингибирует дифференцировку хондроцитов in vivo (рис. 3) [21, 22]. Интересно, что рекомбинантный белок bonemorphogenicprotein-2 (Bmp2), имплантированный в
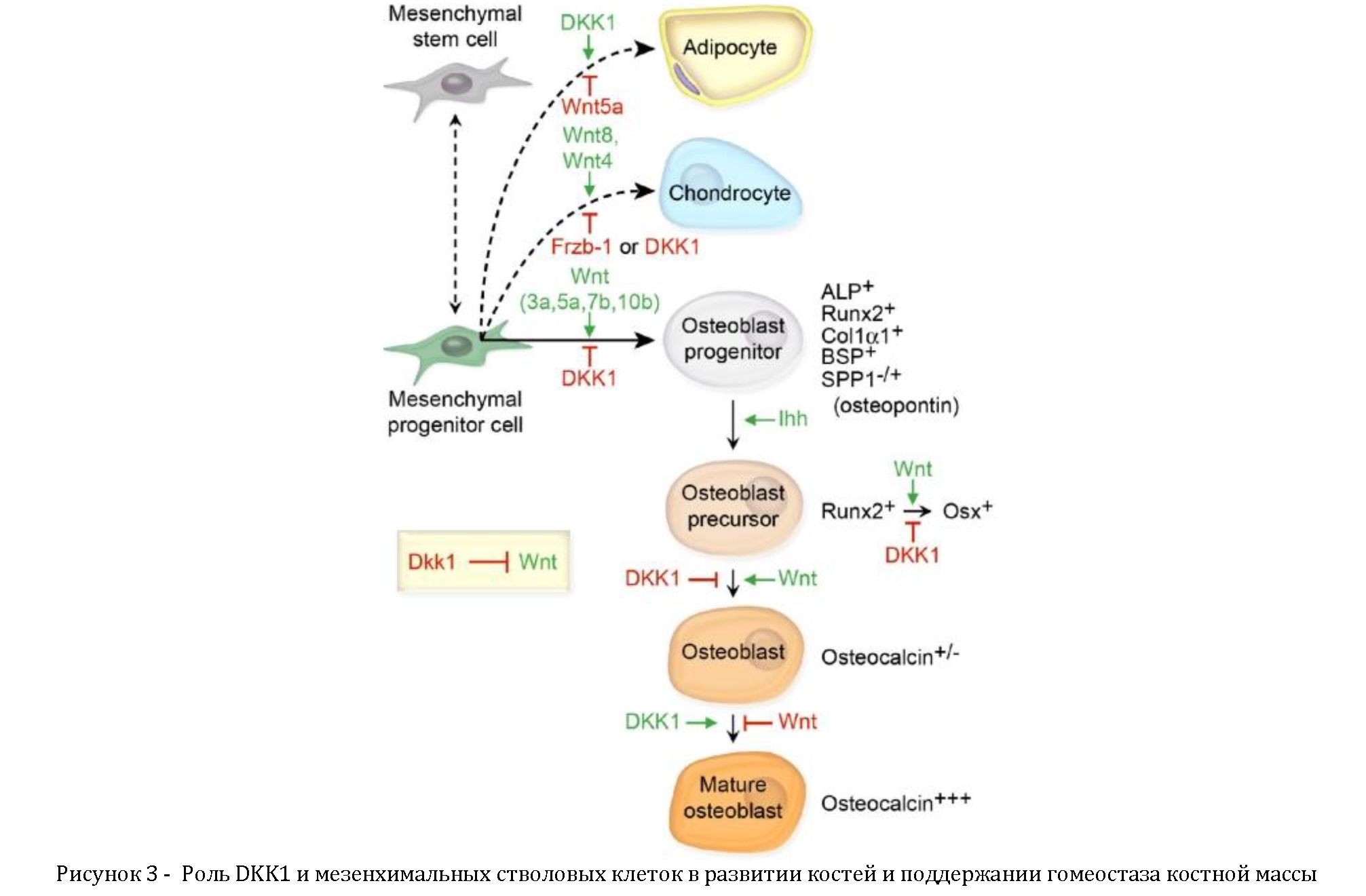
мышцы мышей, усиливает регуляцию Wnt лигандов и рецепторов, активирует ß-катенин-опосредованную TCF- зависимую транскрипционную активность, и способствует эндохондральной костной формации. При этом Dkk1 ингибирует ß-катениновый сигнал, а также хондрогенез и остеогенез, тем самым предотвращая эндохондральную костную формацию [23].
Таким образом, данные, полученные в экспериментах на животных и в исследованиях человека, подтверждают анаболическую роль Wnt сигнального пути в нарастании и поддержании костной массы, опосредованную усилением дифференциации/активности остеобластов с сопутствующим подавлением дифференциации/активности остеокластов [24, 25, 26, 27]. Остеобласты производят Osteoprotegrin (OPG) и рецептор активатор NF-kB (RANK) лиганд (RANKL). RANKL связывается с RANK и усиливает дифференциацию/активность остеокластов. OPG, растворимый рецептор-приманка для RANKL, конкурентно ингибирует RANKL-RANK взаимодействие, и поэтому OPG: RANKL соотношение определяет результирующий эффект на остеокласты [28].
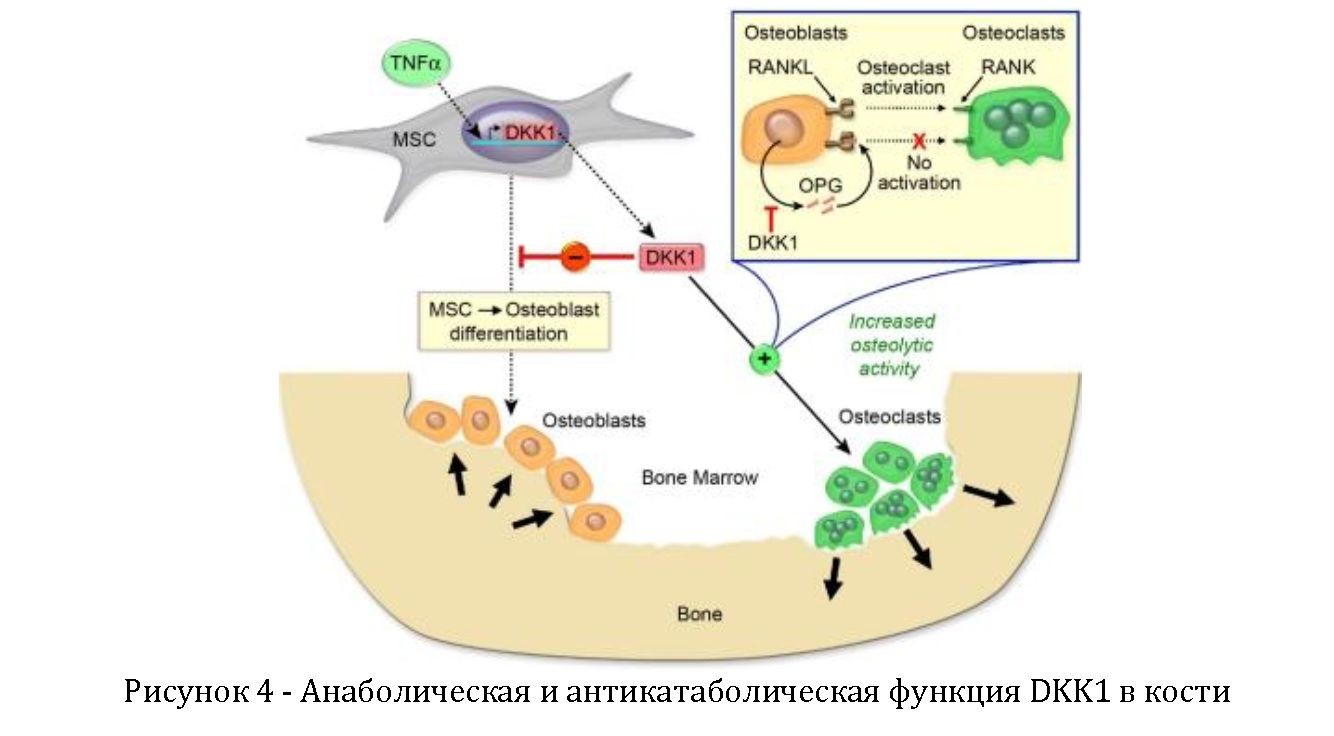
Практика показывает, что DKK1 также является основным фактором, определяющим патологию костей и суставов при воспалительном артрите [2]. Экспрессия белка DKK1 усиливается в синовиальных фибробластах и увеличена в сыворотке пациентов с ревматоидным артритом (РА) по сравнению со здоровым контролем. В отличие от РА, где происходит эрозия кости, концентрация DKK1 в сыворотке у пациентов с анкилозирующим спондилитом, заболеванием, характеризующимся формированием остеофитов, была снижена по сравнению со здоровым контролем. Исследователями было показано, что анти- TNF- α антитела уменьшают уровень DKK1 в сыворотке у пациентов с РА. Dkk1 индуцировали у TNF-α трансгенных мышей с моделью воспалительного артрита; анти- Dkk1 антитела предотвращали эрозию кости и способствовали формированию остеофитов, но не влияли на воспаление [2]. Наконец, было показано, что воздействие Dkk1 на кости было опосредовано ингибированием Wnt сигнального пути, которое непосредственно нарушало образование новой костной ткани и ограничивало экспрессию OPG, тем самым сдвигая OPG: RANKL соотношение в пользу резорбции кости. Эти данные подтверждают концепцию, что DKK1 ингибирует формирование костей и усиливает резорбцию кости (рисунок 4).
Примечание. TNF-α усиливает секрецию DKK1 которая ингибирует остеобластогенез в MSC и снижает уровень OPG, что приводит к снижению срастания кости. Кроме того, DKK1 повышает уровень RANKL, и повышенное RANKL: OPG соотношение активирует активность остеокластов, что приводит к резорбции кости [6].
Баланс между анаболическим формированием костной ткани и резорбцией костной ткани регулирует нормальную плотность костной ткани, в повышение уровня одного или другого процесса снижает плотность костной ткани или приводит к повышенной плотности костной ткани соответственно.
Заключение.
Белок DKK1 играет одну из ключевых ролей в процессах, связанных с развитием и поддержанием гомеостаза костной ткани. DKK1 обеспечивает правильное развитие скелета, участие DKK1 в LRP5-опосредованном сигнальном пути важно для поддержания костной массы, в результате мутаций гена DKK1 возможно возникновение генетических синдромов, связанных с нарушением метаболизма кости.
Кроме того, DKK1 участвует в процессах, связанных с возникновением и развитием эрозивного артрита. DKK1 также играет роль в адипогенезе, хондрогенезе, пролиферации желудочно-кишечного эпителия, потере костной ткани, ассоциированной с ревматизмом. Повышенные уровни DKK1 в сыворотке ассоциированы с раком предстательной железы, а повышенные уровни DKK1 и RANKL в плазме костного мозга и периферической крови пациентов, страдающих множественной миеломой, ассоциированы с присутствием локальных повреждений костной ткани.
Таким образом, изучение и идентификация генетических и метаболических факторов риска, которые способствуют или препятствуют развитию патологических процессов в кости, могли бы обеспечить понимание различной степени выраженности дегенеративных изменений. Исследования в этой области могли бы расширить наше понимание этиологии болезней и привести к разработке стратегических подходов профилактики и лечения этих заболеваний.
СПИСОК ЛИТЕРАТУРЫ
- Dell'Accio F., De Bari C., MF El Tawil N. et al. Activation of WNT and BMP signaling in adult human articular cartilage following mechanical injury.// Arthritis Res Ther.- 2006.-№8(5).-R139.
- Diarra D., Stolina M., Polzer K. et al. Dickkopf-1 is a master regulator of joint remodeling. //Nat Med.- 2007.- №13(2).-p.156-163.
- Schett G., Zwerina J., David J.P. The role of Wnt proteins in arthritis. //Nat Clin Pract Rheumatol.- 2008.- №4(9).-p.473-480
- Polzer K., Diarra D., Zwerina. Inflammation and destruction of the joints--the Wnt pathway.// Joint Bone Spine. -2008 №75(2).-p.105- 107.
- Поворознюк В.В., Григорьева Н.В. Антиостеопоротические препараты в лечении остеоартроза у женщин в постменопаузальном периоде. // Боль. Суставы. Позвоночник. 2011. №4 (04)
- Joseph J. Pinzone, Brett M. Hall, Nanda K. Thudi, Martin Vonau, Ya-Wei Qiang, Thomas J. Rosol, John D. Shaughnessy. The role of Dickkopf- 1 in bone development, homeostasis, and disease. //Blood. -2009.- №15; 113(3).- p.517-525.
- Clevers H. Wnt/beta-catenin signaling in development and disease. //Cell. -2006.- №127.-p.469-480.
- Yamamoto H, Sakane H, Yamamoto H, Michiue T, Kikuchi A. Wnt3a and Dkk1 regulate distinct internalization pathways of LRP6 to tune the activation of beta-catenin signaling. //Dev Cell.- 2008.- №15.-p.37-48.
- Glinka A, Wu W, Delius H, Monaghan AP, Blumenstock C, Niehrs C. Dickkopf- 1 is a member of a new family of secreted proteins and functions in head induction.// Nature.- 1998.- №391.-p.357-362.
- Mao B, Wu W, Davidson G, et al. Kremen proteins are Dickkopf receptors that regulate Wnt/beta-catenin signalling.// Nature.- 2002.- №417.-p.664-667.
- Baksh D, Tuan RS. Canonical and non-canonical Wnts differentially affect the development potential of primary isolate of human bone marrow mesenchymal stem cells.// J. Cell Physiol. - 2007.- №212.- P.817-826.
- Hu H, Hilton MJ, Tu X, Yu K, Ornitz DM, Long F. Sequential roles of Hedgehog and Wnt signaling in osteoblast development.// Development.- 2005.- №132.-p.49-60.
- Baksh D, Boland GM, Tuan RS. Cross-talk between Wnt signaling pathways in human mesenchymal stem cells leads to functional antagonism during osteogenic differentiation.// J Cell Biochem.- 2007.- №101.-p.1109-1124.
- Boland GM, Perkins G, Hall DJ, Tuan RS. Wnt 3a promotes proliferation and suppresses osteogenic differentiation of adult human mesenchymal stem cells.// J Cell Biochem.- 2004.- №93.-p.1210-1230.
- Etheridge SL, Spencer GJ, Heath DJ, Genever PG. Expression profiling and functional analysis of wnt signaling mechanisms in mesenchymal stem cells.// Stem Cells.- 2004.- №22.-p.849-860.
- Day TF, Guo X, Garrett-Beal L, Yang Y. Wnt/beta-catenin signaling in mesenchymal progenitors controls osteoblast and chondrocyte differentiation during vertebrate skeletogenesis.// Dev Cell.- 2005.- №8.-p.739-750.
- Ross SE, Hemati N, Longo KA, et al. Inhibition of adipogenesis by Wnt signaling. //Science.-2000.- №289.-p.950-953.
- Morvan F, Boulukos K, Clement-Lacroix P, et al. Deletion of a single allele of the Dkk1 gene leads to an increase in bone formation and bone mass. J Bone Miner Res. -2006.- №21.-p.934-945.
- Christodoulides C, Laudes M, Cawthorn WP, et al. The Wnt antagonist Dickkopf-1 and its receptors are coordinately regulated during early human adipogenesis.// J Cell Sci.- 2006.- №119.-p.2613-2620.
- Cheng SL, Shao JS, Cai J, Sierra OL, Towler DA. Msx2 exerts bone anabolism via canonical Wnt signaling.// J Biol Chem.- 2008.- №283.- p.20505-20522.
- Enomoto-Iwamoto M, Kitagaki J, Koyama E, et al. The Wnt antagonist Frzb-1 regulates chondrocyte maturation and long bone development during limb skeletogenesis.// Dev Biol.- 2002.- №251.-p.142-156.
- Wang S, Krinks M, Moos M., Jr Frzb-1, an antagonist of Wnt-1 and Wnt-8, does not block signaling by Wnts -3A, -5A, or -11. //Biochem Biophys Res Commun.- 1997.- №236.-P.502-504.
- Chen Y, Whetstone HC, Youn A, et al. Beta-catenin signaling pathway is crucial for bone morphogenetic protein 2 to induce new bone formation.// J Biol Chem.- 2007.- №282.-P.526-533.
- Gong Y, Slee RB, Fukai N, et al. LDL receptor-related protein 5 (LRP5) affects bone accrual and eye development.// Cell.- 2001.- №107.- P.513-523.
- Baron R, Rawadi G. Targeting the Wnt/beta-catenin pathway to regulate bone formation in the adult skeleton. //Endocrinology.- 2007.- №148.-P.2635-2643.
- Glass DA, Bialek P, 2nd, Ahn JD, et al. Canonical Wnt signaling in differentiated osteoblasts controls osteoclast differentiation. //Dev Cell.- 2005.- №8.-P.751-764.
- Glass DA, Karsenty G., 2nd In vivo analysis of Wnt signaling in bone. //Endocrinology.- 2007.- №148.-p.2630-2634.
- Holmen SL, Giambernardi TA, Zylstra CR, et al. Decreased BMD and limb deformities in mice carrying mutations in both Lrp5 and Lrp6.// J Bone Miner Res.- 2004.- №19.-P.2033-2040.