В статье рассматривается методы получения медпрепаратов из дикорастущей шуйской конопли. Лекарства, созданные на основе веществ, выделенных из конопли, которые используют при лечении ВИЧ-инфицированных больных, лейкемии, эпилепсии, астмы, глаукомы, множественных склерозов, язв, и других нервно-мышечных расстройств, а также методы получения химически чистого тетрагидроканнабинола из дикорастущей конопли. Исследования проводились совместно с немецкой фирмой «THC Pharm» GmdH, у которой имеется единственная в Европе лицензия по изготовлению и реализации препарата из конопли – дронабинола.
Цель исследования - наличие в Казахстане Шуйской долины с огромными запасами дикорастущей конопли, отсутствие собственных сильнодействующих медицинских препаратов обусловили необходимость проведения исследований по созданию казахстанского фармпрепарата.
Методология – обзор научных материалов, экспериментальный анализ полученных научных результатов.
Одним из актуальных и горячо обсуждаемых вопросов мировой фармации заключается в рациональности легализации каннабиноидов для использования в медицинских целях. Эти вещества уже достаточно широко применяются в клиниках Канады и в Соединенных Штатах. Cannabis является одним из сильнодействующих лекарственных растений и еще в древности применялась в медицинских целях. В Азии она в различных препаратах рекомендовалась для лечения ряд заболеваний, как кашель, усталость, ревматизм, астма, белая горячка, головная боль, тяжелые формы менструации и др., хотя объем ее потребления снижался из-за внедрения синтетических снотворных препаратов и анальгетиков. Долгое время это растение входила в Фармакопеи многих стран мира, но потом была запрещена. Открытие способа снижения внутриглазного давления с помощью каннабиноидов оживил интерес к ее использованию в терапевтических целях, в частности глакоумы [1].
Для профилактики тошноты и рвоты ассоциированной с химиотерапией рака используется Маринол [2]. Он способен устранять тошноту и рвоту в дозах, которые не влияют на мышление. В течение последних нескольких лет в мире ведется активная работа над созданием новых медицинских препаратов из конопли. Такие страны, как Бельгия, Франция, Германия, Нидерланды, Великобритания и Финляндия, проводят эксперименты с целью определить степень эффективности марихуаны в лечении [3]:
- % тошноты и рвоты в ходе химио- и радиотерапии;
- % глаукомы;
- % множественного склероза;
- % истощенности и потери аппетита при СПИДе;
- % повреждениях или заболеваниях позвоночника;
- % хронических болей, например, при артрите;
- % синдрома Туретта
Каннабиноиды - это биологически активные вещества особого строения, которые в природе встречаются исключительно в растениях семейства коноплёвых (Cannabaceae). Растительные каннабиноиды также называют фитоканнабиноидами. Растение Cannabis содержит более 421 химических веществ, из которых 61 являются каннабиноидами [4].
Предшественником всех растительных каннабиноидов является каннабигероловая кислота, которая под воздействием трёх независимых ферментов класса циклаз превращается в каннабихроменовую, каннабидиоловую и дельта-9-тетрагидроканнабиноловую кислоты (рис.1). Данные кислоты в результате декарбоксилирования дают свободные каннабиноиды - каннабихромен, каннабидиол и дельта-9-тетрагидроканнабинол соответственно.
Остальные каннабиноиды являются продуктами биотрансформации основных каннабиноидов.
В современной литературе много данных по испытанию действия отдельных синтетических и натуральных компонентов марихуаны на лечение отдельных болезней. В настоящее время конопля очень модна среди современных создателей лекарств, т.к. к ней обычно, в отличие от опиатов, у тяжелобольных, не происходит привыкания. Каннабиноиды в растворенном состоянии быстро модифицируются [5]. Только у тетрагидроканнабинола (ТГК) известно более 60 изомеров. Стабилизировав структуру этого соединения можно легко получить мощное лекарство от различных болезней, что и было сделано американской фирмой «ROXANE» (с 1999 г. Unimed. Solvay Pharmaceuticals, Inc, США), выпустившей в продажу в 1985 году лекарственный препарат под названием «Marinol». Отношение к производным конопли сейчас становится положительным. Недавно было доказано, что ТГК не накапливается в жировых клетках мозга человека, не убивает их, и сама по себе не делает его ленивым и тупым. Основной мишенью ТГК является головной мозг, где он взаимодействует со специфическими рецепторами CR1, CR2 (18, 20, 21), максимальное количество которых расположено в коре головного мозга (фронтальных отделах), лимбической системе, гиппокампе и мозжечке [6]. Более того, Alan Leshner [7] уже выделен компонент (его назвали SR141716), который блокирует рецепторы каннабиноидов в головном мозге и тем самым влияние каннабиноидов. Уже доказано, что сами каннабиноидподобные соединения являются обычными компонентами человеческого тела. Их роль в организме пока неизвестна. Хотя выявленный компонент SR141716 тормозит протекание химических процессов в мозге возможно, использовать его для лечения редких случаев ТГК-зависимости.
Когда говорят об использовании конопли, то подразумевают использование листьев соцветий и верхушечных листьев. На их внутренней поверхности формируются ворсинки, наполняемые каннабиноидами. Обычно в сухих листьях дикорастущих и культурных наркотических растений накапливается от 0,03 до 4,8 психоактивного ингридиента - дельта-9- тетрагидроканнабиола или ТНС (англ)-ТГК (рус).
В современных культурных наркотических сортах в верхушках содержится до 20% ТНС (на сухой вес). Другие каннабиноиды, такие как каннабидиол (КБД), каннабинол (КБН) и каннабихромин, содержащиеся в растении не обладают психоактивным действием, но биологически активны, в частности они ингибируют синтез ДНК, РНК и белков [8].
Термин «медицинская марихуана» включает в себя несколько веществ, которые имеют различный юридический и медицинский статус:
- Растение каннабис и его смола - любая часть Cannabis sativa L., indica, ruderalis или смола, полученная из его верхушек.
- Экстракт каннабиса - обычно масло, полученное из растения, а также препараты, полученные из него; известно как гашишное масло.
- Каннабиноиды. Класс химических веществ, имеющих общую структуру. Cannabis содержит более 60 каннабиноидов.
В США официально вместо термина экстракт каннабиса используется термин Ботаническая наркотическая субстанция «Botanical Drug Substances» полученная из растительного материала конопли. Растения каннабис включают в себя дикий генотип Cannabis sativa и его сорта, а также другие хемотипы натурального происхождения, содержащие различное количество индивидуальных каннабиноидов. Согласно «Guidance for industry Botanical Drug Products Draft Guidance, August 2000, US Department of Health and Human Services, Food and Drug Administration Center for Drug Evaluation and Research» она определяется как: «Наркотическая субстанция, полученная из одного или нескольких растений, водорослей или макроскопических грибов приготовляется из сырого ботанического материала с помощью одного или нескольких процессов: простого высушивания, растирания до порошкообразного вида, экстракции водой или спиртом, или сходных процессов». Термин ботаническая наркотическая субстанция не включает химически чистые или модифицированные вещества, полученные из натурального сырья. Т.е. в случае конопли термин «botanical drug substances» не включают в себя химически чистые каннабиноиды.
Полученный из конопли медицинский экстракт (CBMEs), приготовленный одним из вышеперечисленных методов классифицируется как ботаническое наркотическое вещество «botanical drug substances», в соответствии, с определением данном в «Guidance for industry Botanical Drug Products Draft Guidance, August 2000, US Department of Health and Human Services, Food and Drug Administration Center for Drug Evaluation and Research».
Ботаническая наркотическая субстанция «Вotanical drug substances» полученная из растений конопли, включает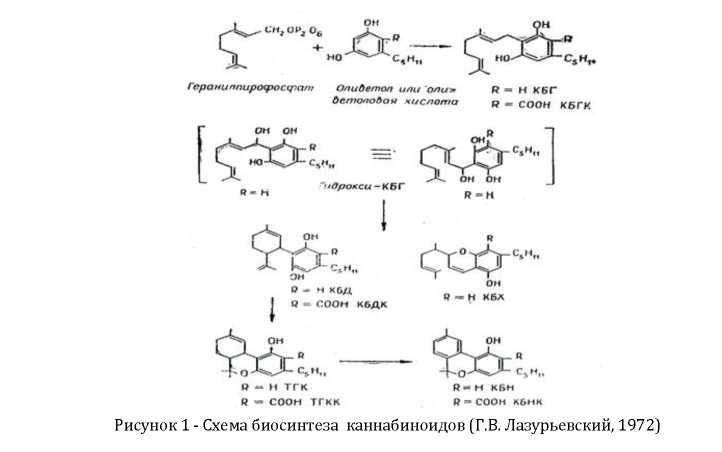
первичный экстракт, полученный таким процессом как, например, мацерия, перколяция, экстракция растворителями, такими как Cl до С5 спирты (т.е. этанол), Norflurane (HFA134a), HFA227 и жидкой двуокисью углерода при низких температурах. Первичный экстракт может быть в дальнейшем очищен с помощью ступенчатой экстракции, возгонки или хромтографии. Дальнейшее превращение ботанического наркотического вещества «Вotanical drug substances» в Ботанический наркотический продукт «Eotanical drug substances» определяется в «Guidance for industry Botanical Drug Products Draft Guidance, August 2000, US Department of Health and Human Services, Food and Drug Administration Center for Drug Evaluation and Research» как: «Ботанический продукт, который намереваются использовать как лекарственное средство или лекарство, полученное из ботанической наркотической субстанции» [9].
Наличие в Казахстане Шуйской долины с огромными запасами дикорастущей конопли, отсутствие собственных сильнодействующих медицинских препаратов обусловили необходимость проведения исследований по созданию казахстанского фармпрепарата. Это и является целью исследований данной работы.
Разработка технологии получения высокоочищенных каннабиноидов из низко- и высококаннабиноидной конопли.
В настоящее время в мире официально выпускается два препарата из конопли - Маринол и Дронабинол. Первый производится в США путем последовательного химического синтеза ∆-9-ТГК начиная из двух углеродных молекул. Дронабинол производится немецкой фирмой «THC Pharm» GmbH путем синтеза из ненаркотических каннабиноидов. В обоих случаях использование в качестве сырья конопли с высоким содержанием ТГК в этих странах запрещено законом.
В литературе имеются сведения о способах получении дельта-9-ТГК из марихуаны [10]. Так, в 1942 году Wolver et all (1942) опубликовали статью, где описали выделение ТГК путем получения этанольного экстракта красного цвета, его очистке эфиром путем многократной дистилляции при вакууме, хроматографии на колонках с силикагелем и пропускания через активированную окисью алюминия и ТХУ. Полученный препарат не был химически чистым.
De Ropp [11] в 1960 году выделил ТГК используя верхушки листьев Cannabis sativa. После экстракции метанолом он хроматографировал экстракт через колонку с Celite с последующей перегонкой при вакууме. Чистота выделения контролировалась путем хроматографии полученных экстрактов на бумаге. Наиболее чистые каннабиноиды были получены Gaoni and Mechoulam [12] в 1964 году из гашиша. Путем многократного хроматографирования через колонки с florisil и окисью алюминия, последующего синтеза промежуточного соединения 3,5-динитрофенилуретана с ТГК, очистки этого соединения и мягкого гидролиза был получен ТГК. Его чистота контролировалась путем хроматографии на пластинках с силуфолом и спектроскопическим анализом (IR и NMR).
Korte et all [13] в 1965 году выделили грубый экстракт из женских растений Cannabis sativa indica и Cannabis sativa non indica. Для удаления примесей типа хлорофилла, каротиноидов, ксантофилла экстракт хроматографировали через колонку с активированным алюминием. Все каннабиноидные фракции были сконцентрированы в виде гашишного масла красного цвета. Дальнейшая очистка производилась по схеме Gaoni и Mechoulam (1964).
В 1967 году Gaoni и Mechoulam повторно сообщили об очистке ТГК. Была использована следующая схема: каннабиноиды извлекали из гашиша гексаном. Экстракт разделяли на кислую и нейтральную фракции. Кислую фракцию хроматографировали через колонку с Frosil или промытой кислотой окисью алюминия. Элюировали смесью пентана с эфиром постепенно увеличивая полярность раствора. ТГК находилась во фракции, содержащей 15% эфира в пентане. Дальнейшая хроматография была связана с получением кристаллического деривата - ТГК-3,5,- динитрофенилуретана и его последующего гидролиза.
В 1972 году Verwey Witte [14] опубликовали методику выделения ТГК-А. Каннабиноиды выделяли гексаном из гашиша, затем экстракт помещали в сосуд с двумя слоями - 2% NaOH и 2% сульфитом натрия. Щелочной слой был подкислен H2SO4 pH≤2, что приводит к выпадению в осадок кислых каннабиноидов. ТГК получали путем выпаривания при 3000С эфирного раствора ТНС-А.
Бриану Вайту [15] пришлось обобщить все эти методы и запатентовать в Американском патентном ведомстве. Положительное решение получено в 2003 году. В качестве лекарственных средств им названы ТНС, CBD, CBN, THCAc, CBDCOOH, THCV как в отдельности, так и в комбинации, как натуральные (из растений), так и синтетические, а также их рецепторы. Отличием от ранее использованных методов является использование жилкой двуокиси углерода для экстракции.
Нами также разрабатывались препаративные методы получения химически чистого ТГК из дикорастщей конопли. Исследования по этому разделу проводились совместно с немецкой фирмой «THC Pharm» GmdH, у которой имеется в Европе лицензия по изготовлению и реализации препарата из конопли - дронабинола. Нами разработана подробная технология получения наркотического вещества ТНС из дикорастущей конопли. Т.к. этот раздел имеет ряд моментов «ноу-хау», некоторые этапы не были описаны подробно.
Краткое описание этапов технологического процесса получения каннабиноидов из шуйской конопли
- Скашивание растений производится в период с июля по сентябрь месяцы. Общая продуктивность сплошных диких зарослей конопли обычно составляет около 10-35 ц/ га, культурных посевов около 30-60 ц/га. После высушивания от стеблей простым встряхиванием отделяются листья и соцветия. Их тщательно перемешивают до однородной массы и эту сухую массу помещают в мешки весом около 1015кг.
- Мешки с сухими листьями и соцветиями под охраной милиции перевозятся в лабораторию и помещаются в специальную комнату хранения.
- Общие потери сырья при высушивании составляет около 80 %. Из общего веса растения около 15% приходится на листья и соцветия. 20% от общего веса листьев остается на ветках. Таким образом, из 1000 кг свежескошенной конопли можно получить около 200 кг сухих растений. Из этих 200кг 30кг приходится на листья и соцветия. После отделения стеблей от листьев мы получаем около 24кг сухих листьев и соцветий. Из них около 2кг камни, песок и другой мусор.
- Обычно в шуйской конопле содержание ТГК составляет от 2 до 8%. Сухие листья и соцветия (5кг) помещают в 30л бочки из нержавеющей стали, заливают петролейным эфиром и закрывают крышкой, время от времени встряхивая. Через 24 часа экстракт переливают в другую бочку со следующими 5 кг листьев и процесс повторяется. Обычно берут 5 бочек. После прохождения экстракта через пять бочек он насыщается, затем выпаривается на роторном испарителе при 60оС и вакууме. Оставшиеся в бочках остатки растительного материала вновь заливаются петролейным эфиром, и процесс повторяется заново. Таким образом, производят многократную экстракцию каннабиноидов из растительного материала петролейным эфиром не содержащего примесей ароматических соединений.
- Полученный экстракт выпаривается под вакуумом и нагреве. После экстракции каннабиноиды очищаются методами жидкостной хроматографии используются хроматографические колонки различного диаметра. Очищенные таким образом различные фракции каннабиноидов эстерифицируются диазометаном. Затем после очищаются путем дистилляции под глубоким вакуумом. В результате получаются каннабиноиды:
- Тетрагидроканнабинол
- Каннабинодиол
- Метилканнабинолат
- Метилтетрагидроканнабинолат
- Процентный выход чистого сырья составляет примерно 45% от исходного содержания ТГК. Таким образом, в тонне чистого сырья конопли содержится тотчас после высушивания 30кг ТГК. Из него можно получить 5-8кг чистых каннабиноидов.
Нами и «ТНС Pharm» GmbH была начата разработка методики получения ТГК из каннабидиола (КБД). Необходимость разработки данной технологии связана с наличием в Шуйской долине зарослей конопли с высоким содержанием этого соединения; более простой по сравнению с ТГК процедурой очистки КБД от сопутствующих веществ путем переосаждения последней; наличием КБД в культурных сортах ненаркотической конопли.
Были взяты образцы культурной ненаркотической конопли. В них содержание каннабидиола составляло 3%. Высушивание и экстракция образцов были проведены как описано выше. СВ⑉ осаждали путем подкисления раствора, перерастворяли и несколько раз очищали путем дистилляции. Затем производили изомеризацию СВ⑉ в ∆1- ТГК. Этот процесс проводили в присутствии катализатора - солей бора в растворе метилен хлорида. Через 30минут добавляли равные количества эфира и воды. Органический слой был отделяли и промывали растворами бикарбоната натрия и сульфата натрия. После выпаривания и хроматографическую колонку с Florisil и элюировали пентаном с возрастающей концентрацией эфира. Первый компонент ∆1- ТГК был элюирован при концентрации эфира 1%, последний ∆9-ТГК при 2-4% эфира в пентане. После многократной дистилляции получали чистый ТГК. Этот метод дешевле, чем разработанный ранее, т.к. очистка ТГК от других каннабиноидов очень трудоемка и дорога. Данный метод намного проще и быстрее. Содержание ТГК составляет 99.5%. По качеству эта ТГК не отличается от той, которая реализуется через сеть аптек фирмой «ТНС Pharm» GmbH в Германии.
В течение ряда лет вся работа была сосредоточена на разработке дешевого метода получения каннабиноидов. Разработанный ранее был очень дорог, т.к. реактивы для экстракции и хроматографии в Казахстане не выпускаются. Кроме того, в большом числе публикаций было доказано, что чистый ТНС не столь терапевтически активен, как в сочетании с другими каннабиноидами. Так, только одно ТГК снимает боль в меньшей степени, чем в присутствии небольшого количества экстракта из соцветий. Фармакологическое обьяснение этого в настоящее время выясняется. Однако в некоторых случаях одноврменного применения ТНС и каннабидиола (СВ⑉) в предклинических испытаниях получаются совершенно разнонаправленные результаты. Например, в некоторых описаниях указано на модификацию психоактивного действия этих каннабиноидов позволяет понять терапевтическое действие грубых экстрактов из разных регионов мира. Обнаружено увеличение эффекта при совместном применении ТНС и СВ⑉, хотя фармакологическое действие обоих компонентов резко отличаются. Клинически доказано, что токсичность ТНС для организма выше, чем смеси ТНС и СВ⑉. Аналог ТГК тетрагидроканнабиноварин имеет более сильно выраженный терапевтический эффект, чем ТНС и CBD. Исследования этого соединения только начались, но его лечебный эффект уже запатентован Brian White[17-18]. Так как в Шуйской долине произрастает огромное количество популяций с разными комбинациями каннабиноидов, то не трудно подобрать нужные растения и создать препарат с нужным сочетанием каннабиноидов.
В основу методов были положены:
- Метод просеивания
- Ступенчатой экстракции
- Холодной экстракции с последующей хроматографией
По первому методу у растений до первых морозов брали листья с верхушек веток и стеблей. Высушивали и просеивали через сита с концентрацией ТНС около 20%. После получения от фирмы «Pollinator» установки просеивание стали вести механизировано и более производительно.
По второму методу экстракцию вели с помощью петролейного эфира, затем экстракт возгоняли. Высушивали. Концетрация ТНС составляла около 62%. В его состав входят также СВ⑉ и СВÑ - не наркотические каннабиноиды.
По третьему методу использовали физические свойства ворсинок листьев: при 0 -4о они отрываются от листа и скатываются в микроскопические шарики. Их пропускали через сита с диаметром пор 100 и 40 мк. В результате получали в экстракте 60% ТНС, 9% СВ⑉, 10% CBN, 5% CBDCOOH.
Полученный с помощью аналога этого метода самый дорогой голландский гашиш ice-o-lator содержит всего 1520% ТНС. Это связано с высоким качеством растительной «пыли», которую мы собирали (без просеивания) в Шуйской долине в конце сентября. С помощью этих простых методов мы получили 3 препарата. Разведенные растворы их были переданы для предклинических испытаний. По предварительным данным они эффективно действуют на животных и модельные системы.
Таким образом, в процессе изучения количественного и качественного состава каннабиноидов Шуйской долины нами были Разработаны 3 схемы получения фармацевтических препаратов из конопли:
- 99% препарат из ТГК. Он был получен путем многократного переосаждения и хроматографии через колонки с силикагелем экстракта из соцветий конопли.
- Препарат с содержанием 62% ТГК. В его состав входят также СВ⑉ и CBN - не наркотические каннабиноиды. Сочетание этих трех каннабиноидов дает синергический эффект. Препарат ближе к природному экстракту и получен путем многократного переосаждения экстракта из соцветий конопли. Схема его получения намного проще и дешевле первой.
- Препарат с содержанием ТГК около 60%. Получается путем осаждения ворсинок, содержащих каннабиноиды при низкой температуре и последующего фильтрования через систему сит с различными размерами пор. Эта схема наиболее простая и дешевая.
Работа с полученными препаратами возможна только в исследовательских целях. Продвижение наших медпрепаратов на рынок требуется множества согласований, что входит в противоречие с УПК Республики Казахстан. Для промышленной переработки конопли с целью реализации дешевого препарата на рынке требуется получение разрешения Правительства и ряд законодательных мер.
СПИСОК ЛИТЕРАТУРЫ
- ElSohly, M. A., Harland, E. and Waller, C.W. Cannabinoids in glaucoma II: The effect of different cannabinoids on the intraocular pressure of the rabbit // Curr. Eye Res.- 1984. - №3(6). - Р. 841-850.
- El-Mallakh, R. S. Marihuanna and migraine // Headanche. - 1987. - №27(3). - Р. 442-443.
- Volfe, Z.; Dvilansky, I. A., and Nathan, I.; Cannabinoids block release of serotonin from platelets induced by plasma from migraine patients // Int. J. Clin Pharmacol. Res. - 1985. - №5(4). - Р.243-246.
- Лазурьевский Г. В., Николаева Л. А. Каннабиноиды. - Кишинев: Штиинца, 1972. - 263 с.
- Turner C. E., M. A. Elsohly and E. G. Boeren Constituents of Cannabis sativa L. XVII. A review of the natural constituents // Journal of Natural Products. - 1980. - №43 (2). - Р. 169—234.
- Svendsen K.B., Jensen T.S., Bach F.W. Does the cannabinoid dronabinol reduce central pain in multiple sclerosis? // Randomised double blind placebo controlled crossover trial. BMJ. - 2004. - №329. - 253 р.
- Тихомиров В.Т., Барашкин В.А., Зеленина О.Н. «Перспективы и основные направления использования продуктов переработки конопли» // Сельскохозяйственная биология, 2001. - №3. - С. 225-229.
- Rodriguez de Fonseca F., Del Arco I., Bermudez-Silva F.J., Bilbao A., Cippitelli A., Navarro M. The endocannabinoid system: physiology and pharmacology // Alcohol Alcohol. - 2005. - №40(1). - Р. 13-19.
- Verwey, A. M. A.; and Witte, A. H.; A rapid method of preparation of THC by isolation of THCA from hashish // Pharm. Weekblad. - 1972. - V. 107. - P. 415-416.
- DeRopp, R. S., Chromatographic separation of the phenolic compounds of Cannabis sativa. //J. Am. Pharmacol. Assoc., Sci. -1960. - №49. - P. 756.
- Gaoni, Y., Mechoulam, R. Isolation, structure, and partial synthesis of an active constituent of hashish. //J. Am. Chem. Soc. - 1964. - №86. - Р. 1646-1647.
- Korte, F.; Sieper, H.; and Tira, S.; New results on hashish-specific constituents // Bull.Narcotics. - 1965. - №17. - P. 35-43.
- Verwey, A. M. A.; and Witte, A. H.; A rapid method of preparation of THC by isolation of THCA from hashish // Pharm. Weekblad. - 1972. - V. 107. - P. 415-416.