Вирус гриппа А, в отличие от вирусов гриппа В и С, поражает многие виды млекопитающих и птиц и отличается весьма значительной вариабельностью. Особенно вариабельными являются поверхностные гликопротеины вириона, гемагглютинин (НА) и нейраминидаза (NA). Целью настоящей работы является подбор праймеров и оптимизация условий для получения нуклеотидной последовательности гена гемагглютинина вируса гриппа птиц и его субъединиц методом полимеразной цепной реакции для дальнейшего определения его трехмерной структуры. В статье изложены результаты исследований по подбору и синтезу праймеров, включающие сайты эндонуклеазного расщепления рестриктаз
NcoI и XhoI, фланкирующие участки гена НА. Данные праймеры характеризуются довольно высокой чувствительностью, специфичностью и воспроизводимостью результатов. Синтезированные специфические праймеры использованы для амплификации гена HA и его определенных участков, а также оптимизированы условия проведения ПЦР. Результаты проведенных исследований целесообразно использовать в работах по получению рекомбинантного белка гемагглютинина вируса гриппа птиц, который будет использован для определения его трехмерной структуры.
Введение
Вирус гриппа типа А распространен повсеместно. Данным вирусом заражаются многие виды диких и домашних птиц, большое количество различных видов млекопитающих и человек. На данный момент значительную обеспокоенность вызывает распространение в мире эпизоотий высокопатогенного вируса гриппа птиц [1].
В составе генома вируса гриппа A имеются восемь генов РНК отрицательной полярности. HA и NA, которые кодируют соответственно гемагглютинин и нейраминидазу, отличаются высоким уровнем генетической изменчивости. Гемагглютинин и нейраминидаза формируют поверхностные пепломеры вириона и являются основными мишенями для противовирусных антител [2-4].
Свойства гемагглютинина привлекают самое пристальное внимание исследователей. Гемагглютинин синтезируется как единый полипептид, что в последующем подвергается протеолитическому расщеплению на две субъединицы (НА1 и НА2). В вирусной частице гемагглютинин представляет собой полимер, складывающийся из трёх мономеров, объединенных нековалентными взаимосвязями [5].
Эволюция вируса гриппа А протекает очень быстро, следовательно, первостепенной задачей исследователей является антигенное картирование гемагглютинина тех подтипов, а также выявление особенностей антигенной структуры [6].
Для определения трехмерной структуры гемагглютинина требуется получение рекомбинантного белка с высокой степенью чистоты. В молекулярных исследованиях для амплификации гена применяют метод полимеразной цепной реакции. Начальным этапом полимеразной цепной реакции является подбор специфических праймеров к целевому гену. Конструирование праймеров осуществляется с помощью биоинформационной программы «Vector NTI 10» и научной базы данных NCBI (National Center for Biotechnological Information, USA) [7].
Целью данной работы является подбор, синтез праймеров и оптимизация условий для проведения ПЦР-амплификации гена HA и его субъединиц вируса гриппа птиц для последующих работ по определению трехмерной структуры белка гемагглютинина вируса гриппа птиц типа А.
Материалы и методы
В качестве объекта исследования был выбран штамм вируса гриппа птиц А/лебедьшипун/Мангистау/3/06 (H5N1), выделенный на территории Республики Казахстан.
Конструирование праймеров. Для поиска последовательности гена HA, к которому необходимо подобрать праймеры, использовали биоинформационную базу данных NCBI. Для конструирования праймеров и оптимизации условий проведения ПЦР использовали программу «Vector NTI 10».
Конструированные праймеры синтезировали на синтезаторе олигонуклеотидов Synthesizer H-16 (производство Германия) согласно инструкции, прилагаемой к прибору. Элюирование синтезированных праймеров с колонок проводили концентрированным раствором аммиака. Затем праймеры высушивали на ротационном испарителе и очищали спиртовым переосажденим. В реакциях амплификации для наработки ПЦР продукта использовали 20 пМ концентрации праймеров.
Выделение РНК. Вирусную РНК выделяли набором «QIAprep Viral RNA kit» фирмы Qiagen.
Амплификация гена HA. Амплификацию проводили на амплификаторе фирмы Applied Biosystem GenAmp 9700.
Для постановки ПЦР использовали набор «SuperScript™ III One-Step RT-PCR System with Platinum Taq High Fidelity DNA Polymerase» (Invitrogen). Состав реакционной смеси: вода — 17,5 мкл; 2x буфер — 25,0 мкл; праймер прямой — 1,0 мкл; праймер обратный — 1,0 мкл; фермент — 0,50 мкл; РНК вируса — 5,0 мкл. Конечный объем — 50 мкл.
Амплифицированные ПЦР продукты анализировали в 1 %-ном агарозном геле с дальнейшей детекцией на трансиллюминаторе Gel Chemi Doc («Bio-Rad» США). Полученные результаты были визуализированы и зарегистрированы с помощью программы «Quantity One».
Результаты исследования и их обсуждение
Одним из основных факторов, влияющих на специфичность реакции, является правильный подбор пар праймеров, способных амплифицировать интересующий нас фрагмент ДНК. Для конструирования олигонуклеотидов необходимо наличие большого количества данных о нуклеотидных последовательностях исследуемого нами генома или фрагмента ДНК. Поиск нуклеотидной последовательности гена НА проводили на сайте NCBI с базой данных GenBank, которая в свое время регулярно проводит обмен данными с Европейской лабораторией молекулярной биологии (EMBL Nucleotide Sequence Database, Europe) и Японской базой данных ДНК (DNA Database Bank of Japan).
Проектированию праймеров предшествует предварительный этап построения подробной модели гена-мишени или иной последовательности нуклеиновой кислоты, которую планируется амплифицировать.
Изначально гемагглютинин синтезируется в виде крупномолекулярного полипептида. В ходе окончания процесса синтеза белка крупномолекулярный полипептид подвергается протеолитическому расщеплению на малую и большую субъединицы, которые в дальнейшем гликолизируются. Образовавшиеся в результате расщепления субъединицы связываются дисульфидными связями, формируя гликопептид. Наибольшее количество активных центров, которые ответственны за антигенные свойства гемагглютинина, локализованы в большой субъединице (НА1) [8, 9].
Анализ нуклеотидной последовательности гена гемагглютинина показал, что ген НА состоит из двух субъединиц и сигнального пептида. Структура гена НА представлена на рисунке 1.
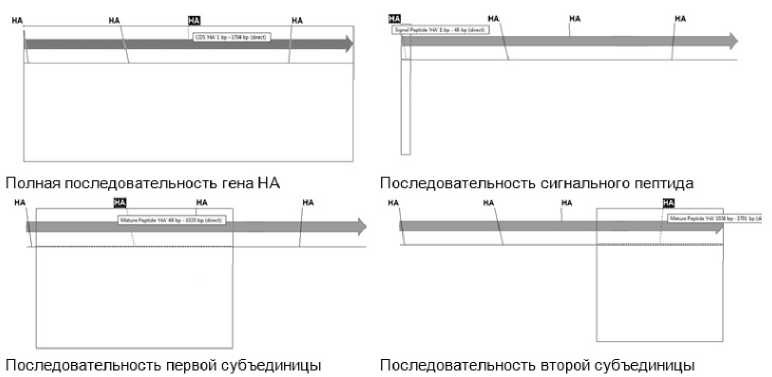
Рисунок 1. Линейная структура гена HA
Для получения нуклеотидной последовательности гена HA необходимо правильно подобрать праймеры, которые содержали бы на концах последовательность ферментов рестрикции, по которой в дальнейшем будут осуществляться вырезание гена и его лигирование с плазмидой.
Характеристика праймеров представлена в таблице 1.
Таблица 1
Последовательность синтезированных праймеров
|
№ |
Участок гена |
Название |
Последовательность |
Рестрик- таза |
Размер продукта |
|
¯т |
Полная последовательность гена HA |
Full FP NcoF |
Gtaccatggagaaaatagtgctt |
NcoI |
1695 п.о. |
|
Full RP XhoI |
Cgactcgagcgatgcaaattctg |
XhoI |
|||
|
2~ |
Последовательность первой субъединицы |
HA1 FP NcoI |
Gtgccatgggtgatcagatttgc |
NcoI |
1000 п.о. |
|
HA1 RP XhoI |
Cgtctcgagtcactctttttcttcttctttct |
XhoI |
|||
|
~ |
Последовательность первой субъединицы+ сигнальный пептид |
Full FP NcoI |
Gtaccatggagaaaatagtgctt |
NcoI |
1035 п.о. |
|
HA1 RP XhoI |
Cgtctcgagtcactctttttcttcttctttct |
XhoI |
|||
|
^4~ |
Последовательность гена HA без сигнального пептида |
HA1 FP NcoF |
Gtgccatgggtgatcagatttgc |
NcoI |
1660 п.о. |
|
HA2 RP XhoI |
Ctgctcgagtatctggtaagttcctattga |
XhoI |
Примечание. п.о. — пар оснований.
Как видно из таблицы 1, были сконструированы и синтезированы 5 праймеров, которые специфичны определенным участкам гена HA. Из 5 праймеров были созданы 4 пары комбинаций для получения полной последовательности гена НА и его субъединиц. С помощью первой пары праймеров получили полную последовательность гена HA; второй пары — последовательность первой субъединицы; третьей пары — нуклеотидную последовательность сигнального пептида и первой субъединицы; четвертой пары праймеров — последовательность первой субъединицы и второй субъединицы. Для всех 4 пар праймеров выбрали эндонуклеазы рестрикции, сайты которых отсутствуют в последовательности самого гена и присутствуют в мультиклональном участке плазмиды.
Таким образом, нами были выбраны рестриктазы NcoI для прямых праймеров и XhoI для обратных праймеров.
Для оптимизации условий ПЦР нами поставлен ряд экспериментов, в ходе которых установили оптимальный вариант проведения ПЦР с подобранными праймерами. В ходе экспериментов были подобраны температура отжига праймеров и время денатурации. Температурно-временной режим амплификации представлен в таблице 2.
Таблица 2
Температурно-временной режим ПЦР
|
Стадии ПЦР |
Температура и время |
Количество циклов |
|
Синтез кДНК |
45 ºС — 60 мин |
|
|
Денатурация |
94 ºС — 2 мин |
|
|
Денатурация 1 |
94 ºС — 20 с |
5 |
|
Отжиг 1 |
45 ºС — 30 с |
|
|
Элонгация 1 |
68 ºС — 3 мин |
|
|
Денатурация 2 |
94 ºС — 30 с |
31 |
|
Отжиг 2 |
57 ºС — 30 с |
|
|
Элонгация 2 |
68 ºС — 7 мин |
|
|
Финальная элонгация |
68 ºС — 7 мин |
|
|
Удерживание температуры |
4 ºС |
Согласно таблице 2, начальной стадией ПЦР в данном случае является синтез кДНК, так как в реакции в качестве матрицы использовали ранее выделенную РНК. Был выбран двустадийный режим амплификации. Значительно увеличено время элонгации во второй стадии амплификации по причине большого размера получаемого продукта (табл. 1).
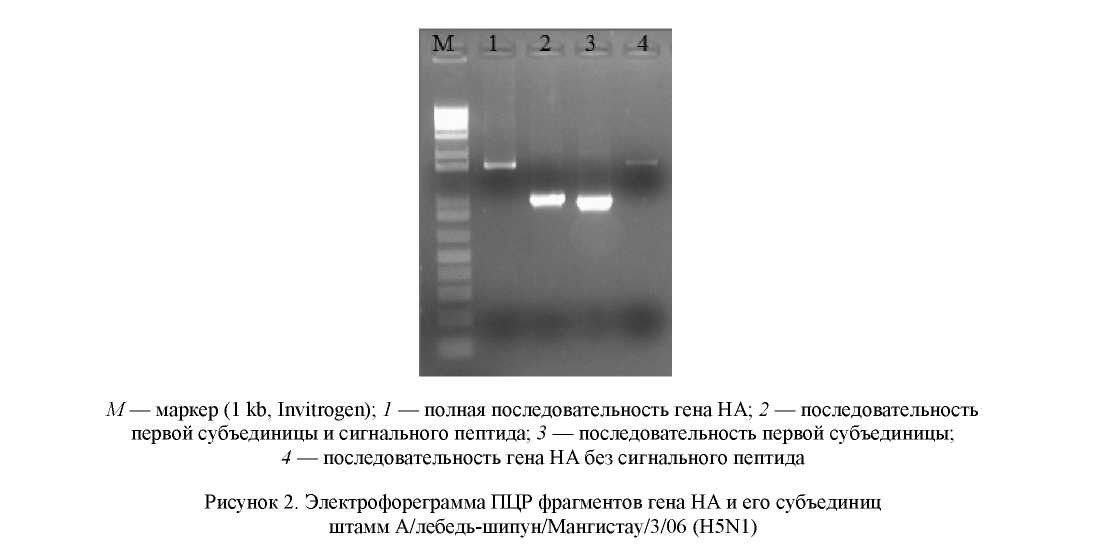
На рисунке 2 представлен электрофоретический профиль результатов ПЦР, согласно которому размеры полученных ПЦР-продуктов соответствуют своим, ранее теоретически рассчитанным размерам (табл. 1).
Наиболее важна при определении трехмерной структуры белка первоначальная наработка гена, который кодирует аминокислотную последовательность исследуемого белка. Необходимой составляющей при проведении ПЦР является конструирование праймеров, которые должны быть специфичными и обеспечивать достаточную точность реакции. Синтезированные нами праймеры отвечают всем общепринятым рекомендациям, которые используются при конструировании праймеров.
Заключение
Таким образом, в результате проведенной нами работы были синтезированы специфические праймеры для амплификации гена HA и его определенных участков, а также оптимизированы условия для проведения ПЦР. При дизайне олигонуклеотидов для наибольшей специфичности учитывали все критерии, предъявляемые праймерам для ПЦР. При помощи пакета компьютерной программы было создано 5 праймеров, которые в дальнейшем проходили апробацию. Данные праймеры характеризуются довольно высокой чувствительностью, специфичностью и воспроизводимостью результатов. Экспериментальные работы по определению состава реакционной ПЦР смеси, а также по подбору оптимальных температурно-временных параметров амплификации позволили отработать условия постановки ПЦР, при которых происходит специфическая наработка ПЦР продукта нужного размера и в достаточном количестве. Полученные праймеры в дальнейшем будут использованы в работах для получения рекомбинантного белка гемагглютинина вируса гриппа птиц, который будет использован для определения его трехмерной структуры.
Работа выполнена в рамках проекта грантового финансирования научных исследований «Изучение процесса патогенеза вируса гриппа при изменении антигенной структуры, путем трехмерного моделирования белков» (2018–2020), № AP05I32243.
Список литературы
- Сюрин В.Н. Грипп птиц / В.Н. Сюрин, Н.Г Осидзе // Малоизвестные заразные болезни животных. — М., 1973.
- Lvov D.K. Avian influenza in Northern Eurasia / D.K. Lvov, N.V. Kaverin, H.D. Klenk, M. Matrosovich, J. Steh // Monographs in Virology. — 2008. — Vol. 27. — P. 41–58.
- Каверин Н.В. Антигенная структура гемагглютинина вируса гриппа Л / Н.В. Каверин, И.Л. Руднева, Т.Л. Тимофеева, Л.В. Игнатьева // Вопросы вирусологии. — 2012. — № 1. — С. 148–158.
- Bedford T. Integrating influenza antigenic dynamics with molecular evolution / T. Bedford, M.A. Suchard, P. Lemey, G. Dudas, V. Gregory, A.J. Hay et al. // Elife. — 2014. — Vol. 3. — P. 14-19.
- Wilson I.A. Structure of the hemagglutinin membrane glycoprotein of influenza virus at 3A resolution / I.A. Wilson, J.J. Skehel, D.C. Wiley // Nature. — 1981. — Vol. 289. — P. 366-373.
- Tong S. A distinct lineage of influenza A virus from bats / Tong S., Li Y., Rivailler P., et al. // Proc. Natl. Acad. Sci. USA. — 2012. — Vol. 109. — P. 4269-4274.
- Лысенко Е.А. Молекулярно-генетические и биохимические методы в современной биологии растений: Полимеразная цепная реакция. Стратегия подбора праймеров для анализа экспрессии генов / Е.А. Лысенко; под общ. ред. Вл.В. Кузнецова, В.В. Кузнецова, Г.А. Романова. — М.: БИНОМ; Лаборатория знаний, 2011. — C. 75-96.
- Stevens J.O. Structure and receptor specificity of the hemagglutinin from an H5N1 influenza virus / J.O. Stevens, T.M. Blixt, J.K. Tumpey, et al. // Science. — 2006. — Vol. 312. — P. 404-410.
- Laver W.G. The Polypeptides of Influenza Viruses / W.G. Laver // Advances in Virus Research. — 1973. — Vol. 18. — P. 57-103.