Метод культуры изолированных панкреатических островков (ОПЖ) имеет два решающих преимущества по сравнению с опытами на животных, а именно: 1) можно исследовать характер прямого влияния исследуемых веществ на клетки тканей; 2) имеется возможность изучать влияние точно заданных концентраций исследуемых веществ на клетки исследуемой ткани. В работе представлены результаты применения изолированных ОПЖ для изучения характера прямого воздействия изучаемых веществ на ß-клетки с помощью нескольких гистологических и гистохимических методик, дополняющих друг друга. Авторами показано, что каждый из нескольких методов обладает определенными очевидными преимуществами перед другими относительно возможностей оценки состояния гистоструктуры ОПЖ, чувствительности метода и содержания инсулина в β-клетках. Выявлены также преимущества технического характера отдельных гистохимических методов при работе с ОПЖ. При получении, очистке и отборе ОПЖ авторами на основании своего опыта установлено, что окончательный отбор материала лучше производить мануально, путем ручного отбора островков при визуальном микроскопическом контроле. В процессе заливки ОПЖ в парафиновые блоки авторы предлагают технологию заливки, обеспечивающую равномерное распределение ОПЖ в процессе заливки в парафиновом блоке по его вертикали, предупреждающую их оседание на дно в виде одного-двух слоев.
Исследование состояния гистоструктуры панкреатических островков и содержания инсулина в β-клетках в опытах на модели животных позволили получить большой объем данных о механизмах развития сахарного диабета и о возможностях его предотвращения. Между тем данная модель, несмотря на наличие положительных сторон, имеет два очевидных недостатка: 1) при изучении действия тех или иных веществ на инсулиноген или 3-ю функцию β-клеток невозможно точно определить, какая концентрация исследуемого вещества, введенного в организм различными способами, достигает β-клеток и действует на них; 2) нельзя также быть уверенным в том, что введенное вещество является причиной возможных изменений β-клеток, а не продукт его метаболизации. Этих недостатков лишена модель культуры изолированных панкреатических островков, а именно: 1) она позволяет задать строго определенную концентрацию исследуемого вещества, введенного в питательную среду; 2) оценивается прямое влияние исследуемого вещества на β-клетки.
В 1967 г. R. Lacy и M. Kostianovsky [1] впервые получили культуру изолированных панкреатических островков с помощью фермента коллагеназы, расщепляющей коллагеновые волокона с последующим получением суспензии изолированных панкреатических островков.
В данном исследовании приведены результаты длительного использования гистологических методов окраски, адаптированных применительно к модели культуры изолированных панкреатических островков.
Цель исследования: адаптация технологий использования гистологических и гистохимических методов окраски инсулина в ß-клетках панкреатических островков в опытах на модели культуры изолированных панкреатических островков.
Материал и методы исследования
Опыты проведены на неонатальных крысятах 4–5-дневного возраста линии LEWIS, предоставленные виварием г. Дюссельдорфа (ФРГ) и линии Вистар. Для изоляции использована коллагеназа, любезно предоставленная фирмами «BoehringerMannheim» (ФРГ), «FLUKA» (Швейцария), «SERVA» (ФРГ), «SIGMA» (США). Изоляцию проводили по методике R. Lacy и M. Kostianovsky [1], усовершенствованной сотрудниками Института Диабета «Герхардт Катч» (г. Карлсбург, ФРГ) и адаптированной нами к применению высокоспецифичных методов окраски инсулина в β -клетках.
Методика изоляции. Поджелудочные железы неонатальных крысят помещали во флакон с притертой пробкой, добавляли 2 %-ный раствор коллагеназы, приготовленный на растворе Hanks и встряхивали 3 мин на водяной бане при температуре +37 ºС. Затем после оседания крупных фрагментов ткани железы, не подвергшейся дезагрегации (около 25–30 с), отсасывали раствор Hanks, содержащий изолированные островки вместе с обрывками экзокринной ткани и помещали его в колбу с охлажденным Hanks объемом 50–60 мл. Оставшуюся в осадке ткань поджелудочной железы вновь заливали теплым раствором коллагеназы и дезагрегацию повторяли еще 2 раза по 3 мин, каждый раз сливая содержащий островки раствор Hanks в колбу. Накопившийся материал четырежды промывали в свежих порциях раствора Hanks и центрифугировали в течение 2 мин при 400 об/мин, после чего разделяли в градиенте плотности декстрана («SERVA», ФРГ) или фиколла («Pharmacia Fine Chemicals», Швеция) или же проводили ручной отбор островков. Островки при этом располагались на уровне, соответствующем плотности раствора, равном 1,060–1,065, откуда их извлекали и 4 раза промывали в холодном растворе Hanks. Окончательный отбор островков проводили вручную под стереомикроскопом, после чего их повторно промывали в растворе Hanks.
Процедура отбора и очистки считалась завершенной после того, как под микроскопом в растворе Hanks обнаруживались только очищенные островки без примесей в виде групп клеток экзокринной ткани и обрывков соединительнотканных волокон. Каждый пул, полученный от 4 крысят, составлял 530-712 островков. Для оценки состояния ОПЖ и содержания в ß-клетках инсулина изолированные островки после предварительного культивирования в питательной среде RPMI-1640 («SERVA», ФРГ) с добавлением 5 %-ной эмбриональной сыворотки и 5,5 мМ глюкозы фиксировали 1 ч в жидкости Буэна, обезвоживали в спиртах возрастающей крепости и заливали в парафин. Срезы толщиной 4 мкм окрашивали альдегидфуксином [2] (Avocado Chemical Company, США), а также на инсулин с помощью высокоспецифичного псевдоизоцианинового метода («SERVA», ФРГ) [3–5] метода с использованием реактива «Виктория 4R» (диметилнафтилметан, цв. инлекс 42563, «FERAK» ФРГ, «MERCK», ФРГ) в комплексе с флоксином, фосфорвольфрамовой кислотой и светлым зеленым по методу F. Wohlrab и соавторов [6] в нашей модификации [7]. Гранулы инсулина в цитоплазме β-клеток окрашиваются в темно-синий цвет. Метод является строго специфичным в отношении выявления инсулина.
Содержание инсулина в β-клетках определяли путем количественной оценки интенсивности флюоресценции или светопоглощения в окрашенных на инсулин препаратах, которые исследовали в светооптическом и люминесцентном микроскопе при длине волны возбуждающего света, равной 350-370 нм и в светооптическом микроскопе. Содержание инсулина в β-клетках определяли фотометрически в относительных единицах [8].
Обнаруженные в препаратах островки были подразделены на 2 группы: 1) неповрежденные; 2) поврежденные со сниженным содержанием инсулина. Их количество подсчитывалось и выражалось в процентном отношении к общему числу ОПЖ.
Иммуногистохимическое выявление инсулина в β-клетках проводили с помощью строго специфичных в отношении инсулина антител иммуно-гистохимическим методом. Для исследования использованы стандартные наборы антител производства фирмы «DAKO» (Дания). Окрашенный этим методом инсулин в β-клетках приобретает темно-коричневый цвет. Данный метод является абсолютно специфичным в отношении выявления инсулина в β-клетках.
Из всех известных методов выявления инсулина наиболее чувствительными являются люминесцентные методы, позволяющие выявлять ничтожные количества гормона. Известно, что и их помощью выявляются различные металлы, содержание которых не превышает 10-7-10-8. Для люминесцентного выявления инсулина нами был использован высокочувствительный и строго специфичный псевдоизоцианиновый люминесцентный метод по T.H. Schiebler и S. Schiessler [3], Coalson [4] в нашей модификации [5]. Гистохимическая псевдоизоцианиновая реакция основана на взаимодействии в ß-клетках Ñ‚Ñ-диэтилпсевдоизоцианина хлорида с А-цепью молекулы инсулина. Образующийся комплекс люми- несцирует ярко-красным светом при исследовании в ультрафиолетовых лучах люминесцентного микроскопа при длине волны возбуждающего света, равной 350–370 нм. С этой целью использован светофильтр УФС-1. В отраженном ультрафиолетовом свете β-клетки, окрашенные псевдоизоцианином, ярко люминесцируют оранжевым цветом на фоне неокрашенной темной экзокринной ткани.
Для количественной оценки содержания депонированного инсулина в β-клетках окрашенных псевдоизоцианином и иммуногистохимическим методом препаратов использовали измерение интенсивности свечения или степени светопоглощения, для чего использовали микрофлюориметрическое устройство [8] на базе ФЭУ-31, совмещенного через микрофотонасадку с люминесцентным или светооптическим микроскопом. Оценка содержания инсулина в панкреатических островках проводилась в относительных единицах (о.е.) по величине показателя флюоресценции К и показателя светопогло- щения К2, определенных по формулам: К = Ф1/Ф2, где Ф1 — величина фототока, возникшего при возбуждении люминесценции флюоресцирующим инсулином в β-клетках (в мкА) и Ф2 — величина фототока, возникшего при возбуждении слабой люминесценции в экзокринной ткани. Расчет содержания инсулина производился на основе прямой зависимости: чем интенсивнее флюоресценция — тем больше света пропускается на фотометр и тем выше содержание инсулина. При использовании аль- дегидфуксинового метода, наоборот, оценивали по формуле с обратной зависимостью (К2 = А2/А1, где Аɪ — интенсивное светопоглощение β-клетками, содержащими инсулин и А2 — слабое светопогло- щение клетками экзокринной ткани, не содержащими инсулин). То есть, чем плотнее окраска — тем больше света поглощается фотометром, соответственно тем меньше величина фототока и тем выше содержание инсулина. Полученные цифровые данные обрабатывали статистически с использованием /-критерия Стьюдента.
Результаты
Анализ процедуры отбора островков при подготовке суспензии к фиксации дал следующие результаты. Разделение в градиенте плотности и последующий отбор островков для фиксации выявил наличие 9,7±2,3 % с внешними признаками повреждений, тогда как мануальный отбор под микроскопом позволил снизить их количество до 2,6±0,4 %, т.е. практически исключить их попадание в исследуемый материал, снизив, таким образом возможность ошибочной оценки при изучении влияния того или иного вещества на состояние гистоструктуры панкреатических островков.
Результаты окраски срезов островков позволили выявить следующую картину. В окрашенных альдегидфуксином препаратах поджелудочной железы интактных животных насыщенная фиолетовая окраска свидетельствует о наличии значительных количеств депонированной формы инсулина в цитоплазме β-клеток соответственно наблюдаемой при исследовании панкреатических островков на модели культуры ткани поджелудочной железы (рис. ɪ.ɪ, ɪ.3, ɪ.5, ɪ.7). В островках, инкубированных в течение ɪ5 мин в питательной среде, содержавшей 3,5 мг/мл (30 мг/ɪ00 мл) раствора дитизона, наблюдались островки, подвергшиеся значительным изменениям: в поле зрения выявлены островки 70-80 % площади которых на срезах подверглась некрозу и деструкции; инсулин в β-клетках практически отсутствовал (рис. ɪ.2, ɪ.4, ɪ.6, ɪ.8). Подобная картина обнаружена нами в 20 из 22 исследованных островках (90 %). Похожая картина выявлена при исследовании окрашенных иммуногистохимическим, псевдоизоцианиновым и Виктория-4 методами.
Особенности подготовки культуры изолированных панкреатических островков к приготовлению гистологических срезов
Исследование состояния гистоструктуры панкреатических островков с использованием модели культуры изолированных панкреатических островков предъявляет несколько иные условия при подготовке суспензии фиксированных изолированных панкреатических островков. Особенности эти следующие:
ɪ. Отбор изолированных островков. Необходимо помнить о том, что даже при самой щадящей процедуре изоляции островков, не предусматривающей предварительное иссечение ткани поджелудочной железы, около ɪ0 % полученного пула имеют те или иные механические повреждения. В случае применения градиента плотности (декстран, фиколл), используемого при необходимости получения большого количества островков (для экспериментальной трансплантации) какое-то их количество попадает в общее число подготавливаемого материала. Нами был применен ручной метод визуального отбора островков из полученной суспензии при небольших увеличениях микроскопа, что позволило практически исключить попадание поврежденных островков и примесей в исследуемый материал.
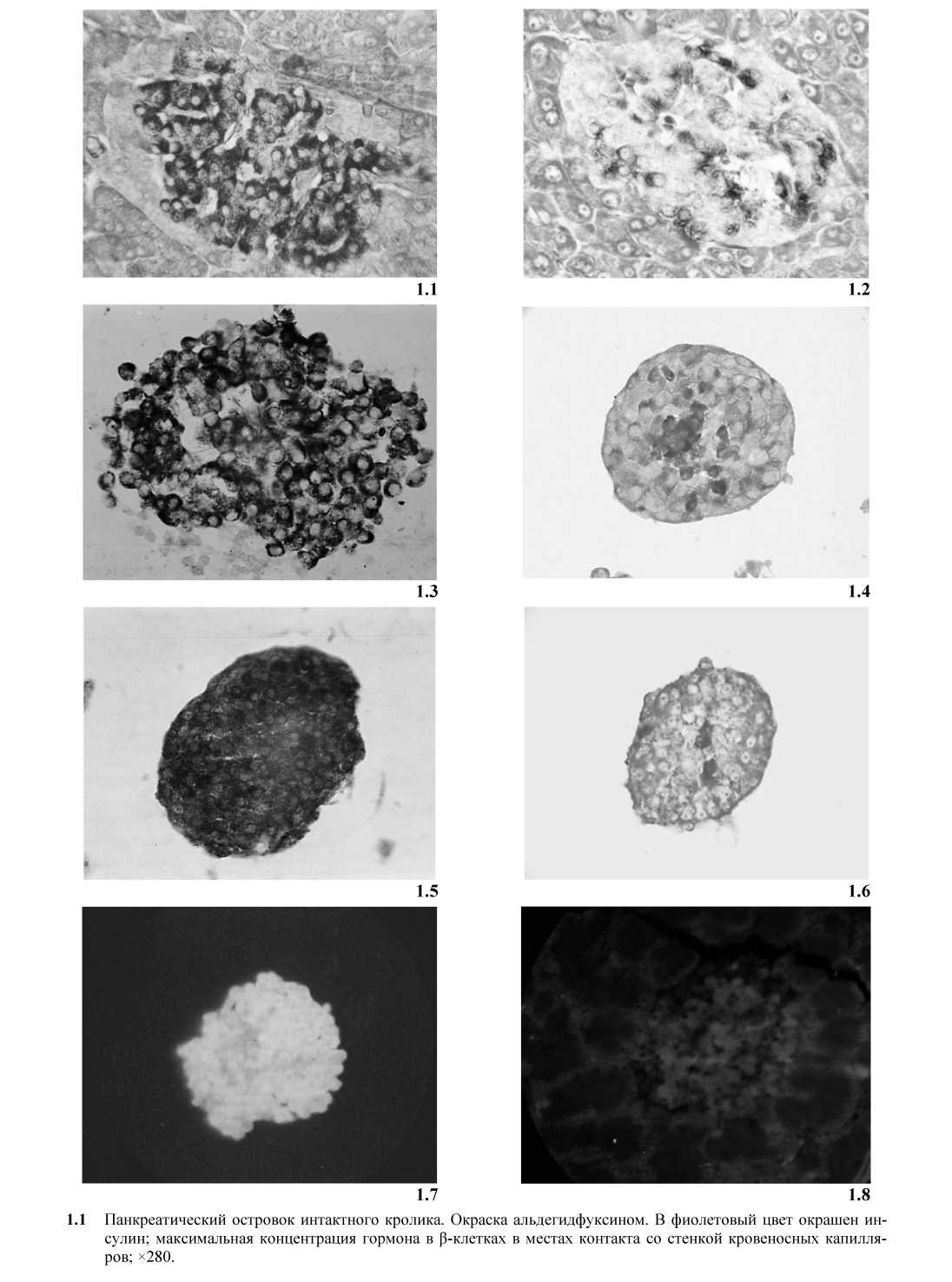
- Панкреатический островок кролика с дитизоновым диабетом. Окраска альдегидфуксином; деструкция и резкое снижение содержания инсулина в большинстве ß-клеток; ×280.
- Изолированный интактный панкреатический островок. Окраска альдегидфуксином. В фиолетовый цвет окрашен инсулин; ×280.
- Изолированный панкреатический островок после воздействия дитизона, 5 мг/100 мл. Окраска альдегидфукси- ном. Деструкция и резкое снижение содержания инсулина в большинстве ß-клеток центральной части островка; ×280.
- Изолированный интактный панкреатический островок. Окраска реактивом Виктория 4R. В темно-синий цвет окрашен инсулин; ×280.
- Изолированный панкреатический островок после воздействия дитизона, 5 мг/100 мл. Окраска реактивом Виктория 4R. Деструкция и резкое снижение содержания инсулина в большинстве β-клеток центральной части островка; ×280.
- Изолированный интактный панкреатический островок. Окраска диэтилпсевдоизоцианином. Ярко-красная флюоресценция А-цепи инсулина; ×140.
- Изолированный панкреатический островок после воздействия дитизона, 5 мг/100 мл. Окраска диэтилпсевдоизоцианином. Резкое снижение содержания инсулина в β-клетках (ослабленная флюоресценция β-клеток); ×140.
Рисунок. Г истоструктура и содержание инсулина в β-клетках ткани поджелудочной железы и изолированных панкреатических островков в норме и при повреждении их дитизоном
- При заливке изолированных островков в парафин необходимо принять меры к тому, чтобы островки распределились по возможности равномерно по вертикали блока, избегая возможности оседания их на дно в виде одного-двух тонких слоев. Из использованных нами нескольких способов лучшие результаты дает следующий метод: отмытые в растворе Хенкса островки помещаются в пробирку для оседания на 15–30 мин, после чего осторожно набирают в шприц объемом 2 мл, содержащий 1–1,5 мл питательной среды 199; опускают вертикально иглу шприца в емкость, содержащую нагретый парафин, не доходя до дна 0,4–0,5 см; далее, постепенно поднимая вертикально вверх шприц, медленно выпускают взвесь островков, заканчивая процесс не доходя 0,5 см до поверхности; наиболее приемлемая высота парафинового блока — 1,5 см. В течение всего времени введения суспензии островков в пробирку она должна находиться на водяной бане при температуре +56 ºС и только по окончании данной процедуры пробирка извлекается с тем, чтобы парафин затвердел.
- После фиксации в жидкости Буэна изолированные островки не подвергаются, в отличие от кусочков ткани поджелудочной железы, обезвоживанию в спиртах возрастающей крепости.
- В отличие от ткани поджелудочной железы, образцы которой должны фиксироваться в жидкости Буэна в течение 24 ч, для фиксации изолированных островков требуется 30–45 мин.
- Депарафинизация срезов в ксилоле требует сокращенного времени — не более 10 с в каждой из двух порций ксилола.
- При приготовлении срезов необходимо менять лезвия после получения 50–60 срезов, так как фиксированные островки менее прочно закреплены в парафине, как это имеет место при работе с тканью железы и могут поэтому выпадать из парафина. Необходимо при окраске гистохимическими методами выявления инсулина строго следить за тем, чтобы при приготовлении срезы контрольных и опытных животных имели одинаковую толщину. Разница в 1 мкм может исказить на 15–20 % результаты определения содержания инсулина в пользу более толстых срезов.
Выводы
- Усовершенствована технология заливки изолированных панкреатических островков, обеспечивающая их равномерное распределение по вертикали парафинового блока.
- Установлены оптимальные сроки фиксации изолированных островков, обеспечивающие хорошее качество фиксации.
- Установлено, что ручной отбор материала в сочетании с визуальным контролем под микроскопом обеспечивает сведение к минимуму возможности попадания островков, поврежденных при проведении процедуры изоляции.
- Высокоспецифичные гистохимические методы окраски инсулина в β-клетках адаптированы к окраске срезов изолированных островков с получением качественных результатов (иммуногистохимический, псевдоизоцианиновый, Виктория-4 и альдегидфуксиновый). Нами не выявлена визуальная разница при окраске всеми методами изолированных островков между материалом животных линий LEWIS и Вистар.
Список литературы
- Lacy R.E. Method for the isolation of intact islets of Langerhans from the rats pancreas / R.E. Lacy, M. Kostianovsky // Diabetes. — 1967. — Vol. 16, No. 1. — P. 35–39.
- Kvistberg D. Staining of Insulin with Aldehyde fuchsin / D. Kvistberg, G. Lester, A. Lasarov // Journal Histochem. and Cytochem. — 1966. —Vol. 14. — P. 609–611.
- Schiebler T.H. Uberden Nachweis von Insulin mitden metachromatisch reagie- renden Pseudoisocyaninen / T.H. Schiebler, S. Schiessler // Histochemie. — 1959. — Vol. 1. — P. 445–465.
- Coalson R.E. Pseudoisocyanin staining of insulin and specifity of emperical islet cell stain / R.E. Coalson // Stain Technol. — 1966. — No. 2. — P. 121–129.
- Meyramov G.G. Fluorescent Histochemical method Staining of Insulin in B-cells of Isolated Pancreatic islets by Diethylpseudoisocyanine Chloride / G.G. Meyramov, A.A. Kikimbaeva, A.G. Meyramova // ACTA DIABETOLOGICA, the International Diabetes Journal. — SPRINGER. — 2005. —Vol. 42, No. 1. — P. 66.
- Wohlrab F. On the specifity of the Insulin staining by Victoria Blue 4R / F. Wohlrab, H. Dorsche, I. Krautschick, S. Schmidt // Histochem. J. — 1985. — Vol. 17. — P. 515–518.
- Meyramov G.G. Victoria 4R Method Staining of Insulin in B-cells of Isolated Pancreatic Islets / G.G. Meyramov, A.A. Kikimbaeva, A.G. Meyramova// ACTA DIABETOLOGICA, the International Diabetes Journal. — SPRINGER. — 2003. — Vol. 40, № 4. — P. 208.
- Мейрамов Г. Г. Гистофлюориметрический метод оценки содержания инсулина в В-клетках поджелудочной железы / Г.Г. Мейрамов, Г.Т. Тусупбекова, А.Г. Мейрамова // Проблемы эндокринологии. — 1987. — Т. 33, № 6. — С. 49–51.