В статье изучена зависимость количественного выхода бетулина из березы киргизской от продолжительности экстракции и концентрации водного раствора щелочи; синтез на основе выделенного бетулина нового фосфорилированного производного; определение с помощью компьютерного прогнозирования биологической активности полученного соединения. Для того, чтобы проследить зависимость выхода бетулина от времени и концентрации раствора щелочи, был проведен ряд опытов. Для этого бересту измельчали и сушили до постоянного веса. Для экспериментов брали одинаковое количество бересты, используя для экстракции бутиловый спирт и щелочь различной концентрации. Для разной серии опытов продолжительность экстракции составляла 2, 3 и 4 ч соответственно. Были получены экспериментальные данные о выходе бетулина в зависимости от времени и концентрации раствора щелочи. Температура плавления выделенного вещества составляла 243 ºС. Бетулин идентифицировали с помощью тонкослойной хроматографии и сравнивали со стандартным образцом. Вещество анализировали методами инфракрасной спектроскопии в таблетках KBr и высокоэффективной жидкостной хроматографии. В Фурье-спектрометре ФСМ-1201 с помощью характеристических частот полос поглощения было определено наличие в молекуле различных групп атомов и связей, характерных для бетулина. Хроматографическое исследование образца проводилось с помощью газового хроматографа Agilent 7890А с масс-селективном детектором 5975 inert XL. Проведена реакция фосфорилирования бетулина. Проведен физико-химический анализ синтезированного соединения. С помощью компьютерной программы PASS проведено компьютерное прогнозирование его биологической активности.
Введение
Изучив научную литературу, посвященную выделению бетулина из различных видов берез, таких как Betula pubescenz, Betula pendula, Betula alba и другие, авторы пришли к следующему выводу, что работы по изучению химического состава березы киргизской (Betula kirghisorum), эндемичного растения флоры Казахстана, не проводились. В данной работе мы преследовали следующие цели: 1) исследовать зависимость количественного выхода бетулина из березы киргизской от продолжительности экстракции и концентрации водного раствора щелочи; 2) получить на основе выделенного бетулина новые фосфорсодержащие производные; 3) определить с помощью компьютерного прогнозирования биологическую активность полученных соединений.
Новые результаты, полученные в настоящем исследовании, представляют собой несомненный научный и практический интерес.
Береза киргизская произрастает на сравнительно небольшой территории Республики Казахстан. По литературным данным, она встречается на территории Наурзумского государственного природного заповедника и Каркаралинского государственного национального природного парка [1, 2]. Она является эндемичным растением.
Ранее нами был получен из березы киргизской бетулин, который был идентифицирован с помощью ИК-спектроскопии и по данным ВЭЖХ.
В последнее время наблюдается неуклонно растущий интерес к бетулину и его производным, обусловленный широким спектром биологической активности этих соединений [3, 4]. Доказано, что бетулин и ряд его производных обладают антиоксидантными, противовоспалительными, антисептическими, гепатопротекторными свойствами [5, 6], также производные бетулина проявляют анти-ВИЧактивность [7, 8]. На основе бетулина синтезированы перспективные фармацевтические препараты с противоопухолевой и антивирусной активностью.
Экспериментальная часть и обсуждение результатов
Экстракцию Betula kirghisorum проводили по известной методике [9]. В исследовании использовали внешнюю часть коры березы (бересту). Бересту измельчали до частиц размером 5–8 мм, сушили при 100 ºС до постоянного веса. Далее проводили 3 серии экспериментов.
Первая серия: в четыре одинаковые колбы объемом 500 мл помещали по 10 г высушенной, измельченной бересты, затем в первую колбу прилили 15 %-ный раствор гидроксида натрия и 250 мл бутанола, во вторую колбу 20 %-ный раствор гидроксида натрия и 250 мл бутанола, в третью — 25 %-ный раствор гидроксида натрия и 250 мл бутанола, в четвертую — 30 %-ный раствор гидроксида натрия и 250 мл бутанола. Каждую колбу снабдили обратным холодильником и мешалкой, кипятили в течение 2 ч. Затем, после прекращения кипения, реакционная масса расслаивалась на два слоя: верхний слой — раствор бетулина в бутаноле, нижний слой представлял собой темно-коричневую вязкую массу гидрогенизированной бересты. Далее, отделив верхнюю часть, ее упаривали досуха на роторном испарителе. К остатку приливали воду. Затем отфильтровывали, остаток на фильтре промывали дистиллированной водой до нейтральной среды и высушивали.
Вторая серия экспериментов была проведена аналогично, однако время экстракции увеличили до 3 ч. В третьей серии экспериментов время экстракции составляло 4 ч.
Выход бетулина, выделенного из бересты, гидролизованной в водном растворе гидроксида натрия, в зависимости от концентрации щелочи и продолжительности гидролиза в присутствии бутанола, приведен в таблице 1.
Таблица 1
Данные о выходе бетулина, экстрагируемого бутанолом из бересты березы киргизской, гидролизованной в присутствии гидроксида натрия
|
Концентрация NaOH, % |
Длительность гидролиза бересты бутанолом, ч |
||
|
2 |
3 |
4 |
|
|
Выход бетулина при экстракции бутанолом, % от аб.с.б. |
|||
|
15 |
2,9 |
4,9 |
2,5 |
|
22 |
6,5 |
10,9 |
5,9 |
|
25 |
5,9 |
7,6 |
5,5 |
|
30 |
3,9 |
5,2 |
2,7 |
Как видно из данных таблицы 1, максимальный выход бетулина наблюдается при гидролизе бересты в 20 %-ном растворе щелочи в течение 3 ч.
Все образцы бетулина, извлекаемые бутанолом из бересты, гидролизованной в присутствии гидроксида натрия после перекристаллизации из этанола, представляют собой порошки белого цвета с температурой плавления 243 ºС.
Полученные вещества идентифицировали с помощью тонкослойной хроматографии (ТСХ) на пластинах Silufol с использованием элюирующих систем: бензол : хлористый метилен : этиловый спирт = 5:5:1. Детектирование пятен осуществляли 10%-ным раствором фосфорномолибденовой кислоты с последующим нагреванием пластины в течение 3–4 мин. Вещества сравнивали с образцом бетулина, предоставленного сотрудниками лаборатории органического синтеза Томского государственного университета. Хроматограмма показала, что образец и исследуемое вещество идентичны. Далее полученное нами вещество анализировали с помощью ИК-спектрокопии и высокоэффективной жидкостной хроматографии.
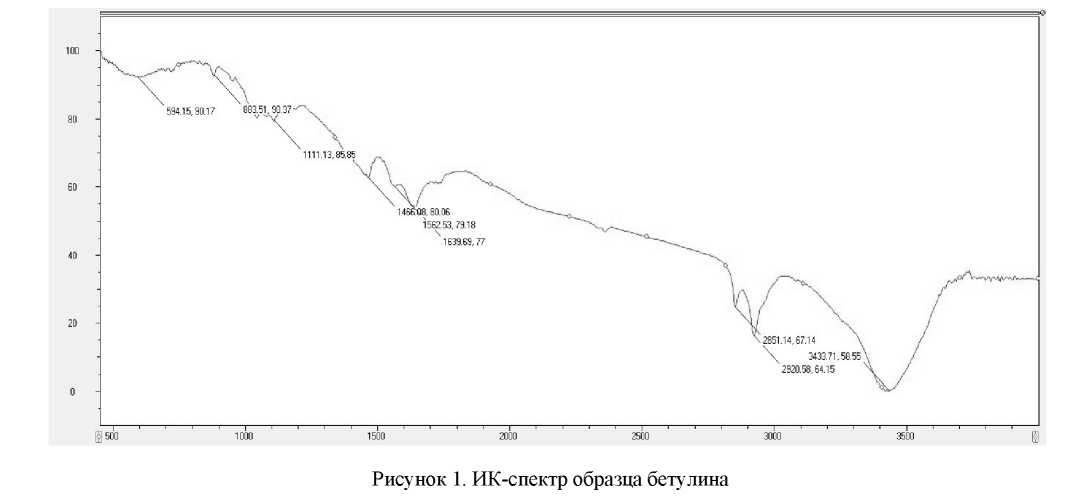
Регистрацию ИК-спектров проводили на Фурье-спектрометре марки ФСМ–1201, в диапазоне длин волн 500–4000 см-1 в таблетках бромида калия (рис. 1).
С помощью характеристических частот полос поглощения было определено наличие в молекуле различных групп атомов и связей, характерных для молекулы бетулина (рис. 1). Были идентифицированы полосы поглощения, характерные для следующих групп атомов: имеется широкая полоса поглощения, принадлежащая валентным колебаниям гидроксильных групп, при 3433 см–1; валентные колебания, характерные для С–Н групп лупанового скелета, при 2920 и 2851 см–1; валентные колебания двойной связи С=С при 1639 см –1; деформационные колебания СН2 групп наблюдаются при 1466 см-1; валентные колебания С–О группы наблюдаются при 1111 см–1; деформационные колебания СН3 групп — при 883 см–1. Сравнение ИК-спектра полученных образцов с ИК-спектрами, приведенными в различных источниках, позволяет сделать заключение, что полученные нами образцы — бетулин.
Следующая часть работа посвящена разработке методов синтеза на основе природного тритерпеноида бетулина новых биологически активных фосфорсодержащих производных. Преимуществами фосфорсодержащих производных бетулина являются высокая растворимость в воде, высокая биодоступность и благоприятная биотрансформация в организме человека и животных [10].
Синтез фосфорилированных производных бетулина проводили по следующей методике: в двухгорлую колбу, снабженную мешалкой и обратным холодильником, поместили 0,8 г (0,01 М) бетулина, 1,6 г (0,01 М) триэтиламина и при нагревании растворили в 40 мл бензола. В эту смесь добавили 0,6 мл (0,01 М) диметилхлорфосфата. Реакцию проводили при температуре 75 ºС в течение 6 ч при непрерывном перемешивании. После упаривания растворителя выпал осадок белого цвета. Присоединение фосфорсодержащего фрагмента к молекуле бетулина происходит по следующей схеме:
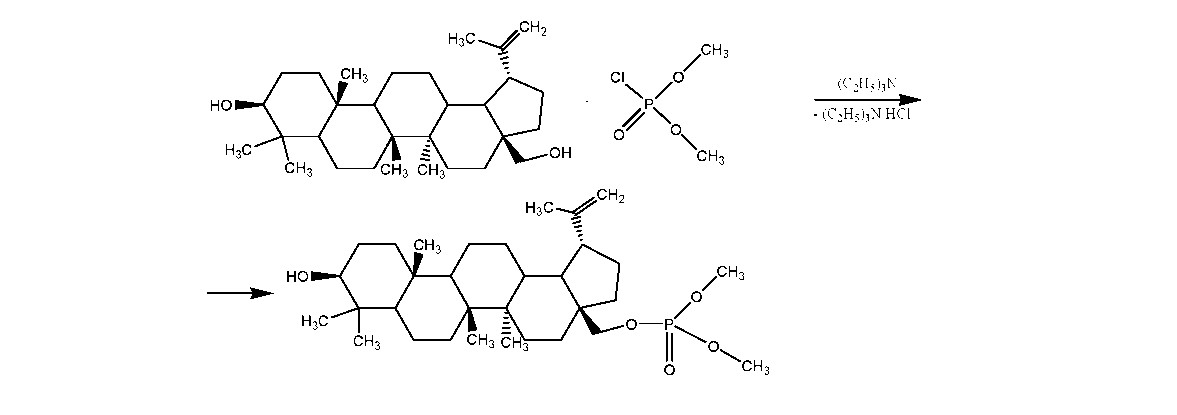
Ход реакции контролировали с помощью тонкослойной хроматографии. Полученное вещество анализировали методами ИК-спектроскопии (рис. 2). По данным ИК-спектроскопии, наряду с полосами поглощения, характерных для бетулинового фрагмента, были идентифицированы полосы поглощения, характерные для групп Р-О-СНз при 1195 см-1 и P=O при 1280 см-1.
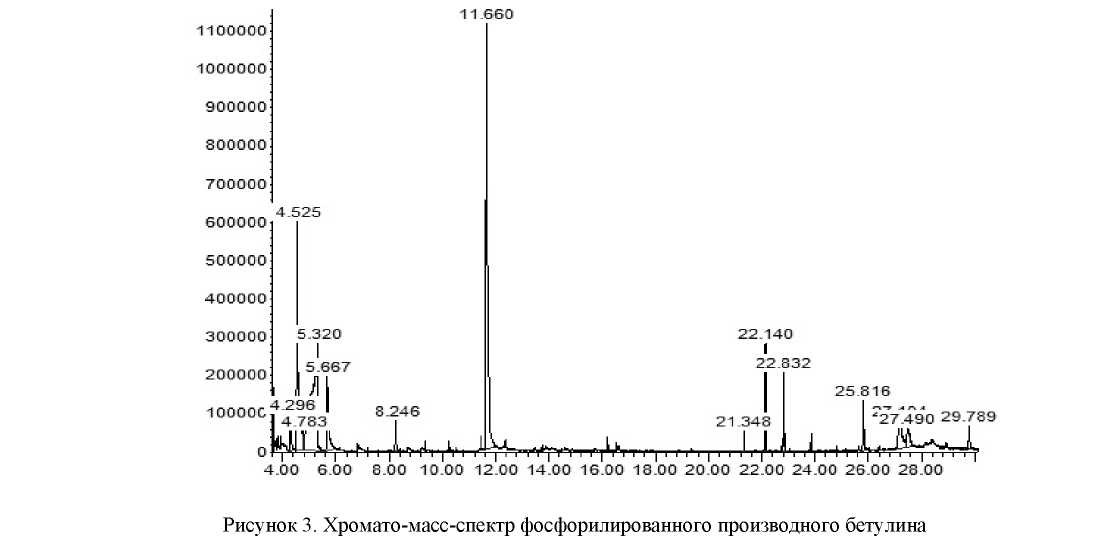
Для хроматографического исследования продукта использовался газовой хроматограф Agilent 7890А с масс-селективном детектором 5975 inert XL. По данным хроматографического анализа также выявлено наличие фосфорного фрагмента в полученном веществе (рис. 3).
Таким образом, по данным ИКи хромато-масс-спектроскопии установлено, что реакция присоединения фосфатных групп к молекуле бетулина происходит в положении С-28.
Синтезированное фосфорилированное производное бетулина проанализировали с помощью компьютерной программы PASS (Prediction of Activity Spectra for Substances) — прогноз спектров биологической активности органических соединений, основанной на анализе взаимосвязей «структура активность» с использованием обучающей выборки, содержащей большое количество разнородных химических соединений с различными видами биологической активности (табл. 2). Использование PASS

позволяет уже на ранних стадиях исследования отобрать из возможных веществ те, которые могут обладать желательными видами биологической активности [11].
Таблица 2
Прогноз спектров биологической активности фосфорилированного производного бетулина
|
Ра |
Pi |
ʌктивность |
|
0,92 |
0,001 |
Транскрипционный фактор NF-κB |
|
0,92 |
0,001 |
Стимулятор транскрипционного фактора |
|
0,89 |
0,005 |
Противоопухолевая |
|
0,85 |
0,004 |
Антипротозойная (лейшмания) |
|
0,83 |
0,004 |
Каспаза 3 стимулятор |
|
0,82 |
0,004 |
Г епатопротекторная |
|
0,79 |
0,002 |
Каспаза 8 стимулятор |
|
0,78 |
0,004 |
Противоопухолевые препараты (меланома) |
|
0,77 |
0,035 |
Ингибитор CDP-глицерол-глицерофосфотрансферазы |
|
0,73 |
0,005 |
Противоопухолевые препараты (рак легких) |
|
0,73 |
0,013 |
Иммунодепрессант |
|
0,73 |
0,012 |
Агонист апоптоза |
|
0,72 |
0,009 |
Ингибитор фосфатазы |
|
0,68 |
0,005 |
Противоопухолевый (колоректальный рак) |
|
0,70 |
0,027 |
Маннотетраозный ингибитор 2-альфа-Ñ-ацетилглюкозаминилтрансферазы |
|
0,67 |
0,006 |
Противоопухолевый (рак толстой кишки) |
|
0,66 |
0,006 |
Ингибитор экспрессии AR |
|
0,65 |
0,005 |
Лечение заболеваний печени |
|
0,64 |
0,004 |
Противоопухолевая (рак яичников) |
|
0,63 |
0,009 |
Ингибитор бета-глюкуронидазы |
|
0,68 |
0,052 |
Противоэкземная |
Таким образом, судя по компьютерному прогнозированию, от синтезированного нами фосфорилированного производного бетулина с большей долей вероятности можно ожидать следующие виды активности: 1) транскрипционный фактор NF-κB (ядерный фактор «каппа-би» — универсальный фактор транскрипции, контролирующий экспрессию генов иммунного ответа, апоптоза и клеточного цикла. Нарушение регуляции NF-κB вызывает воспаление, артроз, артрит, а также развитие вирусных инфекций и рака; 2) антипротозойную активность; 3) гепатопротекторную активность и т.д.
Выводы
Впервые проведено исследование зависимости количественного выхода бетулина из березы киргизской от продолжительности экстракции и концентрации водного раствора щелочи. Выделение бетулина осуществлялось методом экстракции из бутилового спирта, гидролизованного в водном растворе щелочи. Бетулин идентифицировали методом ТСХ на пластинах Silufol и анализировали с использованием методов ИК-спектрокопии, газовой хроматографии. В качестве стандарта использовался образец, предоставленный учеными Томского государственного университета РФ. С помощью характеристических частот поглощения в ИК-спектре было определено наличие в соединении различных групп атомов и связей, характерных для молекулы бетулина.
Впервые синтезировано фосфорилированное производное бетулина, а также установлено, что реакция присоединения фосфатной группы к молекуле бетулина происходит в положении С –28.
С помощью компьютерной программы PASS проведено компьютерное прогнозирование биологической активности синтезированного производного бетулина.
Список литературы
- Сайт Каркаралинского государственного национального природного парка. [Электронный ресурс]. — Режим доступа: https://karkaralinsk-park.ru
- Сайт Наурзумского государственного заповедника. [Электронный ресурс]. — Режим доступа: https:// www.old.unesco.kz
- Кислицын А.Н. Экстрактивные вещества бересты: выделение, состав, свойства, применение / А.Н. Кислицын // Химия древесины. — 1994. — № 3. — С. 3–28.
- Толстиков Г.А. Бетулин и его производные. Химия и биологическая активность / Г.А. Толстиков, О.Б. Флехтер, Э.Э. Шульц и др. // Химия в интересах устойчивого развития. — 2005. — № 13. — С. 1–13.
- Matsuda H. Hepatoprotective, superoxide scavenging and antioxidative activities of aromatic constituens from the bark of Betula platyphylla var. japonica / H. Matsuda, A. Ishikado, N. Nishida // Bioorganic & Medicinal Chemistry Letter. — 1998. — Vol. 8. P. 2939–2944.
- Urban M. Synthesis of A-Seco Derivatives of Betulinic Asid with Cytotoxic Activity / M. Urban // Journal of Natural Products. 2004. — Vol. 67. — P. 1100–1105.
- Кузнецова С.А. Изучение состава этанольного экстракта березы и его токсико-фармакологических свойств / С.А. Кузнецова, Г.П. Скворцова, Г.С. Калачева, И.А. Зайбель, О.В. Ханчич // Химия растительного сырья. — 2010. — № 1. — С. 137– 141.
- Evers M. Betulinic acid derivatives: A new class of human immunodeficiency virus type 1 specific inhibitors with a new mode of action / M. Evers, C.F. Poujade, Soler et al. // J. Med. Chem. — 1996. — Vol. 39. — P. 1056–1068.
- Левданский В.А. Экстракция бетулина алифатическими спиртами С3–С4 из бересты березы, гидролизованной в водном растворе щелочи / В.А. Левданский, А.В. Левданский // Химия растительного сырья. — 2014. — № 1. — С. 131–137.
- Толстиков И.Г. Терпеноиды ряда лупана — биологическая активность и фармакологические перспективы / И.Г. Толстиков, И.В. Сорокина, Г.А. Толстиков и др. // Биоорганическая химия. — 2006. — № 1. — С. 42–55.
- Филимонов Д.А. Прогноз спектра биологической активности органических соединений / Д.А. Филимонов, В.В. Поройков // Журн. Рос. хим. общ-ва им. Д.И. Менделеева. — 2006. — № 2.