В последние годы наблюдается заметное распространение особо опасных инфекционных болезней, которые наносят большой экономический ущерб животноводству. Важнейшим и перспективным методом борьбы с инфекционными болезнями является иммунопрофилактика. Используемые в настоящее время вакцины для профилактики бруцеллёза требуют своего принципиального изменения и совершенствования. Одно из перспективных направлений при разработке безопасных и эффективных средств профилактики — использование протективных антигенных белков Brucella spp. Целью данных исследований являлось получение рекомбинантного белка IalB Brucella spp. методом бактериальной экспрессии в Escherichia coli. В результате проведенных исследований ген, который кодирует инвазивный белок IalB, был амплифицирован с геномной ДНК Brucella suis и клонирован в бактериальный экспрессирующий вектор pET28b (+). Отработаны оптимальные условия экспрессии целевого гена в клетках E. coli, штамм ER2566 и условия очистки рекомбинантного белка — методом металл-аффинной хроматографии. Степень очистки белка составила не менее 95 %. При иммунизации рекомбинантным белком IalB в организме мышей вырабатываются антитела, которые детектируются в иммуноферментном анализе. Полученный рекомбинантный белок будет использован для разработки профилактических препаратов против бруцеллеза животных.
Введение
Бруцеллез является бактериальной болезнью, наносящей большой экономический ущерб животноводству. Объединенный комитет экспертов ФАО информирует о повсеместном распространении бруцеллеза сельскохозяйственных животных [1, 2]. В Казахстане бруцеллез регистрируется практически у всех видов сельскохозяйственных и домашних животных (крупный рогатый скот, овцы, козы, свиньи, северные олени, маралы, лошади, верблюды, яки, буйволы, зебу, собаки). Эпизоотологически и экономически наиболее значимым является бруцеллез крупного рогатого скота [3–6].
Важнейшим и перспективным методом борьбы с инфекционными болезнями является иммунопрофилактика. Против бруцеллеза в разное время было предложено значительное количество инактивированных и живых вакцин. Наибольшее признание во всем мире получила живая вакцина против бруцеллеза из аттенуированного агглютиногенного штамма B. abortus 19, которая широко применялась в СССР, США и многих других странах мира. Существенным недостатком этих вакцин является наличие в крови иммунизированных животных антител, выявляемых в серологических реакциях, принятых для диагностики бруцеллеза, затрудняющих определение эпизоотического статуса животных по бруцеллезу [7, 8].
Таким образом, задача создания эффективной и безопасной вакцины против бруцеллеза остается актуальной. В связи с этим постоянно проводятся исследования по конструированию новых и совершенствованию протективных свойств имеющихся вакцин, как для людей, так и для животных. Перспективным направлением разработки эффективных вакцин против инфекционных заболеваний является создание аттенуированных рекомбинантных векторов, осуществляющих доставку в организм про- тективных антигенов, с которыми связано формирование профилактического или лечебного эффекта вакцинации [9].
На сегодняшний день было выявлено свыше 10 защитных белков Brucella. Как известно, инвазивный белок IalB (BMEI 1584) также является протективным антигеном Brucella, который локализован в цитоплазматической мембране. Данный белок идентичен с основным фактором вирулентности Bartonella bacilliformis, который играет основную роль в инфицировании эритроцитов человека [10, 11].
Целью данных исследований являлось получение рекомбинантного белка IalB Brucella spp. методом бактериальной экспрессии в E. coli.
Материалы и методы
Конструирование экспрессирующего вектора и создание штамма-продуцента E. coli. Нуклеотидную последовательность, кодирующую рекомбинантный белок IalB, амплифицировали с геномной ДНК B. suis, штамм 1330 — с использованием праймеров (FP-tctagatctagcctccctgcccgg, RP-acggtcgacct- tggtcaatgcctg) и клонировали в экспрессирующий вектор pET28b(+) (Novagen) по сайтам BamHI — SalI. Корректность полученной конструкции подтверждали секвенированием. Затем вектор pET28/Bru-IalB трансформировали в компетентные клетки E. coli штамм ER2566 (NEB).
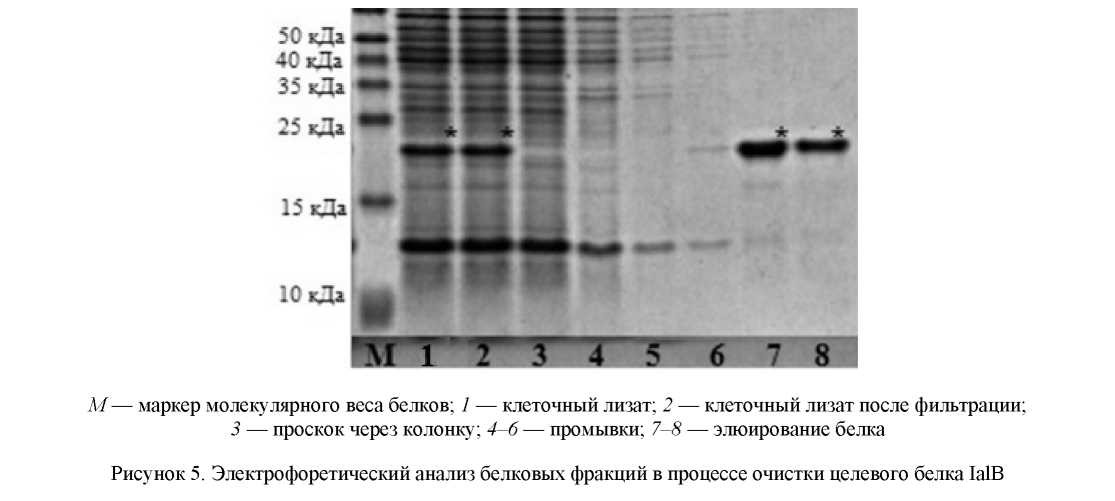
Экспрессия и очистка рекомбинантного белка. Клетки E. coli, штамм ER2566, трансформированные вектором pET28/Bru-IalB, выращивали в среде ĹВ-кан50 (содержание канамицина 50 мкг/мл) при 37 °С на шейкере (250 об/мин) до OD600 = 0,6-0,8, затем добавлением ИПТГ до конечной концентрации 1 мМ индуцировали экспрессию целевого гена. Индуцированную культуру инкубировали в течение 4 ч при тех же условиях. Затем клетки собирали центрифугированием и хранили при -70 °С до использования. Растворимость рекомбинантного белка определяли с использованием реагента B-PER® Bacterial Protein Extraction Reagent (Thermo Scientific, США) согласно инструкции производителя. Для очистки рекомбинантного белка осадок клеток ресуспендировали в буфере (100 мМ Трис HCl pH 8,0, 150 мМ NaCl, 1 % тритон Х-100, 1 % ДОХ) из расчета 15 мл на 1 г сырого клеточного осадка. К полученной суспензии добавляли лизоцим до конечной концентрации 1 мг/мл. Лизис клеток осуществляли путем двукратного замораживания (-70 °С) — оттаивания (+37 °С) суспензии. Фракцию растворимых белков получали центрифугированием лизата клеток при 10000× g в течение 20 мин. Очистку белка проводили методом металл-аффинной хроматографии с использованием HisPur™ Cobalt Superflow Agarose (Thermo Scientific, США) в нативных условиях согласно протоколу производителя. Электрофоретический анализ полипептидов проводили в 12 % ДСН-ПААГ в денатурирующих редуцирующих условиях по Laemmli [12]. Для визуализации белков использовали окрашивание Coo- massie G-250. По интенсивности окрашивания белковых полос определяли чистоту целевого белка.
Иммунизация мышей. B исследовании использовали беспородных белых мышей (самки, 6-8 недель, масса 18-20 г). Очищенный белок соединяли с адъювантом Montanide Gel 01 (SEPPIC) в соотношении 9:1 (об./об.). Конечная концентрация белка составила 180 мкг/мл. Иммунизацию проводили подкожно трехкратно в дозе 25 мкг белка. Забор крови проводили из хвостовой вены. Сыворотки тестировали в ИФА на наличие антител. Период наблюдения — 36 дней.
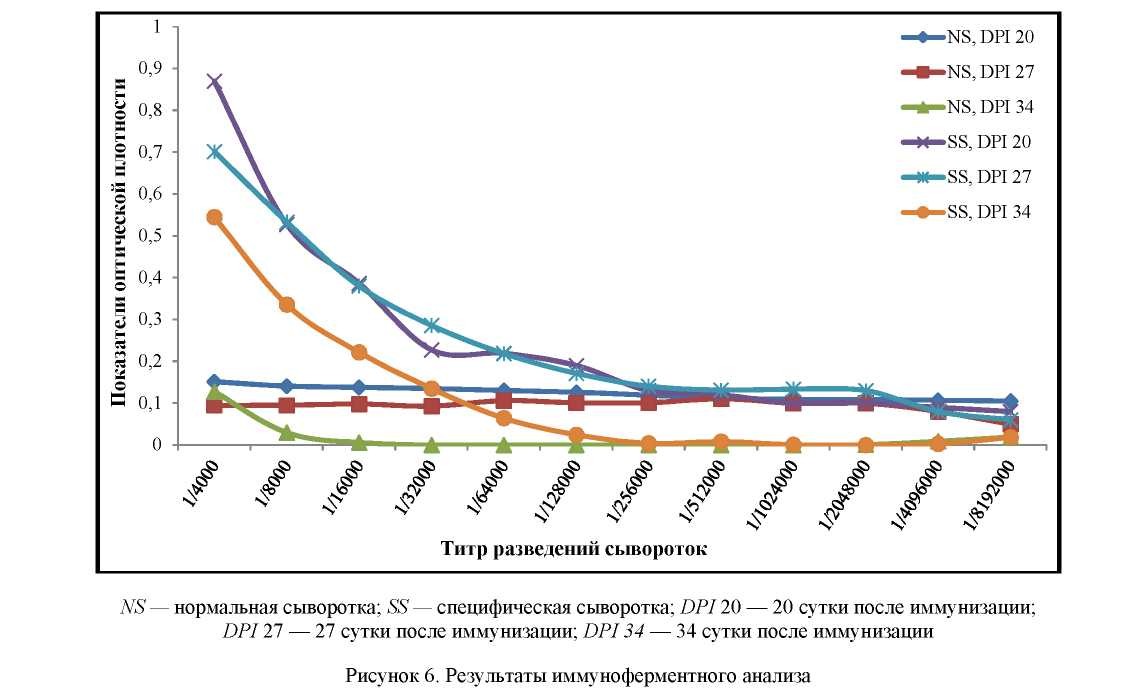
Иммуноферментный анализ. Для постановки ИФА 96-луночные планшеты (TPP, Швейцария) сенсибилизировали рекомбинантным белком IalB. С этой целью в каждую лунку планшета вносили по 100 мкл карбонат-бикарбонатного буфера, содержащего 2 мкг/мл рекомбинантного белка IalB. Планшеты инкубировали в течение ночи при 4 °С. Затем планшеты трехкратно отмывали буфером TBST (150 мМ NaCl, 20 мМ трис-HCl, pH 7,5, 0,1 % твин-20) и блокировали, внося в каждую лунку по 100 мкл блокирующего буфера (150 мМ NaCl, 20 мМ трис-HCl, pH 7,5, 5 % обезжиренное сухое молоко). Двукратные разведения исследуемых сывороток вносили по 100 мкл в лунки планшета, инкубировали в течение 1 ч при 37 °С. После трехкратной отмывки в лунки планшета вносили конъюгаты антимыши- ных IgG с щелочной фосфатазой (Sigma, США) в разведении 1:5000 и инкубировали в течение 1 ч при 37 °С. Планшеты отмывали трехкратно и вносили по 100 мкл субстрата для щелочной фосфатазы (pNPP) (Sigma, США), инкубировали 30 мин. Оптическую плотность (ОП) измеряли с использованием микропланшетного ридера ImmunoChem-2100 при длине волны 405/630 нм. Титром считали наибольшее разведение сыворотки, в которой оптическая плотность специфической сыворотки в два и более раз превышала таковую нормальной сыворотки.
Результаты исследований
Амплификацию нуклеиновой последовательности гена IalB проводили методом ПЦР в объеме 50 мкл: 5 мкл 10× буфера, 1 мкл 10 мМ смеси дНТФ, по 1 мкл прямого и обратного праймеров, 2,5 ед. Taq-полимеразы, 1 мкг ДНК, воды до 50 мкл. Температурный режим: 94 °C — 2 мин; 30 циклов 94 °C — 30 с, 50 °С — 1 мин, 68 °С — 1 мин; 68 °С — 7 мин.
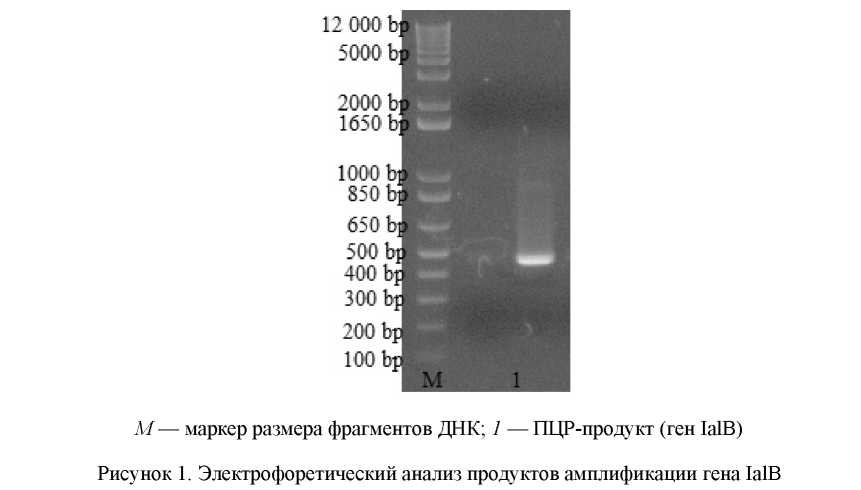
В результате ПЦР получили продукт размером приблизительно 490 п.о. (рис. 1). Расчетный размер гена IalB составляет 489 п.о.
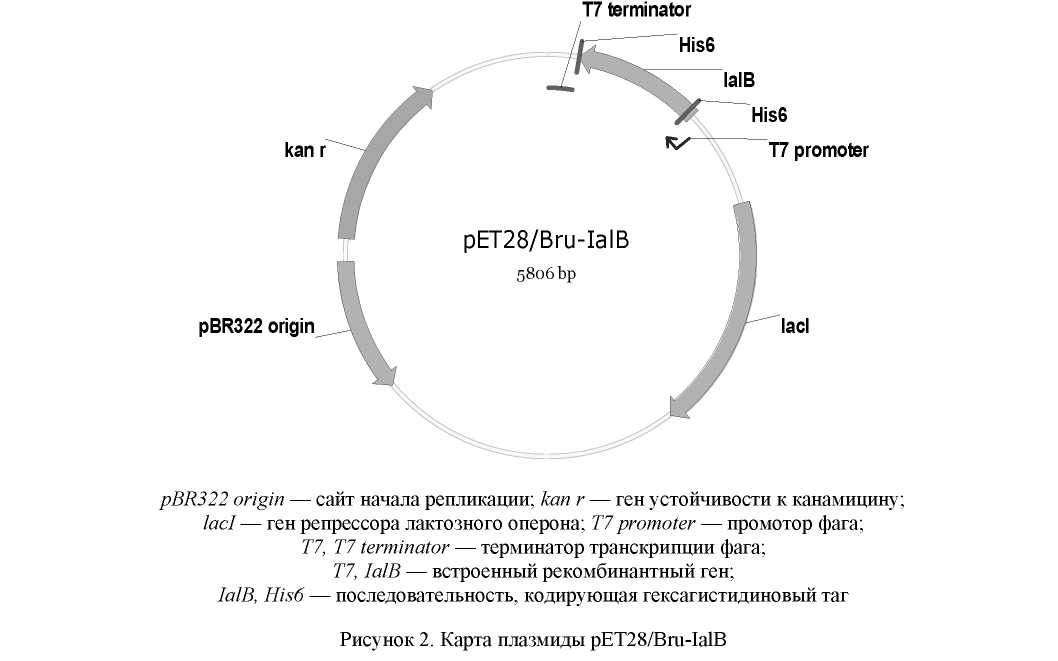
Амплифицированный фрагмент ДНК клонировали в плазмидный экспрессирующий вектор pET28b(+). Полученная рекомбинантная плазмида включала нуклеотидную последовательность белка IalB под контролем промотора Т7. На N- и С-концах аминокислотная последовательность имеет гистидиновые таги His6 (рис. 2).
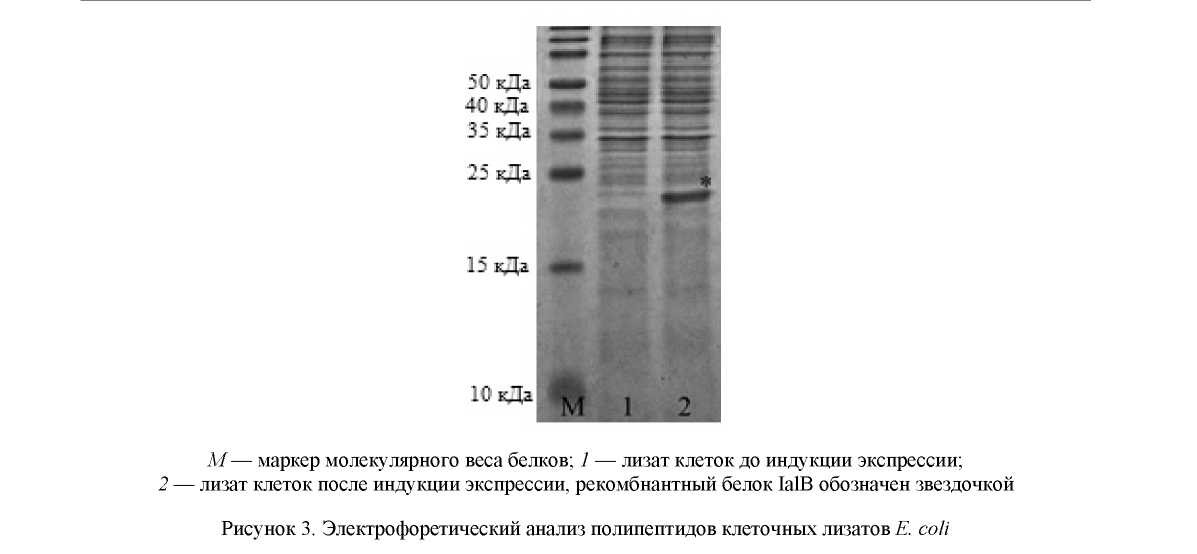
Полученная в результате клонирования плазмида была трансформирована в клетки E. coli штамм ER2566. Индукция экспрессии целевого гена ИПТГ приводила к наработке белкового продукта размером около 21 кДа, что соответствовало расчетной величине молекулярного веса рекомбинантного белка (рис. 3).
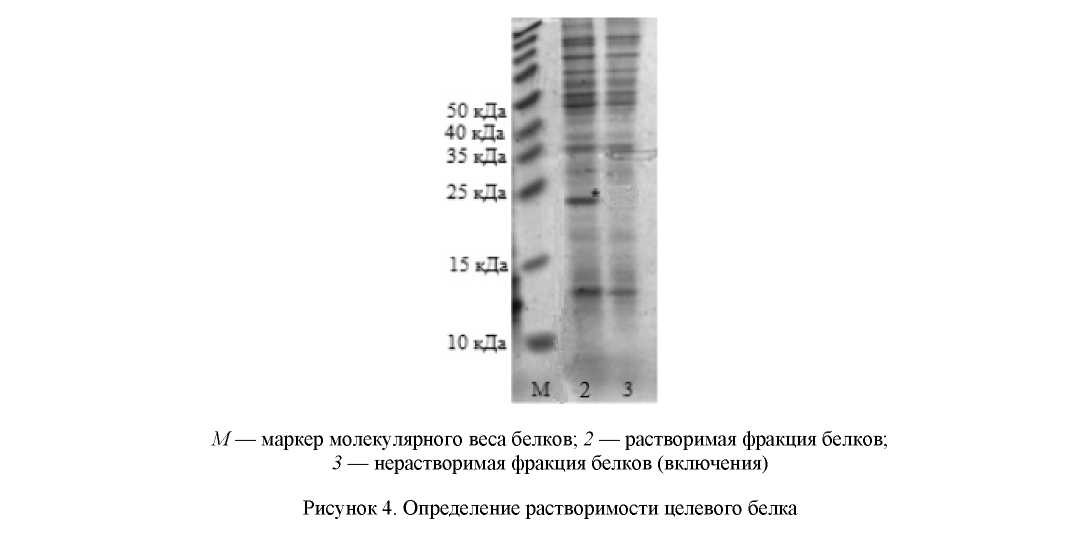
С целью выбора условий очистки рекомбинантного белка IalB определили его растворимость при экспрессии в клетках E. coli. Как видно из рисунка 4, целевой белок накапливается в клетке в растворимой форме.
Металл-аффинная хроматография является высокоспецифичным и надежным методом очистки рекомбинантных белков вследствие относительно высокого сродства и специфичности некоторых металлов к эпитопу, содержащему шесть или более остатков гистидина [13]. При создании генетической конструкции для экспрессии целевого гена в состав нуклеотидной последовательности были включены участки, кодирующие гексагистидиновые таги (рис. 2). Это позволило использовать для очистки целевого белка метод металл-аффинной хроматографии. Очистку белка проводили в нативных условиях.
Из рисунка 5 (дорожки 8, 9) видно, что использованный метод очистки позволил получить препараты рекомбинантного белка с чистотой не менее 95 %.
Также нами была проведена оценка способности рекомбинантного белка IalB стимулировать гуморальный иммунный ответ. Для этого мыши были иммунизированы препаратом рекомбинантного белка с адъювантом. Наличие антител к целевому белку определяли в динамике начиная с 20-х суток после первой иммунизации.
В результате было установлено, что рекомбинантный белок IalB вызывает в организме животных выработку специфических антител. Максимальный титр антител в сыворотке крови животных в ИФА отмечен на 20-е сутки с начала иммунизации и составил 1:64 000.
Выводы
В результате проведенных исследований была создана генетическая конструкция для экспрессии белка IalB в клетках E. coli. Отработаны оптимальные условия экспрессии и очистки целевого рекомбинантного белка. Степень очистки белка составила не менее 95 %. При иммунизации рекомбинантным белком IalB в организме мышей вырабатываются антитела, детектируемые в иммуноферментном анализе. Полученные рекомбинантный белок IalB и специфическая сыворотка к нему будут использованы при разработке профилактических препаратов против бруцеллеза животных.
Список литературы
- Иванов Н.П. Инфекционные болезни животных / Н.П. Иванов, К.А. Тургенбаев // Общая эпизоотология. — 2013. — № 1. — С. 47.
- Иванов Н.П. Бруцеллез животных и меры борьбы с ним: учеб. пос. / Н.П. Иванов. — Алматы: Атамұра, 2007. — 610 с.
- Ашетов И.К. Мониторинг и анализ эпизоотической ситуации по бруцеллезу КРС в РК за 2007-2012 годы / И.К. Аш- метов, А.Е. Ешмухаметов, И.Н. Ашетов. — Алматы, 2012. — С. 79-86.
- Ибрагимов П.Ш. Мониторинг эпизоотической ситуации по особо опасным болезням животных в Республике Казахстан, анализ и ожидаемый прогноз заболеваний за 2007-2012 годы: учеб.пос. / П.Ш. Ибрагимов. — Астана, 2013. — 74 с.
- Еспембетов Б.А. Анализ эпизоотической ситуации по бруцеллезу животных в Казахстане за 2013 год / Б.А. Еспембе- тов, Н.С. Сырым, Н.Н. Зинина // Вестн. Алтайского гос. ун-та. — 2017. — № 11. — С. 25-29.
- Еспембетов Б.А. Мониторинг и анализ эпизоотической ситуации бруцеллеза животных в Казахстане за 2011-2015 гг. / Б.А. Еспембетов, Н.С. Сырым, Н.Н. Зинина // Вестн. Ульянов. гос. с.-хоз. акад. — 2017. — № 1. — С. 92-96.
- Аракелян П.К. Оптимизация мероприятий при бруцеллезе сельскохозяйственных животных в современных условиях / П.К. Аракелян, С.К. Димов // Ветеринария. — 2013. — № 4. — С. 23-27.
- Саяпина Л.В. Современное состояние вакцинопрофилактики особо опасных инфекций / Л.В. Саяпина, В.П. Бондарев, Ю.В Олефир // Проблемы особо опасных инфекций. — 2016. — № 2. — С. 107-110.
- de Figueiredo P. Pathogenesis and immunobiology of brucellosis: review of Brucella-host interactions / P. de Figueiredo, T.A. Ficht, A. Rice-Ficht, C.A. Rossetti, L.G. Adams // American Society for Investigative Pathology. — 2015. — No. 185(6). — Р. 1505-1517.
- Crasta O.R. Genome sequence of Brucella abortus vaccine strain S19 compared to virulent strains yields candidate virulence genes / O.R. Crasta, O. Folkerts, Z. Fei, S.P. Mane, C. Evans, S. Martino-Catt, B. Bricker, G. Yu, L. Du, B.W. Sobral // PLoS ONE.2008. — Vol. 3(5). — P. 21-93.
- Commander N.J. The identification of two protective DNA vaccines from a panel of five plasmid constructs encoding Brucella melitensis 16M genes / N.J. Commander, S.A. Spencer, B.W. Wren, A.P. MacMillan // Vaccine. — 2007. — Р. 43-54.
- Laemmli, U.K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4 / U.K. Laemmli // Nature. 1970. — Vol. 227. — P. 680-685.
- Hochuli E. Genetic approach to facilitate purification of recombinant proteins with a novel metal chelate adsor-bent / E. Hochuli, W. Bannwarth, H. Dobeli, R. Gentz, D. Stu-ber // Biotechnology. — 1988. — Vol. 6. — P. 1321-1325.