АННОТАЦИЯ
Приведены результаты динамического наблюдения 60 пациентов с персистирующей астмой различной степени тяжести, в возрасте от 15 до 73 лет, которым помимо базисной терапии был назначен Миралюст (монтелукаст) перорально курсом на 3 месяца. Исследование проводилось в 3 регионах – г. Алматы, Караганда, Шымкент. Анализировались исходные данные пациентов и результаты через 4 и 12 недель приема препарата Миралюст. Контролировались показатели спирографии, частота эпизодов потери контроля (госпитализаций, вызовов скорой помощи), проводился мониторинг побочных эффектов. За время исследования было отмечено значительное улучшение показателей ФВД (прирост ОФВ1 на 14,4% и ПСВ на 25,5% от базовых значений, соответственно, p<0,05) и высокий профиль (98,3%) в течение 12 недель исследования.
Введение. Бронхиальная астма – одна из самых частых хронических патологических состояний во всем мире. По различным данным, ее распространенность достигает 10%, наибольшие показатели характерны для развитых стран Европы, Северной Америки [1, 2]. Распространенность астмы в Казахстане также повышается с каждым десятилетием. Даже далекая от реальных данных официальная статистика показывает 2,5-кратный рост заболеваемости с середины 2000-х годов [3]. Реальное же количество пациентов, снижение качества их жизни, потери трудовых и учебных дней, прямые и косвенные затраты государства и граждан в РК подсчитать до сих пор не представлялось возможным.
С внедрением системы ОСМС бронхиальная астма (БА) отнесена к заболеваниям, подлежащим динамическому безопасности и комплаентности препарата базисная терапия, монтелукаст.
наблюдению, даже ее диагностика входит в услуги по ГОБМП [4]. Также сохраняется государственное обеспечение астматиков основными лекарственными препаратами. Процессы цифровизации здравоохранения и отход от бумажных носителей идут быстрыми темпами, что должно значительно улучшить сбор данных по эпидемиологии БА в дальнейшем.
Тем не менее, есть и проблемные вопросы в менеджменте БА. В частности, монтелукаст входит в льготный список только для детского возраста, при том что взрослые нуждаются в нем не меньше. Это приводит к увеличению неконтролируемого приема гормональных препаратов, в том числе системных, а также коротко действующих бета-2-агонистах (SABA), развитию побочных эффектов при недостаточной эффективности [5].
Признанным фактом является ведущая роль аллергического воспаления в развитии астмы [1, 6]. Хроническое воспаление характерно для астмы вне зависимости от ее тяжести. Воспаление сопровождается развитием гиперреактивности бронхов и бронхиальной обструкции, являющихся двумя определяющими факторами, лежащими в основе нарушения легочной функции. Гиперреактивность дыхательных путей проявляется в чрезмерной бронхо- констрикторной реакции на различные раздражители [6].
При воспалительной инфильтрации стенок бронхиол эфферентными клетками воспаления преобладают тучные клетки, эозинофилы и актививированные лимфоциты. Эозинофильная инфильтрация дыхательных путей является характерной чертой при астме и позволяет дифференцировать это заболевание от других воспалительных процессов дыхательных путей. Клетки высвобождают различные медиаторы воспаления, включая лейкотриены – LtС4, LtВ4, тромбоксан, кислородные радикалы, основные белки, эозинофильный катионный белок, которые токсичны для эпителия бронхов [7].
Лейкотриены непосредственно приводят к сокращению гладкой мускулатуры дыхательных путей, повышению проницаемости сосудов, увеличению секреции слизи в просвет дыхательных путей, активируют другие воспалительные клетки, высвобождающие вторичные медиаторы воспаления.
История открытия лейкотриенов связана с исследованием медленно реагирующей субстанции анафилаксии (SAS-A), Broklekast, 1960. В 1983 г. B.Samuelsson ин- дентифицировал LtC4, LtD4 и Lt E4. В 1993 г. L.Laltlnen и соавт. и в 1997 г. Z.Diamant и соавт. описали триггерную реакцию при активизации рецепторов цистеинил-лей- котриенов в дыхательных путях и клетках воспаления, эффект бронхоконстрикции, отек тканей, секрецию слизи в дыхательных путях и стимуляцию клеток воспаления в легочной ткани. Цистеинил-лейкотриены являлись медиаторами обструкции дыхательных путей при астме. Лейкотриены синтезируются различными клетками под воздействием специфических стимулов: IgE, IgG, эндотоксинов, факторов фагоцитоза. Основное место синтеза лейкотриенов в организме человека - легкие, аорта и тонкий кишечник. Наиболее интенсивно синтез лейкотриенов осуществляется альвеолярными макрофагами, нейтрофилами и эозинофилами.
Роль лейкотриенов в патогенезе бронхиальной астмы заключается в усилении секреции слизи, подавлении ее клиренса, увеличении выработки катионных белков, повреждающих эпителиальные клетки. Лейкотриены усиливают приток эозинофилов, повышают проницаемость кровеносных сосудов. Они ведут к сокращению гладких мышц бронхов, способствуют миграции клеток, участвующих в развитии воспалительного процесса (активированные Т-клетки, тучные клетки, эозинофилы) [8, 9, 10].
LtC4 и LtD4 обладают мощным брон- хоконстрикторным действием. Эффект бронхоспазма, в отличие от вызванного гистамином, развивается медленнее, но является более продолжительным. Лейкотриены усиливают проницаемость сосудов в 1000 раз эффективнее гистамина [11]. Лейкотриены С4, D4 приводят к ранним изменениям и вызывают миграцию клеток в зону воспаления дыхательных путей [12].
Представления о лейкотриенах, как о медиаторах воспаления, позволили разработать концепцию создания нового класса лекарственных препаратов, получивших название «антилейкотриеновые субстанции». В настоящее время признано, что лучшим противовоспалительным эффектом обладают кортикостероиды. В то же время, при их длительном применении могут возникать серьезные побочные эффекты [1, 5]. Многие пациенты испытывают трудности при пользовании устройствами для ингаляции, так как ее необходимо проводить несколько раз в день. Отмечены случаи развития локальной и системной толерантности к кортикостероидам. Антагонисты лейкотриенов позволяют снизить дозировку других препаратов, используемых для лечения бронхиальной астмы, в частности, b2-агонистов. Необходимы дальнейшие исследования в целях определения их эффективности при совместном применении с ингаляционными кортикостероидами [13].
Использование монтелукаста, зафир- лукаста, пранлукаста в мировой практике сопровождается серьезными доказательствами их терапевтической эффективности и безопасности. Клинические испытания среди взрослых показывают, что монте- лукаст сходен с Беклометазоном по показателю контроля астмы [13, 14], сходен с Триамцинолоном по показателю снижения гиперреактивности бронхов [15] и выступает альтернативой удвоению дозы Будесо- нида на основании мультифакторной оценки контроля астмы [16].
На рынке РК имеется целый ряд генерических препаратов монтелукаста от различных производителей, в различных дозировках (4, 5 или 15 мг) [17], в том числе европейского производства. Проведение постмаркетинговых исследований эффективности и безопасности монтелукаста в РК тем не менее недостаточны, несмотря на их необходимость по международным требованиям.
Целью настоящего исследования была оценка эффективности и безопасности применения генерического монтелука- ста Миралюст у пациентов с БА легкого и среднего течения с недостаточным контролем в составе комбинированной терапии, как альтернативы повышению доз ИГКС.
Материалы и методы. Было проведено открытое многоцентровое, проспективное, контролируемое клиническое исследование. Использовался так называемый «исторический» контроль, соответственно рандомизация и ослепление не применялись.
С учетом того, что исследование носило постмаркетинговый характер (4 фаза), а все назначения препаратов соответствовали международным и национальным рекомендациям, необходимости в одобрении со стороны НЦЭЛС и локальных этических комитетов не было.
Объект исследования – пациенты с БА, персистирующей, легкого или среднего течения, частично контролируемой или неконтролируемой. Возраст – от 15 лет и старше.
В исследовании участвовали аллергологи из трех регионов РК: Алматинский (г. Алматы, Алматинская область), Карагандинский (г. Караганда и область), ЮжноКазахстанский (г. Шымкент, ЮКО).
Критерии включения:
- • Возраст пациента 15 лет и старше
- • Информированное согласие на исследование
- • Наличие верифицированной БА
- • Возможность проведения спирометрии и пикфлоуметрии до включения и после включения в исследование, доступность в течение не менее 3 месяцев.
- • Проживание в регионах, включенных в исследование (Алматинский, Карагандинский, Южно-Казахстанский).
Критерии исключения:
- - Дети в возрасте до 14 лет.
- - Беременные и кормящие
- - Инвалиды, военнослужащие, заключенные
- - Лица, связанные с работой повышенного риска (водители пассажирского транспорта, пилоты и т.п.)
- - Отсутствие возможности контакта с пациентом в контрольные сроки
- - Отказ пациента от приема монте- лукаста
- - Прием системных кортикостероидов
- - Самовольное повышение дозы принимаемых ИГКС
- - Отсутствие возможности проведения функциональных исследований дыхания (глухота, неконтактабельность, языковые барьеры и т.п.)
Методы исследования – эпидемиологические (анкетирование пациентов), клинические, лабораторные, функциональные (исследование функции внешнего дыхания), статистические.
Сроки проведения исследования январь – декабрь 2019 года.
Верификация диагноза проводилась стандартными методами, включающими общую и специфическую аллергодиагностику, ретроспективный анализ данных пациента, экспертную консультацию.
Наука о жизни и здоровье №1, 2020
Сроки наблюдения за пациентами – до 6 месяцев (не менее 3 месяцев на непрерывном приеме монтелукаста) с поэтапным контролем (на входе, через 1 месяц, через 3 месяца, через 6 месяцев).
Схемы лечения – согласно Протоколу «Бронхиальная астма у взрослых», 2014/2019 гг. [18], а также GINA 2018-19 [1], включающие базисные ингаляторы (ДДБА/ ИГКС), короткодействующие ингаляторы (КДБА), монтелукаст (на примере генерического препарата монтелукаста – Миралюст® 10 мг Адамед фарма Польша) у пациентов с БА легкого и среднего течения с недостаточным контролем в составе комбинированной терапии, как альтернативы повышению доз ИГКС).
Все препараты назначались только в соответствии с ИМП [19].
Контроль эффективности – по динамике клиники, функциональных исследований (спирография), фармакоэкономических показателей (потребности в вызовах бригад СНМП, госпитализации, обращения к специалистам).
Контроль безопасности проводился активным выявлением признаков ПДЛС, ожидаемым для применяемых средств (согласно ИМП), а также дополнительной регистрацией всех возникающих эффектов, эпизодов, событий в пределах срока исследования.
При признаках возникновении признаков ПДЛС пациентам было рекомендовано обращение к курирующему аллергологу или обращение за скорой или плановой медицинской помощью, согласно действующим НПА (вплоть до госпитализации в клинику НИИ КВБ).
В ходе исследования было набрано 60 пациентов с неконтролируемой и частично контролируемой астмой разной степени тяжести.
Среди них 43,3% составили мужчины, 56,7% женщины, что в целом отражает общую тенденцию. Средний возраст пациентов составил 42,9 + 4,25 года, самый старший участник 73 года, самый младший 15 лет.
Таблица 1. Индекс массы тела пациентов с БА
|
Недостаточная (ниже 18,5) |
6,7% |
|
Норма (18,5-25,0) |
46,7% |
|
Избыток (25,0-30,0) |
31,7% |
|
Ожирение (30,0-35,0) |
13,3% |
|
Ожирение 2 ст. (35,0-40,0) |
1,7% |
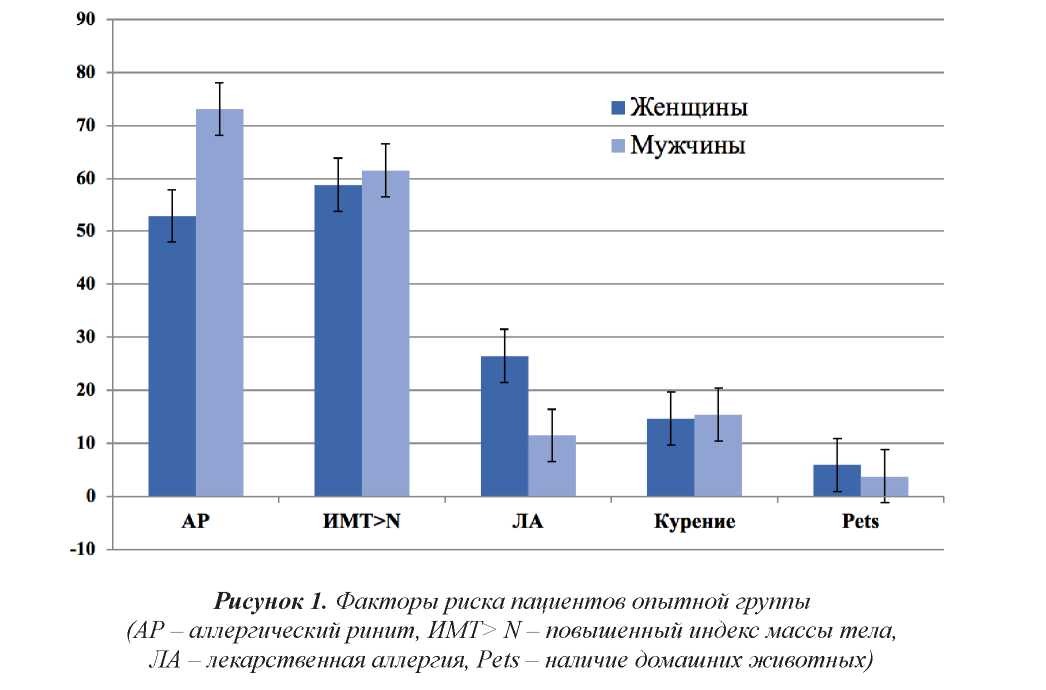
15% пациентов отмечали наличия курения как фактора риска, 5,1% – наличие домашних животных, 20% – наличие лекарственной гиперчувствительнос среди ти в анамнезе. 61,7% пациентов имели подтвержденный аллергический ринит в анамнезе, что также соответствует ожидаемым показателям (2/3 пациентов).
Стратификация обследованного контингента по факторам риска с разделением по полу представлена на рисунке 1.
Как видно из рисунка, выраженных различий по факторам риска между мужчинами и женщинами не было, за исключением аллергического ринита. Мужчины с БА намного чаще отмечали АР в анамнезе (73.1% с 52.9%, соответственно, р<0.05).
Обращает также внимание практически идентичная доля курящих среди мужчин и женщин идентичная доля курящих среди мужчин автоматически, идентичная анализатором рования приступов и повышению толерантности к физической нагрузке [4].
Да, из массы пациентов опытной гр. автоматически, анализатором рования приступов и повышению толерантности к физической нагрузке. Длительность БА составляла 9,4 + 2,5 года, максимальная – 40 лет, минимальная 1 год.
Длительность диспансерного учета по БА составляла 8.6 + 2,4 года, максимальная – 40 лет, минимальная 0.
Средняя частота обострений (потеря контроля над астмой) – 2,9 + 0,8 в год, минимальная 0, максимальная 15 раз в год! Временное снижение трудоспособности за предыдущий год (больничные листы) отмечали 36,7% пациентов.
Госпитализации за предыдущий год отмечали 16,7% пациентов – от 0 до 5 раз, в среднем 0,28 + 0,20. Дневные приступы 4,3 + 1,5, ночные 3,2 + 1,3 в сутки.
69,6% пациентов имели повышенный уровень сывороточного IgE (выше 130 ME/ml).
78,3% пациентов были характеризованы как имеющие тяжелую БА, 21,7% – легкой и средней степени. Контролируемая БА в исследование не включалась.
При включении в исследование пациенту проводились спирография, определение общего IgE, экспертная оценка состояния.
Нормативы спирометрии определялись автоматически, анализаторами BTL- 08, согласно рекомендациям ERS/ATS. Нормативы общего сывороточного IgE в ИФА согласно современным стандартам – до 130 МЕ/мл. Пациенту назначался Ми- ралюст (монтелукаст) в дозе 10 мг 1 раз в сутки, вечером.
Базисную терапию пациент получал в прежнем объеме.
Повторные осмотры проводились после 4-й, 8-й и 12-й неделях приема Ми- ралюст (монтелукаста) или по необходимости. Контрольная спирометрия проводилась на 4-й и 12-й неделе наблюдения.
Спирометрия выполнялась с использованием спироанализатора BTL-08 (Великобритания). Проба на реверсивность проводилась с сальбутамолом в дозе 200400 мкг через дозированный аэрозольный ингалятор с или без спейсера и с отсрочкой в 20 минут.
Статистический анализ выполнялся на программе Excel по общепринятым нормам [20]. Вознаграждение пациентов за участие в программе предусмотрено не было.
Полученные результаты и обсуждение. При включении в исследование, перед назначением монтелукаста, пациенту проводились спирография на спироа- нализаторе BTL-08. С учетом специфики заболевания и типа исследования было невозможно полностью исключить прием ингаляционных средств за 10-14 дней до начала.
Поэтому пациентам было рекомендовано не использовать бронхолитики и комбинированные ИГКС как минимум 24 часа до исследования. Результаты исследования представлены в таблице 2.
Таблица 2. Результаты ФВД (нулевая точка)
|
VC |
FVC |
FEV1 |
PEF |
TI |
test% |
|
|
Среднее |
84,6 |
85,5 |
74,8 |
73,3 |
87,9 |
17,1 |
|
Макс |
121,0 |
121,6 |
110,5 |
126,5 |
121,0 |
61,0 |
|
Мин |
50,0 |
46,0 |
37,0 |
34,0 |
44,0 |
0,0 |
|
СО |
15,3 |
19,1 |
20,3 |
21,0 |
15,7 |
15,7 |
|
ДИ |
3,9 |
4,8 |
5,1 |
5,3 |
4,0 |
4,0 |
Примечание: VC – жизненная емкость легких, FVC – форсированная жизненная емкость легких, FEV1 – объем форсированного выдоха за 1 секунду, TI – индекс Тиффно, PEF – пиковая скорость выдоха, test% - бронходилатационный тест с 200-400 мкг сальбутамола.
Наука о жизни и здоровье №1, 2020
Как видно из таблицы, средние показатели по группе наблюдения были на нижней границе нормы с довольно значительным размахом, однако детальное изучение результатов показало более характерную картину.
У 23 из 60 пациентов наблюдались рестриктивные изменения (38,3%), проявившиеся в снижении ЖЕЛ, у 35 из 60 явные обструктивные нарушения (58,3%) – снижение ОФВ1 ниже 80%. При этом, у 10 пациентов из оставшихся 25 с нормальными показателями на пробе с бронхолитиком был обнаружен скрытый бронхоспазм, что составило 40% от этой подгруппы или 16,7% от общего количества пациентов. Всего положительная проба наблюдалась у 46,7% пациентов.
Таким образом, у 75% астматиков наблюдались обструктивные изменения, у оставшихся 25% показатели ФВД были выше 80%.
Всем пациентам был рекомендован Миралюст (монтелукаст) в дозе 10 мг в качестве дополнения к ИГКС, 1 раз в день, вечером, минимальным сроком на 3 месяца.
Результаты контрольного исследования ФВД через 4 недели приема препарата представлены в таблице 3.
Таблица 3. Результаты ФВД (первая точка, 4 недели)
|
VC |
FVC |
FEV1 |
PEF |
TI |
test% |
|
|
Среднее |
85,2 |
86,8 |
76,7 |
79,2 |
88,8 |
15,6 |
|
Макс |
115,0 |
118,0 |
110,0 |
115,0 |
121,8 |
42,0 |
|
Мин |
55,0 |
50,0 |
45,0 |
50,0 |
47,9 |
0,0 |
|
СО |
14,0 |
17,0 |
18,9 |
17,2 |
15,1 |
11,8 |
|
ДИ |
3,6 |
4,3 |
4,8 |
4,3 |
3,8 |
3,0 |
Примечание: VC – жизненная емкость легких, FVC – форсированная жизненная емкость легких, FEV1 – объем форсированного выдоха за 1 секунду, TI – индекс Тиффно, PEF – пиковая скорость выдоха, test% - бронходилатационный тест с 200-400 мкг сальбутамола.
В течение 4 недель применения препаратов никто из пациентов не обращался за скорой неотложной помощью и, тем более, госпитализацией. Регистрировались звонки и сообщения с уточнениями курирующему доктору, однако серьезных побочных эффектов зарегистрировано не было. В одном случае развилось кратковременное носовое кровотечение (1,7%), возможно обусловленное приемом интраназального спрея. Комплаенс составил 100%.
По результатам исследования функции внешнего дыхания, 24 из 60 пациентов наблюдались рестриктивные изменения (40,0%), проявившиеся в снижении ЖЕЛ, у 35 из 60 явные обструктивные нарушения (58,3%) – снижение ОФВ1 ниже 80%. При этом, у 7 пациентов из оставшихся 25 с нормальными показателями на пробе с бронхолитиком был обнаружен скрытый бронхоспазм, что составило 28,0% от этой
Таблица 4. Результаты ФВД (вторая контрольная точка, 12 недель)
|
VC |
FVC |
FEV1 |
PEF |
TI |
test% |
|
|
Среднее |
91,7 |
91,0 |
85,6 |
91,9 |
94,3 |
7,4 |
|
Макс |
125,0 |
118,0 |
118,0 |
118,0 |
116,1 |
25,0 |
|
Мин |
60,0 |
59,0 |
48,0 |
58,0 |
64,0 |
0,0 |
|
СО |
11,5 |
13,1 |
15,3 |
13,5 |
12,0 |
6,2 |
|
ДИ |
2,9 |
3,3 |
3,9 |
3,4 |
3,0 |
1,8 |
Примечание: VC – жизненная емкость легких, FVC – форсированная жизненная емкость легких, FEV1 – объем форсированного выдоха за 1 секунду, TI – индекс Тиффно, PEF – пиковая скорость выдоха, test% - бронходилатационный тест с 200-400 мкг сальбутамола.
В течение следующих 8 недель применения препарата обращаемость за скорой неотложной помощью и госпитализацией все еще отсутствовала. Естественно, частично данный факт можно объяснить наличием возможности постоянной и быстрой связи с аллергологом, однако само по себе это является лучшим подтверждением фармакоэкономической эффективности примененной схемы, а также общего динамического наблюдения за пациентами подгруппы или 11,7% от общего количества пациентов. Всего положительная проба наблюдалась у половины (ровно 50%) пациентов.
Таким образом, так же, как и в начале исследования, у 75% астматиков наблюдались обструктивные изменения, у оставшихся 25% показатели ФВД были выше 80%.
При сравнении показателей ФВД в нулевой и первой контрольных точках обращает на себя внимание небольшой прирост во всех усредненных показателях, однако без статистически достоверной разницы (p>0.05). Наиболее явными изменения были по снижению количеству лабильности ФВД у пациентов с показателями, близкими к нормальным – с 40% до 28%.
Результаты контрольного исследования ФВД через 12 недель приема препарата представлены в таблице 4. с бронхиальной астмой, утвержденного в данное время Приказом МЗ РК [4]. При этом необходимо отметить, что у ряда пациентов стаж БА составлял более 30 лет.
Побочные эффекты. Продолжали регистрироваться звонки и сообщения курирующему доктору, однако серьезные побочные эффекты не регистрировались. Были упоминания о различных изменениях в общем состоянии больных (головные боли, повышенная температура в течение
1-4 дней, временное усиление кашля и т.п.), однако данные эпизоды были сочтены как незначимые и не привели к отмене препарата. Одна пациентка вышла из исследования в связи с беременностью. Комплаенс составил 98,3%.
По результатам исследования функции внешнего дыхания, рестриктивные изменения снизились и наблюдались у 10 из 60 пациентов (16,7%), то есть у 83,3% пациентов ЖЕЛ к 12 неделе стал выше 80% от нормы. Обструкция по ОФВ1 регистрировалась у 23 из 60 (38,3%) у 2 пациентов из оставшихся 37 с нормальными показателями на пробе с бронхолитиком был обнаружен скрытый бронхоспазм, что составило 5,4% от этой подгруппы или 3,3% от общего количества пациентов. Всего положительная проба наблюдалась у 20,0% обследуемых, что также намного ниже предыдущих данных.
Таким образом, количество лиц с персистирующими обструктивными изменениями снизилось с 75,0% до 41,7% (p=0.008).
При проведении сравнения показателей ФВД во второй и первой контрольных точках обращает на себя внимание гораздо более заметный прирост усредненных показателей ЖЕЛ, ФЖЕЛ (но все еще недостоверный статистически) и достоверный прирост ОФВ1 (71.9-81.5 / 81.7-89.5; 95%; p=0.046).
Наиболее явные изменения касались повышения среднего ПСВ с 79.2 ± 4,3 до 91.9 ± 3,4, а также дальнейшего снижения лабильности ФВД у пациентов с показателями, близкими к нормальным – с 28% до 5,4%. Это может говорить о стабилизации состояния пациентов, снижении гиперреактивности дыхательных путей и подтверждает эффективность применяемой схемы.
Индекс Тиффно также вычислялся при каждом посещении. Среднее повышение данного показателя отмечалось при каждом измерении (в сравнении с предыдущим). Средний прирост индекса Тиффно за 12 недель составил 7,3%, что было статистически незначимо (р=0,11). Не очень большой прирост индекса Тиффно, отразившись на статистических показателях, был обусловлен изначально близким к нормальным показателям, характерным для БА в отличие от ХОБЛ, синхронным повышением ФЖЕЛ и ОФВ1 на фоне терапии, а также относительно небольшим сроком наблюдения.
Улучшение по функциональным показателям отразилось и на клинической картине. За 12 месяцев отмечалось значительное улучшение в отношении дневных симптомов в обеих группах уже начиная со 4-й недели терапии.
Среднее значение дневных симптомов снизилось с 4.3 ± 1,5 в день в начале исследования до 3,3 ± 0,8 на момент его окончания (ДИ=95%; р=0,28). Важнее достигнутое улучшение в отношении ночных симптомов, количество которых снизилось с 3,2 ± 1,3 в неделю в начале исследования до 1,1±0,6 на момент его окончания (ДИ=95%, р=0,04).
Субъективная оценка удобства и переносимости препарата была на очень высоком уровне и практически достигла 100%, так как единственная пациентка, терапия которой прервалась, также отмечала полное удовлетворение от качества препарата и режима приема. Пациенты, не показавшие значительного прироста по показателям ФВД на фоне лечения тем не менее не вышли из исследования и закончили курс, обеспечив высокий комплаенс.
Заключение. Анализ полученных результатов показал, что за 12-недельный курс терапии астмы у пациентов в возрасте от 15 до 70 лет пероральным монтелука- стом (в данном случае Миралюст ® 10 мг, Польша) в качестве альтернативы повышению дозы ингаляционных гормонов, дает хорошие возможности по достижению контроля при минимальных рисках.
Основные значимые моменты:
- Динамическое наблюдение за пациентами с БА имеет первостепенное значение, что доказывает своевременность внедрения данной модели менеджмента астмы, утвержденного последними приказами МЗ РК в условиях перехода на систему ОСМС.
- 4-недельный курс монтелукаста несмотря на положительные сдвиги не показал выраженных отличий от базового уровня, что подтверждает необходимость более длительного курса применения препарата (до 12 недель и более).
- Достоверное повышение ОФВ1 с 74,8 ± 5,1 до 85,6 ± 3,9%, и ПСВ с 73,3 ± 5,3 до 91,9 ± 3,4%за 12-недельный курс лечения (см. рис. 2)
- Снижение количества пациентов с обструктивными нарушениями во второй контрольной точке с 75,0 до 41,7% (р=0,008)
- Снижение гиперреактивности бронхов и скрытого бронхоспазма у пациентов с нормальными показателями ФВД с 40,0 до 5,3 %, что в конечном итоге ведет к снижению применения средств для купирования приступов и повышению толерантности к физической нагрузке.
- Входящие риски госпитализации в связи со значительной потерей контроля составляли 0,28 + 0,20 в год, то есть порядка 0,07 ± 0,05 эпизодов за 1 квартал (12 недель), или 4,2% пациентов (2-4 случая). За время же наблюдения госпитализации отсутствовали, то есть можно говорить о снижении относительного риска госпитализации при применении данного варианта монтелукаста на фоне базисной терапии. И соответственно экономической выгоде для пациента, семьи и страны в целом.
- Только у 1 из 60 (1,7%) пациентов отметились нежелательные эффекты (назальное кровотечение), которое было кратковременным, возможно не связанным с мон- телукастом и не повлекло необходимости отмены препарата. Монтелукаст обоснован к назначению и в пожилом возрасте [21].
- Аллергических реакций в период назначения монтелукаста не наблюдалось, несмотря на 20% пациентов, отметивших наличие лекарственной гиперчувствительности к другим группам препаратов в анамнезе.
- Комплаенс достиг высокой отметки в 98,3%, а удовлетворенность режимом дозирования и органолептическими свойствами препарата составила 100%.
- В формате данного исследования астматики не показали отличий от базовой популяции в приверженности факторам риска (ИМТ, курение, домашние питомцы и др.)

- Миралюст ® является одним из современных представителей монтелукастов на рынке РК, обладающим отличным профилем эффективности и безопасности.
- Имеются все основания включения монтелукаста в льготный перечень не только для детей, но и взрослых. Экономические потери на закуп препарата видимо будут компенсироваться снижением потребности в дорогостоящих комбинированных ингаляторах, снижением количества госпитализаций и ряда других косвенных затрат.
Таким образом, высокая эффективность и безопасность антилейкотриеновых препаратов дает возможность не только успешно применять их в случаях манифестированных форм БА и АР, но и выдвинуть гипотезу о целесообразности их использования даже при наличии подозрений на БА, а также при других состояниях, сопровождающихся свистящим дыханием, длительным кашлем, обструктивным синдромом.
Естественно, все это требует дальнейшего исследования в масштабных проектах, с дальнейшим внесением коррекций в инструкцию к препарату и существующие клинические рекомендации и протоколы.
СПИСОК ЛИТЕРАТУРЫ
- Global Initiative for Asthma. Global strategy for asthma management and prevention. Bethesda, MD: National Heart, Lung and Blood Institute, 2019 (www. ginasthma.com).
- The Global Asthma Report (2018). Accessed: June 5, 2019 (http://www. globalasthmareport. org).
- Статистический сборник «Здоровье населения Республики Казахстан и деятельность организаций здравоохранения в 2019 году» – Астана, 2019 г.
- Приказ МЗ РК №136 от 17 октября 2019 года «Об утверждении перечня социально-значимых заболеваний, заболеваний, подлежащих динамическому наблюдению…» (www.adilet.zan.kz).
- PJ Sharek, D Bergman, FM Duchanne. The effect of Beclome thasone on height in children. 2011 - Summaries.cochrane.org.
- Скепьян Е. Н. Бронхиальная гиперреактивность на фоне физической нагрузки, и ее коррекция у детей с бронхиальной астмой. Автореф. диссертации на соискание ученой степени кандидата медицинских наук по специальности 14.00.09 Педиатрия. Минск. 2009.
- Ishmael FT: The inflammatory response in the pathogenesis of asthma. J AM Osteopath Assoc. 2011, 111:11-7.
- Maslan J., Mims J.W. What is asthma? Pathophysiology, demographics, and health care costs. Otolaryngol Clin North Am. 2014; 47(1):13-22. doi: 10.1016/j.otc.2013.09.010.
- Kuipers H, Lambrecht BN. The interplay of dendritic cells, Th2 cells and regulatory T cells in asthma. Curr Opin Immunol. 2004; 16(6): 702–708.
- Polito A.J., Proud D. Epithelia cells as regulators of airway inflammation. J Allergy Clin Immunol. 1998; 102(5):714–718.
- Liu M., Yokomizo T: The role of leukotrienes in allergic diseases. Allergol Int. 2015, 64:17-26.
- Cohn L., Elias J.A., Chupp G.L. Asthma: mechanisms of disease persistence and progression. Annu Rev Immunol. 2004; 22:789–815.
- Khan S.A., Hashmi Z.Y.: Comparison of therapeutic values between leukotriene receptor antagonist (montelukast) and inhaled glucocorticoid (beclomethasone propionate) in bronchial asthma of adults. Pak J Med Sci. 2008, 24:399-405.
- Israel E., Chervinsky P.S., Friedman B., Van Bavel J., Skalky C.S., Ghannam A.F., et al. Effects of montelukast and beclomethasone on airway function and asthma control. J Allergy Clin Immunol. 2002; 110:847-54.
- Dempsey O.J., Kennedy G., Lipworth B.J. Comparative efficacy and anti-inflammatory profile of once-daily therapy with leukotriene antagonist or low-dose inhaled corticosteroid inpatients with mild persistent asthma. J Allergy ClinImmunol. 2002; 109:68-74.
- Price D.B., Hernandez D., Magyar P., Fiterman J., Beeh K.M., James I.G., et al. Randomized controlled trial of montelukast plus inhaled budesonide versus double dose inhaled budesonide in adult patients with asthma. Thorax. 2003; 58:211 - 6.
- Национальный реестр зарегистрированных в РК лекарственных средств (www. dari.kz).
- Клинический протокол «Бронхиальная астма», РЦРЗ, Нур-Султан, 2019 г. (www. rcrz.kz).
- Миралюст. Инструкция по медицинскому применению. (www.dari.kz).
- Гланц С. Медико-биологическая статистика. – М.: Практика, 1999. –C. 462.
- Columbo M: Asthma in the elderly: a double blind, placebo-controlled study of the effect of montelukast. Asthma Res Pract. 2017, 3:3.