АННОТАЦИЯ
В данной работе представлены результаты применения схемы VCP у пациентов с впервые выявленной множественной миеломой, за период с 2012 по 2017 годы, в отделении гемобластозов КазНИИОиР. Эффективность лечения оценивалась после 4-8 циклов VCP.
Цель исследования: оценить 5-летние результаты терапии ММ (множественной миеломы) ингибиторами протеасом в комбинации с алкилирующими препаратами и глюкокортикоидами.
Методы. В исследование включено 45 пациентов с впервые выявленной ММ, которые получили лечение по схеме VCP в отделение гемобластозов КазНИИОиР с 2012 по 2017 гг. Медиана возраста составила 60 лет (диапазон 44-81 год). Из них повторные курсы VCP получили 13 пациентов.
Результаты. Общая эффективность терапии первой линии по схеме VCP составила 89%, причем у 62,5% пациентов достигнута полная ремиссия, очень хорошая частичная ремиссия составила 15,5%, частичная ремиссия наблюдалась у 33,3% пациентов (таблица 3). Медиана времени до достижения ответа составила 4 месяца. Прогрессирование заболевания на фоне терапии по схеме VCP произошло у 11,1% пациентов. Медиана времени до достижения ответа составила - 3,8 месяца. Медиана продолжительности ремиссии составила 15 месяцев.
При оценке результатов повторного использовании VCP общий клинический ответ достигнут у большинства пациентов - у 10 (77%) из 13. Из них ПР отмечены у 30,7% пациентов, ОХЧР - 23%, ЧР – у 23% пациентов, прогрессирование заболевания - у 23 % пациентов (таблица 3). Среднее число циклов до получения ответа варьировало от 4 до 8. Медиана времени до достижения ответа составила 4,2 месяца. Медиана продолжительности ремиссии составила 7,9 месяцев.
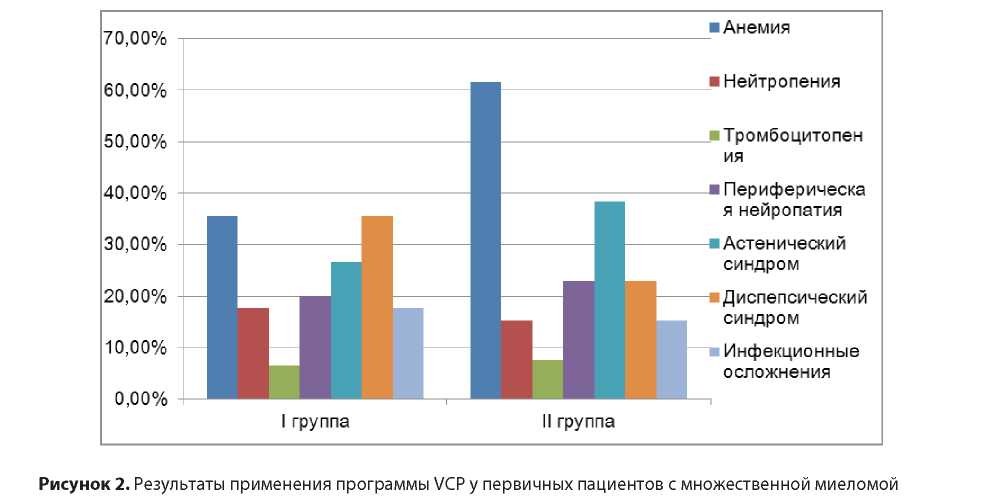
Побочные эффекты схемы VCP были предсказуемыми и контролируемыми, наиболее значимые из них - полинейропатия (19%), астения (29,3%), инфекционные осложнения (17,2%), гематологические симптомы (65,5%), диспепсические симптомы (32,7%).
Заключение. Схема VCP показала высокую эффективность в лечении ММ, как в первой, так и в последующих линиях терапии.
Множественная миелома (болезнь Рустицкого - Калера) характеризуется злокачественной опухолевой пролиферацией плазматических клеток одного клона с гиперпродукцией моноклонального иммуноглобулина (IgG, IgA, IgD либо IgE) и/или свободных моноклональных легких цепей иммуноглобулинов.
Множественная миелома (ММ) относиться к достаточно частым заболеваниям системы крови. Ежегодно регистрируется 30 новых случаев на 1 млн. населения. ММ составляет приблизительно 1% среди всех злокачественных опухолей, 13% среди гемопоэтических опухолей [1,2,3,4,5]. Заболеваемость множественной миеломой (ММ) составляет 5-10 на 100 тыс. чел. в год. У афроамериканцев в США ММ встречается в 2,3 раза чаще, у белых (9,9 и 4,3 на 100 000 населения в год соответственно). В США в 2011г. зафиксировано 20 520 новых случаев ММ, в Европе ежегодно регистрируют примерно 10-15 тыс. впервые заболевших. В Украине, согласно данным Национального канцер-регистра, в 2012 г. выявлено 769 случаев ММ [2], заболеваемость составляет 1,7 случая на 100 тыс. населения. Заболеваемость японцев и китайцев значительно ниже: 1 на 100 000 населения (4). Однако в последние годы во всем мире отмечается увеличение числа больных множественной миеломой.
В России в 2012 г. впервые диагностировано 2782 случая, умерло 2097 больных. Заболеваемость ММ в России составила 2,0 на 100 тыс., возрастная медиана заболеваемости 63,7 года [7], в Казахстане 1,6 на 100 000 (6). Смертность составляет 4,1 на 100 тыс. чел. в год.
В последние годы отмечается «омоложение» ММ, диагностируются пациенты в возрасте от 20 лет, что диктует необходимость разработки эффективных схем лечения.
Согласно литературным данным, последние достижения в лечении ММ значительно увеличили медиану выживаемости больных, сделали ее потенциально излечимым заболеванием [8,9].
Таблица 1. Характеристика пациентов
|
Характеристика |
I группа Первичные, 1я линия VCP |
II группа Повторные, 2я линия VCP |
|
Количество пациентов всего |
45 |
13 |
|
Женщины |
18 (40%) |
9(69,2) |
|
Мужчины |
27(60%) |
4(30,7%) |
|
Возраст |
||
|
<60 |
23(51,1%) |
5(38,4%) |
|
>60 |
14(31,1%) |
7(53,8%) |
|
>70 |
8(17,7%) |
1(7,6%) |
|
Средний возраст |
60 (44-81) |
59 (49-71) |
|
II стадия |
24(53%) |
8(61,5) |
|
III стадия |
16(35,5%) |
5(38,4) |
|
Плазматические клетки в костном мозге, % |
38,5 (18,2-72) |
22,8(16,7-53,2) |
|
Первичные пациенты |
45 |
13 |
Таблица 2. Критерии ответа EBMT
|
Фаза заболевания |
Критерии оценки |
|
ПР. Полная ремиссия |
Менее 5% плазматических клеток нормальной морфологии в пунктате костного мозга, полученного не ранее, чем через 1 мес после завершения курса терапии и отсутствие моноклонального^ в сыворотке крови и/или моче |
|
Близкая к ПР |
100% редукция М-протеина, но выявляемая высокочувствительных методов иммунофлуоресценции. |
|
Очень хорошая частичная ремиссия (ОХЧО) |
Более чем 90% снижение парапротеина (патологического иммуноглобулина) в сыворотке крови или моче |
|
Частичная ремиссии |
≥50% уменьшение сывороточного иммуноглобулина и/или >90% уменьшения белка Бенс-Джонса. |
|
МО. Минимальный ответ |
≥25% снижение уровня моноклонального иммуноглобулина в сыворотке крови, ≥50% белка Бенс-Джонса в моче. |
|
Большой ответ |
≥75% редукция М-протеина, 5% и менее плазматических клеток. |
|
Стабилизация заболевания |
Стабилизация параметров болезни (включая число и размеры костных деструкций), умеренное снижение уровня моноклонального^ в сыворотке крови и белка Бенс-Джонса в моче на фоне не менее 3-х циклов химиотерапии |
|
Резистентность |
Отсутствие уменьшения в сыворотке крови моноклонального иммуноглобулина или белка Бенс-Джонса в моче |
|
Прогрессирование болезни (рецидив) |
Появление моноклонального иммуноглобулина, 25% увеличение его уровня, появление новых очагов деструкции в костях скелета или плазмоцитомы |
Таблица 3. Результаты применения программы VCP у первичных пациентов с множественной миеломой
|
Критерии |
I группа Первичные, 1я линияVCP |
II группа Повторные, 2я линияVCP |
|
Общий ответ на терапии |
40(89%) |
10(77%) |
|
Полная ремиссия |
18(40%) |
4 (30,7%) |
|
Очень хорошая частичная ремиссия |
7(15,5%) |
3(23%) |
|
Частичная ремиссия |
15(33,3%) |
3(23%) |
|
Ме до достижения полной ремиссии |
3,8 месяц |
4,2 месяц |
|
Ме продолжительность ремиссии |
15 месяц |
7,9 месяц |
|
Переведенные на другой протокол лечения |
5(11,1%) |
3(23%) |
Цель исследования - оценить 5-летние результаты терапии ММ ингибиторами протеасом в комбинации с алкилирующими препаратами и глюкокортикоидами.
Материалы и методы: с июля 2012 по 2017гг. в отделении гемобластозов КазИОиР получили лечение по схеме VCP 45 пациентов с ММ, из них повторные курсы VCP получили 13 пациентов. Из них - 27 мужчин и 18 женщин, медиана возраста - 60 лет. У 29 пациентов была диагностирована II стадия, у 16 пациентов III стадия заболевания по B. Durie и S. Salmon. Каждый пациент, включенный в исследование, получил от 4 до 8 курсов VCP: бортезомиб - 1,3 мг/м2 в/в, дни 1,4,8,11; циклофосфамид- 200 мг в/в с 1 по 4-й день; преднизолон - 60 мг/м2 в 1-4 дни. Лечение возобновляется на 22-й день. Всего 4-8 курсов.
В качестве терапии второй линии схема VCP была назначена повторно 13 пациентам с рецидивами ММ. Характеристика пациентов, включенных в исследования представлена в таблице 1.
Противоопухолевый эффект оценивали после 4 и 8 циклов терапии по схеме VCP с использованием унифицированных международных критериев EBMT (таблица 2). Выделяли полную ремиссию (ПР), частичную ремиссию (ЧР) и прогрессирование заболевания (ПЗ). ПР подтверждали, когда число плазматических клеток нормальной морфологии в пунктате костного мозга было менее 5%.
Результаты и обсуждение. В целом, в группе больных, получавших от 4 до 8 циклов терапии по схеме VCP в качестве терапии первой линии, общий клинический ответ достигнут у большинства пациентов - у 40 (89%) из 45. Из них ПР отмечены у 40% пациентов, ОХЧР -15,5%, ЧР- у 33,3% пациентов, прогрессирование заболевания - у 11,1% пациентов. Медиана времени до достижения ответа составила - 3,5 месяца. Медиана продолжительности ремиссии составила 15 месяцев.
зболивающих препаратов - лидокаиновые блокады, опиоиды, трамадол, а также лечение дополняли габапентином или прегабалином, в тяжелых случаях — карбамазепином, амитриптилином, дулоксетином. На фоне указанной терапии наблюдалось улучшение самочувствия. Больные отмечали уменьшение интенсивности боли в нижних и верхних конечностях, восстановление температурной и тактильной чувствительности, подвижности конечностей.
Анемический синдром развился у 16(35,5%)
При оценке результатов повторного использовании VCP общий клинический ответ достигнут у большинства пациентов, у 10 (77%) из 13. Из них ПР отмечены у 30,7% пациентов, ОХЧР - 23%, ЧР – у 23% пациентов, прогрессирование заболевания - у 23 % пациентов (таблица 3). Среднее число циклов до получения ответа варьировало от 4 до 8. Медиана времени до достижения ответа составила 4,2 месяцев. Медиана продолжительности ремиссии составила 7,9 месяцев.
При оценке токсичности VCP режимов было установлено, что периферическая полинейропатия наблюдалась в первой группе у 9(20%) пациентов, во второй группе – у 3(23%). Полинейропатия клинически проявлялась онемением, парестезиями, болевыми ощущениями в кончиках пальцев рук и ног. Пациентам с исходной или развившейся на фоне терапии бортезомибом нейропатии I-II степени назначали витамины группы В, фолиевую и альфалипоевую кислоты с удовлетворительным эффектом. При развитии полинейропатии III-IV степени применение бортезомиба прекращалось. Болевой синдром купировался назаначением обе первичных пациентов в первой линии терапии и у 8(61,5%) пациентов, получивших повторную терапию с бортезомибом. Анемия была легкой и средней степени тяжести, не требовала гемотрансфузионной терапии и корректировалась назначением эритропоэтинов.
Тромбоцитопения на фоне лечения развилась в первой группе у 3(6,6%) пациентов, во второй группе у 7,6% пациентов.
Инфекционные осложнения наблюдались у 8(17,7%)первичных пациентов в первой линии тера-
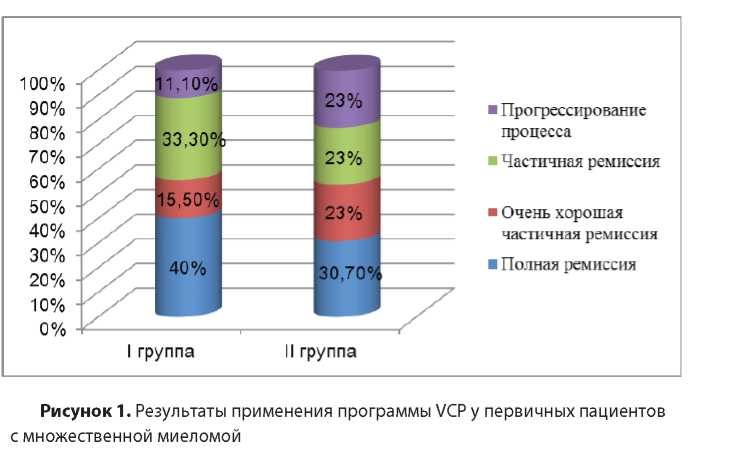
Таблица 4. Побочные эффекты при применении схемы VCP.
|
Побочные эффекты |
I группа Первичные, 1я линия VCP |
II группа Повторные, 2я линия VCP |
|
Количество пациентов |
Количество пациентов |
|
|
Гематологические |
||
|
Анемия |
16(35,5%) |
8(61,5%) |
|
Нейтропения |
8(17,7%) |
2(15,3%) |
|
Тромбоцитопения |
3(6,6%) |
1(7,6%) |
|
Не гематологические |
||
|
Полинейропатия |
9(20%) |
3(23%) |
|
Астенический синдром |
12(26,6%) |
5(38,4%) |
|
Диспепсический синдром |
16(35,5%) |
3(23%) |
|
Инфекционные осложнения |
8(17,7%) |
2(15,3%) |
пии и у 2(15,3%)пациентов, получивших повторную терапию по схеме VCP. Среди инфекционных осложнений преобладали случаи herpes zoster. Пациентам в течение всех циклов VCP профилактически назначался противовирусный препарат ацикловир (400 мг 2–3 раза в сутки) или улкарил (400 мг/сут). Из других инфекционных осложнений встречались респираторные аденовирусные инфекции, острый бронхит, отит, инфекции мочевых путей, которые в целом не повлияли на ход лечения основного заболевания.
Нейтропения наблюдалась в первой группе у 8(17,7%) пациентов, во второй группе – у 2(15,3%) пациентов. Диспепсический синдром наблюдался у 16(35,5%) пациентов первой группы, во второй группе у 3(23%) пациентов. Также наблюдались астенический синдром в виде слабости и утомляемости у 12(26,6%) пациентов первой группы, во второй группе у 5(38,4%) пациентов (таблица 4).
ЗАКЛЮЧЕНИЕ
Анализ собственных данных позволяет заключить, что VCP обладает контролируемым и предсказуемым профилем токсичности, является высокоэффективным методом лечения, играющим важную роль в терапии ММ в качестве первой и последующих линий. Использование VCP улучшает показатели общей выживаемости и прогноз заболевания.
В целом, в группе больных, получавших от 4 до 8 циклов терапии по схеме VCP в качестве терапии первой линии, общий клинический ответ достигнут у большинства пациентов - у 40 (89%) из 45. Из них ПР отмечены у 40 % пациентов, ОХЧР - 15,5%, ЧР - у 33,3% пациентов, прогрессирование заболевания - у 11,1% пациентов. Медиана времени до достижения ответа составила - 3,5 месяца. Медиана продолжительности ремиссии составила 15 месяцев.
При оценке результатов повторного использовании VCP общий клинический ответ достигнут у большинства пациентов - 10 (77%) из 13. Из них ПР отмечены у 30,7% пациентов, ЧР – у 23% пациентов, прогрессирование заболевания - у 23% пациентов (таблица 3). Среднее число циклов до получения ответа варьировало от 4 до 8. Медиана времени до достижения ответа составила 7,9 мес.
Полученные результаты нашей работы коррелируют с результатами международных исследований по применению Бортезомиба в лечении ММ. В частности, эффективность бортезомиба в первой линии терапии ММ (2 фаза) впервые продемонстрирована на сессии Американского гематологического общества (ASH) в 2004 г. Было проведено шесть 3-недельных циклов лечения бортезомибом у 32 больных с впервые выявленной ММ. Если после 2 циклов была получена менее чем ЧР или после 4 циклов менее чем ПР, дополнительно назначался дексаметазон. Эффективность лечения составила 83% (ПР 13%, пПР 17%, ЧР 53%). У 43% больных ответ получен после 2 циклов терапии, у 39% - после 4 и у 13% - после 6. Дексаметазон был добавлен у 14 (61%) больных: у 8 – после 2 циклов и у 6 – после 4. Комбинация с дексаметазоном повысила эффективность в 9 случаях (у 6 пациентов от минимального ответа до ЧР и у 3 – от стабилизации заболевания до ЧР). В последующем успешно выполнена ауто ТГСК у 5 больных. Позже было установлено, что эффективность лечения повышается при использовании бортезомиба в комбинированной терапии. При использовании содержащих бортезомиб режимов (фаза 2) ОО колебался от 60 до 95% с достижением ПР у 10-32% больных. После проведения ауто ТГСК частота ПР возрастала до 30-57%. [10]
По данным исследований SUMMIT [11], в котором схема VD была применена у 202 пациентов с ММ во второй линии, медиана выживаемости без прогрессирования составила 12 месяцев, медиана общей выживаемости 17 месяцев, у 59% пациентов наблюдалась стабилизация или улучшение течения заболевания, в том числе у 35% пациентов – обьективный ответ (минимальный эффект 8 % + полная ремиссия 10% +ча- стичная ремиссия 17%). Среднее время до наступления ответа составило 43 дня (APEX)[12].
Таким образом, Бортезомиб в комбинации с циклофосфамидом и дексаметазоном является высокоэффективной, хорошо переносимой комбинацией для лечения множественной миеломы в первой линии терапии.
ЛИТЕРАТУРА
- Blade J, Samson D, reece D, apperley J, Bjorkstandard B, Gahrton G, et al. Criteria for evaluating disease response and progression in patients with multiple myeloma treated by high-dose therapy and haemopoietic stem cell transplation. Br J haemotol.1998; 1115-23.
- Haemotology. Basic Principles and practice.- 2 nd ed./Eds.R.Hoffmann F., E.B.Benz, S.J.Shattil, B. Furie.-1995.
- Kuehl W.M., Bergsagel P.L. Multiple myeloma: evoling genetic events and host interactoins. Nat rev Cancer.2002; 2:175-87.
- Kyle R.A., Gertz M.A., Witzig T.E, Just J.A., Lacy M.Q., Dispenzieri A., et al. review of 1027 patients with newly diagnosed multiple myelma. mayo Clin proc.2003;78:21-33
- Aslina M, Trudel S, Furman RR, Rosen PJ, O'Connor OA, Comenzo RL, Wong AF, Kunkel L.A, Molineaux CJ, Goy A.A phase 1 single-agent study of twice-weekly consecutive-day dosing of the proteasome inhibitor carfilzomib in patients with relapsed or refractory multiple myelome or lymphoma. Clinical cancer research: an Official Journal of the American Association for Cancer Research.2012 Jul 3.
- Кайдарова Д.Р. с соавт. Показатели онкослужбы Республики Казахстан за 2015г.
- Поддубная И.В., проф. Савченко В.Г, Российские клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний, Москва 2016.
- Neoplastic disease of the blood.-Vol.1.-2nd ed./Eds. P.H.Wiernik, G.P.Cannelos, R.A.Kyle, C.A.Schiffer.-N.Y. - Edinburg-London-Melbourne-Tokyo.1991.-P.325-372.
- El-Amm J., Tabbara I.A. Emerging Therapies in Multiple Myeloma. Am. J. Clin. Oncol. 2013 Aug: 98 [Epud ahead of print].
- Jagannath S., Brian D., Wolf J.L. et al. A Phase 2 Study of Bortezomib as First-Line Therapy in Patients with Multiple Myeloma. Blood (ASH Annual Meeting Abstracts) 2004; 104: Abstract 333.
- Richardson PG, Barlogie B, Berenson J, Singhal S et al. A phase 2 study of velkade in relapsed, refractory myeloma. The new England Journal of Medicine 2003; 348:2609-2617
- Benedotto Bruno, Franceska Patriarca et all. Bortezomib with or without dexametazone in relapsed multiple myeloma following allogenic hemapoetic cell transplation. Journal Haemotolgica EHA, V91, no6, June 2006
- Kumar S.K., Radjkumar S.V., Dispenzieri A. et al. Improved survival in multiple myeloma and the impact of novel therapies. Blood. 2008; 111: 2516-20.
- Вотякова О.М. Современная терапия множественной миеломы. Бюллетень сибирской медицины. 2008; 3 (прилож.): 33-41.
- RichardsonP.G., BritmbergH., JagannathS. et al. Characterization and reversibility of peripheral neuropaty in patients with advanced multiple myeloma treated with bortezomib. Summit and Crest study group. Heamatol. J. 2004; 5 (Suppl.): S129.
- Скворцова Н.В., Поспелева Т.И., Нечунаева И.Н., Фрадкин В.А., Шамаева Г.В. Маслова Л.М. Эффективность повторной терапии бортезомибом у пациентов с рефрактерными и рецидивирующими формами множественной миеломы. Бюллетень Сибирского отделения Российской академии медицинских наук.2013; 33 (1): 76-82.
- Скворцова Н.В., Мельникова Т.В., Мельниченко Е.В., Мишенин А.В. Эффективность таргетной терапии множественной миеломы с использованием ингибиторов протеасом. Бюллетень Сибирского отделения Российской академии медицинских наук.2011; 31 (2): 94-100.
- Поспелова Т.И., Скворцова Н.В., Неучнаева И.Н., Фрадкин В.А., Шамаева Г.В. Результаты лечения реф- рактерны/рецидивирующих форм множественной миеломы. Гематология и трансфузиология. 2012; 57 (3): 21-2.
- NCCN Guidelines TM Version 1. 2018 Multiple myeloma [http://www.nccn.org].