АННОТАЦИЯ
Существующие современные методы лечения эректильной дисфункции имеют множество противопоказаний, в особенности у пожилых пациентов. Это стимулирует постоянный поиск эффективных, безопасных и доступных лекарственных средств для лечения эректильной дисфункции. Особый интерес представляет препарат растительного происхождения Трибестан, получаемый из растения Tribulus terrestris L. (якорцы стелющиеся).
Цель исследования: оценить эффективность и безопасность применения препарата Трибестан в лечении эректильной дисфункции.
Материалы и методы: нами обследовано 32 пациента в возрасте от 29 до 58 лет (средний возраст 44,2±3,4 года) и давностью заболевания ЭД от 6 мес. до 4 лет. Эректильная дисфункция была диагностирована на основании данных анамнеза, объективного клинико-лабораторного исследования и результатов анкеты Международного индекса эректильной функции.
Результаты и обсуждение: на фоне лечения препаратом Трибестан, отмечено достоверное увеличение показателей по шкале Международного индекса эректильной функции: достижения эрекции – на 77,4%, эрекции при сексуальной стимуляции – на 68,4%, достаточности эрекции – на 66,7%. Частота половой жизни пациентов до лечения составляла 3,8±1,3 раза в месяц, после лечения – 6,9±0,7 (p<0.05). При исследовании гормональных показателей пациентов до лечения выделено, что средний уровень тестостерона достигал 11,4±2,2 нмоль/л, после лечения – 12,9±2.8 нмоль/л (p<0.05). Наблюдалось достоверное снижение уровня общего холестерина сыворотки крови (с 5,2±0,5 до 3,6±0,8 ммоль/л (p<0.05).
Выводы: применение препарата Трибестан, у больных эректильной дисфункции приводит к достоверному улучшению параметров, характеризующих сексуальную активность пациентов; к повышению уровня тестостерона, способствующий стимуляции половой функции; препарат эффективен, безопасен, удобен в применении, целесообразен для назначения при лечении мужских сексуальных расстройств, в особенности у лиц пожилого возраста; кроме того, отмечается достоверное снижение содержания общего холестерина.
Расстройство эрекции – наиболее часто наблюдающийся в сексологической практике феномен, частота которого увеличивается с возрастом и ассоциируется с такими состояниями, как частичный возрастной иммунодефицит, сахарный диабет, депрессия, атеросклероз, дислипидемия, эндотелиальная недостаточность и стресс.
В последнее время в сексологии активно используется термин «эректильная дисфункция» (ЭД), под которым понимают неспособность мужчины достигать и поддерживать достаточную для сексуального удовлетворения партнеров эрекцию [1].
В структуре сексуальных расстройств ЭД занимает ведущее место как по частоте возникновения, так и по социальной значимости [1,2]. Этим широко распространенным и прогрессирующим заболеванием страдает примерно 150 млн мужчин во всем мире. По данным ВОЗ, каждый десятый мужчина старше 21 года страдает расстройством эрекции, а каждый третий мужчина старше 60 лет вообще не способен совершить половой акт [2]. В 1993 г. согласительная комиссия Национального института здоровья по импотенции оценила количество мужчин в США, страдающих ЭД той или иной степени выраженности, в 30 млн человек. Распространенность ЭД растет с увеличением возраста пациентов. В 1995 г. в Европе ЭД страдали 31 млн мужчин, к 2025 г. прогнозируется увеличение этого показателя до 43 млн, а всего в мире за тот же период ожидается увеличение числа больных с такой патологией с 152 до 322 млн. человек [1,2].
По данным Массачусетского исследования мужчин различного возраста (MMAS), общая распространенность ЭД среди мужчин в возрасте от 40 до 70 лет составила 52%. Тяжесть ЭД была оценена как минимальная примерно у 17% мужчин, умеренная – у 25% и полная – у 10% [2].
Во втором эпидемиологическом исследовании в США – обследовании национального здоровья и жизни общества (NHSLS) – было установлено, что 31% мужчин в возрасте от 18 до 60 лет когда-либо сталкивались с той или иной степенью ЭД [3].
Основные факторы риска развития ЭД:
- • пожилой возраст;
- • хронические заболевания, заболевания сердца, сахарный диабет, артериальная гипертензия, использование лекарственных средств (тиазиды, бета- блокаторы, антиаритмические препараты, нейролептики, транквилизаторы и др.);
- • образ жизни: стресс, курение, злоупотреблениеалкоголем, гиподинамия, нерегулярное и несбалансированное питание [4,5].
Для Кыргызстана особенно актуален последний фактор, поскольку среди мужчин нашей страны наблюдается пренебрежительное отношение к своему здоровью: распространено табакокурение, малоподвижный образ жизни и неправильное питание, приводящие к избыточному весу. Наряду с этим отмечаются: нестабильные экономическое положение, безработица, неуверенность в завтрашнем дне.
До 1970 г. ЭД считалась общим проявлением психогенных нарушений или изменений метаболизма тестостерона. Однако в последующем было доказано, что, хотя психогенные нарушения и могут обусловить развитие заболевания, ведущим фактором в нарушении эрекции является органический [6,7].
В настоящее время выделяют три формы ЭД: психогенную (депрессия, проблемы в паре, психосоциальный стресс); органическую (нейрогенная, сосудистая (артериальная или венозная), травма/заболевание полового члена, гормональная, лекарственная, мульти- факторная); смешанную, при которой сочетаются психогенные и органические факторы [7].
Использование ингибиторов фосфодиэстеразы 5 (ФДЭ-5), интракавернозное и эндоуретральное применение вазоактивных препаратов, выполнение различных видов эндофаллопротезирования, корригирующих операций на кровеносных сосудах полового члена, использование локальной декомпрессии полового члена позволяет добиваться восстановления утраченной эректильной функции у 70-95% пациентов с ЭД [8].
Однако перечисленные методы лечения применимы не у всех пациентов, а в некоторых случаях они вызывают серьезные побочные эффекты. Указанные обстоятельства стимулируют постоянный поиск эффективных, безопасных и доступных лекарственных средств для лечения ЭД.
В связи с этим особый интерес представляет препарат растительного происхождения Трибестан, основой которого является протодиосцин - вещество, получаемое из надземной части многолетнего растения Tribulus terrestris L. (якорцы стелющиеся), произрастающее по всему миру [9-11].
Активными компонентами субстанции препарата Трибестан являются:
- стероидные гликозиды (сапонины) фуростаноло- вого типа (триллин, диосцин, грациллин, протодиосцин, трибуспонин, кикубасапонин);
- сапогенины (диосгенин, гитогенин, рускогенин, хлоро-генин);
- флавоноиды;
- алкалоиды (гарман, гармол, фуростанол);
- фитостерины (бета-ситостерин, кампестерин, стигмастерин);
- аскорбиновая кислота, смолистые, красящие и дубильные вещества;
- андрогеноподобные вещества.
Имеющиеся в препарате Трибестан, фуростано- ловые соединения содержат биологически активные вещества со следующими свойствами: противоми- кробным (как антибиотики высших растений); противовирусным (главным образом, действуют на вирусы гриппа и герпеса); фунгицидным; гипохолестерине- мическим (нормализуют содержание холестерина в крови); противовоспалительным (кортикостероидоподобный эффект); противоопухолевым; половостиму- лирующим [12-16]. Протодиосцин метаболизируется в организме до дигид-роэпиандростерона (ДГЭА), который оказывает благоприятное влияние на иммунитет, целость клеточной мембраны, эректильную функцию и метаболизм холестерина (гиполипидемический эффект) [9,10,13-17]. При увеличении его количества в организме он стимулирует улучшение физического и психического самочувствия, повышение сексуальной активности, снижение жировых отложений и повышение силы мышц, оптимизацию функции резервных клеток мозга, снижение уровня глюкозы крови, нормализацию чувствительности клеток к инсулину, снижение уровня холестерина, нормализацию иммунных реакций, а также обладает антиканцерогенными свойствами [12-16].
Другие активные фуростаноловые сапонины, входящие в состав экстракта Tribulus terrestris, вероятно, модулируют эффект протодиосцина. ДГЭА и его сульфатный эфир (ДГЭ-АС) играют важную роль в метаболизме холестерина и синтезе стероидных гормонов [9-12]. Известно, что холестерин является исходным соединением для синтеза всех стероидов, включая ДГЭА, тестостерон и эстрадиол. Влияние Трибестана на метаболизм холестерина объясняет гиполипидемическое действие препарата. Действие различных составляющих препарата обеспечивает соответствующие эффекты в организме[15-17]. Сапонины и сапогенины улучшают функцию эндокринных желез: стимулируют выработку ЛГ, ФСГ, СТГ и альдостерона, восстанавливают функцию коры надпочечников, стимулируют секреторную активность поджелудочной железы, увеличивают поглощение йода щитовидной железой; активизируют сперматогенез у мужчин; активизируют работу адаптивных систем; повышают функциональную активность ЦНС; оказывают противовоспалительное, антиаллергическое действие, укрепляют иммунитет [9-12]. Алкалоиды расширяют сосуды, активизируют кровообращение в половых органах. Фитостерины оптимизируют обмен холестерина. Флавоноиды уменьшают вязкость крови, оказывают диуретическое действие, усиливают продукцию и секрецию желчи гепатоцитами, проявляют антиоксидантное, мембраностабилизирующее и противовоспалительное действие, антибактериальный и противовирусный эффекты [9-12].
Особого внимания заслуживают данные о безопасности препарата Трибестан. В ходе поведенческих, гематологических, функциональных, биохимических и морфологических исследований в экспериментальных условиях не было установлено токсических и других побочных эффектов применения препарата.
Показаниями к назначению препарата Трибестан являются мужское бесплодие и сексуальные дисфункции, сопровождающиеся снижением либидо, силы и продолжительности эрекций.
Цель исследования
Оценить эффективность и безопасность применения препарата Трибестан в лечении ЭД.
Задачи исследования:
- изучить влияние препарата Трибестан на состояние эректильной функции пациентов;
- изучить влияние препарата Трибестан на уровень половых гормонов и биохимические показатели крови пациентов;
- изучить переносимость исследуемого препарата и возможные побочные эффекты при его использовании.
Материалы и методы
Нами обследовано 32 пациента в возрасте от 29 до 58 лет (средний возраст 44,2±3,4 года) и давностью заболевания ЭД от 6 мес. до 4 лет.
ЭД была диагностирована путем на основании данных анамнеза, результатов клинико-лабораторного и специализированного исследований.
Для оценки половой функции использовали анкету Международного индекса эректильной функции (МИЭФ), состоящую из 15 вопросов [18].
Заполненная анкета позволяла оценить, как эректильную функцию пациента, так и либидо, оргазм, чувство удовлетворения от полового акта и общую удовлетворенность.
При контрольном обследовании регистрировали наличие побочных эффектов.
Критерии для включения пациентов в исследование:
мужчины в возрасте 20 – 60 лет, имеющие сексуального партнера; ЭД средней степени тяжести (показатель шкалы МИЭФ не более 16 баллов); возможность иметь не менее 2 половых контактов в неделю; информированное письменное согласие пациента на участие в исследовании;
способность пациента к адекватному сотрудничеству во время исследования.
Критерии исключения пациентов из исследования:
наличие сексуальных расстройств, которые считаются первичными по отношению к диагнозу ЭД (например, снижение либидо); отсутствие сексуальной активности; использование других методов лечения нарушений эректильной функции;
любые клинически значимые отклонения лабораторных показателей, требующие дополнительного обследования и интерпретации данных; заболевания или состояния, которые могут повышать риск для пациента либо оказывать какое-либо влияние на задачи исследования; одновременное участие в другом клиническом исследовании.
Всем включенным в исследование больным проводили обследование, включавшее сбор анамнеза, осмотр, выявление сопутствующих заболеваний; клини- ко- лабораторное исследование (общий анализ крови и мочи, биохимический анализ крови с определением общего белка, триглицеридов, холестерина); гормональное исследование (определение уровня тестостерона, лютеинизирующего гормона (ЛГ), пролактина и простатспецифического антигена (ПСА) в крови). На протяжении исследования каждого пациента обследовали дважды: перед началом исследования и через 2 мес. с момента начала лечения.
Основным методом оценки ЭД была динамика показателей шкалы МИЭФ: эректильная функция, удовлетворенность половым актом, оргазм, половое влечение, общая удовлетворенность.
Качество эрекции пациенты оценивали по шкале: 0 – отсутствие эрекции; 1 – тумесценция полового члена без ригидности; 2 – ригидность, достаточная для проведения коитуса; 3 – полная эрекция [18].
Для изучения влияния препарата Трибестан на либидо нами были исследованы изменения концентрации тестостерона в сыворотке крови.
В ходе исследования у 17 больных (53,1%) были установлены психогенные причины расстройства эрекции, у 15 (46,9%) – органические: сосудистые артериальные – у 3 (9,4%) пациентов, сосудистые венозные – у 7 (21,9%), нейрогенные – у 5 (15,6%).
У 17 больных имело место снижение полового влечения (53,1%), у 12 – преждевременная эякуляция (37,5%). Большинство пациентов (56,3%) в прошлом перенесли воспалительные заболевания мужских половых органов, однако в период исследования признаков активного воспаления отмечено не было.
Первоначальные клинические исследования препарата Трибестан показали, что лечение следует отменять постепенно с целью сохранения максимально благоприятного эффекта [9,10]. Исходя из этого, больные получали Трибестан по 1таблетке 3 раза в день течение 60 дней.
Результаты и обсуждение:
На фоне лечения препаратом Трибестан, отмечено достоверное увеличение показателей по шкале МИЭФ: достижение эрекции – на 77,4%, эрекция при сексуальной стимуляции – на 68,4%, достаточность эрекции – на 66,7%.
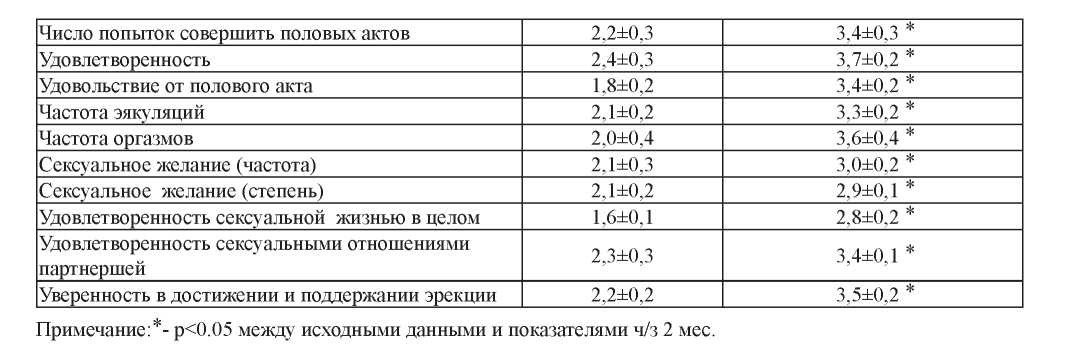
Согласно данным, показанным на рисунке №1, после завершения курса лечения в основной группе отмечены следующие изменения интегративных показателей: эректильная функция возросла на 82%, удовлетворенность половым актом – на 84%, оргазм – на 77,4%, либидо – на 78,9%, общая удовлетворенность – на 50%.
Таблица 1. Показатели шкалы МИЭФ в динамике
|
Показатели |
До лечения |
Ч/з 2 мес. лечения |
|
Достижение эрекции |
2,2±0,2 |
3,9±0,2 * |
|
Эрекция при сексуальной стимуляции |
2,2±0,2 |
3,7±0,2 * |
|
Достаточность эрекции |
2,1±0,3 |
3,6±0,2 * |
|
Сохранение эрекции |
2,2±0,2 |
3,7±0,3 * |
|
Эрекция до конца полов акта |
2,3±0,3 |
3,6±0,2 * |
Данные рисунка № 1 свидетельствуют о тенденции к улучшению эрекции, по субъективной оценке, обследованных пациентов на фоне приема изучаемого лекарственного средства. Так, если до лечения полная эрекция была отмечена у 12 пациентов (37,5%), а частичная – только у 10 (31,25%), то после курса приема препарата Трибестан полная эрекция восстановилась у 23 пациентов (71,9%). В целом способными к прове-
Таблица 2. Показатели гормонального обмена в динамике лечения
|
Гормональный показатель |
До лечения |
Ч/з 2 мес. Лечения |
|
Общ. Тст (нмоль/л) |
11,4±2,2 |
13,9±2,8 (p<0,05) |
|
ЛГ (МЕ/л) |
3,4±1,2 |
3,1±1,2 (p>0,1) |
|
Пролактин (Нг/мл) |
6,4±1,4 |
6,1±1,2 (p>0,1) |
|
ПСА (Нг/л) |
1,3±0,4 |
1,4±0,3 (p>0,1) |
дению коитуса оказались 30 (93,75%) из 32 пациентов.
Частота половой жизни исследуемых до лечения составляла 3,8±1,3 раза в месяц, после лечения – 6,9±0,7 (p<0.05), то есть после курса лечения было достигнуто достоверное увеличение этого показателя.
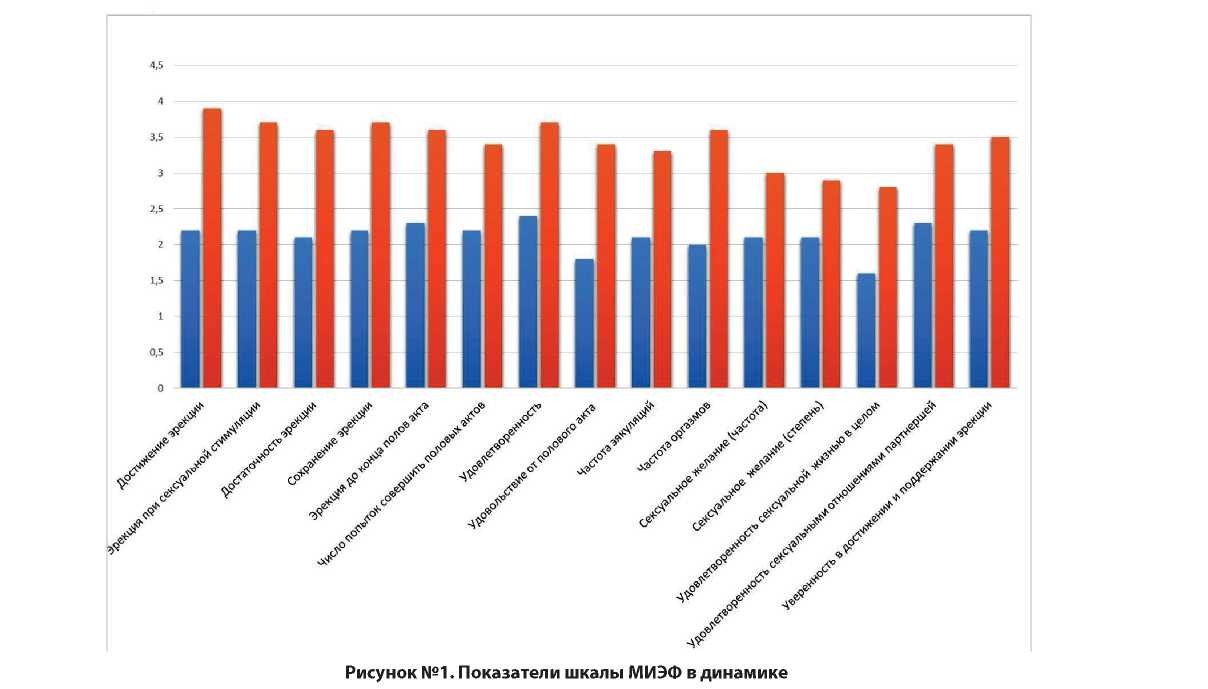
При исследовании гормональных показателей в крови пациентов до и после лечения получены следующие результаты (рисунок № 2). До лечения препаратом Трибестан средний уровень тестостерона составил 11,4±2.2 нмоль/л, после лечения – 12,9±2.8 нмоль/л (p<0.05).
Таким образом, после применения препарата Три- бестан у больных отмечалась некоторая тенденция к приема препарата Трибестан у пациентов не наблюдается достоверных изменений со стороны уровня ПСА, что говорит о безопасности применения данного препарата у пациентов старше 50 лет, в частности с диагнозом доборкачественная гиперплазия предстательной железы (ДГПЖ).
При оценке динамики показателей общего анализа крови и мочи у пациентов включенных в исследование достоверных изменений выявлено не было.
Данные таблицы №1 свидетельствуют о том, что изучаемый препарат практически не влияет на картину периферической крови.
При изучении результатов общего анализа мочи
Таблица №1. Показатели периферической крови
|
Показатели |
До лечения |
Ч/з 2 мес. лечения |
|
Эритроциты 1012/л |
4,0±0,2 |
4,2±0,2 * |
|
Гемоглобин |
141,7±1,2 |
143,5±2,2 * |
|
Лейкоциты 10?/л |
6,3±0,2 |
6,1±0,3 * |
|
Палочкоядерные, % |
2,82±0,27 |
3,26±0,32 * |
|
Сегментоядерные, % |
58,7±1,29 |
55,4±1,21 * |
|
Лимфоциты, % |
37,5±1,31 |
38,1±1,12 * |
|
СОЭ мм/ч |
2,65±0,4 |
2,12±0,2 * |
|
* - p>0,1 |
||
увеличению содержания тестостерона в сыворотке периферической крови, что могло привести к стимуляции половой функции, в частности – либидо. До лечения либидо было сохранено у 7 (21,9%) пациентов, после курса терапии препаратом Трибестан наличие либидо отметили 27 (84,4%) больных.
Отдельно хотелось бы обратить внимание на влияние препарата Трибестан на уровень ПСА (рис. № 2). Как видно из таблицы №2, на фоне двухмесячного до и после проведенного лечения препаратом Трибе- стан патологических изменений обнаружено не было ни одного исследуемого. Белок, глюкоза, ацетон, печеночные пигменты, эритроциты, цилиндры, соли в анализах мочи не определялись. Это свидетельствует об отсутствии у изучаемого лекарственного средства нефротоксического эффекта.
Динамика биохимических показателей крови, характеризующая влияние препарата на функцию пече-
Таблица №4. Биохимические показатели крови
|
Показатели |
До лечения |
Ч/з 2 мес. лечения |
|
Общий холестерин, ммоль/л |
5,2±0,5 |
3,6±0,8* |
|
Триглицериды, ммоль/л |
1,56±0,1 |
1,35±0,11* |
|
Общий белок, г/л |
67,4 ±3,2 |
74,3±3,7* |
* p<0,05
- Lue TF, Giuliano F, Montorsi F, et al. Summary of the recommendations on sexual dysfunctions in men. J Sex Med 2004; 1:6–23.
- Feldman HA, Goldstein I, Hatzichristou DG, Krane RJ, McKinlay JB. Impotence and its medical and psychosocial correlates: results of the Massachusetts Male Aging Study. J Urol 1994; 151:54–61.
- Perez C. Martinez C. Therapy with sildenafil for ED, why to wait one hour? 15th World Congress of Sexology 24 June 2001 Abstract Book: 182.
- Esposito K, Giugliano F, Di Palo C, et al. Effect of lifestyle changes on erectile dysfunction in obese men: a randomized controlled trial. JAMA 2004; 291:2978–84.
- Kostis JB, Jackson G, Rosen R, et al. Sexual dysfunction and cardiac risk (the Second Princeton Consensus Conference). Am J Cardiol 2005; 96:85 M-93M.
- Лопаткин Н.А. Руководство по урологии. В 3 т.- М.: Медицина. 1998, т-2, гл.24. - 768с
- Тиктинский О.Л. Руководство по андрологии. Л.: Медицина,1990. -416с.
- Hatzimouratidis K, Burnett AL, Hatzichristou D, McCullough AR, Montorsi F, Mulhall JP. Phosphodiesterase type 5 inhibitors in postprostatectomy erectile dysfunction: a critical analysis of the basic science rationale and clinical application. Eur Urol 2009; 55:334–47.
- Протич М., Цветков Д. и соавт. Клиническое испытание препарата трибестан на инфертильных мужчинах. // Акушерство и гинекология. — 1983. — Т.12, № 4. — С. 326–329, (болг.яз.)
- Трибестан – фиторегулятор работы эндокринной системы организма. Опыт применения. / Под ред. М.Е. Чалого, О.Н. Сепп, С.В. Ларина, И.В. Хайкова. — М.: 2006. — 50с.
- Kostova I, Dinchev D. Saponins in Tribulus terrestris – chemistry and bioactivity. Phytochem Rev. 2005; 4:111– 37.
- Xu YJ, Xu TH, Zhou HO, Li B, Xie SX, Si YS, et al. Two new furostanol saponins from Tribulus terrestris. J Asian Nat Prod Res. 2010; 12:349–54. [PubMed]
- Wu TS, Shi LS, Kuo SC. Alkaloids and other constituents from Tribulus terrestris. Phytochemistry. 1999; 50:1411–5.
- Santos CA Jr, Reis LO, Destro-Saade R, Luiza-Reis A, Fregonesi A. Tribulus terrestris versus placebo in the treatment of erectile dysfunction: A prospective, randomized, double blind study. Actas Urol Esp. 2014 May; 38(4):244-8.
- Amin A, Lotfy M, Shafiullah M, Adeghate E. The protective effect of Tribulus terrestris in diabetes. Ann N Y Acad Sci. 2006; 1084:391–401.
- Khan S, Kabir H, Jalees F, Asif M, Naquvi KJ. Antihyperlipidemic potential of fruits of Tribulus terrestris linn. Int J BiomedRes. 2011; 2:98–101.
- Tuncer MA, Yaymaci B, Sati L, Cayli S, Acar G, Altug T, Demir R. Influence of Tribulus terrestris extract on lipid profile and endothelial structure in developing atherosclerotic lesions in the aorta of rabbits on a high-cholesterol diet. Acta Histochem. 2009;111:488–500.
- Rosen R.C., Riley A., Wagner G. et al. The International Index of Erectile Function (IIEF): a multidimensional scale for assessment of erectile dysfunction // Urology. 1997; 49:822-830.