АННОТАЦИЯ
Изучен персистентный потенциал условно-патогенных микроорганизмов, возбудителей воспалительного хронического процесса при соматической патологии. Искусственное культивирование аэробов и факультативных анаэробов проведено общеизвестными способами. Статистическая обработка выполнена с использованием методов вариационной статистики. Достоверность показателей оценивалась определением критерия Стьюдента t >0,95. Выявление причинно-следственных связей признаков проводилось регрессионным анализом. Установлена взаимосвязь с антибиотикорезистентностью в среднем в 75,0±2,84 % случаев. Фактически среди изучаемых клинических изолятов УПМ (включая этиопатогены из числа представителей резидентной флоры), две трети (75,3 %) составляли штаммы с множественной и формирующейся устойчивостью к антибактериальным препаратам. Настоящий биологический признак, выявленный у изолятов, допустимо отнести к варианту эволюционно-адаптационной изменчивости в условиях организма пациента. На основании многофакторного анализа выявлены причинно-следственные связи между полирезистентностью штаммов и признаками персистенции, что позволяет расценивать эти свойства микроорганизмов не только как результат реализации потенциала УПМ in vivo, указывающий на безусловную их причастность к возникновению воспалительного процесса любой локализации, но и рекомендовать их как диагностический критерий дифференциации истинных возбудителей от представителей нормофлоры. Установлена высокая информативность 4-х из 5 персистентных признаков клинических изолятов при изученных соматических патологиях, при высоких уровнях СПА - 99,5% случаев, гемолитическая активность - 82,0%, АЛА - 62,4% и СИКА - 56,1 % при низких показателях уреазной активности, в сочетании с полирезистентностью к антибактериальным препаратам влияли на эволюционноадаптационный потенциал микроорганизмов, способствуя хронизации воспалительного процесса.Соответственно изучение персистентного потенциала штаммов, является основополагающим при организации мер по предупреждению возникновения осложнения заболеваний различных систем у пациентов, а также для раннего выявления "госпитальных" штаммов.
Персистенция микробов - одна из важных составляющих, которая обладает способностью патогенных видов микроорганизмов к длительному выживанию (переживанию) в организме хозяина [13]. Именно персистенция свидетельствует о неспособности общества и макроорганизма совладать с микроорганизмом и о возможности последнего выжить в макроорганизме. Механизмы развития персистенции многообразны. Отличительная черта персистенции в том, что она развивается на фоне обретенного иммунитета, который оказывается неэффективным, и что для некоторых бактерий она является патогенетической нормой [ɪ4].
Длительное переживание (персистенция) микроорганизмов, в том числе условно-патогенных (УПМ), в организме больных может быть обусловлено их свойствами. В персистировании микроорганизмов имеют значение их индифферентность к воздействующим внешним факторам физико-химической природы, обеспечение стабильных антагонистических эффектов в биоценозе и сохранением жизнеспособности популяции за счёт приобретения устойчивости к защитным механизмам хозяина [15]. Познание общепатологических механизмов болезни существенно облегчает анализ узловых проблем инфекционного процесса. Эволюционное становление воспалительной реакции определялось прежде всего бактериальной инвазией, что убедительно показано еще И.И. Мечниковым [16,17].
В специальной литературе совокупность подобных свойств общепринято называть персистентным потенциалом, понимая под этим результат микробной эволюции, сформированный под действием "негативного" воздействия на него факторов неспецифической защиты организма пациента.
Цель исследования - изучение персистентного потенциала условно-патогенных микроорганизмов (УПМ) - возбудителей хронического воспалительного процесса при соматической патологии.
Материалы и методы: для изучения персистентных свойств были взяты штаммы, выделенные из различных экологических ниш с учетом клинически установленного диагноза за период 2005-2009 гг. Забор и транспортировка мокроты, мочи, мазков с задней стенки глотки осуществлялись в соответствии с приказом Минздрава СССР № 535 от 1985 г. "Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностических лабораториях лечебно-профилактических учреждений” [18], а также публикацией М.Н.Зубкова [19].
Для доставки биоптатов с СОЖ и СОДПК с целью обеспечения жизнеспособности микроорганизмов с различным способом дыхания успешно зарекомендовала себя среда Кери- Блер фирмы "HiMedia MS-202".
Забор и транспортировка фекалий осуществлялись в соответствии с методическими указаниями М3 PK № 10.05.044.03 "Бактериологическая диагностика дисбактериоза кишечника” [20]. Искусственное культивирование аэробов и факультативных анаэробов вне зависимости от вида клинического материала, проводилось общеизвестными способами в соответствии с приказом М3 СССР № 535 от 1985 г. "Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностических лабораториях лечебно-профилактических учреждений" [18].
Для выделения облигатно-анаэробных микроорганизмов условия анаэробиоза обеспечивались газорегенераторными пакетами Anaero Gas Pack (HiMedia). Селективность среды обеспечивалась путем добавления к питательной основе канамицина (100 мг/л) и 5 % крови. Условия для изоляции нормируемых видов микроорганизмов при исследовании фекалий проводились в соответствии с методическими указаниями М3 PK № 10.05.044.03 "Бактериологическая диагностика дисбактериоза кишечника" [20].
Для культивирования микроаэрофилов, поиск которых велся при исследовании биоптатов, в питательную среду вносилась селективная добавка FD-178, состоящая из ванкомицина, цефоперазона, амфотерицина В и пирувата 5 % крови, использовали газорегенераторные пакеты Anaero HiGas - Campylo PackLE002D фирмы "HiMedia". Данные пакеты в анаэрос- тате обеспечивают продукцию газовой смесью, содержащей 5 % кислорода, 5-10 % углекислого газа, 85-90 % азота. Газорегенераторный пакет одновременно с засеянными агаровыми чашками закладывается в анаэростат на 2-7 суток при температуре 37 0C. При этом первичная оценка наличия роста на поверхности IIIA регистрируется во 2-е сутки. В дальнейшем посевы заново закладываются с обязательным использованием газорегенераторного пакета в анаэростат с последующим просмотром на 3-, 4-, 5-, 6- и 7-е сутки.
В зависимости от происхождения клинического материала применялись 3 метода посева, 2 из которых - количественные: метод Голда и метод десятикратных серийных разведений, и качественный (прямой) метод посева. Для осуществления посева мокроты, мочи, мазков со слизистой задней стенки глотки применен метод секторных посевов по Голду, подробно описанный в работах некоторых авторов [18,19,21]. Идентификация клинических изолятов осуществлялась общепринятыми методами, предлагаемыми в приказе Минздрава СССР № 535 от 1985 г. "Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностических лабораториях лечебно-профилактических учреждений" [18].
Также в работе использованы схемы- "ключи" идентификации, защищенные предварительными патентами: № 17800 от 2006 г. "Способ идентификации микроаэрофилов", № 18874 от 2007 г. "Способ идентификации энтеробактерий", №19106 от 2008 г. "Способ идентификации стрептококков" и № 22776 от 2010 г. "Способ идентификации грамположи- тельных кокков” [22-25]. Все способы были разработаны на основе 9-го определителя Берджи [26].
Исследованы 226 клинических изолятов, среди которых были 92 культуры респираторных штаммов, 61 культура уроштаммов,36 культур клинических биоптатов со слизистого желудка (СОЖ)и 12-перстной кишки (СОДПК) и 37 копрокультур.
Метод определения антилизоцимной активности микроорганизмов (АЛА) подробно описан в работах О.В.Бухарина [27,28], способ выявления у бактерий ингибиторов каталазы микрорганизмов - в работе [29]. Для определения адгезивной активности выделенных микроорганизмов использовали эпителиальные клетки со слизистой щек. Забор эпителиоцитов и их обработку проводили по методу, предложенному В.И.Брилисом. Степень адгезивности штаммов оценивалась также в соответствии со шкалой значений индекса адгезивности по В.И.Брилису [30].
Статистическая обработка анализируемого материала проводилась с использованием методов вариационной статистики с вычислением средней арифметической, средней ошибки. Рассчитывались экстенсивные показатели, при оценке достоверности которых также вычислялась средняя ошибка гл.
Достоверность различия показателей оценивалась в соответствии с критерием Стью- дента. Уровень доверительной вероятности › 0,95 (P<0,05).
При анализе динамических рядов вычислялись темпы роста (снижения) [31]. Построение математических моделей и прогнозных расчетов осуществлялось с использованием прикладной программы STATEXS. Количественные зависимости между признаками изучались при помощи регрессионного анализа и множественной корреляции для выявления причинно-следственных связей между ними. Уравнение множественной регрессии более достоверно отражает долю вклада каждого фактора и объективную закономерность - наличие причинно-следственной связи.
Результаты и обсуждение. Одним из изученных свойств являлась антилизоцимная активность (АЛА), которая широко распространена среди различных клинических изоля- тов. Известно, что подавление лизоцима при патологии инфекционного генеза обусловлено способностью возбудителя инактивировать мурамидазу - важнейшее звено неспецифической резистентности [32]. Ранее была доказана связь наличия этого признака с воспалительными изменениями. Для повышения точности количественной оценки антилизоцимной активности нами был применен метод О.В. Бухарина (2000) [33, 34], при котором активность ан- тилизоцимного фактора была прямо пропорциональна оптической плотности. Показатель антилизоцимной активности исследуемой культуры определяли по формуле с последующим установлением концентрации лизоцима, способной инактивировать эту культуру.
Второе свойство - это средний показатель адгезии (СПА), которую общепринято рассматривать как начальный и необходимый этап развития инфекционного процесса. Бактериальные адгезины играют важную роль в проникновении микроорганизмов из нижних отделов в верхние [35], поэтому вполне закономерен интерес к изучению адгезивной активности, как фактора патогенности микроорганизмов вне зависимости от таксономической принадлежности и места локализации возбудителя. Данный исследуемый признак УПМ имеет общебиологическое значение и, следовательно, позволяет получить дополнительную информацию о вирулентности штамма.
Третье свойство - это степень ингибиции каталазной активности S.aureus (СИКА), позволяющая определить путь инфицирования (экзогенный или эндогенный) и подтвердить этиологическую значимость выделенных штаммов [29].
Высокие показатели степени ингибиции каталазы являются свидетельством естественной принадлежности изучаемого микроорганизма к аутофлорс, рассматриваемой экологической ниши и, следовательно, длительной персистенции. Низкие показатели CHKA указывают на экзогенное происхождение микроорганизма в противовес нормальной микрофлоре. При этом полученные низкие показатели могут быть основополагающим признаком в определении этиологической роли выделенного изолята, даже в случае низких количественных значений об- семененности.
Четвертое свойство - это гемолитическая активность, которая позволяет оценить секрецию гемолизинов как факторов патогенности. Гемолизины, являясь экзотоксинами, могут быть причиной тяжелого, затяжного течения заболевания.
И, наконец, пятое свойство - это уреазная активность, характерная для этиопатогенов желудочно-кишечных и урологических инфекционных процессов, возникающих у госпитали-
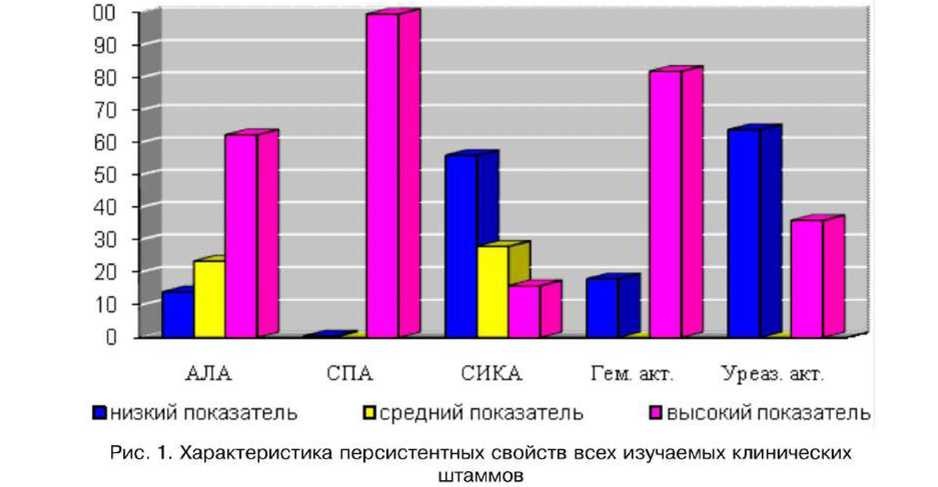
тированных больных, в подавляющем большинстве случаев имеющих микроэкологические и иммунные нарушения [36-38]. Под действием фермента уреазы происходит расщепление мочевины и, как следствие, повышается pH мочи. Сдвиг pH в щелочную сторону способствует поддержанию воспалительного процесса и камнеобразованию. Гемолитическая и уреазная активность изучалась общепринятыми методами [27, 29, 39]. Изучение персистентных свойств с помощью 5 методов показало широкое распространение антилизоцимных и адгезивных признаков, о чем свидетельствуют высокие показатели: АЛА у 62,4+3,22 % штаммов и СИЛ у 99,5+0,46 % штаммов, представленных на рис. 1. В этой связи можно отметить, что чем выше активность признаков персистентного потенциала у клинических штаммов УПМ, тем больше усиливается способность их к выживанию in vivo.
Свидетельством тому являются, кроме указанных свойств, отраженные на диаграмме, у большинства штаммов значения по продукции гемолизинов, зарегистрированные у 82+2,55 % штаммов. Далее по зарегистрированным значениям СИКА у изучаемых штаммов нас интересовал низкий процент активности, поскольку именно он указывал на экзогенный характер инфицирования и происхождение микроба, подтверждая этиологическую роль микроорганизма. В наших исследованиях он выявлен у 56,1+3,3 % штаммов.
Сравнительный анализ копроштаммов, респираторных и уроштаммов, а также культур, выделенных из биоптатов, по оценке персистентных свойств изолятов, выделенных из различных биотопов, показал, что при изучении АЛА выявлено процентное превосходство высоких значений у 89,2+2,06 % копроштаммов. У УПМ, выделенных из СОЖ и СОДПК, это свойство обнаружено у 63+3,21 % штаммов. Несколько реже выявлены высокие показатели АЛА у респираторных изолятов и уроштам мов, составившие 57,6+3,28 % штаммов и 52,4+3,32 % штаммов соответственно.
Делать выводы по зависимости адгезивной активности у УПМ клинических изолятов от наличия распространенности АЛА несколько преждевременно, ведь адгезивные свойства выявлены у 100 % уроштаммов и культур, выделенных из СОЖ и СОДПК с высокими значениями. Незначительно отличаются по данному признаку и показатели респираторных штаммов, составившие 98,9+0,69 %.
В отношении изученной нами уреазной активности обнаружено данное свойство лишь у незначительного числа культур:
- у уроштаммов в 49,2+3,32 % случаев,
- у клинических изолятов, выделенных из биоптатов в 47,2+3,32 %,
- у респираторных изолятов этот признак установлен лишь в 22,8+2,79 % штаммов.
Уреазная активность среди УПМ по уровню обнаружения уступает двум вышеупомянутым признакам. Возможно, ее наличие связано с биологическими различиями в таксоно-
мической характеристике, При этом доказано, что урсазопозитивныс условно-патогенные энтеробактерии являются причиной желудочно- кишечных заболеваний.
В противовес распространенность выявления гемолитической активности зарегистрирована у большинства клинических изолятов:
- у респираторных штаммов - в 84,7±2,39 % случаев,
- среди уроштаммов - в 78,7±2,72 %,
- среди выделенных из биоптатов СОЖ, СОДПК - 80,6±2,63 %.
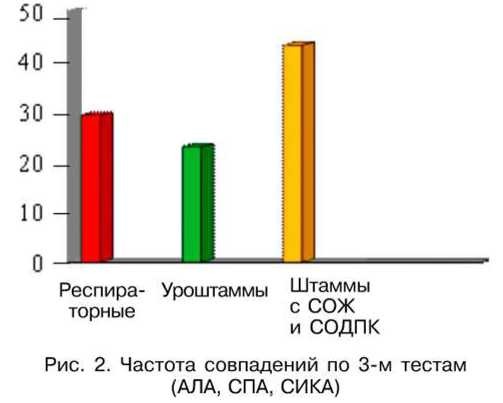
На наш взгляд, представляло интерес выявление относительной доли совпадений у культур персистентных свойств по 3 из 5 изученных тестов - АЛА высокие + СПА высокие + низкие значения СИКА.
В соответствии с данными преимущество в процентном соотношении по наличию вышеупомянутых признаков составляет 43,2±3,29 % штаммов и приходится на изоляты, выделенные из СОЖ и СОДПК. Следующими по частоте обнаружения высоких значений АЛА СПА и низких значений СИКА являлись респираторные культуры, составившие 29,3±3,0 %. Среди уроштаммов уровень совпадений достиг 23±2,8 %.
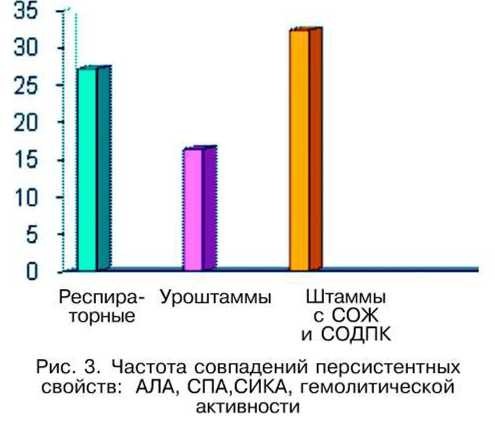
Далее нами разбирался другой вариант суммы совпадений уже 4-х признаков, приобретенных клиническими изолятами: выявление высоких значений АЛА, СПА, низких СИКА и обнаружение гемолитической активности. Как видно (рис. 3), лидирующее положение вновь занимают штаммы, выделенные из биоптатов СОЖ и СОДПК, составившие 32,4±3,11 %. На втором месте зарегистрированы респираторные штаммы - 27,2±2,96 %, и с 4-мя совпадениями выявлено лишь 16,4±2,46 % уроштаммов. Безусловно, комплексно оценивая установленные значения приобретенных свойств УПМ, представляется возможным трактовать эти особенности как "адаптивные решения" микроорганизмов, ведь посредством приобретения персистирующих свойств микроорганизмами, в условиях организма пациента, клинические изоляты противостоят естественной защите организма человека.
Вполне очевидной является возникшая возможность негативного влияния микроба и на степень, и на длительность клинического течения заболевания.
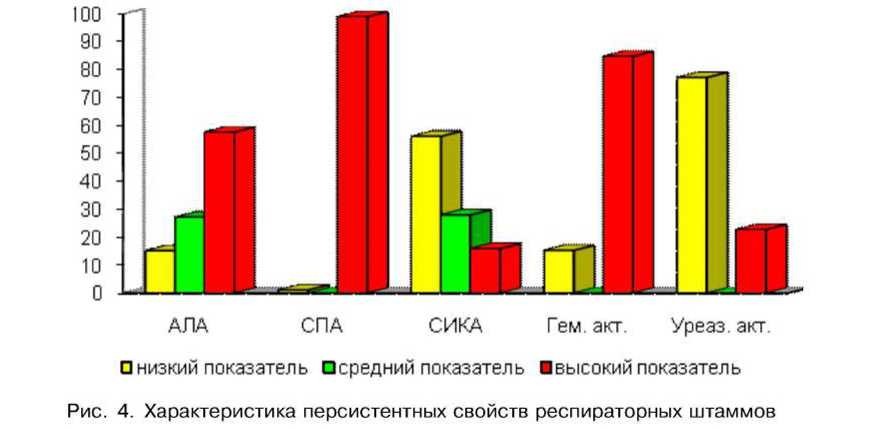
Как видно из представленного рис. 4, изученные нами 92 респираторных штамма от больных с заболеваниями верхних дыхательных путей (ВДП) и нижних дыхательных путей (НДП) обладали высокими значениями AJTA в 57,6±5,15 % случаев, высокими значениями СПА - в 98,9±l,08 %, низкими, но информативными, значениями СИКА - в 56,1±5,1 % случаев. Гемолитической активностью обладали в 84,7±3,75 % случаев при низкой уреазной активности, которая была выявлена лишь в 22,8±4,37 % случаев.
Для анализа результатов изучения антибиотикорсзистснтности клинически значимых штаммов и их связи с данными по выявлению персистентного потенциала. Все случаи совпадений по 4-м признакам персистенции были приняты за 100 %. Так, среди штаммов, выделенных с СОЖ и СОДПК, в 77,8±6,92 % случаев высокие значения АЛА и СПА в комбинации с низкими данными СИКА и наличием гемолитической активности совпадали с их
полирезистентностью к антибиотикам. В отношении респираторных штаммов такая зависимость установлена в 84,8±5,96 % случаев. Среди уропатогенов коррелятивная связь обнаружена в 62,3±8,01 % случаев.
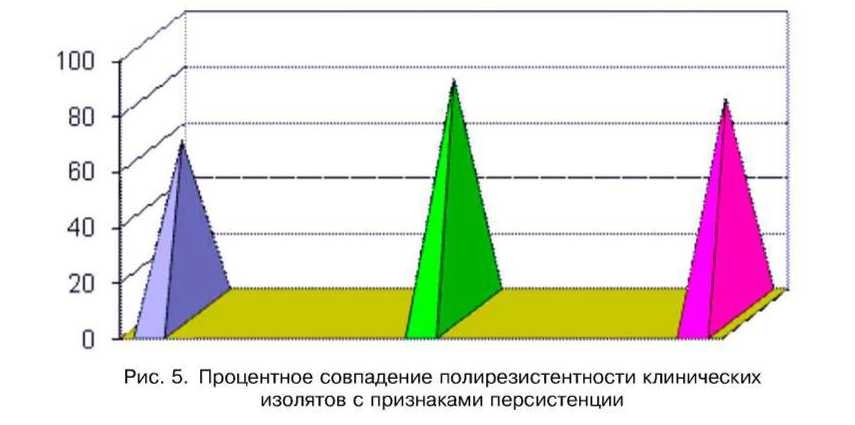
Анализ результатов изучения персистентного потенциала штаммов, выделенных их 3-х источников (экологических ниш) (рис. 5), показал совпадение высоких значений АЛА, СПА, низких значений СИКА и наличие гемолитической активности с полирезистентностью клинических изолятов к антибиотикам. Среди респираторных штаммов такая зависимость установлена в 84,8÷3,72 % случаев, среди штаммов, выделенных с СОЖ и СОДПƘ - 77,8±6,94 %, среди уропатогенов - в 62,36±6,22 % случаев.
Таким образом, при анализе полученных данных по изучению персистентных свойств (АЛА, СПА, СИКА, гемолитическая активность) клинически значимых штаммов, изолированных из 3-х экониш, установлена взаимосвязь с антибиотикорезистентностью в среднем - в 75,0±2,84 % случаев. Следовательно, факт получения полирезистентности клинических штаммов, выделенных из любой экологической ниши пациента с хронической патологией, допустимо принимать за косвенный признак персистентного потенциала этиопатогена.
Изучение количественных зависимостей между названными явлениями проводилось при помощи регрессионного многофакторного анализа и при полной адекватности сравниваемых факторов. Большой интерес представили причинно-следственные связи между полирезис- тентностыо к антибиотикам, присущей различным видам микроорганизмов, выделенных из различных органов и систем (респираторного тракта, мочевыводящей системы, слизистой
желудка и 12-псрстной кишки, толстого кишечника), определяющих персистентный потенциал этих патогенов в формировании хронической патологии. Данные взаимосвязи могут быть определены:
Коэффициент корреляции 0,9 показывает выраженную положительную связь, т.е. рост количества энтерококков с высокими значениями СПА отражает рост количества колоний энтерококков с полирсзистснтностью. Выраженная отрицательная связь - 0,91 показывает, что если рост количества энтерококков с низкими значениями СИКА совпадает с достоверным снижением количества энтерококков полирезистентных, то коэффициент детерминации 90,1 % свидетельствует о хорошем качестве связи, а полученная зависимость и результаты исследований достоверны:
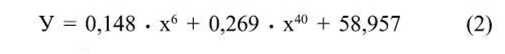
Полирезистентность энтерококка зависит на 41,7 % от роста количества энтерококков с высокими значениями СПА и на 48,4 % от уменьшения количества энтерококков с низкими значениями СИКА. Эта зависимость прослеживается во всех объектах исследований - респираторные штаммы, штаммы, выделенные с СОЖ и СОПДК, и уроштаммы. Коэффициент вариации показывает, что эти данные стабильны и их влияние достоверно (таблица и уравнение регрессии (1).
Таким образом, изучение персистентного потенциала клинических изолятов (этиопатоге- нов) некоторых органов и систем позволяет использовать комплексный подход в оценке биологических свойств этиопатогенов для коррекции антибактериальной терапии и понимания причин длительного вегетирования микроорганизмов в организме пациентов с хронической формой соматических заболеваний. Фактически среди изучаемых нами клинических изолятов УПМ (включая этиопатогены из числа представителей резидентной флоры), две трети (75,3 %) составляли штаммы с множественной и формирующейся устойчивостью к антибактериальным препаратам. Настоящий биологический признак, выявленный у респираторных изолятов, допустимо отнести к варианту эволюционно-адаптационной изменчивости в условиях организма пациента.
На основании вышеприведенного уравнения и расчета многофакторного анализа видно, что существуют причинно-следственные связи между выявленными микробиологическими исследованиями полирезистентности штаммов, выделенных из различных экологических ниш человека, и изученными признаками персистенции. Микроорганизмы различных таксономических групп, выделенные из различных экологических ниш, относительно в равной степени проявляли свой персистентный потенциал. Полученные нами сведения о фенотипической изменчивости (диссоциация культуры, изменение биохимических свойств), высокие показатели антилизоцимной, адгезивной, гемолитической активности, низкая степень ингибиции каталазы, присущие клинически значимым изо- лятам УПМ, определение частоты встречаемости этих признаков, безусловно, связаны с особенностями организации структуры различных видов микроорганизмов.
Проведенный совокупный анализ позволяет расценивать эти свойства микроорганизмов не только как результат реализации потенциала УПМ zw vivo, указывающий на безусловную их причастность к возникновению воспалительного процесса любой локализации, но и рекомендовать их как диагностический критерий дифференциации истинных возбудителей от представителей нормофлоры. Установленные среди УПМ базовые признаки персистенции в

совокупности с полирезистентностью к антибактериальным препаратам приводят к длительному их вегетированию на слизистой исследованных органов и систем с параллельной хронизацией воспалительного процесса.
Высокий процент совпадений полирезистентности и других факторов персистенции у клинических штаммов, выделенных из любой экологической ниши пациента, позволяет считать множественную лекарственную устойчивость признаком персистентного потенциала этиопатогена, вызывающего длительное течение заболевания. Соответственно информация, полученная по изучению персистентного потенциала штаммов, выделенных от пациентов с хронической формой соматической патологии, способна стать основополагающей для применения при организации мер по предупреждению возникновения осложнения заболеваний одной из рассматриваемых нами систем, раннего выявления "госпитальных” штаммов, также для осуществления прогнозно-аналитических исследований в регионах PK.
Выводы
Установлена высокая информативность четырех из пяти персистентных признаков клинических изолятов при изученных соматических патологиях. Доля высоких результатов была выше при СПА - 99,5 % случаев, гемолитическая активность - 82,0 %, АЛА - 62,4 % и СИКА - 56,1 % при низких показателях уреазной активности. Эти данные в сочетании с полирезистентностью к антибактериальным препаратам влияли на эволюционно-адаптационный потенциал микроорганизмов, способствуя хронизации воспалительного процесса. На основании проведенных исследований можно сделать практические рекомендации. Поскольку в практическом здравоохранении внедрение методики определения АЛА, безусловно, представляет сложности воспроизведения, предлагается ограничиться восприятием полирезистентности и атипичности штаммов как косвенных показателей персистентного потенциала.
ЛИТЕРАТУРА
- Громаиıевский Л.В. Общая эпидемиология. - M., 1941. - 324 с.
- Давыдовский И.В. Общая патология человека. - M.: Медицина, 1969. - 612 с.
- Саркисов Д.С., Пальцев М.А., Хитрое Н.К. Общая патология человека. - M., 1997. - 3257 с.
- Саркисов Д.С. Патогенез туберкулеза // Проблемы туберкулеза. - 2000. - № 5. - С. 3-6.
- Анохин ПК. Узловые вопросы теории функциональной системы. - M., Наука, 1980. - 196 с.
- Судаков К.В. Информационный феномен жизнедеятельности. - M., 1999. - 379 с.
- Зотин А.И., Зотин А.А. Направление, скорость и механизмы прогрессивной эволюции: термодинамические и экспериментальные основы. Ч. 4. // Макроскопические механизмы биоэнергетического прогресса. - M., 1999. - С. 252-291.
- Ceeepuoe А.С. Направленность эволюции. - M., 1990. - 272 с.
- Azzone G.F What is controlling life? // Innsbruck, 1994. - С.178-180.
- Гарганеева Н.П, Тетенев Ф.Ф. Психосоматическая ориентация в общей врачебной практике... // Клин, медицина. - 2001. - № 9. - С. 60-63.
- Абаев Ю.К. Эволюция болезней и нозологический принцип в медицине // Медицинские новости. - 2008. - №4. - С. 8-15.
- Лыкова А.Г., Боковой А.Г., Бурова А.А. и др. Персистенция пневмотропных возбудителей при острых бронхолегочных заболеваниях у детей // Микробиол. - 2000. - № 4. - С. 43-47.
- Персистенция - Академикđíс.асаđеɪпİс.пı›Большой медицинский словарь http://reftrend.ru/ 583745.html
- Бухарин О.В., Гинцбург А.Л., Романова Ю.М. и др. Механизмы выживания бактерий - M.: Медицина, 2005. - 367 с.
- Воũно-Ясенецкиũ М.В. Биология и патология инфекционных процессов. - Л.: Медицина, 1981. - 208 с.
- Пııменов Е.В., Тотолян А.А., Бывалое А.А. и др. Современные представления о патогенезе инфекционных болезней H Вести. РАМН. - 2003. - № 6. С. - 3-9.
- Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностических лабораториях лечебно-профилактических учреждений: приказ № 535 М3 СССР. - M., - 22.04.1985 г. - С. 15.
- Зубков М.Н. Сбор биологического материала для бактериологического исследования // Клин, микробиол. антимикроб, химиотерапия. - 2004. - № 2. - С. 144-148.
- Бактериологическая диагностика дисбактериоза кишечника H МУК М3 Республики Казахстан № 10.05.044.03. - Алматы, 2003. - 39 с.
- Фельдман Ю.М., Маханеева Л.Г., Шапиро А.В. и др. Количественное определение бактерий в клинических материалах // Лаб. дело. - 1988. - № 4. - С. 616-618;
- Баǔмуратова М.А., Воронина В.Э., Тулепбаева С.Ж., Светлова З.С. Предварительный патент Республики Казахстан № 17800 "Способ идентификации микроаэрофилов" // Бɪол. PK "Промышленная собственность". - 2006. - № 9. - С. 19-20.
- Баǔмуратова М.А., Воронина В.Э., Есенаманова Т.Б., Абишева Д.С., Тасмагамбето- ва А.Е. Способ идентификации энтеробактерий: Предварительный патент Республики Казахстан № 18874 // Бюл. PK "Промышленная собственность". - 2007. - № 10. - С. 33.