Артериальная гипертония (АГ), являясь крупнейшей в мире неинфекционной пандемией, представляет собой одну из серьезнейших проблем современного здравоохранения [1]. Прогрессирование данного заболевания значительно увеличивает риск развития таких тяжелых осложнений, как инфаркт миокарда, мозговой инсульт, сердечная и почечная недостаточности, а высокие показатели смертности определяют значимость проблемы для общества [2].
По данным мировой статистики, в последние десятилетия отмечается неуклонный рост хронической обструктивной болезни легких (ХОБЛ) [3]. В структуре заболеваемости ХОБЛ входит в число лидирующих по числу дней нетрудоспособности, причинам инвалидности и занимает четвертное среди причин смерти в промышленно развитых странах [4]. Заболеваемость ХОБЛ составляет 7-8% у взрослого населения, неуклонно растет и доминирует в структуре хронических легочных заболеваний, составляя около 90% [5].
АГ и ХОБЛ представляют одно из частых коморбидных состояний в клинике внутренних болезней [6]. По данным последних исследований АГ выявляется у больных ХОБЛ с частотой от 6,8% до 76,3%, составляя в среднем 34,3% [7, 8]. Частота аддитивности АГ с ХОБЛ и их ведущие единые стратификационные факторы риска в Казахстане, в частности в его крупнейшем мегаполисе в городе Алматы, не определены.
В связи с вышеизложенным, целью настоящего исследования явилось определение по результатам скрининга репрезентативной выборки населения г.Алматы частоты встречаемости и ведущих стратификационных факторов риска артериальной гипертонии в сочетании с хронической обструктивной болезнью легких.
Материал и методы
Источником формирования выборки явилось взрослое население, проживающее в Медеуском районе г.Алматы. Данный район в качестве объекта исследования был выбран из других городских районов в результате простой рандомизации методом «закрытых конвертов». Из общего числа взрослого населения в возрасте 30-65 лет методом таблицы случайных чисел была отобрана 10% выборка из 5905 человек. Репрезентативный размер последующей выборки был определен методами эпидемиологического анализа с учетом распространенности АГ среди городских жителей Казахстана (52%), согласно данным Б.У. Абдукаримова и соавт. (2004), с заданной ошибкой выборки (±3%) и доверительным интервалом (99%) [9]. С этой целью был использован сайт Свердловского Общества Доказательной медицины (www.OSDM.org) (рисунок 5).
Согласно расчету, для получения достоверных данных, объем выборки должен был составить 1090 человек. Для минимизации ошибки выборки и увеличения степени участия населения в исследовании, окончательный размер репрезентативной выборки составил 1200 респондентов,

отобранных по таблице случайных цифр.
С каждым потенциальным респондентом был установлен контакт по телефону. В ходе телефонного опроса состав выборки был окончательно уточнен, и ее общая численность составила 870 человек, т.е. отклик на исследование по телефону составил 72,5%. Для достижения контакта с респондентом допускалось до 5 попыток дозвона по каждому телефонному номеру. 556 (64%) респондентов были опрошены в ходе первой попытки телефонного контакта. 314 (36%) респондентов были проинтервьюированы после 3-й попытки. Откликом на исследование считали согласие в проведении телефонного опроса. За отсутствие отклика считали отказ от участия в проведении опроса, случаи не установления контакта с респондентом, невозможность проведения опроса по другим причинам (незнание казахского, русского языков, психически болен) [10].
В ходе телефонного опроса были заданы следующие вопросы: 1). Знаете ли Вы цифры своего артериального давления (АД)? 2). Какое у Вас систолическое (верхнее) АД? 3). Какое у Вас диастолическое (нижнее) АД? 4). Принимали ли Вы последние 2 недели лекарства, понижающие АД?
К респондентам, приглашенным для дальнейшего обследования были отнесены лица, указавшие на: 1). Наличие САД≥140 и/ или ДАД ≥ 90 мм рт.ст. 2). Наличие САД<140 мм рт.ст. и ДАД<90 мм рт.ст., при приеме гипотензивных препаратов последние 2 недели. В случае отсутствия возможности самостоятельной регистрации АД респондентами, его измерение производилось исследователями в условиях клиники.
В результате из 870 респондентов АГ была верифицирована у 418 человек, которые подверглись дальнейшему анкетированию и скрининговому обследованию с целью выявления сопутствующей ХОБЛ. В результате анкетного и спирометрического скрининга было выявлено 92 больных АГ с респираторными симптомами и признаками бронхиальной обструкции.
Обследование включало опрос по сокращенному варианту опросника CINDI [11, 12] (паспортные данные, жалобы, сведение о курении, семейном анамнезе ранних ССЗ, приеме антигипертензивных препаратов в течение 2 недель до обследования, перенесенных осложнений АГ); трехкратное измерение АД; подсчет частоты сердечного сокращения (ЧСС); измерение роста, массы тела, объема талии (ОТ) и объема бедер (ОБ); запись ЭКГ покоя; исследование уровней глюкозы и общего холестерина (ОХС) крови.
Отношение к курению выясняли при помощи стандартного опроса. К курильщикам относились лица, выкуривающие не менее 1 сигареты или папиросы в день. К некурящим относились лица, не употребляющие табачные изделия либо курящие от случая к случаю (не ежедневно) [13].
Согласно Рабочим критериям экспертов Национального института здоровья США 2002 г. (Adult Treatment Panell III -ATR III) абдоминальный тип ожирения выявляли при ОТ ≥102 см у мужчин и ≥88 см у женщин [14].
ЭКГ регистрировали на аппарате «Nihon Konden ECG- 9320K» в положении лежа в 12 стандартных отведениях. ЭКГ-признаки гипертрофия ЛЖ (ГЛЖ) определяли по индексу Соколова-Лайона (Sv1 + Rv5/v6 >35 мм у лиц старше 40 лет и >45 мм у лиц моложе 40 лет), а также по Корнельскому вольтажному индексу (Ravl + Sv3 >28 мм у мужчин и >20 мм у женщин) [15].
Лодыжечно-плечевой индекс (ЛПИ) определяли ртутным монометром по соотношению уровней САД, измеренного на плече и в области лодыжки. Согласно рекомендациям Европейского общества по АГ 2007 г. снижение ЛПИ менее 0,9 свидетельствует о поражении сосудов.
Определение уровней глюкозы и ОХС крови проводили в утренние часы натощак c с помощью портативного набора «Accutrend® GC» тест-полосками «Accutrend® Glucose» и «Accutrend® Cholesterol» фирмы «Roche». Значения сывороточных уровней глюкозы крови натощак≥5,6 ммоль/л и ОХС>5,0 ммоль/л согласно рекомендациям Европейского общества по АГ 2007 г. принимали за повышенные [16].

Для выявления респираторных симптомов всем пациентам с АГ был осуществлен анкетный скрининг с помощью стандартизированного вопросника, рекомендованного GOLD [17].
Далее всем исследуемым лицам с АГ, независимо от наличия или отсутствия респираторных симптомов, проводилась скрининговая спирометрия на портативном электронном аппарате «Спиротест УСПЦ – 01».
Анализировались следующие показатели функции внешнего дыхания: форсированная жизненная емкость легких (ФЖЕЛ), объем форсированного выдоха за 1-ю секунду (ОФВ1), индекс Тиффно (ОФВ1/ ФЖЕЛ). Полученные данные спирографии оценивались по номограмме, сравнивая с должными величинами, соответствующими полу, возрасту и росту.


ХОБЛ верифицировалась при соответствии следующим условиям [18]: 1) хронический кашель с мокротой и одышка; 2) наличие факторов риска в анамнезе – действие табачного дыма, поллютантов внутри и вне помещения; 3) ОФВ1/ ФЖЕЛ <70% от должного и/или ОФВ1≤80% от должного.
Статистическая обработка полученных результатов производилась с использованием компьютерной программы «Statistica 6.0» («Statsoft», США). При проверке гипотезы о равенстве средних в двух независимых выборках использовали непарный критерий Стьюдента (в случае нормального закона распределения) и критерий Mann-Whitney (в случае закона распределения отличного от нормального). Дискретные величины сравнивали по критерию χ2 Pearson, коррекцию Yates применяли для таблиц сопряженности с 1-й степенью свободы (2х2). При сравнении набора частот в случае общего количества наблюдений менее 50 и количества наблюдений каждого варианта значения менее 7 использовали точный критерий Фишера. При сравнении 3-х групп использовали параметрические дисперсионный анализ (ANOVA) и критерий Стьюдента с поправкой Бонферрони, а также непараметрический критерий Kruskal-Walus. Данные представлены в виде M±m. Достоверными считали различия при p<0,05.
Результаты исследования
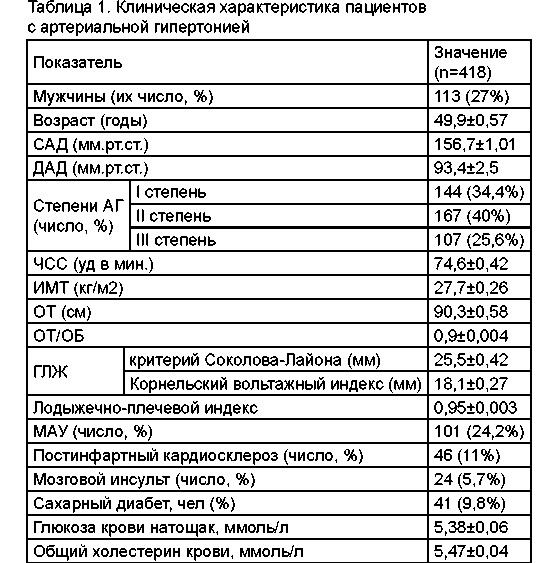
Из 870 лиц репрезентативной выборки г. Алматы артериальная гипертония была установлена у 418 пациентов, что составило 48%. Клиническая характеристика данных больных с АГ представлена в таблице 1. Отмечено преобладание среди выявленных лиц с повышенным АД пациентов со II степенью АГ (34,4%), среднего возраста (51,1±1,36 лет), повышенного питания (27,7±0,26 кг/ м2), женщин (73%). Средние значения глюкозы крови натощак и ОХС в целом по группе находились в пределах нормы.
Установлено, что пациенты с АГ имели значительное число факторов, неблагоприятно влияющих на прогноз развития ССО (таблица 2).
Наибольшее количество пациентов имели наследственную отягощенность по ранним ССЗ, гиперхолестеринемию и абдоминальное ожирение.
Распределение больных АГ по количеству стратификационных факторов риска, исключая гипертонию, представлено на рисунке 2. Не обнаружены факторы риска ССО лишь у 22 (5,3%) пациентов с АГ. У 89 (21,3%) больных выявлен один ФР, у 124 (29,7%) – два ФР, У 117 (30%) – 3 ФР, у 50 (12%) – 4 ФР, у 12 (3%) – 5 ФР и 4 (1%) – 6 ФР. В целом, три и более ФР ССО, органов-мишеней у пациентов с АГ мужского пола в сравнении с женским. При этом показано нарастание частоты гипертонического поражения сердца, сосудов и почек с увеличением возраста и уровня АД.
наличие которых является по Европейским рекомендациям по АГ 2007 г. критерием высокого/очень высокого сердечнососудистого риска, имели 43,7% больных АГ.
Дальнейшая оценка суммарного сердечно-сосудистого риска у пациентов с АГ предусматривала выявление гипертонического поражения органов-мишеней (таблица 3).
В результате установлена сопоставимая частота поражения сердца, сосудов и почек в целом по всей группе больных АГ (26,3; 21; 24,2% соответственно; χ2=3,2, р=0,2), отражающая процесс единого гипертонического ремоделирования.
Дальнейший опрос пациентов с помощью респираторного вопросника, а также проведение скрининговой спирометрии показал наличие у 92 (22%) пациентов с АГ респираторных симптомов и признаков бронхиальной обструкции.
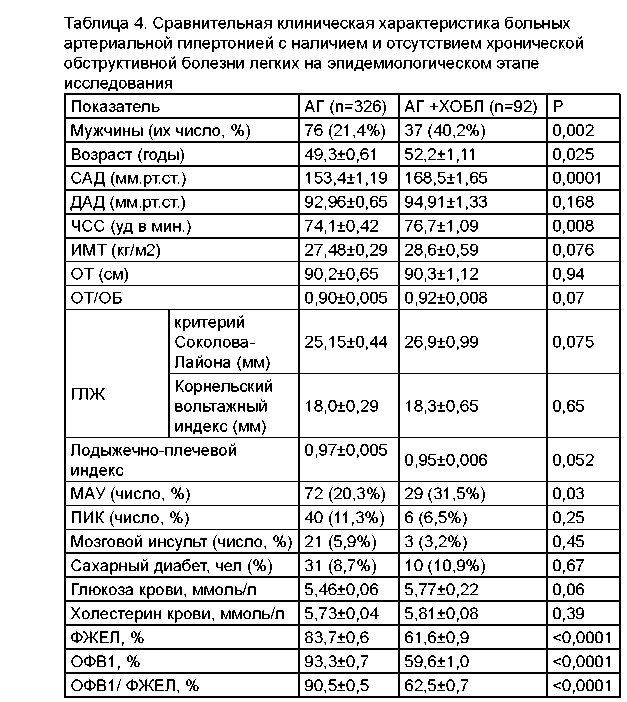
Клиническая характеристика по данным скрининговых методов исследования пациентов с АГ в сочетании с ХОБЛ в сравнении с больными АГ без ХОБЛ показана в таблице 4.
Оказалось, что больные АГ в сочетании с ХОБЛ, были частоты гипертонического поражения органов-мишеней (таблица 6).
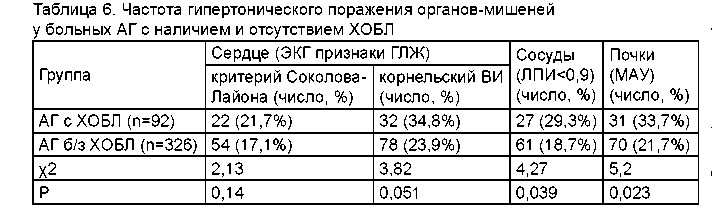
У больных АГ с сопутствующей ХОБЛ выявлено значимое преобладание частоты поражения сосудов (в виде снижения лодыжечно-плечевого индекса меньше нормативных 0,9), почек (в виде наличия микроальбуминурии) и тенденция к повышению частоты поражения сердца (в виде гипертрофии левого желудочка по критерию Соколова- Лайона и Корнельскому вольтажному индексу).
Далее мы сравнили частоту гипертонического поражения органов-мишеней у больных АГ с наличием и отсутствием ХОБЛ с учетом пола (таблица 7).
Показано, что гипертрофия ЛЖ по критерию Соколова- Лайона, сниженный лодыжечно-плечевой индекс и микроальбуминурия чаще встречались у больных АГ в сочетании с ХОБЛ мужского пола, а у женщин с АГ и ХОБЛ установлено повышение частоты поражения сосудов и почек.
Оценка встречаемости гипертонического поражения органов-мишеней у больных АГ с наличием и отсутствием ХОБЛ с учетом возраста, выявила у пациентов с АГ старше 50 лет преобладающую частоту встречаемости поражения сердца и сосудов при сочетании с ХОБЛ (таблица 8).
Сравнение частоты органного поражения у больных АГ с наличием и отсутствием ХОБЛ с учетом степени повышения АД, выявила у пациентов с АГ II-III степенями преобладающую частоту встречаемости поражения сердца и почек при сочетании с ХОБЛ (таблица 9).
Таким образом, результаты скринингового обследования случайной репрезентативной выборки населения г. Алматы показали, что распространенность ХОБЛ среди пациентов с АГ в данной популяции составляет 22%. Больные АГ в сочетании с ХОБЛ старше по возрасту, среди них преобладают мужчины. Эти пациенты имеют доминирующий уровень АД, ЧСС и преобладающую частоту таких стратифика-
старше по возрасту и среди них преобладали мужчины. Эти пациенты имели также доминирующий уровень САД, ЧСС и частоты МАУ. Последний показатель, вероятно, отражает большую степень эндотелиальной дисфункции при коморбидности АГ и ХОБЛ. Также в названной группе можно отметить тенденцию к возрастанию ИМТ, соотношения ОТ/ОБ, выраженности ГЛЖ по критерию Соколова-Лайона, ЛПИ и глюкозы крови, что скорее обусловлено превалированием метаболических нарушений и гипертонического поражения органов-мишеней.
Сравнение изучаемых групп больных АГ с наличием и отсутствием ХОБЛ по частоте стратификационных сердечно-сосудистых факторов риска изображено на рисунке 3. Отмечено значимое доминирование в группе АГ с ХОБЛ в сравнении с больными с АГ - мужчин старше 55 лет (χ=18,5, р<0,001), курящих больных (χ=4,0, р=0,04), пациентов с абдоминальным ожирением (χ=4,9, р=0,026) и гиперхолестеринемией (χ=5,2, р=0,022).
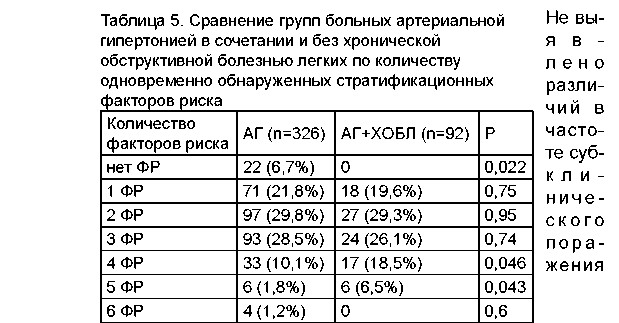
Сравнительный анализ групп по количеству одновременно обнаруженных у больного ФР ССО представлен в таблице 5 и на рисунке 4.
В группе больных АГ с ХОБЛ значимо меньше встречались пациенты без ФР и преобладали больные с наличием одновременно четырех и пяти ФР ССО. Среди больных АГ в сочетании с ХОБЛ 47 (51%) относились к пациентам высокого/очень высокого сердечно-сосудистого риска, в сравнительной группе – 136 (41,7%).
Последующим шагом явилась сравнительная оценка у больных АГ с наличием и отсутствием ХОБЛ обуславливает большую частоту встречаемости среди них (51% против 41,7%) пациентов с высоким/очень высоким суммарным сердечно-сосудистым риском. У больных АГ с сопутствующей ХОБЛ показано превалирование частоты гипертонического поражения органов-мишеней (сердца, сосудов и почек), которое определяется полом и возрастом пациента, а также степенью повышения артериального давления.
ционных факторов риска сердечнососудистых осложнений, как возраст у мужчин старше 55 лет, курение, абдоминальное ожирение и гиперхолестеринемия. В группе больных АГ с ХОБЛ реже встречаются пациенты без факторов риска и преобладают больные с наличием одновременно четырех и пяти стратификационных факторов риска, что


Литература
- Профилактика, диагностика и лечение первичной артериальной гипертонии в Российской Федерации. Первый Доклад экспертов научного общества по изучению Артериальной Гипертонии Всероссийского научного общества кардиологов и Межведомственного совета по сердеч- ноөсосудистым заболеваниям (ДАГ 1) //Клин. фармакология и терапия. – 2000. – Т. 9, №3. – С. 5–30.
- Оганов Р.Г., Шальнова С.А., Деев А.Д. и др. Артериальная гипертония и ее вклад в смертность от сердечно-сосудистых заболеваний // Профил. заболев. и укрепление здоровья. – 2001. - № 4. – С . 11-15.
- Buist A.S., McBurnie M.A., Vollmer W.M. et al. International variation in the prevalence of COPD (The BOLD Study): a population-based prevalence study // The Lancet. – 2007. – 370(9589). – P. 741-750.
- Mannino D.M. Epidemiology and global impact of chronic obstructive pulmonary disease //Semin. Respir. Crit. Care Med. – 2005. – Vol. 26(20). – P. 204-210.
- Marguis K., Maltais F., Poirier P. Cardiovascular manifestations in patients with COPD //Rev. Mal. Respir. – 2008. – Vol. 25(6). – P. 663-673.
- Schneider C, Bothner U, Jick SS, Meier CR. et al. Chronic obstructive pulmonary disease and the risk of cardiovascular diseases // Eur. J. Epidemiol. – 2010. - Vol. 27. – P. 34-39.
- Falk J.A., Kadiev S., Criner G.J. et al. Cardiac disease in chronic obstructive pulmonary disease //Proc. Am. Thorac. Soc. – 2008. – Vol. 5(4). – P. 543-548.
- Дворецкий Л.И. Артериальная гипертония у ольных ХОБЛ //Русский медицинский журнал . – 2003. http://www.rmj.ru/articles_883.htm.
- . Абдукаримов Б.У., Ошакбаев К.П., Рысмендиев .Ж. Специализированная кардиологическая помошь аселению Казахстана. - Алматы, 2004. - 120 с.
- 0. Потемкина Р.И., Глазунов И.С., Кузнецова О.Ю. соавт. Изучение распространенности поведенче- ких факторов риска неинфекционных заболеваний реди населения Москвы, Санкт-Петербурга и Твери етодом телефонного опроса //Профил. забол. и крепл. здоровья. – 2005. - №3. – С. 21-25.
- Арабидзе Г.Г. Схема поэтапного обследованияАканов А.А., Тулебаев К.А., Нургабылова А.Б.
- Аканов А.А., Сейсенбаев А.Ш., Айтжанова Г.Б. и соавт. Алгоритмы действий медицинских работников на уровне ПМСП по основным факторам риска хронических неинфекционных заболеваний. - Алматы, 2000. – 40 с.
- Потемкина Р. А ., Глазунов И . С., Оганов Р. Г. и соавт. Мониторирование поведенческих факторов риска неинфекционных заболеваний среди населения //Профилак. заболеван. и укрепл. здоровья. – 2005. - № 4. – С . 3-11.
- Метаболический синдром / под ред. чл.-корр. РАМН Ройтберга Г.Е.. – Москва: Медпресс-информ, 2007. – 224 с.
- Кобалава Ж.Д., Котовская Ю.В. Артериальная гипертония 2000: ключевые аспекты диагностики и дифференциальной диагностики, профилактики, клиники и лечения. – М., 2000. – 208 с.
- Кобалава Ж .Д., Котовская Ю.В., Виллевальде С .В . Рекомендации по артериальной гипертонии 2007: текст, контекст и размышления //Кардиология. – 2008. - №2. –С. 72-87.
- Global Initiative for Chronic Obstructive Lung Disease. Global Strategy for the Diagnosis, Management and Prevention of Chronic Obstructive Pulmonary Disease. NHLBI/WHO workshop report. Bethesda, National Heart, Lung and Blood Institute, update 2006 (www. goldcopd.com).